典型相图分析
蔡氏电路

(1)
非线性负阻 蔡氏电路示意图 (截自实验中心讲义)
f(U1)是分段函数,每一段是线性 函数,但整体呈非线性 分别在上区、中区、下区考虑方 程组(1)的特性(此时分别为 线性微分方程组),然后再联合 起来考虑
上区
上区
中区
中区
中区
下区
下区
整体(双吸引子)
整体(双吸引子)
整体(双吸引子)
整体(单吸引子)
整体(单吸引子)
整体(单吸引子)
混沌的特性:初值敏感性
R=2000Ω 双吸引子
初值分别为: [I3, U2, U1](T=0)=[0.001, 0, 0](蓝线); [I3, U2, U1](T=0)=[0.001+10^-10, 0, 0](红线); 作U1随T的时序图
混沌的特性:初值敏感性
混沌的特性:初值敏感性
R=2105Ω
[I3, U2, U1](T=0)=[0.001, 0, 0]
混沌的特性:初值敏感性
R=2105Ω
[I3, U2, U1](T=0)=[-0.0析
蔡氏电路
I3、U2、U1张成一个 三维相空间,相空间 中的轨迹(I3(t), U2(t),U1(t)) 描述电路的状态变化, 称为相图 U2 U1
I3
实验中通过调节电阻 R来得到不同参数下 的相图,反映电路不 同的变化规律
非线性负阻 蔡氏电路示意图 (截自实验中心讲义)
非线性负阻的伏安特性
蔡氏电路现象及分析蔡氏电路蔡氏电路示意图截自实验中心讲义非线性负阻u2u1i3i3u2u1张成一个三维相空间相空间中的轨迹i3tu2tu1t描述电路的状态变化称为相图实验中通过调节电阻r来得到不同参数下的相图反映电路不同的变化规律非线性负阻的伏安特性ga761041gb4091041e165v参考值典型相图双吸引子三维相图二维相图典型相图单吸引子三维相图二维相图典型相图单周期三维相图二维相图典型相图不动点三维相图二维相图非线性负阻蔡氏电路示意图截自实验中心讲义u2u1i3分析方法fu1是分段函数每一段是线性函数但整体呈非线性分别在上区中区下区考虑方程组1的特性此时分别为线性微分方程组然后再联合起来考虑dtdudtdudtdi上区上区中区中区中区下区下区整体双吸引子整体双吸引子整体双吸引子整体单吸引子整体单吸引子整体单吸引子混沌的特性
相图分析——精选推荐

相图分析物理化学复习总结之相平衡f组分数,⾃由度,相图,相点,露点,泡点,共熔点,(连)结线,三相线,步冷(冷却)曲线,低共熔混合物(固相完全不互溶)本章主要要求掌握相律的使⽤条件和应⽤,单组分和双组分系统的各类典型相图特征、绘制⽅法和应⽤,利⽤杠杆规则进⾏有关计算1、相律: F = C - P + n , 其中:C=S-R-R’U+ }3 Q0 G- D4 L$ \6 e- D) l(1) 强度因素T,p可变时n=2/ n) \+ r' I3 G" P5 [3 q* A) f(2) 对单组分系统:C=1, F=3-P j(3) 对双组分系统:C=2,F=4-P;应⽤于平⾯相图时恒温或恒压,F=3-P。
Y% z2 ]7 h' z5 d- X- 2、相图(1)相图:相态与T,p,x的关系图,通常将有关的相变点联结⽽成。
(2)实验⽅法:实验主要是测定系统的相变点。
常⽤如下四种⽅法得到。
4 Z r! M- J2 u! s( _. ms 对于⽓液平衡系统,常⽤⽅法蒸⽓压法和沸点法;" A+ d4 S0 D/ v! r液固(凝聚)系统,通常⽤热分析法和溶解度法。
$ l( m3 N$ j5 a" ^3、单组分系统的典型相图对于单组分系统C=1,F=C-P+2=3-P。
当相数P=1时,⾃由度数F=2最⼤,即为双变量系统,通常绘制蒸⽓压-温度(p-T)相图,见下图。
(a) 正常相图(b) ⽔的相图(c) 硫的相图图6-1 常见的单组分系统相图/ ]. g/ W. Y' n* ?" ^# _⼆组分系统的相图j类型:恒压的t-x(y)和恒温的p-x(y)相图。
相态:⽓液相图和液-固(凝聚系统)相图。
5 f% ^( `8 E0 e; h; W! y1 |8 SB(1)⽓液相图根据液态的互溶性分为完全互溶(细分为形成理想混合物、最⼤正偏差和最⼤负偏差)、部分互溶(细分为有⼀低共溶点和有⼀转变温度的系统)和完全不溶(溶液完全分层)的相图。
相、组分数和自由度的概念,相律,典型二组分相图分析,绘制

四、条件自由度
f* :在f 中人为固定一些因素或某一个因素对系统影响不大,则可将此因素略
去,此时的自由度即为条件自由度;
如:对凝聚系统,p 影响不大。
f* = C-Φ +1
求 HCN(aq)体系的的 S ,C, f ,
若 S=2,C=2 f = C-Φ +2=2-1+2=3。
若 S=5,C=2 (R=2,R′=1) f = 3 。
图。 4.能看懂和分析相图,并能用相律来说明相图中点、线、面的意义及体系在不同
情况下的相变过程,掌握杠杆规则的使用 5.掌握各种典型二组分相图分析,掌握利用相图在分离、提纯等方面的应用。 6.了解三组分体系的组成表示方法,了解部分互溶的三液体系三组分盐水体系的
相图及其应用。 重点和难点:
相、组分数和自由度的概念,相律,典型二组分相图分析,绘制
(2) 每一相中有一组分不独立,则共有Φ 个。
(3) 由相平衡条件决定 C(Φ -1)-1 个不独立。
则 f = CΦ –1-Φ -C(Φ -1)+1+2= C-Φ +2
注: +2 假设外界影响因素只有温度、压力;若只有温度或压力中之一,则+1;
若共有 n 个其它影响因素,则+n 即 f =C—Φ + n(最一般式)。
一、物种数(S):体系中物质总的种类数。 注:其数值可变,如 NaCl(aq)体系,S 可取 2、3、5 等。
二、独立组分数(C):体系中可独立变化的物种数。 引入原因:
1.若有独立化学反应 S 间不能独立变化,每个反应使一个物种不独立; 注:化学反应必须独立;如对由CO、H2 O、CO2 、H2、O2 组成的平衡体系, 化学反应有:
铁碳合金相图分析
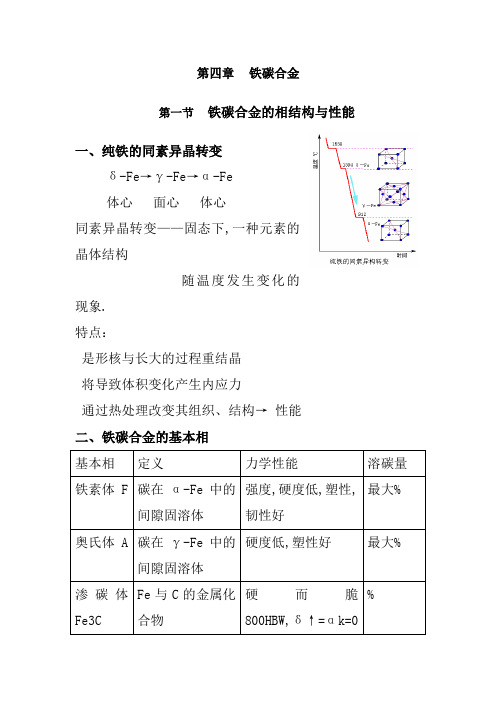
第四章铁碳合金第一节铁碳合金的相结构与性能一、纯铁的同素异晶转变δ-Fe→γ-Fe→α-Fe体心面心体心同素异晶转变——固态下,一种元素的晶体结构随温度发生变化的现象.特点:是形核与长大的过程重结晶将导致体积变化产生内应力通过热处理改变其组织、结构→ 性能二、铁碳合金的基本相基本相定义力学性能溶碳量铁素体 F碳在α-Fe中的间隙固溶体强度,硬度低,塑性,韧性好最大%奥氏体 A碳在γ-Fe中的间隙固溶体硬度低,塑性好最大%渗碳体Fe3C Fe与C的金属化合物硬而脆800HBW,δ↑=αk=0%第二节铁碳合金相图一、相图分析两组元:Fe、 Fe3C上半部分图形二元共晶相图共晶转变:1148℃ 727℃→ + Fe3C →P + Fe3C莱氏体Ld Ld′2、下半部分图形共析相图两个基本相:F、Fe3C共析转变:727℃→ + Fe3C珠光体P二、典型合金结晶过程分类:三条重要的特性曲线① GS线---又称为A3线它是在冷却过程中由奥氏体析出铁素体的开始线或者说在加热过程中铁素体溶入奥氏体的终了线.② ES线---是碳在奥氏体中的溶解度曲线当温度低于此曲线时就要从奥氏体中析出次生渗碳体通常称之为二次渗碳体因此该曲线又是二次渗碳体的开始析出线.也叫Acm线.③ PQ线---是碳在铁素体中的溶解度曲线.铁素体中的最大溶碳量于727oC时达到最大值%.随着温度的降低铁素体中的溶碳量逐渐减少在300oC以下溶碳量小于%.因此当铁素体从727oC冷却下来时要从铁素体中析出渗碳体称之为三次渗碳体记为Fe3CⅢ.工业纯铁<%C钢——亚共析钢、共析钢%C、过共析钢白口铸铁——亚共晶白口铸铁、共晶白口铸铁、过共晶白口铸铁L → L+A → A → PF+Fe3CL → L+A → A → A+F →P+FL → L+A → A → A+ Fe3CⅡ→P+ Fe3CⅡ4、共晶白口铸铁L → LdA+Fe3C →LdA+Fe3C+ Fe3CⅡ → Ld′P+Fe3C+Fe3CⅡ5、亚共晶白口铸铁L → LdA+Fe3C + A →Ld+A+ Fe3CⅡ → Ld′+P+ Fe3CⅡ6、过共晶白口铸铁L → LdA+Fe3C + Fe3C → Ld + Fe3C→ Ld′+ Fe3C三、铁碳合金的成分、组织、性能之间的关系1、含碳量对铁碳合金平衡组织的影响2、含碳量对铁碳合金力学性能的影响四、铁碳合金相图的应用1、选材方面的应用2、在铸造、锻造和焊接方面的应用3、在热处理方面的应用第三节碳钢非合金钢碳钢是指ωc≤%,并含有少量锰、硅、磷、硫等杂质元素的铁碳合金.铁碳合金具有良好的力学性能和工艺性能,且价格低廉,故广泛应用.一、杂质元素对碳钢性能的影响1、锰Mn + FeO → MnO + Fe 脱氧Mn+ S → MnS 炉渣去硫Mn溶入铁素体→ 固溶强化Mn溶入Fe3C → 形成合金渗碳体Fe, Mn3C Mn <%,对性能影响不大2、硅Si + FeO → SiO2 + Fe 脱氧Si溶入铁素体→ 固溶强化Si<%,对性能影响不大3、硫钢中S+Fe → FeS.FeS与Fe形成低熔点的共晶体985℃分布在晶界上,当钢在热加工1000~1200℃时,共晶体熔化,导致开裂——热脆消除热脆:Mn+ S → MnS熔点高1620℃并有一定塑性硫是一种有害元素4、磷钢中磷全部溶于铁素体,产生强烈固溶强化,低温时更加严重——冷脆磷是一种有害元素二、碳钢的分类按含碳量分:低碳钢~、中碳钢~、高碳钢~%按质量分类:普通碳钢、优质碳钢、特殊碳钢S、P含量按用途分类:碳素结构钢、碳素工具钢三、碳钢的牌号、性能和应用1、碳素结构钢GB700-88 Q195, Q215, Q235, Q255, Q275五大类,20个钢种GB700-79 A1, A2, A3, A4, A5Q235-AF表示:σs≥235Mpa,质量等级为A,沸腾钢.应用:Q195, Q215——塑性高,用于冲压件、铆钉、型钢等; Q235——强度较高,用于轴、拉杆、连杆等;Q255, Q275——强度更高,用于轧辊、主轴、吊钩等.2、优质碳素结构钢优质碳素结构钢:优质钢、高级优质钢A、特级优质钢E 牌号:08F ——冲压件;45——齿轮、连杆、轴类;65 Mn——弹簧、弹簧垫圈、轧辊等.3、碳素工具钢牌号:T8、T8A——木工工具;T10、T10A——手锯锯条、钻头、丝锥、冷冲模;T12、T12A——锉刀、绞刀、量具.4、铸钢表示方法:用力学性能表示ZG200-400σs≥200Mpa,σb≥400Mpa用化学成分表示ZG30%C用于制作形状复杂且强度和韧性要求较高的零件,如轧钢机架、缸体、制动轮、曲轴等.. 状态图中的特性点Fe- Fe3C相图中各点的温度、浓度及其含义Fe-Fe3C 相图中各特性点的符号及意义二. 状态图中的特性线Fe-C合金相图中的特性线三. 状态图中的相区在Fe-Fe3C相图中共有五个单相区、七个两相区和三个三相区.五个单相区是:ABCD以上——液相区LAHNA——δ固溶体区δα、δNJESGN——奥氏体区γ或AGPQG——铁素体区α或FDFKL——渗碳体区Fe3C或Cm两相区是:L+δ、L+γ、L+ Fe3C、δ+γ、α+γ、γ+ Fe3C和α+ Fe3C.三个三相区是:HJB线、ECF线和PSK线.1. 工业纯铁含C≤%——其显微组织为铁素体+Fe3CⅢ.2. 钢含C在~%——其特点是高温组织为单相奥氏体具有良好的塑性因而适于锻造.根据室温组织的不同钢又可分为三类:① 亚共析钢< C <%——其组织是铁素体+珠光体② 共析钢C=%——其组织为珠光体③ 过共析钢< C≤%——其组织为珠光体+渗碳体3. 铁在1538ºC结晶为δ-FeX射线结构分析表明它具有体心立方晶格.当温度继续冷却至1394ºC时δ-Fe转变为面心立方晶格的γ- Fe通常把δ-Fe←→γ- Fe的转变称为A4转变转变的平衡临界点称为A4点.当温度继续降至912ºC时面心立方晶格的γ- Fe又转变为体心立方晶格的α-Fe把γ- Fe←→α-Fe的转变称为A3转变转变的平衡临界点称为A3点.4. 三条重要的特性曲线① GS线---又称为A3线它是在冷却过程中由奥氏体析出铁素体的开始线或者说在加热过程中铁素体溶入奥氏体的终了线.② ES线---是碳在奥氏体中的溶解度曲线当温度低于此曲线时就要从奥氏体中析出次生渗碳体通常称之为二次渗碳体因此该曲线又是二次渗碳体的开始析出线.也叫Acm线.③ PQ线---是碳在铁素体中的溶解度曲线.铁素体中的最大溶碳量于727ºC时达到最大值%.随着温度的降低铁素体中的溶碳量逐渐减少在300ºC以下溶碳量小于%.因此当铁素体从727ºC冷却下来时要从铁素体中析出渗碳体称之为三次渗碳体记为Fe3CⅢ.四. 名词1. 铁素体:是碳在α-Fe中形成的固溶体常用“δ”或“F”表示.铁素体在770ºC以上具有顺磁性在770ºC以下时呈铁磁性.通常把这种磁性转变称为A2转变把磁性转变温度称为铁的居里点.碳溶于δ-Fe中形成的固溶体叫δ铁素体在1495ºC时其最大溶碳量为%.2. 顺磁性:就是在顺磁物质中分子具有固有磁矩无外磁场时由于热运动各分子磁矩的取向无规宏观上不显示磁性;在外磁场作用下各分子磁矩在一定程度上沿外场排列起来宏观上呈现磁性这种性质称为顺磁性.3. 铁磁性:就是磁性很强的物质在未磁化时宏观上不显示出磁性但在外加磁场后将会显示很强的宏观磁性.4. 奥氏体:是碳溶于γ-Fe中所形成的固溶体用“γ”或“A”表示.奥氏体只有顺磁性而不呈现铁磁性.碳在γ-Fe 中是有限溶解其最大溶解度为%1148ºC.5. 渗碳体:是铁与碳的稳定化合物Fe3C 用“C”表示.其含碳量为%.由于碳在α-Fe中的溶解度很小所以在常温下碳在铁碳合金中主要是以渗碳体的形式存在.渗碳体于低温下具有一定的铁磁性但是在230ºC以上铁磁性就消失了所以230ºC是渗碳体的磁性转变温度称为A0转变.渗碳体的熔点为1227ºC.它不能单独存在总是与铁素体混合在一起.在钢中它主要是强化相它的形态、大小及分布对钢的性能有很大的影响.另外渗碳体在一定的条件下可以分解形成石墨状的自由碳.即Fe3C——→3Fe+C石墨6. 珠光体:是由铁素体和渗碳体所组成的机械混合物常用“P”表示.珠光体存在于727ºC以下至室温.五. 铁碳合金相图的应用一在选材方面的应用若需要塑性、韧性高的材料应选用低碳钢含碳为~%;需要强度、塑性及韧性都较好的材料应选用中碳钢含碳为~%;当要求硬度高、耐磨性好的材料时应选用高碳钢含碳为~%.一般低碳钢和中碳钢主要用来制造机器零件或建筑结构.高碳钢主要用来制造各种工具.二在制定热加工工艺方面的应用铁碳相图总结了不同成分的合金在缓慢加热和冷却时组织转变的规律即组织随温度变化的规律这就为制定热加工及热处理工艺提供了依据.钢处于奥氏体状态时强度较低、塑性较好便于塑性变形.因此钢材在进行锻造、热轧时都要把坯料加热到奥氏体状态.各种热处理工艺与状态图也有密切的关系退火、正火、淬火温度的选择都得参考铁碳相图.六. 应用铁碳相图应注意的几个问题1. 铁碳相图不能说明快速加热或冷却时铁碳合金组织的变化规律.2. 可参考铁碳相图来分析快速加热或冷却的问题但还应借助于其他理论知识.3. 相图告诉我们铁碳合金可能进行的相变但不能看出相变过程所经过的时间.相图反映的是平衡的概念而不是组织的概念.铁碳相图是由极纯的铁和碳配制的合金测定的而实际的钢铁材料中还含有或有意加入许多其他元素.其中有些元素对临界点和相的成分都有很大的影响此时必须借助于三元或多元相图来分析和研究.第二部分晶体结构一. 金属键1. 金属键:金属原子依靠运动于其间的公有化的自由电子的静电作用而结合起来这种结合方式叫金属键.2. 在固态金属及合金中众多的原子依靠金属键牢固的结合在一起.二. 晶体结构1. 晶体:凡是原子或离子、分子在三维空间按一定规律呈周期性排列的固体均是晶体.液态金属的原子排列无周期规则性不为晶体.2. 晶体结构:是指晶体中原子或离子、分子、原子集团的具体排列情况也就是晶体中这些质点原子或离子、分子、原子集团在三维空间有规律的周期性的重复排列方式.3. 三种典型的金属晶体结构a. 体心立方晶格:晶胞的三个棱边长度相等三个轴间夹角均为90º构成立方体.除了在晶胞的八个角上各有一个原子外在立方体的中心还有一个原子.b. 面心立方晶格:在晶胞的八个角上各有一个原子构成立方体在立方体6个面的中心各有一个原子.c. 密排六方晶格:在晶胞的12个角上各有一个原子构成六方柱体上底面和下底面的中心各有一个原子晶胞内还有3个原子.三. 固溶体1. 固溶体:合金的组元以不同的比例相互混合混合后形成的固相的晶体结构与组成合金的某一组元的相同这种相就称为固溶体.2. 置换固溶体:是指溶质原子位于溶剂晶格的某些结点位置所形成固溶体.3. 间隙固溶体:是指溶质原子不是占据溶剂晶格的正常结点位置而是填入溶剂原子间的一些间隙中.4. 金属化合物:是合金组元间发生相互作用而形成的一种新相又称为中间相其晶格类型和性能均不同于任一组元一般可以用分子式大致表示其组成.除了固溶体外合金中另一类相是金属化合物.四. 金属的结晶1. 金属的结晶:金属由液态转变为固态的过程称为凝固由于凝固后的固态金属通常是晶体所以又将这一转变过程称之为结晶.2. 杠杆定律的应用.在合金的结晶过程中合金中各个相的成分以及它们的相对含量都在发生着变化.为了了解相的成分及其相对含量就需要应用杠杆定律.对于二元合金两相共存时两个平衡相的成分固定不变.五. 同素异构转变当外部条件如温度和压强改变时金属内部由一种晶体结构向另一种晶体结构的转变称为多晶型转变或同素异构转变.六. 晶体的各向异性各向异性是晶体的一个重要特性是区别于非晶体的一个重要标志.晶体具有各向异性的原因是由于在不同的晶向上的原子紧密程度不同所致.原子的紧密程度不同意味着原子之间的距离不同从而导致原子之间的结合力不同使晶体在不同晶向上的物理、化学和机械性能不同.第三部分元素的影响1. 锰和硅的影响:锰和硅是炼钢过程中必须加入的脱氧剂用以去除溶于钢液中的氧.它还可以把钢液中的F eO还原成铁并生成MnO和SiO2.脱氧剂中的锰和硅总会有一部分溶于钢液中冷至室温后即溶于铁素体中提高铁素体的强度.锰对钢的机械性能有良好的影响它能提高钢的强度和硬度当含锰量低于%时可以稍微提高或不降低钢的塑性和韧性.碳钢中的含硅量一般小于%它也是钢中的有益元素.硅溶于铁素体后有很强的固溶强化作用显著的提高了钢的强度和硬度但含量较高时将使钢的塑性和韧性下降.2. 硫的影响:硫是钢中的有害元素.硫只能溶于钢液中在固态中几乎不能溶解而是以FeS夹杂的形式存在于固态钢中.硫的最大危害是引起钢在热加工时开裂这种现象称为热脆.防止热脆的方法是往钢中加入适量的锰形成MnS可以避免产生热脆.硫能提高钢的切削加工性能.在易切削钢中含硫量通常为%~%同时含锰量为%~%.3. 磷的影响:一般来说磷是有害的杂质元素.无论是高温还是低温磷在铁中具有较大的溶解度所以钢中的磷都固溶于铁中.磷具有很强的固溶强化作用它使钢的强度、硬度显著提高但剧烈地降低钢的韧性尤其是低温韧性称为冷脆磷的有害影响主要就在于此.4. 氮的影响:一般认为钢中的氮是有害元素但是氮作为钢中合金元素的应用已日益受到重视.5. 氢的影响:氢对钢的危害是很大的.一是引起氢脆.二是导致钢材内部产生大量细微裂纹缺陷——白点在钢材纵断面上呈光滑的银白色的斑点在酸洗后的横断面上则成较多的发丝壮裂纹.存在白点时钢材的延伸率显著下降尤其是断面收缩率和冲击韧性降低的更多有时可接近于零值.因此具有白点的钢是不能用的.6. 氧及其它非金属夹杂物的影响:氧在钢中的溶解度非常小几乎全部以氧化物夹杂的形式存在于钢中如FeO、AL2O3、SiO2、MnO、CaO、MgO等.除此之外钢中往往存在FeS、MnS、硅酸盐、氮化物及磷化物等.这些非金属夹杂物破坏了钢的基体的连续性在静载荷和动载荷的作用下往往成为裂纹的起点.它们的性质、大小、数量及分布状态不同程度地影响着钢的各种性能尤其是对钢的塑性、韧性、疲劳强度和抗腐蚀性能等危害很大.因此对非金属夹杂物应严加控制.第四部分热处理一. 热处理的作用1. 热处理:是将钢在固态下加热到预定的温度保温一定的时间然后以预定的方式冷却下来的一种热加工工艺.钢中组织转变的规律是热处理的理论基础称为热处理原理.热处理原理包括钢的加热转变、珠光体转变、马氏体转变、贝氏体转变和回火转变.在临界温度以下处于不稳定状态的奥氏体称为过冷奥氏体.钢在加热和冷却时临界温度的意义如下:Ac1——加热时珠光体向奥氏体转变的开始温度;Ar1——冷却时奥氏体向珠光体转变的开始温度;Ac3——加热时先共析铁素体全部转变为奥氏体的终了温度;Ar3——冷却时奥氏体开始析出先共析铁素体的温度;Accm——加热时二次渗碳体全部溶入奥氏体的终了温度;Arcm——冷却时奥氏体开始析出二次渗碳体的温度.通常把加热时的临界温度加注下标“C”而把冷却时的临界温度加注下标“r”.2. 珠光体转变——是过冷奥氏体在临界温度A1以下比较高的温度范围内进行的转变.珠光体转变是单相奥氏体分解为铁素体和渗碳体两个新相的机械混合物的相变过程因此珠光体转变必然发生碳的重新分布和铁的晶格改组.由于相变在较高温度下发生铁、碳原子都能进行扩散所以珠光体转变是典型的扩散型相变.无论珠光体、索氏体还是屈氏体都属于珠光体类型的组织.它们的本质是相同的都是铁素体和渗碳体组成的片层相间的机械混合物.它们之间的差别只是片层间距的大小不同而已.珠光体的片层间距:450~150 nm形成于A1~650℃温度范围内.索氏体的片层间距:150~80nm形成于650~600℃温度范围内.屈氏体的片层间距:80~30nm形成于600~550℃温度范围内.3. 马氏体转变——是指钢从奥氏体化状态快速冷却抑制其扩散性分解在较低温度下低于Ms点发生的转变.马氏体转变属于低温转变.钢中马氏体是碳在α-Fe中的过饱和固溶体具有很高的强度和硬度.由于马氏体转变发生在较低温度下此时铁原子和碳原子都不能进行扩散马氏体转变过程中的Fe的晶格改组是通过切变方式完成的因此马氏体转变是典型的非扩散型相变.二. 热处理工艺1. 退火和正火:将金属及其合金加热保温和冷却使其组织结构达到或接近平衡状态的热处理工艺称为退火或回火.A. 低温退火去应力退火:是指钢材及各类合金为消除内应力而施行的退火.加热温度< A1 碳钢及低合金钢550~650℃高合金工具钢600~750℃B. 再结晶退火:加热温度> Tr Tr+150~250℃C. 扩散退火:是指为了改善和消除在冶金过程中形成的成分不均匀性而实行的退火.1 通过扩散退火可以使在高温下固溶于钢中的有害气体主要是氢脱溶析出这时称为脱氢退火.2 均匀化退火的任务在于消除枝晶成分偏析改善某些可以溶入固溶体夹杂物如硫化物的状态从而使钢的组织与性能趋与均一.扩散退火的加热温度> Ac3 Acm 在固相线以下高温加热同时也要考虑不使奥氏体晶粒过于长大.碳钢1100~1200℃D. 完全退火:是指将充分奥氏体化的钢缓慢冷却而完成重结晶过程的退火.加热温度 Ac3+30~50℃E. 等温退火:是指将奥氏体用较快的速度冷却到临界点以下较高温度范围进行珠光体等温转变的退火. 加热温度 Ac3~Ac12. 正火:是指将碳合金加热到临界点Ac3以上适当温度并保持一定时间然后在空气中冷却的工艺方法.过共析钢正火后可消除网状碳化物而低碳钢正火后将显著改善钢的切削加工性.所有的钢铁材料通过正火均可使锻件过热晶粒细化和消除内应力.正火比退火的冷却速度快正火后的组织比退火后的组织细.3. 淬火与回火1. 淬火:是指将钢通过加热、保温和大于临界淬火速度Vc的冷却是过冷奥氏体转变为马氏体或贝氏体组织的工艺方法.2. 钢的淬透性:就是钢在淬火时能够获得马氏体的能力它是钢材本身固有的一个属性.3. 当淬火应力在工件内超过材料的强度极限时在应力集中处将导致开裂.4. 回火:本质上是淬火马氏体分解以及碳化物析出、聚集长大的过程.它与淬火不同点是由非平衡态向平衡态稳定态的转变.4. 化学热处理:是将工件放在一定的活性介质中加热使非金属或金属元素扩散到工件表层中、改变表面化学成分的热处理工艺.如:渗入碳、氮、硼、钒、铌、铬、硅等元素第五部分宏观检验一. 宏观检验主要可分为低倍组织及缺陷酸蚀检验、断口检验、硫印检验等.二. 酸蚀试验在宏观检验领域中酸蚀检验是最常用的检验金属材料缺陷、评定钢铁产品质量的方法.如果一批钢材在酸蚀中显示出不允许存在的缺陷或超过允许程度的缺陷时其它检验可不必进行.1. 酸蚀试验:是用酸蚀方法来显示金属或合金的不均匀性.1 热酸浸蚀实验方法2 冷酸浸蚀实验方法3 电解腐蚀实验方法2. 酸蚀试验所检验的常见组织和缺陷A:偏析:是钢中化学成分不均匀现象的总称.在酸蚀面上偏析若是易蚀物质和气体夹杂物析集的结果将呈现出颜色深暗、形状不规则而略凹陷、底部平坦的斑点;若是抗蚀性较强元素析集的结果则呈颜色浅淡、形状不规则、比较光滑微凸的斑点.根据偏析的位置和形状可分为中心偏析、锭型偏析或称方框偏析、点状偏析、白斑和树枝状组织.中心偏析:出现在试面中心部位形状不规则的深暗色斑点.锭型偏析:具有原钢锭横截面形状的、集中在一条宽窄不同的闭合带上的深暗色斑点.B. 疏松:这种缺陷是钢凝固过程中由于晶间部分低熔点物最后凝固收缩和放出气体而产生的孔隙.在横向酸蚀面上这种孔隙一般呈不规则多边形、底部尖狭的凹坑这种凹坑多出现在偏析斑点之内.根据疏松分布的情况可分为中心疏松和一般疏松.C. 夹杂:宏观夹杂可分为外来金属、外来非金属和翻皮三大类.D. 缩孔:由于最后凝固的钢液凝固收缩后得不到填充而遗留下来的宏观孔穴.E. 气泡:由于钢锭浇注凝固过程中所产生和放出气体所造成的.一般可分为皮下气泡和内部气泡两类.a. 皮下气泡: 由于浇注时钢锭模涂料中的水分和钢液发生作用而产生的气体.b. 内部气泡:又可分为蜂窝气泡和针孔气泡.蜂窝气泡是由于钢液去气不良所导致一般为不允许存在的缺陷存在钢坯内部在试面上较易浸蚀象排列有规律的点状偏析但颜色更深暗些;针孔是因为较深的皮下气泡在锻轧过程中未焊合而被延伸成细管状在横试面上呈孤立的针状小孔.白点:也称发裂是由于氢气脱溶析集到疏松孔中产生巨大压力和钢相变时所产生的局部内应力联合造成的细小裂缝.在横试面上呈细短裂缝三. 硫印检验是一种定性检验是用来直接检验硫元素并间接检验其它元素在钢中偏析或分布情况的操作.硫印检验时先用5~10%的稀硫酸水溶液浸泡相纸5分钟左右后取出去除多余的硫酸溶液把湿润的相纸感光面贴到受检表面上应确保相纸与试样面的紧密接触不能发生任何滑动排除相纸与试样面的气泡和液滴.其化学反应大致为:MnS+H2SO4→MnSO4+H2S↑FeS+H2SO4→FeSO4+H2S↑H2S+2AgBr→2HBr+Ag2S↓几秒到几分钟后将从试面上揭下的相纸在水中冲洗约10分钟然后放入定影液中定影10分钟以上取出后在流动水中冲洗30分钟以上干燥后既成.四. 断口检验1. 脆性断口:通常工程上把没有明显塑性变形的断裂统称为脆性断裂发生脆性断裂的断口为脆性断口.脆性断口也称晶状断口是指出现大量晶界破坏的耀眼光泽断口断口中晶状区的面积与断口原始横截面积的百分比则是脆性断面率也称晶状断面率.2. 结晶状断口:此种断口具有强烈的金属光泽有明显的结晶颗粒断面平齐而呈银灰色.是一种正常的断口.属于脆性断口.3. 纤维状断口:这种断口呈无光泽和无结晶颗粒的均匀组织.通常在断口的边缘有明显的塑性变形.一般情况下是允许存在的.属于韧性断口.4. 瓷状断口:是一种类似瓷碎片的断口呈亮灰色、致密、有绸缎的光泽和柔和感.是一种正常的断口.5. 台状断口:这种断口出现在纵向断面上呈比基体颜色略浅、变形能力稍差、宽窄不同、较为平坦的片状平台状.多分布在偏析内.6. 撕痕状断口:这种断口出现在纵向断面上沿热加工方向呈灰白色、变形能力差致密而光滑的条带.7. 层状断口:这种断口出现在纵向断面上呈劈裂的朽木状或高低不平的、无金属光泽的、层次起伏的条带条带中伴有白亮或灰色线条.8. 缩孔残余断口:出现在纵向断口的轴心区是非结晶状条带或疏松区有时伴有非金属夹杂物或夹杂沿条带常带有氧化色.9. 石状断口:在断口表面呈现粗大而凹凸不平的沿晶界断裂的粗晶颜色暗灰而无金属光泽象有棱角的沙石颗粒堆砌在一起.。
铁碳合金相图解析

b
14
三、过共析钢的结晶过程分析
图1-36 过共析钢结晶过程示意图
图1-37 过亚 共析钢的显 微组织
b
15
四、共晶白口铸铁的结晶过程分析
图1-38 共晶白口铸铁结晶过程示意图
图 1-39 共 晶 白 口 铸铁的显微组织
b
16
五、亚共晶白口铸铁的结晶过程分析
图1-40 亚共晶白口铸铁结晶过程示意图
b
5
知识点二 Fe- Fe3C相图分析
b
6
图1-30 Fe- Fe3C相图
简化的Fe- Fe3C相图
b
7
1、主要特性点
表1-4简化Fe- Fe3C相图中的特性点
特性点 符号
A
温度/℃ ωc(%)
1538
0
含义 熔点:纯铁的熔点
C
1148
4.3 共晶点:发生共晶转变L4.3—→Ld(A2.11%+Fe3C共晶)
四个单相区。
(2)两相区 简化的Fe- Fe3C相图中有五个两相区,即
L+A两相区、L+Fe3C两相区、A+Fe3C两相区、A+F两相
区和F+ Fe3C两相区。
每个两相区都与相应的两个单相区相邻;两条三相共存线,
即共晶线ECF,L、A和Fe3C三相共存,共析线PSK,A、F
和Fe3C三相共存。
b
10
图1-46 铁碳相图与铸锻 工艺间的关系
b
22
3、在锻压生产上的应用
钢在室温时组织为两相混合物,塑性较差,变形困难。而奥氏体的强 度较低,塑性较好,便于塑性变形。因此在进行锻压和热轧加工时, 要把坯料加热到奥氏体状态。加热温度不宜过高,以免钢材氧化烧损 严重,但变形的终止温度也不宜过低,过低的温度除了增加能量的消 耗和设备的负担外,还会因塑性的降低而导致开裂。所以,各种碳钢 较合适的锻轧加热温度范围是:始锻轧温度为固相线以下100~200℃; 终锻轧温度为750~850℃。对过共析钢,则选择在PSK线以上某一温 度,以便打碎网状二次渗碳体。
材料科学基础 -二元合金相图

1、相图分析
(1)相区 单相区:L, a, b 两相区: L+a, L+ b,a+b
(2)相变线
TAP及TBP:L→a, L→b。
TAC及TBD:初生a及b结晶终了线。
CE及DF:
a
→bII,b→
a
。
II
CDP: L+ a →b。
液相线:TAPTB
固相线:TACDTB
(3)相变点 P:包晶转变点,发生包晶反应的液相成分点。
相区
单相区:L, a, b 两相区: L+a, L+ b,a+b
相变线
TAE及TBE:初生(初晶)a及b析出线 即L→a, L→b
TAM及TBN:初生a及b结晶终了线 MF及NG: a及b溶解度变化线
即a→bII,b→aII MEN: 共晶线,即L→a+b
相变点
TA及TB:纯组元A、B的熔点 M及N:a及b的最大溶解度点 F及G:a及b室温溶解度点 E:共晶点,发生共晶反应的液相成分点
问题:假定合金分别冷却到1,2,3,4温度开始结晶,获得的组织特点有何不同?
(2)晶内偏析共晶
晶内偏析共晶: 端部固溶体合金非平衡结晶时出现共晶组织
的现象。 由于晶内偏析共晶数量较少,往往以离异
共晶形式存在。 两种情况促使离异共晶形成: ►靠近极限溶解度的端部固溶体的非平衡冷却。 ►靠近极限溶解度的亚共晶合金的平衡冷却。
(3)x2合金
组织组成物:a0+ b包+aII +bII
Wa II
DF EF
Cx2 CD
100%
相 对 量
Wb II
CE Dx2 EF CD
100%
计 算
Wa0
金属共晶相图
5.3.2 二元共晶相图①共晶相图:当两组元在液态能无限互溶,在固态只能有限互溶,并具有共晶转变,这样的二元合金系所构成的相图称为二元共晶相图。
如Pb-Sn,Pb-Sb,Cu-Ag,Al-Si等合金的相图都属于共晶相图。
Pb-Sn合金相图是典型的二元共晶相图,见图, 下面以它为例进行讲解。
首先分析相图中的点,线和相区。
图铅锡相图一、相图分析1、点:t A,t B点分别是纯组元铅与锡的熔点,为和。
M点:为锡在铅中的最大溶解度点。
N点:为铅在锡中的最大溶解度点。
E点:为共晶点,具有该点成分的合金在恆温183℃时发生共晶转变L E→αM+βN共晶转变:是具有一定成分的液相在恆温下同时转变为两个具有一定成分和结构的固相的过程。
F点:为室温时锡在铅中的溶解度。
G点:为室温时铅在锡中的溶解度。
2、t A Et B线:为液相线,其中t A E线:为冷却时L→α的开始温度线,Et B线:为冷却时L→β的开始温度线。
t A MENt B线:为固相线,其中t A M线:为冷却时L→α的终止温度线,t B N线:为冷却时L→β的终止温度线。
MEN线:为共晶线,成分在M~N之间的合金在恒温183℃时均发生共晶转变L E→(αM+βN)形成两个固溶体所组成的机械混合物,通常称为共晶体或共晶组织。
MF线:是锡在铅中的溶解度曲线。
NG线:是铅在锡中的溶解度曲线。
3、相区(1)单相区:在t A Et B液相线以上,为单相的液相区用L表示,它是铅与锡组成的合金溶液。
t A MF线以左为单相α固溶体区,α相是Sn在Pb中的固溶体。
t B NG线以右为单相β固溶体区,β相是Pb在Sn中的固溶体。
(2)两相区:在t A EMt A区为L+α相区,在t B ENt B区为L+β相区。
在FMENGF区为α+β相区。
(3)三相线:MEN线为L+α+β三相共存线。
由相律可知三相平衡共存时,f=2-3+1=0,只能在恒温下实现。
具有共晶相图的二元系合金,通常可以根据它们在相图中的位置不同,分为以下几类:①成分对应于共晶点(E)的合金称为共晶合金,如Pb-Sn相图中含%的合金。
铁碳相图详解
三、典型铁碳合金的平衡结晶过程铁碳相图上的合金,按成分可分为三类:⑴ 工业纯铁(〈0.0218% C ),其显微组织为铁素体晶粒,工业上很少应用。
⑵ 碳钢(0.0218%~2。
11%C ),其特点是高温组织为单相A,易于变形,碳钢又分为亚共析钢(0.0218%~0。
77%C)、共析钢(0.77%C )和过共析钢(0。
77%~2.11%C )。
⑶ 白口铸铁(2。
11%~6。
69%C ),其特点是铸造性能好,但硬而脆,白口铸铁又分为亚共晶白口铸铁(2。
11%~4。
3%C )、共晶白口铸铁(4.3%C )和过共晶白口铸铁(4.3-6.69%C)下面结合图3-26,分析典型铁碳合金的结晶过程及其组织变化.图3—26 七种典型合金在铁碳合金相图中的位置㈠ 工业纯铁(图3-26中合金①)的结晶过程合金液体在1~2点之间通过匀晶反应转变为δ铁素体.继续降温时,在2~3点之间,不发生组织转变。
温度降低到3点以后,开始从d 铁素体中析出奥氏体,在3~4点之间,随温度下降,奥氏体的数量不断增多,到达4点以后,d 铁素体全部转变为奥氏体。
在4~5点之间,不发生组织转变。
冷却到5点时,开始从奥氏体中析出铁素体,温度降到6点,奥氏体全部转变为铁素体。
在6-7点之间冷却,不发生组织转变.温度降到7点,开始沿铁素体晶界析出三次渗碳体Fe 3C III 。
7点以下,随温度下降,Fe 3C III 量不断增加,室温下Fe 3C III 的最大量为:%31.0%1000008.069.60008.00218.03=⨯--=ⅢC Fe Q .图3—27为工业纯铁的冷却曲线及组织转变示意图。
工业纯铁的室温组织为a+Fe 3C III ,如图3—28所示,图中个别部位的双晶界内是Fe 3C III 。
图3-27 工业纯铁的冷却曲线及组织转变示意图 图3-28 工业纯铁的显微组织 400× ㈡ 共析钢(图3-26中合金②)的结晶过程共析钢的含碳量为0.77%,超过了包晶线上最大的含碳量0。
2.3典型二元相图的应用2.4凝固与结晶的理论
1.5
2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 6.0 Wc%
0.0218
0.77
2.11
4.3
6.69
图2-20 简化的Fe—Fe3C相图
2) Fe-Fe3C相图中的特性点 characteristic points
A点 1538℃ Wc=0 纯铁的熔点; D点 1227℃ Wc=6.69% 渗碳体的 熔点; G点 912 ℃ Wc=0 纯铁的同素异 晶转变点;
4)铁碳合金的分类 classification of iron carbon
类别 纯铁 钢
铸铁
合金名称 工业纯铁 亚共析钢 共析钢 过共析钢 亚共晶白口铁 共晶白口铁 过共晶白口铁
碳质量分数/% <0.0218
0.0218~0.77 0.77
0.77~2.11 2.11~4.30
4.30 4.30~6.69
F+A FP
700
1
1
2 2
A
1
L+A
2
E
3
3 A+Fe3CII
S
727
4
3
4
Q
F+P F+ Fe3CIII
P+Fe3CII
ⅣⅥ
L
1148 C
1
1
1227
D 2 L+FFe3C
Fe3C+Ld
Ld
2
3
K
Fe3C+Ld’
温度 t /℃ P
Ld’
100
0 0.2 0.4 0.6 0.8 1.0
1.5
2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 6.0 Wc%
铅锡共晶相图分析
1、相图分析图3-12为一般共晶型的Pb-Sn合金相图。
其中AEB线为液相线,ACEDB线为固相线,A点为铅的熔点(327℃),B点为锡的熔点(232℃)。
相图中有L、α、β三种相,形成三个单相区。
L代表液相,处于液相线以上。
α是Sn溶解在Pb中所形成的固溶体,位于靠近纯组元Pb的封闭区域内。
β是Pb溶解在Sn中所形成的固溶体,位于靠近纯组元Sn的封闭区域内。
在每两个单相区之间,共形成了三个两相区,即L+α、L+β和α+β。
图3-12 Pb-Sn二元合金相图相图中的水平线CED称为共晶线。
在水平线对应的温度(183℃)下,E点成分的液相将同时结晶出C点成分的α固溶体和D点成分的β固溶体:LE ⇄ ( αC+ βD)。
这种在一定温度下,由一定成分的液相同时结晶出两个成分和结构都不相同的新固相的转变过程称为共晶转变或共晶反应。
共晶反应的产物即两相的机械混合物称为共晶体或共晶组织。
发生共晶反应的温度称为共晶温度,代表共晶温度和共晶成分的点称为共晶点,具有共晶成分的合金称为共晶合金。
在共晶线上,凡成分位于共晶点以左的合金称为亚共晶合金,位于共晶点以右的合金称为过共晶合金。
凡具有共晶线成分的合金液体冷却到共晶温度时都将发生共晶反应。
发生共晶反应时,L、α、β三个相平衡共存,它们的成分固定,但各自的重量在不断变化。
因此,水平线CED是一个三相区。
相图中的CF线和DG线分别为Sn在Pb中和Pb在Sn中的溶解度曲线(即饱和浓度线),称为固溶线。
可以看出,随温度降低,固溶体的溶解度下降。
2、典型合金的结晶过程⑴含Sn量小于C点成分合金的结晶过程(以合金Ⅰ为例)由图3-12可见,该合金液体冷却时,在2点以前为匀晶转变,结晶出单相α固溶体,这种从液相中结晶出来的固相称为一次相或初生相。
匀晶转变完成后,在2、3点之间,为单相α固溶体冷却,合金组织不发生变化。
温度降到3点以下,α固溶体被Sn 过饱和,由于晶格不稳,便出现第二相—β相,显然,这是一种固态相变。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
体中的一小区域内,尽管温度比界面
处高,却存在一定的过冷度,这种由
成分的不均匀而产生的过冷度称为
‘成分过冷’。
固溶体凝固过程中,由于析出的
固体的成分和原液体有一定的差别,
排放到液体中的某些组元来不及均匀,
这种因成分偏差对应的凝固温度也不
同而造成的附加过冷度称为成分过冷。
精品文档
16
第二节 二元匀晶相图与固溶体的凝固
精品文档
19
第三节 二元共晶相图
二、共晶体的形成
过程
成分为E点合金的凝固
在TE温度以上仅是液体的冷却
到达略低于TE的温度,按L+α相区分析应为从液体中析出C成分的α相,而 按L+β相区分析应从液体中析出D成分的β相。如果α和β按一定的比例析 出,最终液体的成分不变,两固相不断同时析出,即共同结晶,故称为共晶 转变,直到液体完全消失,结晶过程完成,得到的是两固相的混合物,称为 共晶体。
第二节 二元匀晶相图与固溶体的凝固
四、固溶体材料非平衡冷却
非平衡凝固的特点有:①凝固过程中,液、固两相的成分偏离液、固相线; ②凝固过程进行到一更低的温度才能完成;③生成固体的成分是不均匀的。 随着冷却速度的加大,这些差别特点表现的愈明显。
结果:生成固体的成分不均匀较偏析,快速冷却时在一个晶粒内部先后结晶 的成分有差别,所以称为晶内偏析,金属的晶体往往以树枝晶方式生长,偏 析的分布表现为不同层次的枝晶成分有差别,因此这种偏析又称枝晶偏析。
精品文档
14
第二节 二元匀晶相图与固溶体的凝固
六、成分过冷
成分过冷现象:
在相图中,成分为C0的合金凝 固时,开始析出的固相为k0C0,多 余的B组元排放到液体中,在界面
处B组元的浓度高于平均值,逐渐
向液体中扩散。在液体未达到均匀
时,结晶继续进行,新析出的固体
成分中B的量也随着上升,同时液
体中界面处B浓度上升到更高的水
设mL和m分别为两相的数量, 由物质不灭可推导出:
一般用占总体数量的百分 比的相对值来表示。如果 把线段axc当成一杠杆,则 他们满足杠杆力的平衡原 理,所以称之为杠杆定律。
用杠杆定律来分析在理解和使用都精有品好文的档 直观性和方便。适用所有两相6平衡。
第二节 二元匀晶相图与固溶体的凝固
三、固溶体材料冷却时组织转变
相线之上为液相的单相区,
常用L表示;下面的一条曲
线称为固相线,固相线之下
为固溶体的单相区,常用α
表示;两条曲线之间是双相
区,标记L+α表示。
精品文档
5
第二节 二元匀晶相图与固溶体的凝固
二、两相平衡时的数量分配规律--杠杆定律
如图,合金x在温度T1将由两相长期并存,这时两相的成分 和数量保持不变。过x点作水平线交液相线和固相线于a、c点, 经热力学证明a、c点的成分分别为平衡的液体和固体的成分,
的温度,利用这一特点,由实测的冷却曲线可以作出相图。
精品文档
4
第二节 二元匀晶相图与固溶体的凝固
一、相图形式
两组元在液态和固态都能无限互溶。如Cu—Ni、Ag—Au形 成二元合金对应的相图就是二元匀晶相图。
相图的构成:由两条曲线将
相图分为三个区。左右两端
点分别为组元的熔点。上面
的一条曲线称为液相线,液
特点:
1.与纯金属凝固一样由 形核和长大来完成结晶 过程,实际进行在一定 的过冷度下。
2.凝固在一温度范围内 进行。只有在温度不断 下将时固体量才增加, 温度不变,液固数量维 持平衡不变。
3.凝固过程中液体和固 体的成分在不断变化。
精品文档
8
第二节 二元匀晶相图与固溶体的凝固
四、固溶体材料非平衡冷却
当x0时, CS(0)C0 CL(0)C0k0
精品文档
12
第二节 二元匀晶相图与固溶体的凝固
五、固溶体中溶质的分布
例二:关于区域熔炼
精品文档
13
第二节 二元匀晶相图与固溶体的凝固
六、成分过冷
在正温度梯度下,纯金属的生长方式为平面推进,而固 溶体凝固时,却有树枝状生长和胞状生长存在,这是由于凝 固过程中,成分是在不断变化,液体和固体的成分均不能达 到平衡状态,产生了成分过冷现象。
α上形核并长大,同理在β相外将附着α的形核长大。这种方
式就是交替形核。此外也有人认为交替形核是以边缘桥接生长
方式来实现的。
精品文档
21
第三节 二元共晶相图
二、共晶体的形成
生长特点
共同生长 两个相长大时都要 排放相应的溶质组元,排出的溶 质将阻碍自身的生长,但两相同 时生长时,一相排出的组元正是 另一相生长所需要的,所以两相 的生长过程将互相促进,最后是 两相共同携手长大。由于两固相 的成分是固定的,综合成分应和 液体的成分相同,它们的数量反 映在二者的厚度相对比例上。
精品文档
过程:
1点以上液体冷却
1点开始凝固,固体成 分在对应固相线处
1-2之间,温度下降, 液体数量减少,固体数 量增加,成分沿液相线 和固相线变化,
到2点,液体数量为0, 固体成分回到合金原始 成分,凝固完成
2点以下固体冷却,无 组织变化
7
第二节 二元匀晶相图与固溶体的凝固
三、固溶体材料冷却时组织转变
平,扩散的速度因浓度差的提高而
加快。远处液体的成分依然为C0, 到B组元的扩散量和固体排放平衡
时,析出固体的成分也为C0,这时
的成分分布如图b所示。
精品文档
15
第二节 二元匀晶相图与固溶体的凝固
六、成分过冷
成分过冷现象:
对照相图,液体的开始凝固温度
随着液体的成分变化而变化,图c给
出其分布曲线TL(x),如果G2为实际 温度,对比可以看出在界面前沿的液
相图用途:
• 由材料的成分和温度预知平衡相; • 材料的成分一定而温度发生变化
时其他平衡相变化的规律; • 估算平衡相的数量。
预测材料的组织和性能
精品文档
3
第一节 相图知识
二、相图与冷却曲线的关系:
成分一定,在冷却过程中,不同的相热容量不相同,如果 系统散热能力一样,温度随时间的变化(冷却)曲线上的斜率将 不同,曲线的转折点对应温度就是某些相开始出现或完全小时
f=变数-条件数=
精品文档
p(c-1)+1- c(p-1)=c-p+1
2
第一节 相图知识
一、相律
二元相图:当存在两个组元时,成分也是变量,但一种组元的含 量为独立,另一组元则为余下部分。为在二维平面上表示, 通常只考虑在常压下,取两个变量温度和成分。横座标用线 段表示成分,纵座标表示温度。平面上以按这时平衡状态下 存在的相来分隔。(如图)
典型相图分析
➢相图知识 ➢二元匀晶相图与固溶体的凝固
➢二元共晶相图
➢二元包晶相图
➢复杂二元相图的分析方法
➢三元相图
精品文档
1
一、相律 第一节 相图知识
对于恒压条件:f = c – p + 1
系统中有p相,c个组元,则成分引起的变数p(c-1)个。系 统总的变数为p(c-1)+1
在多相平衡时,任一组元在各相间的化学位相等, 每个组 元可写出个p-1等式,平衡条件总数为c(p-1)
关系,同时生长过程要求的动态过冷度也有差异,往往有一个
相在生长中起主导作用,决定了两相的分布,共晶体的形态也
具有独特性,这时常见的形态有针状、骨肋状、蜘蛛网状、螺
旋状等。
精品文档
23
第三节 二元共晶相图
二、共晶体的形成
精品文档
24
第三节 二元共晶相图
二、共晶体的形成
精品文档
25
第三节 二元共晶相图
精品文档
17
第二节 二元匀晶相图与固溶体的凝固
六、成分过冷
成分过冷对凝固过程的影响
• 中区域的成分过冷可能生成胞 状到树枝晶的各种过渡组织。
• 成分过冷区较大,凸起发展较 长,在凸起上再生新的凸起, 就可生成树枝晶。
• 如果成分过冷区域特别大,得到的成分过冷度也十分大,若
达到形核要求的过冷度时,在成分过冷区可能形成新的晶核,
如图所示相图的一部分,在温度t时,平衡 的液—固相成分的比,称为平衡分配系数。
k0 CS /CL
实际凝固时原子的迁移需要一过程,液体 和固体的成分达不到相图所示的平衡状态, 这时分析采用“有效分配系数”,它定义为:
ke 凝边固界时层固以-外液的界 相 液 浓 面 的 体 度 (处 C 浓 平 L(C )固 B度 S)均 i
新晶核的生长阻碍原晶粒生长,对柱状晶的发展产生隔断作
用。
精品文档
18
第三节 二元共晶相图
一、相图形式
两组元在液态下无限互溶,固态下有限溶解,一组元溶入 另一组元中时都使凝固温度下降,并发生共晶转变。如Pb—Sn、 Ag—Cu等形成二元合金对应的相图就是二元匀晶相图。
相图的构成:tAE和tBE为两液相线, 与其对应的tAC和tBD为两固相线; CG和DH固溶体α、β的溶解度随温 度变化线;CED为水平共晶线。将 相图分成三个单相区 L、α、β; 三个双相区L+α、L+β、α+β 和 一个三相区L+α+β,即CED 为共晶线。
精品文档
22
第三节 二元共晶相图
二、共晶体的形成
组织特点
当两个固相都是金属性较 强相时,共晶体一般生长成层 片状。当两相的相对数量比相 差悬殊时,在界面能的作用下, 数量较小的相将收缩为条、棒 状,更少时为纤维状,甚至为 点(球)状。
当有一相或两相都具有较强的非金属性时,它们表现出较
强的各向异性,不同方向的生长速度不同,并且有特定的角度
在TE温度以下仅是固体的冷却
精品文档
20
