西南大学2005级有机化学(下)A卷答案
1095《有机化学(二)》西南大学网教19秋作业答案
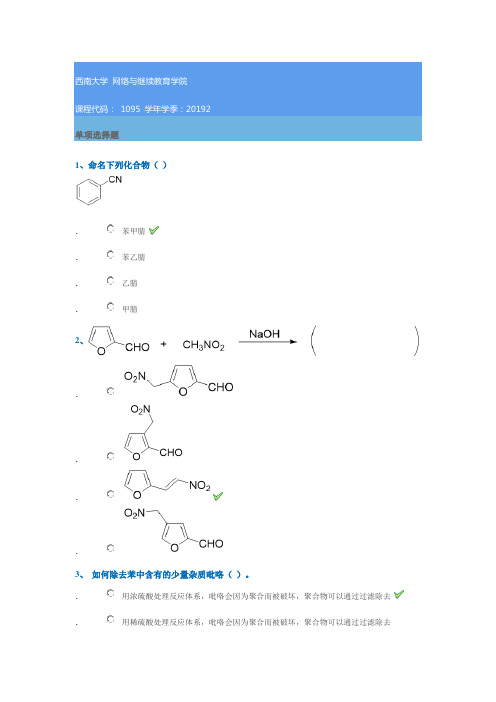
1095 20192单项选择题1、命名下列化合物( ).苯甲腈. 苯乙腈. 乙腈 .甲腈2、....3、 如何除去苯中含有的少量杂质吡咯( )。
. 用浓硫酸处理反应体系,吡咯会因为聚合而被破坏,聚合物可以通过过滤除去.用稀硫酸处理反应体系,吡咯会因为聚合而被破坏,聚合物可以通过过滤除去.用浓硫酸处理反应体系,吡咯很容易与浓硫酸发生磺化反应而溶解在浓硫酸中,从苯中分离出去。
.用稀硫酸处理反应体系,吡咯很容易与稀硫酸发生磺化反应而溶解在稀硫酸中,从苯中分离出去。
4、........5、()是最常用的淀粉鉴定试剂。
.茚三酮.2,4-二硝基氟苯.碘.异硫氰酸苯酯6、命名下列化合物().戊二酸酐.反丁烯二酸酐.丁二酸酐.顺丁烯二酸酐7、下列化合物中,碱性最强的是()。
....8、下列化合物中,()可以用作化学合成染料。
....9、蛋白质的基本组成单位是()。
.氨基酸.脱氧核糖核酸.核糖核酸.葡萄糖10、()是一切糖类甜味剂中甜味最大的单糖。
.D-木糖.D -半乳糖.D-果糖.D-葡萄糖11、....12、....13、....14、下列化合物中,()不能与水形成氢键。
.甲胺.二甲胺.甲烷.三甲胺15、....16、命名下列化合物().2-甲基呋喃.1-甲基四氢呋喃.2-甲基四氢呋喃.1-甲基呋喃17、... .18、写出对氨基苯乙酮的结构( )....19、....20、....21、....22、( )和亚硝酸或亚硝酸盐及过量的酸在低温下反应可生成芳香重氮盐 。
. 芳香铵盐 . 芳香三级胺. 芳香一级胺.芳香二级胺23、为何酰胺熔沸点比分子量相近的酯高( )。
. 范德华力 . A and B. 分子间氢键作用 .分子间静电作用24、下列氨基酸中,( )不属于必需氨基酸。
. 蛋氨酸 . 异亮氨酸. 精氨酸.赖氨酸25、两个或两个以上的异戊二烯分子以头尾相连的方式结合起来的化合物称为______。
.生物碱.甾体化合物.萜类化合物.蛋白质26、....27、....28、下列基团中____不能用来保护羟基. THP (四氢吡喃基). 对甲氧基苄氧基甲基p -MeOC6H4CH2OCH2―简写为PMBM. 硅保护基,例如三乙基硅基(TES ) .苄基29、下列反应中,( )不属于周环反应。
有机化学第五版下册课后答案

第十二章羧酸P32-331.命名下列化合物或写出结构式:1 3-甲基丁酸2 3-对氯苯基丁酸3 间苯二甲酸4 9,12-十八碳二烯酸5 4-甲基己酸 CH3CH2CHCH3CH2CH2COOH6 2-羟基丁二酸 HOOCCHOHCH2COOH7 2-氯-4-甲基苯甲酸8 3,3,5-三甲基辛酸2.试以反应式表示乙酸与下列试剂的反应3.区别下列各组化合物:4.指出下列反应的主要产物:第四版保留4.完成下列转变:5、怎样由丁酸制备下列化合物6、解:7、指出下列反应中的酸和碱;按lewis酸碱理论:凡可接受电子对的分子、离子或基团称为酸,凡可给予电子对的分子、离子或基团成为碱;8.1按酸性降低的次序排列下列化合物:①酸性: 水>乙炔>氨;②酸性: 乙酸>环戊二烯>乙醇>乙炔2按碱性降低的次序排列下列离子:①碱性:CH3HC C CH3O>>②碱性:(CH3)3CO>(CH3)2CHO>CH3O9. 解:化合物A有一个不饱和度,而其氧化产物B含有两个不饱和度;产物DC5H 10有一个不饱和度;从题意可知:D的结构式可能为环戊烷;C的结构为环戊酮;B的结构为己二酸;A的结构式为环己醇;10.解:1由题意:该烃氧化成酸后,碳原子数不变,故为环烯烃,通式为CnH2n-2;2该烃有旋光性,氧化后成二元酸,所以分子量=662=132;故二元酸为CH3CHCH2COOHCOOH11.由题意:m/e=179,所以马尿酸的分子量为179,它易水解得化合物D和E,D 的IR 谱图:3200-2300cm-1为羟基中O-H键的伸缩振动;1680为共扼羧酸的>C=O的伸缩振动;1600-1500cm-1是由二聚体的O-H键的面内弯曲振动和C-O 键的伸缩振动之间偶合产生的两个吸收带;750cm -1和700cm-1是一取代苯的 C-H键的面外弯曲振动;再由化学性质知D为羟酸,其中和当量为121±1,故D的分子量为122,因此,又由题意:E为氨基酸,分子量为75,所以E的结构为H 2NCH2COOH;第十三章羧酸衍生物P77-781.说明下列名词:酯、油脂、皂化值、干性油、碘值、非离子型洗涤剂;酯:是羧酸分子和醇分子间脱水形成的产物;油脂:是高级脂肪酸的甘油醇酯;皂化值:是指完全皂化1克油脂所需的KOH的质量以mg为单位;干性油:是指那些在空气中放置后能逐渐变成有韧性的固态薄膜的油;碘值:是指100克油脂完全加成时所能吸收的碘的质量以克为单位;非离子型洗涤剂:此处实指非离子型表面活性剂,即在水溶液中不离解出正负离子的表面活性剂此处的非离子型表面活性剂起主要的洗涤去污作用;2.试用方程式表示下列化合物的合成路线:(1)由氯丙烷合成丁酰胺;2 由丁酰胺合成丙胺3 由邻氯苯酚、光气、甲胺合成农药“害扑威”或先醇解后氨解也可;3.用简单的反应来区别下列各组化合物:解:前一化合物与水几乎不反应,而后一化合物因水解而冒烟;2 丙酸乙酯与丙酰胺解:分别与氢氧化钠水溶液作用,并加热,有氨气放出使红色石蕊试纸变蓝色者为丙酰胺,否则为丙酸乙酯;3 CH3COOC2H5和 CH3CH2COCl解:前一化合物与水不反应,而后一化合物因水解而冒烟;4 CH3COONH4和CH3CONH2解:在常温下与氢氧化钠水溶液作用,有氨气放出使红色石蕊试纸变蓝色者为乙酸铵,否则为乙酰胺;注:此试验不需加热,否则乙酰胺因水解也有氨气放出;5 CH3CO2O 和 CH3COOC2H5解:用适量热水试之,乙酸酐因水解而溶解于水,乙酸乙酯因难以水解而不溶于水; 或用碱性水溶液彻底水解,再将水解液进行碘仿反应,呈阳性者为乙酸乙酯,呈阴性者为乙酸酐;4.由合成解:5.由丙酮合成 CH33CCOOH解:种用酮的双分子还原,片呐醇重排反应和碘仿反应进行合成;6.由五个碳原子以下的化合物合成:解:顺式烯烃,最常用的合成方法是炔烃的顺式还原,用Lindlar催化剂最好;7.由ω-十一烯酸CH2=CHCH28COOH合成H5C2OOCCH213COOC2H5;解:目标产物比原料增加了碳原子,为此必须选用合适的增长碳链方向;8、由己二酸合成解:从6个碳缩成为5个碳,正好是一个α位碳进攻酯基碳的结果,宜用酯缩合反应;目标分子中的乙基酮的α位,可以用卤代烃引入;9.由丙二酸二乙酯合成解:分析乙酸单元后可见,目标产物只需在丙二酸分子中引入亚乙基即可;合成路线如下10.由合成解:或11.由合成解:硝酸具有氧化性,易将酚类氧化,需先进行“保护”;12、由合成解:目标产物是在原甲基的邻位再导入烃基,显然要用上苯环上的烷基化反应或酰基化反应,即以Freidel-Crafts反应为主;13.由合成解:14.由苯合成解:15.某化合物A的熔点为85°C,MS分子离子峰在480m/e,A不含卤素、氮和硫;A的IR在1600cm-1以上只有3000~2900cm-1和1735cm-1°C,B和C的NMR证明它们都是直链化合物;B用铬酸氧化得到一个中和当量为242的羧酸,求A和B的结构; 解:1 MS分子离子峰在480m/e,说明化合物分子量为480;2 题目已知醇为直链醇,酸为直链酸;3 A能皂化,说明A为羧酸酯;4 B氧化后所得羧酸的分子量为242,则其式量符号下式关系:C n H2n+1COOH = 242,解得: n = 14所以B为: CH3CH214OH ,式量为228;5 C的分子量为480-227+17 = 270,则C的式量应符合:C n H2n+1COOH = 270,解得: n = 16所以C为: CH3CH215COOH ;综合起来,化合物A的结构为: CH3CH215COOCH214CH31735处为C=O伸缩振动吸收,3000~2900处为饱各C—H键伸缩振动吸收;注:此题有误,中和当量为242的羧酸改为中和当量为256A C15H31COOC16H33 B的结构为C16H33OH第十四章含氮有机化合物P125-1291.给出下列化合物的名称或写出结构式:1对硝基氯化苄21,4,6-三硝基萘 3苦味酸4 6 3-氨基戊烷72-氨基丙烷或异丙胺8二甲基乙基胺或N,N-二甲基乙胺9N-乙基苯胺10顺-4-甲基环己胺 11N-甲基间甲苯胺122,4-二羟基偶氮对硝基苯或对硝基偶氮-2,4-二羟基苯133-氰基-5-硝基氯化重氮苯2.按其碱性的强弱排列下列各组化合物,并说明理由:1 吸电子基使碱性降低,供电子基使碱性增强,所以有:2 吸电子基使碱性降低,供电子基使碱性增强,所以有:2.比较正丙醇、正丙胺、甲乙胺、三甲胺和正丁烷的沸点高低并说明理由:解:五种化合物中,按形成氢键的可能、能力可推知其沸点从高到低的次序是:正丙醇 > 正丙胺 > 甲乙胺 > 三甲胺 > 正丁烷4.如何完成下列转变:12345.完成下列反应,并指出最后产物的构型是R或S:解:反应的前两步都不涉及到手性碳,反应的第三步为Hofmann重排,转移基团在分子内转移,其构型保持不变;由于分子组成而变了,旋光性可能改变,也可能不变,此处测定结果为左旋;6.完成下列反应:1该题如果改换一下甲基的位置,则情况不同,如下:234或5利用Hofmann重排反应降级反应来完成缩碳:6利用卤代烃的氰解来增加一个碳原子:78芳环上的亲核取代反应,先加成后消去:9不对称酮形成烯胺后,再进行烃基化时,烃基化主要发生在取代基较少的α位;与普通碱催化反应正好相反;NOH:10含β-H的氧化叔胺在加热时发生顺式消除反应协同反应生成烯烃和R27.指出下列重排反应的产物:1碳正离子的形成及其重排:2碳正离子的形成及其重排:3碳正离子的形成及其重排:片呐醇重排反应:4碳正离子的形成及其重排:片呐醇重排反应:5碳正离子的形成及其重排:片呐醇重排反应:6Wolff重排:7Beckmann重排:8Baeyer-Villiger重排:8.解释下述实验现象:1对溴甲苯与NaOH在高温下反应,生成几乎等量的对和间甲苯酚;22,4-二硝基氯苯可以由氯苯硝化得到,但如果反应产物用NaHCO3水溶液洗涤除酸,则得不到产品;解:1溴苯一般不易发生亲核取代反应,该反应是经过苯炔中间体历程进行的,表示如下:解:2氯苯可以直接硝化生成2,4-二硝基氯苯,但2,4-二硝基氯苯因两个硝基的吸电子作用,使其很易水解,生成2,4-二硝基苯酚,所以得不到2,4-二硝基氯苯的产物;9.请判断下述霍夫曼重排反应能否实现,为什么原第四版解:该反应不能实现,因为仲胺分子中N原子上没有两个可被消去的基团,无法形成氮烯中间体.9. 完成下列反应的反应历程;3解:本题为Hofmann重排类型的题目;只是反应体系发生了变化,NaOH水溶液改变了CH3ONa的甲醇溶液,所以最后形成的是较稳定的氨基甲酸甲酯,,而不是易分解的氨基甲酸;10.从指定原料合成:1从环戊酮和HCN制备环己酮;2从1,3-丁二烯合成尼龙-66的两个单体-己二酸和己二胺;3由乙醇、甲苯及其他无机试剂合成普鲁卡因4由简单的开链化合物合成(1)解:2解:3解:4解:11.选择适当的原料经偶联反应合成:12,2′-二甲基-4-硝基-4′-氨基偶氮苯第四版第五版: 2,2′-二甲基-4′-氨基偶氮苯2解:12.从甲苯或苯开始合成下列化合物:1间氨基苯乙酮2邻硝基苯胺3间硝基苯甲酸41,2,3-三溴苯5613.试分离下列各组化合物1PhNH2、PhNHCH3和PhNCH32的混合物:214.试剂丙胺甲基乙基胺三甲胺1对甲基苯环磺酰氯生成白色固体生成白色固体不反应15.892C,C用HNO 2处理,再与H 3PO 2反应生成3,3-二乙基联苯D;试写出A 、B 、C 和D 的结构式; 解:16.某化合物A,分子式为C 8H 17N,其核磁共振谱无双重峰,它与2mol 碘甲烷反应,然后与Ag 2O 湿作用,接着加热,则生成一个中间体B,其分子式为C 10H 21N;B 进一步甲基化后与湿的Ag 2O 作用,转变为氢氧化物,加热则生成三甲胺、1,5-辛二烯和1,4-辛二烯混合物;写出A 和B 的结构式;解:能与两摩尔碘甲烷反应,说明为一个仲胺;根据产物烯的位置可推知: NMR 无双重峰,说明其旁没有单个H;这句话排除了如下结构式的可能:16.化合物A 分子式为C 15H 17N,用苯磺酰氯和KOH 溶液处它没有作用,酸化该化合物得到一清晰的溶液,化合物A 的核磁共振谱如下图所示,试推导出化合物A 的结构式; 解:化合物分子式为,C 15H 17N,不饱和度为8,分子中可能含2个苯环;结合NMR 谱图可得:18.请用概念图或思维导图的形式总结芳香烃衍生物的合成方法;第十五章 含硫和含磷有机化合物 P 163-1651.写出下列化合物的结构式:(1) 硫酸二乙酯 2甲磺酰氯 3对硝基苯磺酸甲酯 4磷酸三苯酯 5对氨基苯磺酰胺 62,2’-二氯代乙硫醚 7二苯砜 8环丁砜 9苯基亚膦酸乙酯 10苯基亚膦酰氯 119-BBN 9-硼双环3,3,1-壬烷 9-BBN 2.命名下列化物:2-羟基乙硫醇 巯基乙酸 对磺酸基苯甲酸 对甲苯磺酸甲酯 羟甲基乙基硫醚或乙硫基甲醇 碘化二甲基环己基锍 氯化四羟甲基鏻 N -甲基-对甲苯磺酰胺 苯基膦酸二乙酯或O,O -二乙基苯膦酸酯 甲基乙基亚膦酰氯 11C 6H 53SiOH 12 CH 33O-SiCH 33三苯基硅醇三甲基叔丁氧基硅烷3.用化学方法区别下列化合物:1234解:1乙硫醇能溶于稀的氢氧化钠溶液中,而二甲硫醚不溶;2分别加入碳酸钠溶液,有二氧化碳气体逸出的为乙磺酸,无则为甲磺酸甲酯;3硫醇可溶于稀的氢氧化钠溶液中,而醇不溶;4前者不易水解,后者更易水解,后者不潮湿的空气中会水解冒烟;4.试写出下列反应的主要产物:解:1 23 4 55.完成下列转化:123456786.使用有机硫试剂或有机磷试剂,以及其他有关试剂,完成下列合成:123解:123第十七章周环反应1.推测下列合物电环化时产物的结构:2.推测下列环加成反应的产物的结构:3.马来酸酐和环庚三烯反应,给出的产物如下;试说明这个产物的合理性;环庚三烯的π电子是4n+2体系,加热是进行对旋电环化,然后再与马来酸酐进行4+2环加成反应,由于环状二烯的LUMO相互作用,可产生对称性允许的次级效应,有利于形成内型过渡态,最后生成内型产物;4.指出下列反应过程所需条件:5.试说明下列反应从反应物到产物的过程:该反应是反应经过两次碳的1,5同面迁移,且C构型保持;6.自选材料通过环加成反应合成下列化合物;7.自选材料通过环加成反应合成下列化合物;8.下面的反应按光化学进行时,反应产物可得到哪一种I或II解:1反应物π电子数属4n体系,光照下对旋是允许的,产物是I;2反应物中起电环化反应的π电子数属4n+2体系,光照下顺旋是允许的;产物是II;9.通过怎样的过程和条件,下列反应能得到给出的结果;10.通过什么办法反-9,10-二氢萘转化为顺-9,10-二氢萘11.确定下列反应在加热反应时所涉及的电子数;6个π电子电环化反应4个π电子电环化反应4+2环加成反应4+2环加成反应12.解释下列现象:1 在狄尔斯-阿尔德反应时,2-叔丁基-1,3-丁二烯反应速率比1,3-丁二烯快;2 在-78℃时,下面反应b的反应速率比a快1022倍;3解:1在狄尔斯-阿尔德反应中,双烯体是用其HOMO轨道提供电子的,属亲核部分,双烯体上有供电子叔丁基的存在时,使反应速率加快;2 a2+2环加成反应的逆反应,b 4+2环加成反应的逆反应,温度有利于4+2反应,光照有利于2+2环加成反应;3化合物是一个π-π共轭体系,本身有一定的稳定性,但它不是芳香环,而甲苯是一个芳香环,,从非芳香环重排成芳香环因芳香体系的形成将放出大量的热量;第十八章杂环化合物P2321.命名下列化合物:2.为什么呋喃能与顺丁烯二酸酐进行双烯合成,而噻吩及吡咯则不能试解释之;解:五元杂环的芳香性比较是:苯>噻吩>吡咯>呋喃;由于杂原子的电负性不同,呋喃分子中氧原子的电负性较大,π电子共轭减弱,而显现出共轭二烯的性质,易发生双烯合成反应,而噻吩和吡咯中由于硫和氮原子的电负性较小分别为和3,芳香性较强,是闭合共轭体系,难显现共轭二烯的性质,不能发生双烯合成反应;3.为什么呋喃、噻吩及吡咯容易进行亲电取代反应,试解释之;解:呋喃、噻吩和吡咯的环状结构,是闭合共轭体系,同时在杂原子的P轨道上有一对电子参加共轭,属富电子芳环,使整个环的π电子密度比苯大,因此,它们比苯容易进行亲电取代反应;4.吡咯可发生一系列与苯酚相似的反应,例如可与重氮盐偶合,试写出反应式;5、比较吡咯与吡啶两种杂环;从酸碱性、环对氧化剂的稳定性、取代反应及受酸聚合性等角度加以讨论;解:吡咯与吡啶性质有所不同,与环上电荷密度差异有关;它们与苯的相对密度比较如下:6、写出斯克劳普合成喹啉的反应;如要合成6-甲氧基喹啉,需用哪些原料4-甲氧基苯胺、甘油、浓硫酸、硝基苯7、写出下列反应的主要产物:8、解决下列问题:1 区别吡啶和喹啉;2 除去混在苯中的少量噻吩;3 除去混在甲苯中的少量吡啶;4 除去混在吡啶中的六氢吡啶;解:1吡啶溶于水,喹啉在水中的溶解度很小这是由于多了一个疏水性苯基的结果;2噻吩溶于浓H2SO4,苯不溶;用分液漏斗振荡后分液;3吡啶溶于水,甲苯不溶;4苯磺酰氯与六氢吡啶生成酰胺,蒸出吡啶;或根据六氢吡啶的碱性比吡啶的碱性强得多,将混合物先溶于乙醚等有机溶剂,再向溶液中加入适量的酸,将六氢吡啶和酸生成的盐沉淀出来;9、合成下列化合物:解:1210.杂环化合物C5H4O2经氧化后生成羧酸C5H4O3,把此羧酸的钠盐与碱石灰作用,转变为C 4H4O,后者与钠不起反应,也不具有醛和酮的性质,原来的C5H4O2是什么11. 写出下列Friedlnder反应机理;Friedl nder合成Friedl nder synthesis,又称Friedl nder喹啉合成或和任何含有-CH2CO-的或生成;反应以德国化学家 Paul Friedl nder 1857-1923 的名字命名;反应可用、、或其他;反应机理如下:反应有两种可行的机理;一是邻氨基苯甲醛或酮 1与羰基化合物 2发生生成 3,然后水生成4并再次失水化,得喹啉 7;另一种是 1 先与 2 缩合成,然后再发生分子内羟醛并失水,生成 7;注:R1:-H,R2:-CH3 R3:-COOC2H512.用浓硫酸将喹啉在220~230°C时磺化,得喹啉磺酸A,把A与碱共熔,得喹啉的羟基衍生物B;B与应用斯克劳普法从邻氨基苯酚制得的喹啉衍生物完全相同,A和B是什么磺化时苯环活泼还是吡啶环活泼解:磺化时苯环比吡啶环更活泼;A、B的结构如下:13.α、β-吡啶二甲酸脱羧生成β-吡啶甲酸烟酸,为什么脱羧在α-位解:脱羧是以偶离子的形式进行的,可表示如下:脱羧时涉及到碳-碳键的异裂,吡啶环持有负电荷;碳-碳键断裂时联想一下该决定速率步骤的过渡态,负电荷处在α-位能被电负性大的氮所分散,负电荷处在β-位则不能被有效的分散;因此,脱羧发生在α-位;14.毒品有哪几类,它的危害是什么解:一种类1.兴奋剂如:肾上腺素、安非他明、甲基安非他明、3,4-亚甲二氧基-N-甲基-1-苯基丙胺、咖啡因、尼古丁、柯卡因2.幻觉剂:麦角二乙酰胺、大麻3.抑制剂:巴比土酸盐、阿普唑仑、维利眠、鸦片制剂海洛因、可待因、吗啡二危害:略;第十八章糖类化合物p257-2581. 解释概念1还原糖p232:凡能被托伦试剂或菲林试剂等若氧化剂氧化的糖类,都称为还原糖; 2非还原性糖p232:凡不能被托伦试剂或菲林试剂等若氧化剂氧化的糖类,都称为非还原糖;3醛糖的递升和递降p236:醛糖经与HCN发生亲核加成增加一个碳原子后,再经水解,还原可生成多一个碳原子的醛糖,这个方法称为递升;反之去掉一个碳原子而生成低一级的糖的过程称为递降;4糖的变旋现象p240:在水溶液中糖的比旋光度发生变化的现象,称为变旋现象;5糖苷p240:糖的半缩醛羟基苷羟基与另一羟基化合物失水而生成的缩醛均称为“配糖物”简称为“苷”2.写出D-+-甘露糖与下列化合物的反应、产物及其名称:解:D-+-甘露糖在溶液中存在开链式与氧环式α型和β型的平衡体系,与下列 物质反应时有的可用开链式表示,有的必须用环氧式表示,在用环氧式表示时,为简单起见,仅写α-型;3. D-+-半乳糖怎样转化成下列化合物的 写出其反应式;4.果糖是酮糖,为什么也可像醛糖一样和托伦试剂或斐林试剂反应,可是又不与溴水反应 解:在碱性条件下,果糖可是通过差向异构化转化为醛糖葡萄糖和甘露糖,与托伦试剂或斐林试剂反应;在酸性条件下,不能发生异构化,转化为醛糖,所以不能与溴水反应; 5. 解 推导过程:1 戊糖与胲反应生成肟,说明有羰基存在;2 戊糖与4NaBH 反应生成C 5H 12O 4说明是一个手性分子;3C 5H 12O 4与乙酐反应得四乙酸酯说明是四元醇有一个碳原子上不连有羟基;4C 5H 12O 4与CH 3OH 、HCl 反应得糖苷C 6H 12O 4,说明有一个半缩醛羟基与之反应;糖苷被HIO4氧化得C 5H 10O 4,碳数不变,只氧化断链,说明糖苷中只有两个相邻的羟基,为环状化合物,水解得和,说明甲基在分子末端,氧环式是呋喃型;递推反应如下:C 5H 10O 4可能的结构式为:6.解:推导过程:1蜜二糖是还原性双糖,说明它有游离的半缩醛羟基;2蜜二糖是+-乳糖的异构物,能被麦芽糖酶水解,说明它是由半乳糖和葡萄糖以α-苷键结合的双糖;37.解:1糖水杨苷用苦杏仁酶水解得D-葡萄糖和水杨醇,说明葡萄糖以β-苷键与水杨醇结合;(CH)SO和NaOH处理得五甲基水杨苷,说明糖水杨苷有五个羟基,产物2水杨苷用324酸化水解得2,3,4,6-四甲基-D-葡萄糖和邻甲氧基甲酚邻羟基苄甲醚,说明葡萄糖以吡喃式存在并以苷羟基与水杨醇的酚羟基结合;此糖水杨苷的结构如下:8.推导过程:1茜根酸不与拖伦试剂反应,说明无游离半缩醛羟基存在;可见茜根酸的结构未肯定之处在于:1D-木糖和葡萄糖的构型α,β型;2樱草糖是否是还原糖,因此,樱草糖出现两种结构式;9.解:可见,I是D-型还原性单糖,不成脎说明α-位上无羟基,I经氧化,甲基化,酸的α-溴代,水解生成四羟基正戊酸说明了此点,I经Ruff降解得内消旋的酒石酸,证明3,4-位上羟基同侧,由题意,可推出II~VII的结构10.解:成脎反应发生在C1和C2上,这三种糖都能生成同一种脎D-葡萄糖脎,则可证明它们的C3,C4,C5具有相同的构型:11.解:推导过程:A的可能结构如下:B的可能结构如下:。
西南大学2022年有机化学考试及答案

解释"场效应"1.是由于取代基的大小和形状引起分子中特殊的张力或阻力的一种效应。
2.由于原子或集团电负性的影响沿着分子中键传导,引起分子中电子云按一定方向转移或键的极性通过键链依次诱导传递的效应。
3.分子中原子之间相互影响的电子效应,不是通过键链而是通过空间传递的效应4.分子中原子或原子团相互联接的方式和次序。
2、解释"空间效应"1.由于原子或集团电负性的影响沿着分子中键传导,引起分子中电子云按一定方向转移或键的极性通过键链依次诱导传递的效应。
2.是由于取代基的大小和形状引起分子中特殊的张力或阻力的一种效应。
3.分子中原子之间相互影响的电子效应,不是通过键链而是通过空间传递的的效应。
4.分子中原子或原子团相互连接的方式和次序。
3、解释"诱导效应":1.是由于取代基的大小和形状引起分子中特殊的张力或阻力的一种效应。
2.分子中原子或原子团相互连接的方式和次序。
3.在分子构造、构型确定的基础上因为单键的旋转而产生的分子中原子或原子团在空间的排列。
4.由于原子或集团电负性的影响沿着分子中键传导,引起分子中电子云按一定方向转移或键的极性通过键链依次诱导传递的效应。
判断题4、C=C不能发生亲核加成1. A.√2. B.×5、烯烃的硼氢化反应得到反Markovnikov(马氏)规则的产物。
1. A.√2. B.×6、在烯烃与卤化氢的加成反应中,卤化氢的活性顺序为:HI > HBr > HCl。
1. A.√2. B.×7、自由基是一类含有一个或多个未配对电子的中性物种1. A.√2. B.×8、典型的E2反应,新键的生成和旧键的断裂是协同进行的1. A.√2. B.×9、内消旋体是混合物1. A.√2. B.×10、亲电试剂是提供电子的反应物。
1. A.√2. B.×11、“邻基参与”是在亲核取代反应中,取代基能够与反应中心形成过渡态或中间体,从而影响反应的进行。
西南大学网络学院高等有机化学答案已整理

请简述根据反应中键断裂及其形成方式不同的 反应分类及其特点
[论述题] 参考答案:
有机反应的数目和范围十分庞大,根据反应中键的断裂及形成方式可将 有机反应分为:自由基反应、离子反应和分子反应。 任何反应都有键的断裂和/或键的形成,若化学键断裂的方式是每个碎片 各有一个电子,则形成自由基(或称游离基),称之为均裂。自由基性 质非常活泼,能继续引起一系列反应。自由基反应一般在光、热或引发 剂的作用下进行。 若化学键断裂的方式是一个碎片上有两个电子,另一碎片上没有电子, 称之为异裂。有机化合物由碳-碳键异裂可产生碳正离子、碳负离子。 碳正离子、碳负离子都是有机反应过程中产生的活泼中间体,其化学性 质非常活泼,往往在生成的瞬间就参加反应。由共价键异裂产生离子而 进行的反应称为离子型反应。离子型反应一般在酸或极性物质催化下进 行。 近几十年来,人们在有机反应中又发现某些反应,不受溶剂极性的影 响,不被酸或碱所催化,亦不受引发剂的影响。反应时共价键的断裂和 生成是经过多中心环状过渡态协同地进行。这类反应属于分子反应,又 称为周环反应或称协同反应。
5 [论述题] 请区别试剂的“碱性”和“亲核性”。 参考答案: 1.亲核试剂的性能
在亲核取代反应中,亲核试剂的作用是提供一对电子与RX的中心碳 原子成 键,若试剂给电子的能力强,则成键快,亲核性就强。亲核试 剂的强弱和浓 度的大小对SN1反应无明显的影响。亲核试剂的浓度愈 大,亲核能力愈强,有 利于SN2反应的进行。试剂的亲核性与下列因 素有关: 1)试剂所带电荷的性质 带负电荷的亲核试剂比呈中性的试剂的亲核能力强。 例如,OH - > H2O;RO- > ROH等。 2)试剂的碱性 试剂的碱性(与质子结合的能力)愈强, 亲核性(与碳原子结合的能力)也愈强。 例如: C2H5O- > HO- > C6H5- > CH3COO3)试剂的可极化性 碱性相近的亲核试剂,其可极化性愈大,则亲核能力愈强。原子半径 大的原 子的可极化度大 例如:试剂OH -与SH –的可极化度是OH -< SH–, 则其亲核性是OH -< SH –。
21春西南大学[1095]《有机化学(二)》作业辅导资料
![21春西南大学[1095]《有机化学(二)》作业辅导资料](https://img.taocdn.com/s3/m/956e250d50e2524de4187e4d.png)
1095 20211单项选择题1、命名下列化合物()1.苯甲腈2.苯乙腈3.乙腈4.甲腈2、在合成多肽时,一些侧链的基团需要保护起来,特别是巯基,很容易发生氧化还原反应,一般是用______将1.二氢吡喃2.1,2-乙二醇3.Fmoc4.苯甲基3、选择保护基时须考虑()。
1.保护基在随后的反应和后处理中具有较高的容忍性2.A,B and C3.保护基的来源以及经济性4.保护基必须能很容易高产率地进行保护反应,也能被选择性和高效率地除去4、樟脑是一个二环系的()化合物。
1.甾族2.萜类3.糖类4.生物碱5、在多肽的合成中,羧基可以通过将其变成苄酯来进行保护,接肽完成后,由于酯比酰胺易于水解,苄酯可以1.温和酸性水解法2.强酸水解法3.催化氢解法4.稀碱水解法6、1.2.3.4.7、1.2.3.4.8、苯胺制对溴苯胺应在()介质中进行。
1.强碱2.弱酸3.强酸4.弱碱9、1.2.3.4.10、1.2.3.4.11、葡萄糖是典型的醛糖,可被()氧化。
1.溴水2.硝酸3.Fehling试剂4. A , B and C12、1. F.2.3.4.13、下列化合物中,()不能用于保护氨基。
1.氯代甲酸三级丁酯2.1,2-乙二醇3.氯代甲酸苯甲酯4.FmocCl14、1.2.3.4.15、1.2.3.4.16、下列化合物中,()是常见的羰基保护基。
1.1,2-乙二醇2.1,2-二硫醇3. A and B4.硅保护基17、下列方法中,()可以使糖的碳链增长。
1.佛尔递降法2.芦福递降法3.克利安尼氰化增碳法4.碳二亚胺法18、1.2.3.4.19、下列化合物中,()不能与水形成氢键。
1.甲胺2.二甲胺3.甲烷4.三甲胺20、1.2.3.4.21、下面四个β-二羰基化合物酸性最强的是()。
1.2.3.4.22、Edman方法中,用______和N端的氨基反应,生成苯氨基硫代甲酸衍生物。
1.茚三酮2.异硫氰酸苯酯3.2,4-二硝基氟苯4.碘23、下列氨基酸中,()属于碱性氨基酸。
18秋西南大学[1095]《有机化学(二)》作业答案
![18秋西南大学[1095]《有机化学(二)》作业答案](https://img.taocdn.com/s3/m/91ac225c336c1eb91a375dfb.png)
1、D-葡萄糖及______互为C-2差向异构体。
1. D-果糖2. D-木糖3. D-甘露糖4. D-半乳糖2、下列反应是通过()机理进行的。
1.消除-加成2.加成-消除3.加成4.消除3、1.2.3.4.4、如何除去苯中含有的少量杂质吡咯()。
1.用浓硫酸处理反应体系,吡咯会因为聚合而被破坏,聚合物可以通过过滤除去2.用稀硫酸处理反应体系,吡咯会因为聚合而被破坏,聚合物可以通过过滤除去3.用浓硫酸处理反应体系,吡咯很容易与浓硫酸发生磺化反应而溶解在浓硫酸中,从苯中分离出去。
4.用稀硫酸处理反应体系,吡咯很容易与稀硫酸发生磺化反应而溶解在稀硫酸中,从苯中分离出去。
5、下列描述中,()不属于环糊精的特点。
1.用环糊精作为柱色谱的填充剂,可将外消旋异构体分离成为醇的光活性异构体。
2.环糊精中含有二硫键。
3.环状糊精为圆筒形,圆筒中间有一空穴,其孔径与芳环尺度相近,可以与一些小分子化合物或离子形成分合物—包合化合物。
4.环状糊精的环状结构具有刚性,不易反应,因此在热的碱性水溶液中很稳定,在酸中慢慢水解,对α-淀粉β-淀粉酶有很大的阻抗性。
6、下列试剂中,()可用来制备苯炔。
1.苯甲酸2.间氨基苯甲酸3.对氨基苯甲酸4.邻氨基苯甲酸7、1. D.2.3.4.8、1.2.3. A、B、C都可以4.9、1.2.3.4. 10、1.2.3.4. 11、1.2.3.4.12、1.2.3.4.13、Fmoc保护的氨基常用________去保护。
1. DDQ氧化2.酸性条件3.氯化汞的甲醇溶液4.一些含氟离子的试剂或在温和条件下14、1.2.3.4.15、下列化合物中,()不属于糖类化合物。
1.纤维素2.淀粉3.环状糊精4.维生素A16、青霉素内含有()与β-内酰胺环系。
1.四氢咪唑2.咪唑3.四氢噻唑4.噻唑17、氨基酸自动分析仪可用来()。
1.分析N-端氨基酸单元2.分析C-端氨基酸单元3.测定氨基酸组成及其相对比例4.切断二硫键18、下列化合物中,水解反应活性最弱的是()。
西南大学(有机化学)
西南大学(有机化学)第一篇:西南大学(有机化学)西南大学(有机化学)单项选择题1、2、蛋白质的基本组成单位是()。
氨基酸脱氧核糖核酸核糖核酸葡萄糖3、E.、5、6、下列方法中,()可以使糖的碳链增长。
佛尔递降法芦福递降法克利安尼氰化增碳法碳二亚胺法7、请对下列分子进行合理的切断,并写出其合成子()8、9、写出对氨基苯乙酮的结构()10、胡萝卜素类化合物广泛地存在于植物和动物的脂肪内,属于___萜化合物。
二单三四11、下列氨基酸中,()不属于必需氨基酸。
蛋氨酸异亮氨酸精氨酸赖氨酸12、下列基团中____不能用来保护羟基THP(四氢吡喃基)对甲氧基苄氧基甲基p-MeOC6H4CH2OCH2―简写为PMBM硅保护基,例如三乙基硅基(TES)苄基13、下列反应中,(Aldol缩合反应)不属于周环反应。
14、判断题15、芳香胺的碱性比氨强。
A.√B.×16、乳糖用酸水解,得一分子D一半乳糖和一分子D一葡萄糖酸。
A.√B.×17、氨基酸的熔点很高,多数氨基酸受热分解而不熔融。
A.√B.×18、胺很容易氧化,特別是芳香胺,大多数氧化剂使胺氧化成焦油状的复杂物质,但是过氧化氢、过酸能使三级胺氧化为氧化胺。
A.√B.×19、羧酸比酰卤、混合酸酐或活泼酯都活泼,因为一X,一OR(R 中有吸电子基),一OCOOR,都是比一OH较好的离去基团。
A.√B.×20、Hinsberg反应可用于分离鉴别一级胺、二级胺和三级胺。
A.√B.×21、喹啉、异喹啉是三级胺,具有碱性。
A.√B.×22、Fehling试剂或Benedict试剂常与醛糖及酮糖反应产生氧化亚铜红色沉淀,这类糖称为还原糖。
A.√B.×23、氨具有棱锥形的结构,氮用sp3杂化轨道与三个氢的s轨道重叠,形成三个sp3-s σ键,成棱锥体。
A.√B.×24、A.√ B.×25、吡咯的α-C、β-C和N上均能发生质子化反应。
最新西南大学有机化学作业一答案
简单题(共8题)1.比较下列化合物的酸性并加以解释?乙炔甲烷环戊二烯乙烯参考答案:酸性:环戊二烯> 乙炔> 乙烯> 甲烷;环戊二烯负离子具有芳香性,后三者杂化状态不同。
2. 比较下列化合物的酸性并加以解释?甲醇乙醇异丙醇叔丁醇在水中和在气相参考答案:水溶液中酸性:(水)> 甲醇> 乙醇> 异丙醇> 叔丁醇;醇ROH的共轭碱RO-在水中的溶剂化效应越大酸性越强,甲基的存在阻碍溶剂化作用。
在气相:叔丁醇> 异丙醇> 乙醇> 甲醇;甲基在气相为吸电子基团,具有-I 效应。
3. 比较下列各组的碱性强弱,并从结构上予以解释。
参考答案:(1)苯胺中,N上孤电子与苯环p-π共轭,电子分散,接受质子能力降低,碱性变弱。
(2)OH是好的供电子基,NO2是强的吸电子基(3)苯胺中,N上孤电子与苯环p-π共轭,电子分散,接受质子能力降低,碱性变弱。
(4)吡咯中,N上的孤对电子与二烯共轭,形成芳香体系,因此接受质子的能力降低。
4. 比较下列各组羰基化合物的活性?①3,3-二甲基丁酮,1,1,1-三氯丙酮;②乙酸乙酯,乙酰氯;③环丁酮,环戊酮,3-戊酮参考答案:①②Cl3CCOCH3 > (CH3)3CCOCH3;③CH3COCl > CH3COOC2H5;④环丁酮> 环戊酮> 3-戊酮5. 试解释亲核加成反应中,ArCH2COR的反应活性为何比ArCOR高?参考答案:Ar直接与羰基-CO-相连时,羰基和芳环共轭使羰基碳的正电荷离域分散,使羰基碳正电性减少,活性降低。
在ArCH2COR中,Ar与羰基无共轭效应,只有吸电子诱导作用,增加羰基碳正电性。
故加速亲核加成反应进行。
6. 下列羰基化合物分别与亚硫酸氢钠溶液加成,哪一个反应速率最快?哪一个最慢?为什么?①CH3COCH2CH3②HCHO ③CH3CH2CHO参考答案:反应速率:② >③ > ①羰基化合物的亲核加成反应,其速率主要由空间效应决定。
有机化学A智慧树知到课后章节答案2023年下西南大学
有机化学A智慧树知到课后章节答案2023年下西南大学西南大学第一章测试1.有机分子中碳原子之间主要是通过共价键结合的。
()A:对 B:错答案:对2.共价键是指两个或多个原子通过共用电子对而产生的一种共价键。
()A:错 B:对答案:对3.在Lewis结构式中,两个原子间通常用一对电子表示共价单键,用两对电子表示双键,用三对电子表示叁键,孤对电子用黑点表示。
()A:对 B:错答案:对4.在Lewis结构式的书写中,可用一根短线或一对共用电子对表示一个共价键,要将所有的价电子(含孤对电子)都表示出来。
()A:对 B:错答案:对5.在Lewis结构式中,有机分子中形成共价键的一对电子分别属于成键的两个原子,孤对电子则只属于其中某一个原子,通过这种方式可以计算出分子中每一个原子周围的外层价电子总数,与其原子状态下的外层价电子总数相比,可以得出分子中各原子形成的形式电荷情况:若少了一个电子,则相当于失去了一个电子,就在该元素符号上加上一个正号,以表示该原子带了一个正电荷;若多了一个电子,则相当于得到了一个电子,就在该元素符号上加上一个负号,以表示该原子带了一个负电荷。
()A:错 B:对答案:对6.在Lewis结构式中,有机分子中原子的外层价电子一般不包括孤对电子。
()A:对 B:错答案:错7.凡是烷烃中的碳原子形成的四个σ键的键轴均指向正四面体的四个顶点,键角均为109˚28´。
()A:对 B:错答案:错8.烷烃中的碳原子是通过sp3杂化轨道形成4个σ键的,由于杂化轨道的对称轴均指向正四面体的四个顶点,因此烷烃中的碳原子形成的4个σ键均指向四面体的四个顶点,但如果与该碳原子成键的四个原子或原子团不完全相同时,键角不一定是109˚28´。
()A:对 B:错答案:对9.烯烃中双键上的碳原子是通过sp2杂化轨道形成σ键的,其杂化轨道的对称轴指向平面正三角形的三个顶点,彼此之间的夹角为120˚,因此双键上两个碳原子形成的5个σ键共面;双键两个碳原子上未参与杂化的p轨道彼此平行、侧面“肩并肩”重叠形成的1组π键电子云则对称分布于双键碳原子所形成的σ键所在平面的上方和下方。
西南大学考试答案生物化学
生物化学一、[判断题]1:水溶液或结晶状态下的氨基酸都以两性离子形式存在。
正确2:若双螺旋DNA中一条链的核苷酸排列顺序为pGpCpTpApTpC,那么,互补链的核苷酸顺序应为:pCpGpApTpApG. 错误3:酶是生物催化剂,只能在体内起催化作用。
错误4:DNA分子中的G和C的含量愈高,其熔点(Tm)值愈大。
正确5:核酸中的修饰成分大部分是在tRNA中发现的。
正确6:当[ES]复合物的量增加时,酶促反应速度也增加。
正确7:辅酶与酶蛋白的结合不紧密,可以用透析的方法除去。
正确8:呼吸链的全套酶都分布在线粒体的基质中。
错误9:机体缺少某种维生素会导致缺乏病,是因为缺乏维生素能使物质代谢发生障碍. 正确10:PPP途径能产生ATP,所以可以代替TCA途径,作为生物供能的主要途径。
错误11:氨基酸因含有不对称碳原子,所以都有旋光异构体。
错误12:构型的改变必须有旧的共价健的破坏和新的共价键的形成,而构象的改变则不发生此变化正确13:蛋白质生物合成所需的能量都由A TP直接供给。
错误14:RNA的合成和DNA的合成一样,在起始合成前亦需要有RNA引物参加。
误15:DNA半不连续复制是指复制时一条链的合成方向是5′→3′而另一条链方向是3′→5′。
错误15:脂肪酸合成酶催化的反应是脂肪酸-氧化反应的逆反应。
错误16:生物遗传信息的流向,只能由DNA―→RNA而不能由RNA―→DNA。
错误17:脂肪酸的从头合成需要NADPH+H+作为还原反应的供氢体。
正确二、名词解释:1. 构型:一个有机分子中各个原子特有的固定的空间排列。
这种排列不经过共价键的断裂和重新形成是不会改变的。
构型的改变往往使分子的光学活性发生变化。
2. 构象:指一个分子中,不改变共价键结构,仅单键周围的原子旋转所产生的原子的空间排布。
一种构象改变为另一种构象时,不要求共价键的断裂和重新形成。
构象改变不会改变分子的光学活性3. 结构域:结构域是生物大分子中具有特异结构和独立功能的区域,特别指蛋白质中这样的区域。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
西南大学课程考核
《 有机化学(下) 》课程试题 【A 】卷参考答案和评分标准
4、
5、
6、 (内型)(未画出立体结构或画成外型的扣一分)
三、合成题,无机试剂可任选(共4小题,第1小题6分,其余为8分/小题,共30分)
1、
(羰基保护后,也可利用格氏试剂法,与甲醛反应得伯醇,再氧化而得酸)
2、
O N N
OH
-
COOEt
COOEt
COOH
O
H
H O
O
O
O
OH
CH
3CH 2OH CH 3COOH H
+
CH 3COOC 2H 5
CH 3COCH 2COOC 2H 5
C H ONa/C H OH CH 3COOH,H 2O
CH 3COCH 2COOC 2H 5
CH
3COCHCOOC 2H 5
C 2H 5ONa/C 2H 5OH
C 2H 5
HOCH 2CH 2OH
Cl
H CH 3CCHCOOC 2H 5
C 2H 5
CH 3CH 2MgBr O
H 3O O
Br
O
O
COOH
OH OH
Cl
H Br
O
O
NaCN
O
H 3+
西南大学课程考核(试题【A】卷参考答案和评分标准)
——————————————
密————————————
封————————————
线——————————————3、
4、
O
Br
NaOH,H
2
O
OH
3
V
2
O
5
HOOC(CH
2
)
4
COOH
O
O
C H Br
,
O
O
C H Br,C H OH,
N
C
6
H
6
,H
2
O,
HOOC(CH
2
)
4
COOH H
5
C
2
OOC(CH
2
)
4
COOC
2
H
5
C H OH
H
C
2
H
5
ONa,C
2
H
5
OH
O
COOC
2
H
5
C
2
H
5
ONa,C
2
H
5
OH
C
2
H
5
Br
O
COOC
2
H
5
O
N
N
OH
N
OCC
6
H
5
O
CH
3
COCH HCHO
3
)
2
NH
(CH
3
)
2
CHMgBr
O
H
2
C H COCl
C
5
H
5
N
HCHO Cl
H CH
2
Cl COOH
《 有机化学(下) 》课程试题 【A 】卷参考答案和评分标准
四、完成下列反应式,注明产物的构型为R 或S ,并给出合理的反应机理(10分) 产物结构:
(2分)
产物构型为( S )型 (1分)
反应机理:伯酰胺的Hofmann 降解,过程如下:(7分)
( 其中,
)
五、应用题:(10分)
(
1)反应方程式 (各
2分,共4分)
①
② (2) 共4分
反应①是羟醛缩合(1分),甲醛提供醛基,乙醛提供α-H 。
(1分) 反应②是歧化反应(1分),三羟甲基乙醛是氧化剂,甲醛是还原剂。
(1分) (3)共2分
为了使反应向我们希望的方向进行,要防止乙醛发生自身缩合反应。
(1分) 因此,实验时,甲醛的总体用量要稍微过量一些;操作时,先把所有甲醛全部投入,
然后把乙醛和石灰乳同时慢慢滴入。
这是一个放热反应,所以在整个反应过程中还要注意控制反应温度和散热效果。
(1分,答出甲醛需过量即可给1分))
(HOCH 2)3CCHO (HOCH 2)4C HCHO OH-(HCOO)2
Ca
CH 3CHO (HOCH 2)3CCHO H
C 6
H 5
CH
3NHCOOC 2H 5H C 6H 5CH 3C R RCONH 2RCONH RCONHBr EtONa
N
O R N C O CH 3CH 2OH
RNHC O
OC 2H 5。
