苯乙酮制备 思考题
苯乙酮的制备研究

苯乙酮的制备研究苯乙酮,在有机化学中也称为酮类。
它是一种重要的中间体,广泛用于食品、化妆品和药物等领域。
苯乙酮的制备方法有许多种,其中比较常用的方法包括芳香族酰胺水解法、芳香族硫醇氧化法、苄基溴化为酮等。
芳香族酰胺水解法是苯乙酮的一种重要制备方法。
该方法的反应物是苯乙酰胺和水,在催化剂的促进下,苯乙酰胺与水发生水解反应,即生成苯乙酮和氨。
水解反应的方程式为:C6H5CONH2 + H2O => C6H5COCH3 + NH3。
催化剂通常是醋酸或硫酸,反应进行时需要保持适当的温度和pH值。
使用醋酸作为催化剂时,反应温度通常保持在80~100℃之间,反应溶液的pH值控制在3~4之间。
苯乙酸在水中较为容易溶解,所以水解反应可以在水相中进行。
反应完成后,将产物分离出来,并通过蒸馏和结晶等步骤进行纯化。
该反应通常在10%氢氧化钾和乙醇混合溶液中进行催化,反应温度保持在50℃左右。
苯乙酮和水可以形成混合溶液,通过蒸馏、结晶等步骤进行分离和纯化,得到高纯度的苯乙酮。
该反应需要在大量溴和催化剂存在的情况下进行,其中催化剂通常使用过渡金属催化剂如Pd、Pt等。
反应温度较高,通常在80~120℃之间。
反应后,通常需要进行萃取和纯化等步骤来提高产物的纯度。
以上几种制备苯乙酮的方法,各有优缺点。
芳香族酰胺水解法是简单易行、成本低,但产物纯度有限。
芳香族硫醇氧化法产物纯度高,但反应较为复杂。
苄基溴化为酮反应条件苛刻,但产物纯度较高。
选择何种方法制备苯乙酮,应根据具体需求和实验条件进行选择。
十,苯乙酮的制备

十、苯乙酮的制备一、实验目的1. 学习并掌握傅-克酰基化反应的基本原理。
2. 掌握无水操作及机械搅拌的使用方法二、反应式C OCH 33+ (CH 3CO)2+ CH 3COOH三、主要物料及其物理常数四、主要试剂用量及规格醋酸酐 7.5g(7ml ,0.072mol),无水苯 30ml(0.34mol),无水三氯化铝 20g. 浓盐酸,苯,5%氢氧化钠溶液,无水氯化钙。
五、操作步骤1. 安装带搅拌、滴液漏斗、回流、干燥及气体吸收的反应装置2. 加料:迅速称取20g 无水AlCl 3放入250ml 三口瓶中,再加入30ml 无水苯。
3. 自滴液漏斗慢慢滴加7ml 乙酸酐,边加边摇,约15min 加完。
沸水浴上回流20min ,直到无氯化氢气体放出。
4. 将反应物冷至室温,搅拌下加入100ml 配制好的1:1盐酸溶液。
5. 当固体溶解完后,分液,用10ml 苯萃取两次,合并有机层。
6. 依次用50ml 等体积的5%NaOH 和水洗涤有机层无水CaCl 2干燥。
7. 干燥后的产物分批加入50ml 的圆底烧瓶中,水浴或电热套小火加热蒸去苯。
8. 升高温度至140℃,稍冷后改空冷管,收集194-198℃的馏分。
9. 称重、计算产率。
注意事项:1.所用仪器和试剂必须干燥,称取和加入AlCl3时应快速。
2.注意正确安装氯化氢气体吸收装置,防止倒吸。
3.乙酸酐的滴加速度要慢。
4.蒸馏时,尽可能用小瓶,以减少损失。
思考与讨论1.本装置为何要干燥,加料要迅速?2.反应完成后,为何要加入浓盐酸和在冰水中冰解(加入1:1的浓盐酸和水)?。
有机化学实验实验十二 苯乙酮的制备

六、成功关键
1、反应所用仪器、量筒、研钵等均需干燥;
2、药品的称量、研细和投料都必须迅速,防止吸湿;
3、乙酸酐滴加速度要缓慢,太快温度过高,对反应不利;热 水浴加热回流时要不断搅拌,水温控制在95℃为宜。
七、课后习题
1.在苯乙酮的制备中,水和潮气对本实验有何影响?在仪器 装置和操作中应注意哪些事项。 2.反应完成后为什么要加入浓盐酸和冰水的混合物来分解产 物? 3.为什么硝基苯可作为反应的溶剂?芳环上有OH、 NH2等基 团存在时对反应不利,甚至不发生反应,为什么?
4.请总结friedel-Craft酰基化反应和烷基化反应各有何特点。
2、苯和氯化氢有毒,实验中应尽量不让其散发在空气
中。 3、注意正确安装氯化氢气体吸收装置,防止倒吸。 4、滴加乙酸酐的速度要缓慢(约7秒一滴),太快反应不 易控制,易发生危险。 5、控制火焰的大小至刚好回流,水温控制在95℃为宜, 以防产生的泡沫冲至冷能管,严重时发生凶险。 6、加入稀HCl时,开始慢滴,后渐快。
性状 名称 (CH3CO)2 O 苯乙酮 苯 分子量 无色 液体 无色 液体 无色 液体 比 重 熔点 沸点 ℃ ℃ -73 20.5 5.5 139 202 80.5 溶解度:克/100ml溶 剂 水 分解 微溶 不溶 醇 易溶 溶 易溶 醚 ∞ 溶 ∞
102 120.15 78
1.082 1.028 0.879
酸都与当量的三氯化铝生成络合物,三氯化铝不能再参与反应, 失去催化活性,故必须过量)。
(2)反应体系必须严格无水,否则三氯化铝水解失效。
(3)产物有有毒气体氯化氢,故装置应考虑吸收。
另外,反应放热,且要反应完全,还需加热,反应体系温度
高于反应物和溶剂沸点,故应采用回流、滴加装置。
苯乙酮的制备(精)
苯乙酮的沸点文献值为202.0℃,熔点为20.5℃, 折光率l.5372。
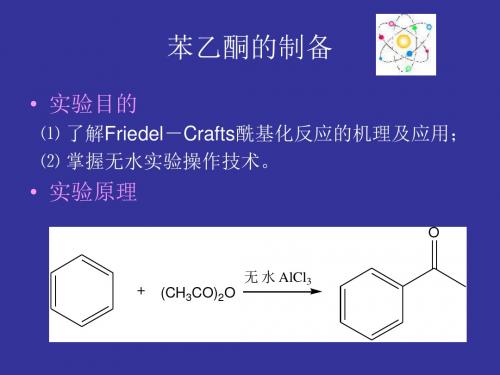
图1、带滴 液漏斗和 气体吸收 装置的反 应装置
乳胶管联结 气体吸收
NaOH水 溶 液
苯乙酮的制备
• 实验目的
⑴ 了解Friedel-Crafts酰基化反应的机理及应用; ⑵ 掌握无水实验操作技术。• Fra bibliotek验原理O
+
无 水 AlCl3 (CH3CO)2O
操作步骤
迅速称取25g经研碎的无水AlCl3(放入三颈瓶中)+ 30 mL 经金属钠干燥过的苯,启动搅拌,由滴液漏斗滴加重新 蒸馏过的醋酸酐6mL(约6.5g,0.06mol)和无水苯10mL的 混合溶液(约20min滴完)。反应立即开始,伴随有反应混 合液发热及氯化氢急剧产生。控制滴加速度,勿使反应过 于激烈。滴加完后,在水浴(或电热套)上回流0.5h, 至无氯化氢气体逸出为止(此时三氯化铝溶完)。
将三颈瓶冷却,在搅拌下慢慢滴加100 mL冷却的稀盐酸。 当瓶内固体物质完全溶解后,分出苯层。水层每次用 15mL苯萃取两次。合并苯层,依次用5%的氢氯化钠溶 液、水各20mL洗涤,然后用无水硫酸钠(镁)干燥。
将干燥后的粗产物过滤,蒸去苯以后(温度升到140 ℃左右,停止加热) ,将粗产物转移到50mL的蒸馏
思考题
1、水和潮气对本实验有何影响?在仪器的装 置和操作中应注意哪些事项?为什么要迅速称 取研磨三氯化铝? 2、反应完成后为什么要加入冷却的稀盐酸? 3、指出如何由傅—克反应制备下列化合构:(1) 二苯甲烷;(2)苄基苯基酮;(3)对硝基二苯酮。
苯乙酮的制备研究

苯乙酮的制备研究苯乙酮,又称丙酮苯,是一种无色液体有机化合物,化学式为C6H5COCH3。
它具有独特的香味,在化工领域有着广泛的应用。
苯乙酮通常用作香水、药品和塑料制造的原料,也被用来生产染料,树脂和农药等化工产品。
苯乙酮的生产工艺以及制备方法在化工领域一直备受关注。
本文着重研究苯乙酮的制备方法,探究其生产工艺和优化措施。
一、苯乙酮的制备方法苯乙酮的制备方法主要包括酸碱法、酸酮偶合法、苯甲酮氧化、苯甲酮硝化等多种工艺。
其中以酸碱法和酸酮偶合法较为成熟和广泛应用。
1.酸碱法酸碱法是苯乙酮生产的传统工艺,也是经济实用的一种制备方法。
其反应如下:2 C6H5CH2Cl + 2 NaOH → C6H5COCH3 + 2 NaCl + 2 H2O苯乙酮生产工艺在操作和控制上较为简单,但废气处理较为复杂。
目前,酸碱法苯乙酮生产工艺已经具备较高的稳定性和成熟度,但由于产物纯度较低、副反应严重等问题,越来越多的企业将目光转向其他更为先进的制备方法。
二、苯乙酮的生产工艺苯乙酮的生产工艺主要包括原料处理、反应制备、产品分离等多个环节,整个工艺复杂且关联紧密。
1.原料处理苯乙酮的原料处理主要包括底物氧化、催化剂制备等多个环节。
底物氧化是指将前体物质如乙苯氧化为苯乙酮,该步骤需要合适的氧化剂以及适当的催化剂参与反应。
催化剂的制备则需要先进的制备工艺以及严格的质量控制,以确保产品的稳定生产。
2.反应制备反应制备是苯乙酮生产的核心环节,其反应条件的控制和催化剂的添加对产品质量影响极大。
目前,酸酮偶合法生产苯乙酮的反应制备中,催化剂的选取和稳定性是重点研究的方向。
3.产品分离产品分离是苯乙酮生产工艺中的最后一步,该环节直接影响产品的质量和产率。
目前,常用的产品分离方法主要包括单级结晶、溶剂萃取等。
三、苯乙酮的制备技术改进苯乙酮的制备技术改进主要包括反应条件的优化、催化剂的改进以及产品分离技术的改进等多个方面。
1.反应条件的优化反应条件的优化是苯乙酮制备中的重点方向之一,通过对底物浓度、反应温度、反应时间等参数进行调整,可以提高产品的产率和纯度。
苯乙酮的制备
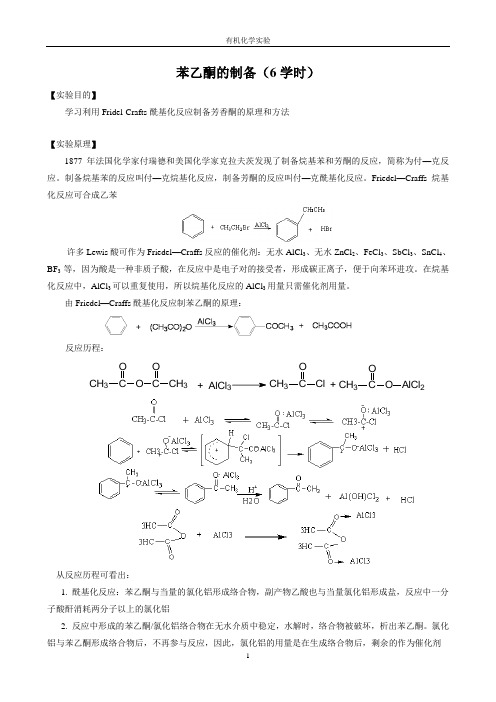
苯乙酮的制备(6学时)【实验目的】学习利用Fridel-Crafts 酰基化反应制备芳香酮的原理和方法【实验原理】1877年法国化学家付瑞德和美国化学家克拉夫茨发现了制备烷基苯和芳酮的反应,简称为付—克反应。
制备烷基苯的反应叫付—克烷基化反应,制备芳酮的反应叫付—克酰基化反应。
Friedel —Craffs 烷基化反应可合成乙苯许多Lewis 酸可作为Friedel —Craffs 反应的催化剂:无水AlCl 3、无水ZnCl 2、FeCl 3、SbCl 3、SnCl 4、BF 3等,因为酸是一种非质子酸,在反应中是电子对的接受者,形成碳正离子,便于向苯环进攻。
在烷基化反应中,AlCl 3可以重复使用,所以烷基化反应的AlCl 3用量只需催化剂用量。
由Friedel —Craffs 酰基化反应制苯乙酮的原理:反应历程:O C O CH 3C OCH 3+ AlCl 3OC CH 3Cl + OC CH 3O AlCl 2从反应历程可看出:1. 酰基化反应:苯乙酮与当量的氯化铝形成络合物,副产物乙酸也与当量氯化铝形成盐,反应中一分子酸酐消耗两分子以上的氯化铝2. 反应中形成的苯乙酮/氯化铝络合物在无水介质中稳定,水解时,络合物被破坏,析出苯乙酮。
氯化铝与苯乙酮形成络合物后,不再参与反应,因此,氯化铝的用量是在生成络合物后,剩余的作为催化剂3. 氯化铝可以与含羰基的物质形成络合物,所以原料乙酸酐也与氯化铝形成分子络合物;另外,氯化铝的用量多时,可使醋酸盐转变为乙酰氯,作为酰化试剂,参与反应:OC CH 3Cl O C CH 3O AlCl 2+ AlOCl4. 苯用量是过量的,苯不但作为反应试剂,而且也作为溶剂,所以乙酸酐才是产率的基准试剂。
5. 酰基化反应特点:产物纯、产量高(因酰基不发生异构化,也不发生多元取代)【实验仪器及药品】药品:乙酸酐 苯 硫酸镁 盐酸 氯化铝 氢氧化钠仪器:圆底烧瓶 冷凝管 滴液漏斗 蒸馏装置 干燥管 搅拌装置【主要反应试剂及产物的物理常数】【实验装置图】图8-1 无水滴加搅拌气体吸收反应装置【实验步骤】向装有10ml 恒压滴液漏斗、机械搅拌装置和回流冷凝管(上端通过一氯化钙干燥管与氯化氢气体吸收装置相连)的100ml 三颈烧瓶中迅速加入13g (0.097mol )粉状无水三氯化铝和16ml(约14g, 0.18mol)无水苯。
实验十四 苯乙酮的制备(预习指导)
实验十四 苯乙酮的制备(6学时)一、实验目的1.学习利用Friedel-Crafts 酰基化反应制备芳香酮的原理与方法。
2.巩固无水实验操作的基本技巧。
3.学会电磁搅拌器的作用,掌握有毒气体的处理方法。
4.巩固醛酮的化学性质及鉴别方法。
二、实验原理Friedel-Crafts 酰基化反应是制备芳香酮的最重要和常用的方法之一,酸酐是常用的酰化试剂,无水FeCl 3,BF 3,ZnCl 2 和AlCl 3等路易斯酸作催化剂,分子内的酰基化反应还可用多聚磷酸PPA 作催化剂。
酰基化反应常用过量的液体芳烃、二硫化碳、硝基苯、二氯甲烷等作为反应的溶剂。
该类反应一般为放热反应,通常是将酰基化试剂配成溶液后,慢慢滴加到盛有芳香族化合物的反应瓶中。
用苯和乙酸酐制备苯已酮的反应方程式如下:主反应: + (CH 3CO )2O3COCH 3CH 3COOHCOCH 3AlCl 3CH 3COOAlCl 2HClAlCl 3CH 3COOH3O AlCl 3+3O反应机理:傅—克酰基化反应催化剂的用量大,乙酸酐:AlCl 3=1:2.2(苯乙酮和乙酸都与当量的三氯化铝生成络合物,三氯化铝不能再参与反应,失去催化活性,故必须过量)。
三、试剂及器材1.器材: 50mL 三颈烧瓶,25mL 圆底烧瓶,球形冷凝管,空气冷凝管,恒压滴液漏斗,温度计,电磁搅拌器,电热套(酒精灯),分液漏斗,250 mL烧杯1个,长颈漏斗1个,干燥管,10 mL、5 mL、100mL量筒。
2.试剂:醋酸酐、无水苯、无水三氯化铝、浓盐酸、氢氧化钠、无水硫酸镁,沸石,碎冰四、主要试剂及产品的物理常数五、实验内容与仪器装置1.实验内容(1)合成向装有恒压滴液漏斗、电磁加热搅拌器和回流冷凝管(上端通过一氯化钙干燥管与氯化氢气体吸收装置相连)的50 mL三颈(或二颈)烧瓶中迅速加入研细的6.0g无水三氯化铝和8.0mL无水苯。
在电磁搅拌下自滴液漏斗慢慢滴加2 mL乙酐(加2 mL苯稀释),开始少加几滴,待反应发生后再继续滴加,切勿使反应过于激烈,滴加速度以烧瓶稍热为宜。
7.1苯乙酮的合成(6学时)
实验答案:3.2正常情况下,这时所得馏出液约50一60ml。
用酒精比重计测定馏出液的重量百分浓度一般可达88%一92%,记录馏出液的馏出温度范围、体积、浓度以及初馏液和残余液的体积。
实验约需时间2h。
3.41、在怎样的情况下才用减压蒸馏?答:沸点高的物质以及在普通蒸馏时还没达到沸点温度就已分解,氧化或聚合的物质才用减次蒸馏。
2、在进行减压蒸馏时,为什么必须用热浴加热,而不能用直接火加热?为什么进行减压蒸馏时须先抽气才能加热?答:用热浴的好处是加热均匀,可防止暴沸,如果直接用火加热的话,情况正好相反。
因为系统内充满空气,加热后部分溶液气化,再抽气时,大量气体来不及冷凝和吸收,会直接进入真空泵,损坏泵改变真空度。
如先抽气再加热,可以避免或减少之。
3、当减压蒸完所要的化合物后,应如何停止减压蒸馏?为什么?答:蒸馏完毕移去热源,慢慢旋开螺旋夹,并慢慢打开二通活塞,(这样可以防止倒吸),平衡内外压力,使测压计的水银柱慢慢地回复原状(若放开得太快,水银柱很快上升,有冲破压力计的可能)然后关闭油泵和冷却水。
3.91)重结晶时,溶剂的用量为什么不能过量太多,也不能过少?正确的应该如何?答:过量太多,不能形成热饱和溶液,冷却时析不出结晶或结晶太少。
过少,有部分待结晶的物质热溶时未溶解,热过滤时和不溶性杂质一起留在滤纸上,造成损失。
考虑到热过滤时,有部分溶剂被蒸发损失掉,使部分晶体析出留在波纸上或漏斗颈中造成结晶损失,所以适宜用量是制成热的饱和溶液后,再多加20%左右。
2)用活性炭脱色为什单要待固体物质完全溶解后才加入?为什么不能在溶液沸腾时加入?答:活性炭可吸附有色杂质、树脂状物质以及均匀分散的物质。
因为有色杂质虽可溶于沸腾的溶剂中,但当冷却析出结晶体时,部分杂质又会被结晶吸附,使得产物带色。
所以用活性炭脱色要待固体物质完全溶解后才加入,并煮沸5-10min。
要注意活性炭不能加入已沸腾的溶液中,以一免溶液暴沸而从容器中冲出。
苯乙酮的制备方案
苯⼄酮的制备⽅案苯⼄酮的制备⼀、⼯作⽬标1.学习实验室中利⽤Friedel-Crafts酰基化法制备苯⼄酮的原理与⽅法。
2.掌握带有机械搅拌和⽓体吸收的加热回流装置的操作⽅法。
3.掌握带⼲燥管和吸收有害⽓体的回流装置使⽤4.掌握终点监控的⽅法原理5.掌握有机液体的⼲燥及⾼沸点化合物的蒸馏6.掌握使⽤分液漏⽃洗涤和分离液体有机物的操作技术⼆、⼯作内容1.解读⽅案,并确定初步⽅案2.列出准备单(仪器、试剂以及相关溶液的配制)3.进⾏试验1)带⼲燥管和吸收有害⽓体回流装置的搭建2)物料的投放3)⽔浴回流装置的搭建4)反应⼀段时间,进⾏反应终点的监控5)粗产物的⼲燥(有机液体的分离与⼲燥)6)粗产物的蒸馏提纯7)空⽓冷凝的装置的搭建4.对馏出物进⾏称重5.结束⼯作(装置的拆除、清洗、归还)6.数据的处理与总结7.计算产率并撰写报告三、⼯作进程与安排四、苯⼄酮合成准备单1.试剂:2.仪器:五、苯⼄酮的合成原理芳酮⼀般通过辅克反应来制备,该反应在⽆⽔三氯化铝存在下由酰氯或酸酐与芳烃反应得到⾼产率的芳酮。
本实验以⼄酸酐为酰化试剂,与苯发⽣⼄酰化反应制备苯⼄酮,其中苯既是反应物,⼜作为反应溶剂,可⽤下列反应式表⽰:+CH 3COCCH 3O O⽆⽔ AlCl 3CCH 3O+ CH 3COOH具体反应过程:CH 3C O O CCH 3O+ AlCl 3CH 3C O O CCH 3O AlCl 3AlCl 3(红⾊溶液)CCH 3O AlCl 3+ H 2O CCH 3O+ Al(OH)Cl 2 + HCl⽩(放热)CH 3COO AlCl 2 + H 2O Al(OH)Cl 2 + CH 3COOH (放热)Al(OH)Cl 2 + HCl AlCl 3 + H 2O 六、苯⼄酮合成⼯作步骤1. 在250mL 三⼝烧瓶中,分别安装搅拌器,滴液漏⽃及球形冷凝管。
在冷凝管上端装上氯化钙[1]⼲燥管,并连接⽓体吸收装置[2],⽤⽔做吸收液。
规范答题系列(四)实验操作的原因、目的和作用
【类题试解】 1.(2012·安徽高考节选)亚硫酸盐是一种常见食品添加剂。为 检验某食品中亚硫酸盐含量(通常以1 kg样品中含SO2的质量
计)。某研究小组设计了如下两种实验流程:
甲方案流程
乙方案流程
气体A的主要成分是
。为防止煮沸时发生暴沸,必须先
向烧瓶中加入
;通入N2的目的是___________________
后加热回流1小时。
(Ⅱ)分离与提纯:
①边搅拌边慢慢滴加一定量浓盐酸与冰水混合液,分离得到有
机层 ②水层用苯萃取,分液 ③将①②所得有机层合并,洗涤、干燥、蒸去苯,得到苯乙酮粗 产品 ④蒸馏粗产品得到苯乙酮
回答下列问题:
(2)合成过程中要求无水操作,理由是____________________
___________________________________________________。
____________________________________________________。 答案:SO2 碎瓷片(或沸石) 将生成的SO2全部赶出
2.(2010·江苏高考节选)对硝基甲苯是医药、染料等工业的一
种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,
通过甲苯的硝化反应制备。
一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂, 固体NaHSO4为催化剂(可循环使用),在CCl4溶液中,加入乙酸酐 (有脱水作用),45℃反应1 h。反应结束后,过滤,滤液分别用
5% NaHCO3溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
上述实验中过滤的目的是 答案:回收NaHSO4 。
【规范答案】
(2)防止三氯化铝和乙酸酐水解(只答三氯化铝水解或乙酸酐水
