尼妥珠单抗 nimotuzumab—2020版各系统肿瘤的药物临床应用指导原则
尼妥珠单抗注射液说明书--泰欣生

尼妥珠单抗注射液说明书【药品名称】通用名称:尼妥珠单抗注射液商品名称:泰欣生英文名称:Nimotuzumab Injection汉语拼音:NiTuoZhu DanKang ZhuSheYe【成份】每瓶含50mg尼妥珠单抗、4.5mg磷酸二氢钠、18.0mg磷酸氢二钠、86.0mg氯化钠、2.0mg聚山梨醇酯80。
【性状】本品为无色澄明液体。
【适应症】试用于与放疗联合治疗表皮生长因子受体(EGFR)表达阳性的Ⅲ/Ⅳ期鼻咽癌。
【规格】50mg/瓶(10 mL)。
【用法用量】将两瓶(100mg)尼妥珠单抗注射液稀释到250mL生理盐水中,静脉输液给药,给药过程应持续60分钟以上。
在给药过程中及给药结束后1小时内,需密切监测患者的状况。
首次给药应在放射治疗的第一天,并在放射治疗开始前完成。
之后每周给药1次,共8周,患者同时接受标准的放射治疗。
【不良反应】在中国进行的晚期鼻咽癌II期临床试验中,共有137例晚期鼻咽癌患者入组,试验组70例用药,尼妥珠单抗注射液每周给药1次,每次100mg,共8周。
与本品相关的不良反应主要表现为轻度发热、血压下降、恶心、头晕、皮疹,见表1:表1 与药物相关的不良反应发生率不良反应发生率%Ⅰ/Ⅱ级发生率%Ⅲ/Ⅳ级总发生率%Ⅰ-Ⅳ级缓解方法/是否影响治疗发热 4.28% (发热,最高39℃)- 4.28%用药缓解,未影响治疗血压下降、头晕 2.86%(最低80/50毫米汞柱)- 2.86%休息后缓解,未影响治疗恶心 1.43%- 1.43%自行缓解,未影响治疗皮疹 1.43%- 1.43%自行缓解,未影响治疗在古巴、德国、加拿大等国家进行了本品单药或联合放化疗治疗头颈部肿瘤、神经胶质瘤、胰腺癌、结直肠癌和非小细胞肺癌的临床试验。
尼妥珠单抗的剂量范围为100~400 mg/次,用药1~6次,其中86.5%的患者用药6次,每周1次。
患者平均年龄55岁(20~75岁),男性57例,女性32例,共89例。
肿瘤靶向治疗药——尼妥珠单抗介绍PPT课件

印尼 Clinical Trials anti EGFR Antibody And Ganglioside Vaccines
巴西 New fermentation technologies and culture media Clinical trials anti RGF Antibody and Ganglioside Vaccines
尼妥珠单抗下调A431细胞株VEGF表达
Int. Journal Of Cancer 101:567-575, 2002
尼妥珠单抗的体外研究
抑制细胞周期 :G1 期
Control
Nimotuzumab
流式细胞仪分析显示尼妥珠单抗处理A431细胞株后,S期细胞下降,并有G1期阻滞
Int. Journal Of Cancer 101:567-575, 2002
Heregulins
NRG2 NRG3 Heregulins Betacellulin
TK
ErbB-1 HER1 EGFR
TK
ErbB-2 HER2 neu
ErbB-3 HER3
TK
ErbB-4 HER4
尼妥珠单抗的靶向分子-EGFR
-EGFR:
-癌基因c-erbB1的表达 产物
-I 型受体酪氨酸激酶跨 膜糖蛋白,分子量
头颈部肿瘤 (SCCHN)
肿瘤类型 结直肠癌 头颈部癌 肺癌 (NSCLC) 乳腺癌 卵巢癌 肾癌
% 72–89 95–100 40–80 14–91 35–70 50–90
Cunningham et al. N Engl J Med 2004;351:337–345; Grandis et al. Cancer 1996;78:1284–1292; Salomon et al. Crit Rev Oncol Hematol
泰欣生(尼妥珠单抗注射液)说明书

泰欣生(尼妥珠单抗注射液)说明书【泰欣生药品名称】通用名称:尼妥珠单抗注射液商品名称:泰欣生英文名称:Nimotuzumablnjection汉语拼音:NiTuoZhuDanKangZhusheye【泰欣生成份】每支10mL含50mg尼妥珠单抗、4.5mg磷酸二氢钠、18.0mg磷酸氢二钠、86.0mg氯化钠、2.0mg聚山梨醇酯80。
【泰欣生性状】外观澄清、无色无味,无不溶物的液体。
【泰欣生适应症】泰欣生与放疗联合适用于治疗表皮生长因子受体(EGFR)阳性表达的Ⅲ/Ⅳ期鼻咽癌。
使用泰欣生前,患者应先确认其肿瘤细胞EGFR表达水平,EGFR中、高表达的患者推荐使用泰欣生。
检验操作应由熟练掌握EGFR检测试剂盒检测技术的实验室完成。
检验中的某些失误,如使用较差的组织样本、未能严格遵从操作规程、使用不当的对照等均可能导致不可靠的结果。
【泰欣生规格】13.5毫升西林瓶装量10毫升(±0.5毫升),尼妥珠单抗浓度为5mg/mL,每支含50毫克。
【泰欣生用法用量】100mg尼妥珠单抗稀释于250ml生理盐水中,前臂静脉输液给药,进药过程在60分钟以上。
次给药时间为放射治疗的天,于放疗前完成,以后每周一次,共8次。
患者同时接受标准的鼻咽癌放射治疗。
【泰欣生不良反应】该药物的不良反应主要表现为发热、血压下降、恶心、头晕、皮疹。
在70例晚期鼻咽癌患者中进行的Ⅱ期临床试验中发现,用药后发热的发生率为4.28%,体温39℃,对症处理后缓解,不影响治疗;血压下降,头晕发生率2.86%,达80/50mmHg,休息后缓解,不影响治疗;恶心发生率为1.43%,轻度,可自行缓解,不影响治疗;头晕发生率2.86%,时有头晕,可自行缓解,不影响治疗;皮疹发生率1.43%,轻度,可自行缓解,不影响治疗。
在古巴和加拿大进行的临床试验发现该药常见的不良反应有发热、寒颤、恶心、呕吐、发冷、贫血、血压降低。
不常见的不良反应有肌肉痛、运动语言障碍、口干、潮红、下肢无力、嗜睡、丧失方向感、肌酐水平升高、白细胞减少、血尿、胸痛、口腔绀紫。
药物说明书drins-尼妥珠单抗-百泰

对本品或其任一组份过敏者禁用。
【注意事项】
本品应在具有同类药品使用经验的临床医师指导下使用,并具备相应抢救措施。 冻融后抗体的大部分活性丧失,故本品在储存和运输过程中严禁冷冻。本品稀释于生理盐水后,在2℃-8℃可保持稳定12小时,在室温下可保持稳定8小时。如稀释后储存超过上述时间,不宜使用。 应由熟练掌握EGFR检测技术的专职人员进行EGFR表达水平的检验。检验中若出现组织样本质量较差、操作不规范、对照使用不当等情况,均可导致结果偏差。
尼妥珠单抗注射液
说明书来源: 百泰生物药业有限公司
【药品名称】
通用名称:尼妥珠单抗注射液 英文名称:NimotuzumabInjection 商品名称:泰欣生
【成份】
每瓶含50mg尼妥珠单抗、4.5mg磷酸二氢钠、18.0mg磷酸氢二钠、86.0mg氯化钠、2.0mg聚山梨醇酯80。
【性状】
本品为无色澄明液体。
【适应症】
试用于与放疗联合治疗表皮生长因子受体 (EGFR) 表达阳性的III/IV期鼻咽癌。
【规格】
50mg/瓶(10mL)。
【用法用量】
将两瓶 (100mg) 尼妥珠单抗注射液稀释到250mL生理盐水中,静脉输液给药,给药过程应持续60分钟以上。在给药过程中及给药结束后1小时内,需密切监测患者的状况。首次给药应在放射治疗的第一天,并在放射治疗开始前完成。之后每周给药1次,共8周,患者同时接受标准的放射治疗。
【老年用药】
在70例接受尼妥珠单抗注射液联合放射治疗的患者中,4例(5.7%)年龄在65岁或以上。尚未确定老年患者使用本品安全性和疗效方面的特殊性。
【药物相互作用】
尚缺乏本品与其它药物相互作用的数据。
尼妥珠单抗联合同步放化疗对局部晚期头颈部鳞状细胞癌的疗效评价

DOI:10.19368/ki.2096-1782.2023.06.069尼妥珠单抗联合同步放化疗对局部晚期头颈部鳞状细胞癌的疗效评价吕晓伟1,邓丹2,刘方丽11.菏泽市牡丹人民医院,山东菏泽274000;2.曹县人民医院,山东菏泽274400[摘要]目的分析在局部晚期头颈部鳞状细胞癌患者的治疗中实施尼妥珠单抗联合同步放化疗治疗的效果。
方法选择2021年5月—2022年4月期间来菏泽市牡丹人民医院接受治疗的局部晚期头颈部鳞状细胞癌患者60例作为研究样本,经双盲法分为研究组与参照组,各30例,参照组接受放化疗治疗,研究组在放化疗基础上联合尼妥珠单抗治疗,比较患者治疗前后血清肿瘤标志物水平、治疗效果、不良反应发生率。
结果治疗前,两组患者的血清肿瘤标志物水平对比,差异无统计学意义(P>0.05);治疗后,研究组比参照组低,差异有统计学意义(t=10.194、5.519、5.920,P<0.05);研究组的治疗效果(100.00%)比参照组(80.00%)高,差异有统计学意义(χ2=4.630,P<0.05);研究组的不良反应发生率(23.33%)与参照组(26.67%)比较,差异无统计学意义(P>0.05)。
结论在局部晚期头颈部鳞状细胞癌患者的治疗中实施尼妥珠单抗联合同步放化疗的治疗效果显著,能改善患者的血清肿瘤标志物,值得推广。
[关键词]尼妥珠单抗;同步放化疗;局部晚期;头颈部;鳞状细胞癌[中图分类号]R59 [文献标识码]A [文章编号]2096-1782(2023)03(b)-0069-04Efficacy Evaluation of Nimotuzumab Combined with Concurrent Chemo⁃radiotherapy in Locally Advanced Squamous Cell Carcinoma of the Head and NeckLYU Xiaowei1, DENG Dan2, LIU Fangli11.Mudan People's Hospital of Heze, Heze, Shandong Province, 274000 China;2.Caoxian People's Hospital, Heze, Shandong Province, 274400 China[Abstract] Objective To analyze the effect of nimotuzumab combined with concurrent chemoradiotherapy in the treat⁃ment of patients with locally advanced squamous cell carcinoma of the head and neck. Methods A total of 60 patients with locally advanced squamous cell carcinoma of the head and neck who were treated at Mudan People's Hospital of Heze from May 2021 to April 2022 were selected as research samples. They were divided into research group and ref⁃erence group by double-blind method, 30 cases in each group. The reference group received radiotherapy and chemo⁃therapy, and the study group received nimotuzumab on the basis of radiotherapy and chemotherapy. Serum tumor marker levels, therapeutic effects, and incidence of adverse reactions were compared before and after treatment. Results Before treatment, there was no statistically significant difference in serum tumor markers between two groups (P> 0.05). After treatment, the study group was lower than the reference group, and the difference was statistically signifi⁃cant (t=10.194, 5.519, 5.920, P<0.05). The therapeutic effect of the study group (100.00%) was higher than that of the control group (80.00%), and the difference was statistically significant (χ2=4.630, P<0.05). There was no statistically significant difference in the incidence of adverse reactions between the study group (23.33%) and the reference group (26.67%) (P>0.05). Conclusion Nimotuzumab combined with concurrent chemoradiotherapy has a significant thera⁃[作者简介] 吕晓伟(1986-),女,本科,主治医师,研究方向为肺癌、食管癌等多种恶性肿瘤的综合治疗。
尼妥珠单抗治疗15例非小细胞肺癌临床疗效及不良反应的回顾性分析

尼妥珠单抗治疗15例非小细胞肺癌临床疗效及不良反应的回顾性分析倪军;斯晓燕;王汉萍;张力【摘要】Objective To retrospectively analyze the therapeutic efficacy and adverse events of nimotuzumab in advanced non-small cell lung cancer (NSCLC). Method Nimotuzumab was administrated to 15 cases of stage IV NSCLC, including 9 cases of adenocarcinoma and 8 cases of squamous cell carcinoma. All patients were confirmed by either histopathology or cytopathology, and were treated by nimotzumab (nimotuzumab 400 mg, i.v., qw). The ef-ficacy was evaluated after six weeks of treatment according to RECIST standards. For adverse events, the NCI-CTC 3.0 was applied. Result There were 11 cases that were qualified for efficacy evaluation and 15 cases for safety evaluation. Among the 11 cases included in efficacy evaluation, there were 8 cases achieving SD and 3 cases of PD. The disease control rate was 72.2% (8/11). The safety evaluation results showed that the incidence of skin rash relat-ed to nimotuzumab was low, and which was in no association with clinical benefit. All adverse events related with nimotuzumab were mild. Conclusion Nimotuzumab combined with chemotherapy or radiotherapy for patients with NSCLC increases disease control rate and has a better safety profile.%目的:回顾性分析尼妥珠单抗治疗晚期非小细胞肺癌(NSCLC)的临床疗效及不良反应。
尼妥珠单抗注射液说明书--泰欣生
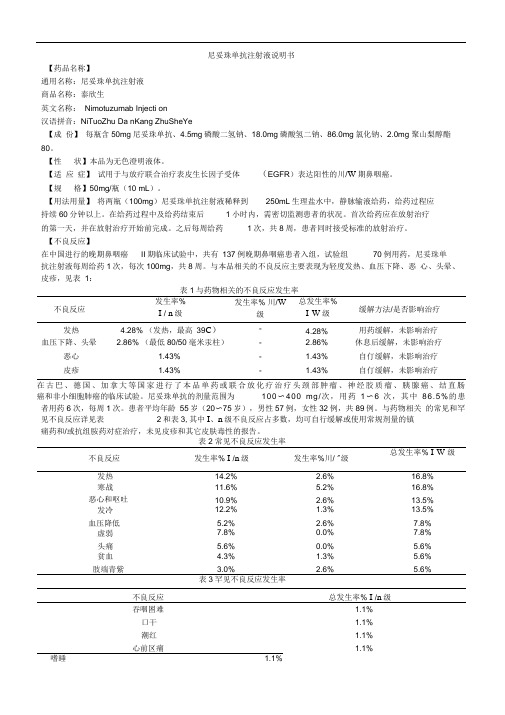
尼妥珠单抗注射液说明书【药品名称】通用名称:尼妥珠单抗注射液商品名称:泰欣生英文名称:Nimotuzumab Injecti on汉语拼音:NiTuoZhu Da nKang ZhuSheYe【成份】每瓶含50mg尼妥珠单抗、4.5mg磷酸二氢钠、18.0mg磷酸氢二钠、86.0mg氯化钠、2.0mg 聚山梨醇酯80。
【性状】本品为无色澄明液体。
【适应症】试用于与放疗联合治疗表皮生长因子受体(EGFR)表达阳性的川/W期鼻咽癌。
【规格】50mg/瓶(10 mL)。
【用法用量】将两瓶(100mg)尼妥珠单抗注射液稀释到250mL生理盐水中,静脉输液给药,给药过程应持续60分钟以上。
在给药过程中及给药结束后1小时内,需密切监测患者的状况。
首次给药应在放射治疗的第一天,并在放射治疗开始前完成。
之后每周给药1次,共8周,患者同时接受标准的放射治疗。
【不良反应】在中国进行的晚期鼻咽癌II期临床试验中,共有137例晚期鼻咽癌患者入组,试验组70例用药,尼妥珠单抗注射液每周给药1次,每次100mg,共8周。
与本品相关的不良反应主要表现为轻度发热、血压下降、恶心、头晕、皮疹,见表1:表1与药物相关的不良反应发生率不良反应发生率%I / n级发生率% 川/W级总发生率%I-W级缓解方法/是否影响治疗发热 4.28% (发热,最高39C)- 4.28%用药缓解,未影响治疗血压下降、头晕 2.86% (最低80/50毫米汞柱)- 2.86%休息后缓解,未影响治疗恶心 1.43%- 1.43%自仃缓解,未影响治疗皮疹 1.43%- 1.43%自仃缓解,未影响治疗在古巴、德国、加拿大等国家进行了本品单药或联合放化疗治疗头颈部肿瘤、神经胶质瘤、胰腺癌、结直肠癌和非小细胞肺癌的临床试验。
尼妥珠单抗的剂量范围为100〜400 mg/次,用药1〜6次,其中86.5%的患者用药6次,每周1次。
患者平均年龄55岁(20〜75岁),男性57例,女性32例,共89例。
尼妥珠单抗治疗大肠癌1例报告

尼妥珠单抗治疗大肠癌1例报告
郭翔宇;孙涛;于绍芬;姜翠
【期刊名称】《癌症进展》
【年(卷),期】2010(008)001
【摘要】近年来,我国大肠癌发病率呈逐年上升趋势,随着对其发病机制研究的
不断深入,也为临床大肠癌的诊治提供了更多依据,使治疗方案的制定逐渐趋于个体化。
目前,国内大肠癌的分子靶向治疗临床应用广泛,与传统放化疗方法结合使用的疗效也得到更多专家认可。
作为以表皮生长因子受体(epidermal growth factor receptor,EGFR)为靶点的人源化单抗药物,尼妥珠单抗(nimotuzumab)于2009年被《NCCN头颈部肿瘤临床实践(中国版)》推荐,【总页数】2页(P100-101)
【作者】郭翔宇;孙涛;于绍芬;姜翠
【作者单位】辽宁省肿瘤医院内一科,沈阳110000;辽宁省肿瘤医院内一科,沈阳110000;辽宁省肿瘤医院内一科,沈阳110000;辽宁省肿瘤医院内一科,沈阳110000
【正文语种】中文
【相关文献】
1.尼妥珠单抗联合GP方案治疗晚期肺鳞癌脑转移完全缓解1例报告 [J], 赵静;王
华庆;钱正子;任旭升;张馨允
2.尼妥珠单抗靶向治疗联合TC化疗方案治疗晚期非小细胞肺癌患者的效果观察[J], 李山岭;王杰;陈素芳;王振兴
3.尼妥珠单抗降低BRCA1蛋白表达提高大肠癌SW480细胞对伊立替康敏感性的研究 [J], 孙晓东
4.尼妥珠单抗联合化疗一线治疗晚期大肠癌的临床研究 [J], 陈望花;王文玲;张若荣;董洪敏;王刚;李小凯
5.尼妥珠单抗靶向治疗联合常规化疗方案治疗晚期非小细胞肺癌临床研究 [J], 王学森
因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、尼妥珠单抗 nimotuzumab
制剂与规格:注射液:50mg(10ml)/瓶
适应证:与放疗联合治疗EGFR基因阳性表达的Ⅲ~Ⅳ期鼻咽癌。
合理用药要点:
1.尼妥珠单抗冻融后抗体大部分活性将丧失,故在储存
过程中严禁冷冻。
2.尼妥珠单抗配制的溶液在输液容器中2~8℃时,其
物理和化学稳定性可保持12小时,在室温下可保持8小时。
储存时间超过上述时间,不宜继续使用。
3.尼妥珠单抗与放疗联合适用于治疗EGFR基因阳性表
达的Ⅲ~Ⅳ期鼻咽癌。
4.使用尼妥珠单抗前,建议先确认肿瘤组织的EGFR基
因表达水平,针对EGFR基因中、高表达的患者推荐使用
本品。
5.免疫组化法检验EGFR基因表达,操作应由熟练掌握EGFR基因检测试剂盒检测技术的实验室完成。
检验中的某
些失误,如组织样本质量较差、操作不规范、对照使用不
当等均可影响结果。
6.治疗期间因毒性不可耐受时可在同一代药物之间替换,因疾病进展不能在同一代药物之间替换。
