【图文】顺反异构和对映异构
合集下载
第二章 立体化学

(Z)-1,2-二氯-1-溴乙烯 反-1,2-二氯-1-溴乙烯
(E)-1,2-二氯-1-溴乙烯 顺-1,2-二氯-1-溴乙烯
(E)-3, 4-二甲基-2-戊烯 顺-3, 4-二甲基-2-戊烯
(Z)-3, 4-二甲基-2-戊烯 反-3, 4-二甲基-2-戊烯
二、顺反异构体的性质
▪ห้องสมุดไป่ตู้物理性质不同 ▪ 化学性质:基本相同,与空间构型有关的有差别。
次互换,使最不优先的基团位于顶部,剩下3个原子或基团按照从优先到不优
先的顺序,顺时针方向排列为R-构型,逆时针方向排列为S-构型。
(二)对称中心
如果有机分子中存在一个假想的点,从分子中任一原子或基团向该点作一直 线,再从该点将直线延长,在等距离处遇到相同的原子或原子团,则该点即 为该分子的对称中心。
四、判断对映体的方法
➢ 比较一个分子和它的镜像,如果两者不能重合,则为对映体。 ➢ 有对称面或对称中心的分子为非手性分子(没有对映体)。 ➢ 仅有一个手性碳原子(或手性中心)的分子为手性分子(有对映体)。
第三节
手性、手性分子和对映体
一、手性
镜像与实物不能重合的现象称为手性(chirality)。
二、手性分子和对映体
手性分子:与镜像不能重合的分子。 手性碳(不对称中心):连接4个不同原子或基团的碳。
手性碳
与镜像不能重合的分子彼此互为对映异构体(手性异构体)
三、分子中常见对称因素
(一)对称面
对称面:能将分子切分为具有实物与镜像关系的假想平面。有对称面的化合 物不是手性分子。
第二章
立体化学
立体化学:研究有机分子的立体结构、反应的立体选择性 及其相关规律和应用。
碳链异构
位置异构 构造异构
无机化学 第十一章配合物结构

配合物是具有空的价层轨道的原子或离子(统称中 心原子)和一组能够给予孤对电子或π电子的分子或离 子(统称配体)以配位键结合而形成的具有一定稳定性和 空间结构的化合物。 配合物不一定是离子,也可以是中性分子。 配体中只有一个配位原子叫单齿配体,有多个配 位原子的叫多齿配体(又分双齿、三齿、四齿等等)。由 多齿配体形成的配合物又被形象地叫做螯合物。
顺反异构:平面四边形和八面体的配合物中配位体不
止一种时,相同配体处于对位(180°)则为“反式”, 相同配体处于邻位(90°)则为“顺式”。(p339) 组成为[MX2Y2]、[MX2YZ]的平面四边形和组成为 [MX4Y2]、[MX4YZ]、[M(XX)2YZ]、[M(XX)2Y2]、 [MABCDX2] 的八面体配合物有顺反异构体。
配合物的异构现象
11.2.1 构造异构
构造异构(structural isomerism)是由原子间连 接方式不同引起的异构现象。
1)溶剂异构 溶剂分子在配合物内外界分布不同而引起的异构现 象叫溶剂异构。溶剂为水,则叫水合异构。 例如: [Cr(H2O)6]Cl3、 [Cr(H2O)5Cl]Cl2· 2O 和 H [Cr(H2O)4 Cl2]Cl· 2O 2H
..
N
.. ..
N N
..
2
NOH
+ Ni2+
NOH ..
H3C 镍试剂 (双齿配体) 氮是配位原子(电子对给予体)
镍离子与镍试剂形成的配合物
Ni(CN)42-、CuCl42-也是平面四边形的配离子。
镍和铜也形成四面体形的配合物,例如它们的
四氨合物、NiCl42-这时配原子的电子对进入中心原
子的一个s轨道和3个p轨道,形成sp3杂化轨道。锌的
第八章 立体化学对映异构
l ??
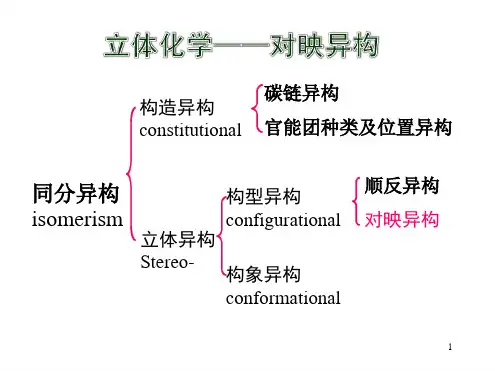
? : 旋光度;c: 溶液浓度 (g/mL);ρ: 纯液体密度(g/mL) ;l: 管长(dm)
? ? 通常要标出测定时的温度和偏振光的波长:
?
t
?
溶剂对比旋光度也有影响,要注明所用溶剂。
例: 在20℃时,以钠光灯为光源测得葡萄糖水溶液的比旋光度为
右旋52.5°,记为:
??
?20 D
?
? 52.5?(水)
返回
26
R-S 标记法
? 根据手性碳原子所连接的四个基团在空间的排列来标记: (1)先把手性碳原子所连接的四个基团设为: a、b、c、d,并
将它们按次序规则排队。 (2)若a,b,c,d 四个基团的顺序是 a(较优基团)>b>c>d ,将该手
性碳原子在空间作如下安排:
? 把排在最后的基团 d放在离观察者 最远的位置,然后按 先后次序观察其他三个基团。 ? 即从最先的a开始看,经过b,再到c。 ? 若方向是 顺时针 的,则该手性碳原子的构型标记为 “R”;若为逆时针,则标记为“S”
-31.3°(乙酸乙酯 )
+31.3°(乙酸乙酯
外消旋体153
)
(III) (2R,3S)-(-) 167
-9.4°(水)
(IV) (2S,3R)- 167
+9.4°(水)
?非对映(+体) 可用一般的物理方法分离.
37
例:酒石酸的立体异构体
COOH
COOH
O HO C
HH *C C* OH OH
COOH
OH
乳酸(2-羟基丙酸)
H3C
C H
COOH
手性分子
乳酸的分子模型图
两个乳酸模型不能叠合
? : 旋光度;c: 溶液浓度 (g/mL);ρ: 纯液体密度(g/mL) ;l: 管长(dm)
? ? 通常要标出测定时的温度和偏振光的波长:
?
t
?
溶剂对比旋光度也有影响,要注明所用溶剂。
例: 在20℃时,以钠光灯为光源测得葡萄糖水溶液的比旋光度为
右旋52.5°,记为:
??
?20 D
?
? 52.5?(水)
返回
26
R-S 标记法
? 根据手性碳原子所连接的四个基团在空间的排列来标记: (1)先把手性碳原子所连接的四个基团设为: a、b、c、d,并
将它们按次序规则排队。 (2)若a,b,c,d 四个基团的顺序是 a(较优基团)>b>c>d ,将该手
性碳原子在空间作如下安排:
? 把排在最后的基团 d放在离观察者 最远的位置,然后按 先后次序观察其他三个基团。 ? 即从最先的a开始看,经过b,再到c。 ? 若方向是 顺时针 的,则该手性碳原子的构型标记为 “R”;若为逆时针,则标记为“S”
-31.3°(乙酸乙酯 )
+31.3°(乙酸乙酯
外消旋体153
)
(III) (2R,3S)-(-) 167
-9.4°(水)
(IV) (2S,3R)- 167
+9.4°(水)
?非对映(+体) 可用一般的物理方法分离.
37
例:酒石酸的立体异构体
COOH
COOH
O HO C
HH *C C* OH OH
COOH
OH
乳酸(2-羟基丙酸)
H3C
C H
COOH
手性分子
乳酸的分子模型图
两个乳酸模型不能叠合
对映异构-有机化学
泳衣品牌
它们不同对映体
表现出相反作用。
对于含手性碳原子的药物,即便是同一药物,
产生的生物活性,有的强弱不一,有的甚至
这是因为生物大分子(如酶、受体、抗体等)或它的 活性部位具有手性,具有一定的立体构型和构象,所以 它要求和它相互作用的的生物活性分子(如神经递质、
激素、药物、毒物等)也要具有和它相适应的立体化学
二 含一个手性碳原子化合物的对映异构
手性碳原子:
泳衣品牌与四个不同的原子或原子团相
* CH CH CO O H 3 OH
连的碳原子。 例如:乳酸分子
(一) 对映异构体
COOH C CH3 H OH H HO COOH
对
互为实物与镜
影关系,不能 相互重叠的两
C CH3
映 体
S-(+)-乳酸
R-(-)-乳酸
5、迅猛增长的市场需求,刺激了手性药物的研究与开发。
§9.1 偏振光和旋光性
一、偏振光和物质的旋光性
光是一种电磁波,光波的振动方向与其前进方向垂直。
光束先进方向
光源
尼可尔棱镜 (偏振片)
与棱镜晶轴 平行的振动 平面
晶轴 b a c d
普通光
a 平面偏振光
有无数个振动平面,振动平面与光的前进方向 相垂直
-1 2 °
0° ( m) 酒 石 酸
0°
内消旋体(分子中有对称面)
内消旋体(meso):分子内部形成对映两半的化合物。
(有平面 对称因素)。内消旋体无旋光性。 具有两个手性中心的内消旋结构一定是(R、S)构 型。 外消旋体与内消旋体异同: 外消旋体与内消旋体的共同之处是:二者均 无旋光性,但本质不同。 外消旋体:是混合物,可拆分出一对对映体。 内消旋体:是化合物,不能拆分。
顺反异构和对映异构

C CH2
CH3 CH2
CH3
Z型
CH3
H
CH2 CH3
CC
CH3
H
E型
-I>-Br>-Cl>-SO3H>-F>-OCOR>-OR >-OH>-NO2>-CCl3>-CHC12>-COCl> -CH2Cl>-COOR>-COOH>-CONH2> >-CHO>-C6H5>-CHR2>-CH2R>-CH3> -D>-H
-C(CHH),C(CHH),C(CHH)
③与—C=C—相连的取代基团为不饱和基 团时,应把双键或叁键原子看作是它以单 键和多个原子相连接。
CC
CH CH2 相当于 CH CH2
C CH 相当于
CC C CH CC
NC C N 相当于 C N
NC CC
C CH 相当于 C C H
CC
H2C
CH C
a
d
C=C
b
f
Z--型
a
f
C=C
b
d
E--型
即把两个优先基团在双键同侧的定 为Z型,在不同一侧的定为E型。
①与—C=C—相连的第一个原子的原子序 数由大到小排列,大者为“优先”基团;
按此规定,在取代基团-CH3、-H、-Br、 -OH、-NH2之中,先后次序应为: -Br>-OH>-NH2>-CH3> -H ②若第1个原子相同,比较第2……个原子。 例:-CH2CH3 > -CH3 又如 -CH(CH3)2与—CH2CH3相比较,第一 原子都是碳,与第一原子相连的原子。前
* CH3CHCH2CH3
OH
CH3C*H*CH*CHCH2CH3
Cl Cl Cl
对称性
对称轴(Cn)
C2
第四章 立体异构
Cl
C CH3
C Br
CH3
C
C H
(E)- 2-氯-1-溴丙烯
(Z)- 2-氯-1-溴丙烯
2. 次序规则
(1)将与双键碳原子直接相连的原子按原 子序数大小排列,原子ቤተ መጻሕፍቲ ባይዱ数大者为“较优”基 团;若为同位素,则质量高者为“较优”基团。
I > Br > Cl > S > P > F > O > N > C > D > H
H C CH3
这种在有双键或环状结构的分子中,由于旋转受阻 使与双键或环相连接的原子或原子团在空间的排布方式不 同所引起的立体异构现象叫做顺反异构现象。各种异构 体互称为顺反异构,又称几何异构。
2.产生顺反异构的原因和条件
产生的原因:由于双键中的π键限制了σ键 的自由旋转,使得两个甲基和两个氢原子在空间 有两种不同的排列方式。
三、含一个手性碳原子的化合物的旋光异构
1.对映体和外消旋体 H3C
C
CH3 H HO
C
HOOC
H OH
COOH
乳酸的一对对映体(透视式) 对映体:互为实物和镜像关系的异构体叫做对 映异构体,简称对映体。
外消旋体;它们的等量混合物可组成一个外消 旋体,用(±)表示 。外消旋体无旋光性。
2.构型的表示方法
构象的两种表示方法
透视式
H
H H C H H C H H
H C H H H
C H
交叉式
重叠式
纽曼投影式:
H H H H
H H
H H
HH
H H
交叉式
重叠式
交叉式构象为优势构象
乙烷处于交叉式构象时,两个碳 上的氢原子相距最远,相互排斥力最 小,因而内能最低。重叠式构象内能 最高。但二者内能相差仅12.5kJ/mol, 室温时,分子热运动所提供的能量就 能使各个构象相互转化,因而不能分 离出乙烷的某一构象异构体。
对映异构-PPT课件
钠光(D),λ=589.3nm,
为使旋光度成为物质的特征性质,使测量条件标准化.
比旋光度:
当浓度为1g/mL(纯液体:密度),测定管的长度为1dm (10cm) ,光源为 钠灯(D)时测定的旋光度 称比旋光度
t
测 定 温 度 旋 光 度 ( 旋 光 仪 上 的 读 数 ) α L× C 溶 液 的 浓 度 ( g /m l) =
A
乳 酸
α
目 镜 ( 亮 )
起 偏 镜
盛 液 管
检 偏 镜
功能: 产生偏振光
使偏振面旋转
检测旋转角度
2、旋光度与比旋光度 旋光度:
使偏振光的振动平面旋转的角度, 称旋光度, 用 α 表示; 影响因素? 影响旋光度大小的因素:
1. 溶液的浓度、2. 测定管的长度、 3. 测定温度、 5. 溶剂等因素 4. 所用光源波长(单色光)
20 20 20
肌肉运动时产生的乳酸 3 . 82 , m . p 53 C
0 0
(右旋体)
乳糖发酵得到的乳酸, 3 . 82 , m . p 53 C
0 0
(左旋体)
化学合成制备的乳酸, 0 , m . p 18 C
0 0
(外消旋体)
第三节 外消旋体
1. 外消旋体: 表示“±”
**
C H C H C H C H 3 3 C lC l
* *
酒石酸 立体异构体:
2,3-二氯丁烷
COOH
H HO OH H
HO H
COOH
H OH
COOH
H H OH OH
HO HO
COOH
H H
COOH
COOH
COOH
为使旋光度成为物质的特征性质,使测量条件标准化.
比旋光度:
当浓度为1g/mL(纯液体:密度),测定管的长度为1dm (10cm) ,光源为 钠灯(D)时测定的旋光度 称比旋光度
t
测 定 温 度 旋 光 度 ( 旋 光 仪 上 的 读 数 ) α L× C 溶 液 的 浓 度 ( g /m l) =
A
乳 酸
α
目 镜 ( 亮 )
起 偏 镜
盛 液 管
检 偏 镜
功能: 产生偏振光
使偏振面旋转
检测旋转角度
2、旋光度与比旋光度 旋光度:
使偏振光的振动平面旋转的角度, 称旋光度, 用 α 表示; 影响因素? 影响旋光度大小的因素:
1. 溶液的浓度、2. 测定管的长度、 3. 测定温度、 5. 溶剂等因素 4. 所用光源波长(单色光)
20 20 20
肌肉运动时产生的乳酸 3 . 82 , m . p 53 C
0 0
(右旋体)
乳糖发酵得到的乳酸, 3 . 82 , m . p 53 C
0 0
(左旋体)
化学合成制备的乳酸, 0 , m . p 18 C
0 0
(外消旋体)
第三节 外消旋体
1. 外消旋体: 表示“±”
**
C H C H C H C H 3 3 C lC l
* *
酒石酸 立体异构体:
2,3-二氯丁烷
COOH
H HO OH H
HO H
COOH
H OH
COOH
H H OH OH
HO HO
COOH
H H
COOH
COOH
COOH
环烷烃的顺反异构对映异构.
• D型为拉丁文Dexter,右 • L型为拉丁文Laevus,左
• 这样旋光方向和构型联系起来,也即D( + ) - 甘 油 醛 , 它 的 对 应 体 L-(-)- 甘 油 醛。其他化合物的构型以甘油醛的构型 为参照标准,在保持手性碳构型不变中, 可由D型甘油醛转化来的化合物就是D型,
• 可由L型甘油醛转化来的化合物就是L型。
D-(+)-甘油醛
D-(-)-甘油酸
• 与甘油醛相关联的手性化合物都可用D/L 来标记。此种命名法主要对葡萄糖、氨 基酸类化合物。适用范围有限。
• 与甘油醛不相关联的手性化合物就不可 用D/L法来标记只能用IUPAC规定的R/S 法来标记。
• R/S构型标记法(绝对)规定:
• A、首先按次序规则确定与手性碳原子连 接的四个不同的原子或基团a,b,c,d的先后 次序(排大小)a>b>c>d ‘>’表示“优先 于”
• 分析分子中有无对称元素。若分子中没有对称 面也没有对称中心,一般为手性分子,具有旋 光性;否则为非手性分子。
•
• 1 对称面(Plane of symmetry):如果假想一 个平面将分子一分为二切开,两部分互为镜像, 这个平面就成为该分子的对称面,用σ表示。 有对称面的分子一定是非手性分子,没有旋光 性。
• ·手性化合物的特点: • 结构:镜像与实物不重合。 • 内能相同(左、右旋)
• 物理性质与化学性质在非手性环境中相 同,在手性环境中有区别。
• 旋光能力相同,但旋光方向相反。
• 3. 手性分子构型表示法
• 构型是表示分子中原子或基团在空间 的排列,手性分子构型就是表示手性碳 原子相连的四个原子或基团在空间的排 列。它的表示方法有:
• 这样旋光方向和构型联系起来,也即D( + ) - 甘 油 醛 , 它 的 对 应 体 L-(-)- 甘 油 醛。其他化合物的构型以甘油醛的构型 为参照标准,在保持手性碳构型不变中, 可由D型甘油醛转化来的化合物就是D型,
• 可由L型甘油醛转化来的化合物就是L型。
D-(+)-甘油醛
D-(-)-甘油酸
• 与甘油醛相关联的手性化合物都可用D/L 来标记。此种命名法主要对葡萄糖、氨 基酸类化合物。适用范围有限。
• 与甘油醛不相关联的手性化合物就不可 用D/L法来标记只能用IUPAC规定的R/S 法来标记。
• R/S构型标记法(绝对)规定:
• A、首先按次序规则确定与手性碳原子连 接的四个不同的原子或基团a,b,c,d的先后 次序(排大小)a>b>c>d ‘>’表示“优先 于”
• 分析分子中有无对称元素。若分子中没有对称 面也没有对称中心,一般为手性分子,具有旋 光性;否则为非手性分子。
•
• 1 对称面(Plane of symmetry):如果假想一 个平面将分子一分为二切开,两部分互为镜像, 这个平面就成为该分子的对称面,用σ表示。 有对称面的分子一定是非手性分子,没有旋光 性。
• ·手性化合物的特点: • 结构:镜像与实物不重合。 • 内能相同(左、右旋)
• 物理性质与化学性质在非手性环境中相 同,在手性环境中有区别。
• 旋光能力相同,但旋光方向相反。
• 3. 手性分子构型表示法
• 构型是表示分子中原子或基团在空间 的排列,手性分子构型就是表示手性碳 原子相连的四个原子或基团在空间的排 列。它的表示方法有:
2019年对映异构.ppt
观察
b CH3
Br a
次序: Br>CH3>D>H
S-构型
d H
aC H2N
H3Cc
b COOH
S-构型
b CH=CH2
d H
C
Pah
CcH(CH3)2
R-构型
对Fischer投影式中C* 构型的标定 (1)、当最小基在竖键上时:
例如:
COOH
观察 COOH
HO
CH3
HO C
CH3
H
R构型
H
观察者远离了最小基
H
S
COOH
HOOC
S
H
COOH
H
R
R
H
HOOC
反:有对异构映体
当两个取代基不同时:
Br
Cl
Br Cl Cl Br H Cl Cl H
S
RS
RR
RS
S
HH
HH
顺
Br H H 反
Br
无论顺、反,分子中都无对称面,都有 对映异构体。
六元环 1,2-二取代
Cl Cl
HH
有对称面 无对映异构体
H Cl
Cl H
O
B. 构象异构体
CH3 CH3
CH3
1
CH3
2
CH3 CH3
1
C. 顺反异构体
• 构型异构中的对映异构和非对映异构 偏振光 —— 普通光在通过尼克尔棱镜
后形成的只在一个方向传播的平面光。
光学活性 —— 物质能使偏振光发生 偏转的性质。
旋光仪
旋光度 旋光活性物质使偏振光振动平面旋转的
角度,用“a ”表示。
顺反异构和对映异构
H2C
CH C
CCH 2 CH3
CH3 CH 2 CH3
Z型
可编辑ppt
10
H
CH2 CH3
CC
CH3
H
E型
-I>-Br>-Cl>-SO3H>-F>-OCOR>-OR >-OH>-NO2>-CCl3>-CHC12>-COCl> -CH2Cl>-COOR>-COOH>-CONH2> >-CHO>-C6H5>-CHR2>-CH2R>-CH3> -D>-H
可编辑ppt
18
可编辑ppt
19
平面偏振光
普通光在所有可能的平面上
振动。
普通光
如果使单色光通过尼可尔( Nicol) 棱镜,只有同棱镜晶轴平行的平面上
振动的光线才可以通过棱镜,因此通
过振这 动种 ,棱 这镜种的只光在线一就 个只 平在 面一 上个 振平 动面 的上光平面偏振光
就是平面偏振光。
可编辑ppt
20
旋光仪
旋光仪示意图
在盛液管中放入旋光性物质后,偏振光将发生偏
转。能使偏振光向右旋转的,称为右旋化合物,用
(+)表示; 能使偏振光向左旋转的,称为左旋化合物
,用(-)表示。
可编辑ppt
21
旋光度
旋光性物质使偏振光旋转的角度称为旋光 度,用α表示.
物质旋光度α的大小与盛液管的长度、溶液 的浓度、光源的波长、测定时的温度、所用 的溶剂的有关。
然的联系。顺式构型不一定是Z构型;反式构 型也不一定是E构型。
H3C
CH3
CC
Cl
H
H3C
H
CC
Cl
CH3
顺-2-氯-2-丁烯
反-2-氯-2-丁烯
