chapter2环烷
有机化学课件Chapter环烷烃和芳香烃

9
2
1
3
8 6
4
7
5
8-甲基二环[4. 3. 0]壬烷
8-methylbicyclo[4. 3. 0]nonane
7
6 54
1 2
3
2, 7, 7-三甲基二环[2. 2. 1]庚烷
2, 7, 7-trimethylbicyclo [2. 2. 1]heptane
7
4
5
3
1
6
2 用","隔开
三环[2. 2. 1. 02, 6]庚烷
23
第四章 环烷烃和芳香烃
有机化学课件
24
第四章 环烷烃和芳香烃
4
Boat Conformer
Conformational Energy
有机化学课件
25
第四章 环烷烃和芳香烃
有机化学课件
26
第四章 环烷烃和芳香烃
直立键和平伏键(Axial and Equatorial Bonds)
四、单取代环己烷
Long-chain
有机化学课件
14
第四章 环烷烃和芳香烃
二、环大小与化学性质
五元以上 环烷烃
性质相似
链状烷烃
Cl2 / hv
Cl 自由基取代反应
H2 / Pt 催化加氢
HI
不反应 不反应
有机化学课件
15
第四章 环烷烃和芳香烃
三、小环化合物的特殊性质 —— 开环加成
1. 催化加氢
H2 / Pt, 50oC or Ni, 80oC
椅式构象的画法
有机化学课件
35
第四章 环烷烃和芳香烃
有机化学课件
36
Chapter 2 summary

Chapter 2 summary所有的碳碳键都为单键的烃称为烷烃。
烷烃常常被看作饱和烃,偶尔也称为脂肪族化合物。
他们的分子通式为C n H2n+2. 所有的碳原子都连接成环状的烷烃称为环烷烃。
环烷烃比开链烷烃少两个氢原子,所以他的通式为C n H2n ,在烷烃中的所有碳原子都为SP3杂化,碳碳键和碳氢键都为σ键。
在乙烷中的C─C单键是C的SP3杂化轨道头碰头重叠形成的。
异构体是由于碳原子连接方式的不同造成的,可以分为碳链异构和骨架异构体。
根据他们键的程度分四种碳原子,伯碳原子,仲碳原子,叔碳原子,季碳原子。
通常,烷烃的命名有两种方式,普通命名法和IUPAC 命名法。
原子绕C─C键旋转造成的不同的空间排列方式称为构象。
构象异构属于立体异构。
但是,不同的构象稳定性是不同的,最稳定的构象是交叉式,最不稳定的是重叠式。
甲烷的氯代反应是典型的自由基取代反应,反应是被光或热激发的。
自由基取代反应通常要求3个步骤,链引发,链增长,链终止。
烷基自由基的稳定性顺序按下列次序排列,叔碳自由基>仲碳自由基>伯碳自由基>甲基自由基。
氢原子的反应活性和氢原子被取代的类型之间存在相关性。
叔氢最活泼,其次是仲氢,最不活泼的是伯氢。
环烷烃可以被分成单环化合物,双环化合物等。
因为C─Cσ键的完全旋转是不可能的,二元取代的环烷烃存在顺反异构体,顺式异构体两个取代基在环的同一侧,反式的在环两侧。
环烷烃发生卤代反应但不容易发生氧化反应。
环戊烷和环丁烷都容易发生开环的加成反应。
环己烷存在船式(pucker折叠车)和无张力的椅式构象,所有的键角都是109o,所有相邻的C─H键都是交叉式的。
椅式环己烷有两种键,直立键和平伏键,椅式环己烷可以发生环的翻转,使直立键与平伏键的位置互换。
环上有取代基时,取代基在平伏键比在直立键更稳定。
New words and phrasesHydrocarbonesCycloalkaneHybridizedSigmaOverlapIsomerismPrimarySecondaryTertiaryQuaternaryNomenclatureStagger staggeredEclipsed 月食,蚀,使……黯然失色ChlorinationInitiation propagation terminationMonocyclic Hydrogen Stereoisomers Halogenated Pucker Equatorial Axial。
二环壬烷结构式

二环壬烷结构式
二环壬烷是一种有机化合物,化学式为C9H18,属于烷烃类化合物。
它的结构式如下所示:
CH3-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH3
二环壬烷是由九个碳原子和十八个氢原子组成的。
在这个分子中,九个碳原子形成了一个环状结构,每个碳原子周围都有两个氢原子。
这使得二环壬烷具有较为稳定的分子结构。
二环壬烷是一种无色无味的液体,在常温下为常见的有机溶剂之一。
它具有较低的沸点和闪点,能够在室温下蒸发。
这使得它在工业生产和实验室中有着广泛的应用。
二环壬烷在有机合成中常用作溶剂,能够溶解许多有机物质,提高反应物质的反应速度和反应效率。
二环壬烷的化学性质相对较为稳定,不容易发生化学反应。
它是一种非极性溶剂,不溶于水,但能够溶解一些极性有机物质。
由于其独特的化学性质,二环壬烷在许多领域得到了广泛的应用。
在有机合成中,二环壬烷常用作溶剂来促进反应的进行。
它能够与许多有机物质发生相互作用,提供一个合适的反应环境。
此外,二环壬烷还可用于提取和分离有机物质,具有较好的溶解性能。
除了在实验室中的应用外,二环壬烷还被广泛用于工业生产中。
例如,它可以用作涂料、油漆和染料的溶剂。
此外,二环壬烷还可以
用于制备其他化合物,如表面活性剂、香料和医药中间体等。
二环壬烷是一种常见的有机化合物,具有广泛的应用领域。
它的结构简单,化学性质稳定,能够作为溶剂在有机合成和工业生产中发挥重要作用。
通过对二环壬烷的深入研究和应用,我们可以进一步拓展其在化学领域的应用前景,为人类社会的发展做出更大的贡献。
《有机化学(第二版)》第3章:环烷烃

1-甲基-3-乙基环戊烷
CH2 CH3
1-甲基-4-异丙基环己烷 含双键的脂环烃称为环烯
4 5 6 1 3
1-甲基-4-异丙烯基环己烯 苧烯 4-甲基-1-环己烯
2
如取代基为较长的碳链,将环作为取代基: 3-环己基己烷
19:46
环烷烃的异构
环的大小、侧链的长短及位置不同而产生构造异构体 4C
椅式(chair form)
H H H H H
H H H H
19:46
H H H 透视式
相邻两个碳原子 的C-H键都处在 交叉式的位置
1、3、5碳在同一平面上 2、4、6碳在另一平面上 两个平面相互平行 C3轴对称
纽曼式
丁烷的邻位交叉式
(2)船式构象
H H H
3
19:46
H
1
4
H
5
2
6
H
H
H H
★ 环己烷多元取代物中,体积大的取代基在e位的构象较稳定
H
19:46
两个规则
Hassel规则
带有相同基团的多取代环己烷,如果没有其它因素 的参与,那末在两个构象异构体之间,总是有较多取代基 取e键向位的构象为优势构象。
Barton规则
带有不同基团的多取代环己烷,如果没有其它因素的 参与,那末其优势构象总是趋向于使作用最强的和较强的 基团尽可能多地取e键的向位。
2-溴丁烷
(键断裂的位置是在含氢最多和含氢最少的碳原子之间)
4 氧化反应:
+ KMnO4 不反应
19:46
可与烯烃或炔烃区别开来。
+
O2
++ Co , P
HOOC(CH2)4COOH
有机化学课件有机化学4环烃脂环烃

椅型 稳定
船型 不稳定
环己烷的两种构象可通过C-C单键的旋 转而相互转变;室温下,99.9%以上主要在 椅型构象存在(优势构象)。
为什么椅式构象稳定?
船式环己烷比椅型能量高30kJ/mol,常温下平 衡体系主要以稳定的椅式构象存在。
0.25nm
5
6
1
3
4 2
椅式构象
0.18nm
4
5
6
1
3
2
船式构象
H2 Ni/100℃
CH3CH2CH3 CH3(CH2)2CH3
H2 Pt/300℃
CH3(CH2)3CH3
× H2
(2)加X2 (3)加HX
+ Br2 CCl4 (褪色)
+ HBr
Br
Br
CH2CH2CH2
Br
CH3CH2CH2
用于 鉴别
+ HBr
Br
H
CH3C- CHCH2 CH3 CH3
??
定;大基团在e键上稳定。 • 3.烷烃的化学性质 • 小环似烯,大环似烷
12
谢谢 Thank you
室温下只有环丙烷能反应; 断裂连接取代基最多和最少的键,H加在含H多的C上。
2、取代反应
Cl2 光 Cl2 hv Br2 hv
Cl Cl
Br
(优先取代叔H)
环烷烃总结
• 1. 环的稳定性 • 环己烷 > 环戊烷 > 环丁烷 > 环丙烷 • 2. 环己烷的构象 • 优势构象三原则:椅式构象稳定;e键稳
2
命名:
(1)单环化合物,在同数碳原 子前面加“环”字。
(2)环上有取代基,以环为 母体,按“最先碰面”、“先 小后大”原则编号,一个取代 基可以不标位置。
第二章烷烃

与伯,仲,叔碳原子相连的H原子,分别称为伯,仲,叔H原子
如:
■5. 烷基
——烷烃去掉一个氢原子后的原子团.常用R-,或 (CnH2n+1-)表示,所以烷烃又可用通式RH表示. ◎正烷基:直链烷烃去掉一个末端氢原子所得的原 子团.命名时“正”字常用n-代表. eg:正丙基CH3CH2CH2-, n-丙基 ◎仲烷基:直链烷烃去掉一个仲氢原子所得的烷基。用 “sec-”表示. eg:仲丁基 CH3CH2CH sec-丁基
Chapter 2
烷
烃
(一) 烃的定义 ◎分子中只含有C、H两种元素的有机化合物叫 碳氢化合物,简称烃.
(二) 烃的分类: (1)开链烃(链烃),又叫脂肪烃. 可分为:烷烃 、烯烃 、二烯烃 、炔烃等
(2)闭链烃(环烃).
又分为:脂环烃和芳香烃两类.
§2-1 烷烃的通式、同系列和构造异构
• 烃:分子中只含有C和H两种元素的有机化合物。 • 烷烃:分子中只有C-C和C-H键的脂肪烃, 又叫饱和烃。
§2-5 烷烃的物理性质
1.聚集状态:C1~C4(g) C5~C17 (l) >C17 (s)
2.沸点(b.p.)
①与范德华引力有关: 相对分子量增加,分子间的范德华引力增 加, 导致沸点升高。 ②支链增加影响沸点:降低接触面从而减低分子间 引力。
■同数碳原子的构造异构体中,分子的支链越多, 则沸点越低。 例如: 正丁烷 b.p. - 0.5℃
H2 H2 H3C C C CH3
H H3C C CH3 CH3
烷烃分子中,随着C原子数的增加,构造异构体的数目也越多。
练习:C6H14有多少同分异构体,并写出它们
同分异构体是两种不同的化合物.物理性质有一定的差异.
Chapter 02 饱和烃(烷烃和环烷烃)

1,7-二甲基螺[4.5]葵烷
CH3
2.3 烷烃和环烷烃的结构
2.3.1 碳的SP3杂化和σ键的形成 基态时 C:1S2 2S2 2Px1 2Py1 2Pz0
英文名
结构
methyl
ethyl
H2 C
propyl
H2 C
Iso-propyl
CH3
butyl
Iso-butyl
H2 C CH3 CH
CH3
CH3
C H2
CH3
CH
CH3
CH2(CH2)2CH3
CH3
中文名 英文名 结构
仲丁基 Sec-butyl
CH3
叔丁基 Tert-butyl
CH3 CH3
CH3
单 环 (上 ) 环 炔 烃 碳环数目 双环 多环
(1) 单环环烷烃 1)按成环碳原子数目称为环某烷。
1-甲基-3-乙基环己烷 2)长链作母体,环作取代基。(以下两种情况) 3-甲基-4-环丁基庚烷
1,3-二环己基丙烷
练习:命名以下化合物
H 3C H 2C
C H 2 (C H 2 ) 4 C H 3
H
H
顺-1, 4-二甲基环己烷
反-1, 4-二甲基环己烷
(2) 双环环烷烃(分子的碳架中含有两个饱和碳环的烃) 按两个环的不同的连接方式分为联环、螺环、稠环和桥环 四种。
a)双环桥环烃命名 桥头碳原子:两环共用的碳原子。
桥:两个桥头碳原子之间的碳链或一个键。
(1 ) 桥 (2) 桥 桥头碳 桥 (3) 桥头碳
第二章 饱和烃(Saturated hydrocarbons) (烷烃alkane和环烷烃cyclic alkane )
2 烷烃
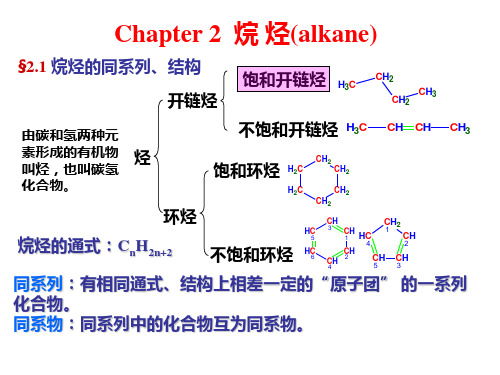
熔点(m.p.) ——直链烷烃随C数增加而升高,趋势变缓。
注意: (1)对同碳数的烃来说,结构对称的分子熔点高;结构对称 的分子在固体晶格中可紧密排列
(2) 含偶数碳原子的正烷烃比奇数碳原子的m.p.高
比重:随分子量的增加而升高!
溶解性:非极性或弱极性,不溶于水及强极
性溶剂中,可溶于氯仿、乙醚、四氯化碳等
4C (季碳,四级碳)
§2.2 烷烃的命名 2.2.1 普通命名法
C1 C2 C3
CH4 CH3CH3 CH3CH2CH3
甲烷 乙烷 丙烷
碳原子数目 + 烷
碳原子数为1~10用天干(甲、乙、丙、……壬、 癸)表示。
⑴ 正:表示直链; ⑵ 异:表示有(CH3)2CH—结构; ⑶ 新:表示有(CH3)3C—结构。
R
H
R
一些常见的烷基
R
CH3 CH3CH2
(烷基)
中文名
甲基 乙基
英文名
methyl ethyl
缩写
Me Et
CH3CH2CH2 CH3 CH3CH
(正)丙基
n-propyl
n-Pr
异丙基
isopropyl
i-Pr
R
(烷基)
中文名
(正)丁基
英文名
n-butyl
缩写
n-Bu
CH3CH2CH2CH2 CH3 CH3CH2CH
溶剂中。(相似相溶)
§2.5 烷烃的化学性质
烷烃的结构
C
电负性 2.5
H
2.2
C
C
H
sp3 杂化 已饱和,不能加成
弱极性共价键 H 酸性小,不易被置换
一般情况下烷烃化学性质不活泼、耐酸碱(常用作低极性溶
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1. 氧化反应
环丙烷对氧化剂稳定,不被高猛酸钾、臭氧等氧化剂氧化。 例如:
故可用高猛酸钾溶液来区别烯烃与环丙烷衍生物。 环烃性质小结: (1)小环烷烃(3,4元环)易加成,难氧化,似烷似烯。 普通环以上难加成,难氧化,似烷。 (2)环烯烃、共轭二烯烃,各自具有其相应烯烃的通性。
脂环烃的化学性质与脂肪烃相似,可发生卤化和 氧化反应等。
(甲)加氢
Ni + H2 80。 C Ni + H2 200。 C
+ H2
CH3 CH2 CH3
CH3 CH2 CH2 CH3
Ni 。 300 C
CH3 CH2 CH2 CH2 CH3
(乙)加卤素
+ Br2
CCl4
CH2 CH2 CH2 Br Br
1,3-二溴丙烷
+ Br2 heat
CH2 CH2 CH2 CH2 Br Br
名 称 环丙烷 环丁烷 环戊烷 环己烷 环庚烷 成环 分子燃烧热 碳数 /KJ·mol-1 3 4 5 6 7 2091 2744 3320 3951 4637 -CH2-的 平均燃烧热 /KJ·mol-1 697 686 664 659 662 名称 环辛烷 环壬烷 环癸烷 环十五烷 开链烷烃 成环 碳数 8 9 10 15 -CH2-的 分子燃烧热 平均燃烧热 /KJ·mol-1 /KJ·mol-1 5310 664 5981 665 6636 664 9885 660 659
• 按照分子中所含碳环的数目,可分为:
单环脂环烃
环己烷
CH3
环戊二烯甲基环己烷二环脂环烃十氢化萘 降冰片烷 螺[2,4]庚烷
多环脂环烃
立方烷 棱烷
篮烷 金刚烷
P27习题2.14
(二) 脂环烃的命名
• 单环脂环烃
(1) 在相应烷烃名称前加“环”字,称为“环某烷”; CH3 (2) 使所有取代基编号尽可能小;
The molecular orbital of cyclopropane
在环丙烷分子中,每个C原子中有两个杂化轨道发 生了弯曲,以便倾斜着重叠成键,这样形成的σ键的 电子云不是分布在一条直线上,而是分布在一条曲 线上,这样的σ键称为弯曲σ键,简称弯曲键。
弯曲键的特点:
① σ键的电子云分布在一条曲线上,无对称轴; ② σ键键能小,因而易断裂,易开环; ③ 环的张力大,分子能量高,易开环。
第六章
脂环烃
•(一)环烷烃的分类 •(二)环烷烃的命名 •(三)环烷烃的性质 •(四) 环烷烃的结构与稳定性 •(五) 环己烷及其衍生物的构象 •(六) 脂环化合物的立体异构 •(七) 脂环烃的主要来源和制法 •(八) 环戊二烯 •(九) 甾族化合物
脂环烃是由碳和氢两种元素组成的一类碳环化合物。
(一) 脂环烃的分类
不能用溴褪 色的方法来 区别环烷烃 与烯烃!
1,4-二溴丁烷
(丙) 加卤化氢
+ HBr
CH3CH2CH2 Br
环的断裂发生在取代基最多和取代基最少的碳 原子之间。(符合马氏规则)即:氢加到含氢多的 碳原子上,卤素加到含氢少的碳原子上。
CH3
+ HBr
CH3CH CCH3 CH3 Br
CH3 CH CH2
a a a a a
e e e e e e
环己烷由一种椅型构象翻转为另一种椅型构象 时,原来的a键都变为e键,原来的e键都变为a键。
处于同一平面上 的三个碳原子 椅式构象 立体图
a键
e键
取代环己烷的构象
一、一元取代环己烷的构象 一元取代环己烷中,取代基可占据a键,也可占据e键,但占 据e键的构象更稳定。例如:
环戊烷 “信封式”构象 环的稳定性:环丙烷<环丁烷<环戊烷~环己烷
环己烷是非常重要的环烷烃,这种结构单元在自 然界中广泛存在,其6个碳原子不共平面,碳碳 键角保持正常的109.5,无角张力,它有两种典型 的构象船式构象比椅式构象能量高30KJ/mol,椅 式构象是环己烷最稳定的构象式。
椅式构象
船式构象
另外,环丙烷结构中六对氢原子相重叠,这 也促使环丙烷结构不稳定。
从环丁烷开始,成环碳原子均不在同一平面上。 最大程度地避免了氢原子之间的重叠而引起的分
子的不稳定,尽管如此环丁烷的角张力仍然很大。
蝴蝶型(环丁烷)
环戊烷分子中四个C原子在一个平面,另外一个亚甲基偏离 出平面,整个分子象一个信封,这种结构使碳碳键角保持正 常的109.5。在这种结构中,围绕不同碳碳键轴旋转,不同的 亚甲基转换成信舌,他们处在动态平衡中。
由环丙烷到环戊烷,随环增大,每个亚甲基单元 的燃烧热依次降低;由环己烷开始,亚甲基单元的 燃烧热趋于恒定。
C C C
环丙烷分子轨道图
环丙烷三个碳原子处在同一个 平面,三元环键角应是60,但 环上C原子sp3杂化要求轨道夹 角保持109. 5,这样,在三元环 中每个碳碳单键向内压缩24.8, 以适应环的几何构造。压缩产 生了角张力,使分子能量升高, 环不稳定。易开环。 由于角张 力作用,使得环丙烷和环丁烷 分子稳定性下降,容易发生加 成反应使环打开。
CH2 + HBr
CH3 CH CH2 CH3 Br H
CH3 CH CH3 CH2 CH2 CH3 + HBr
CH3 CH3 CH3 C Br CH CH2 H
(4) 环烯烃的化学性质
亲电加成
+ Br2
反式加成
Br H H Br
反-1,2-二溴环己烷
(四) 环烷烃的结构与稳定性
燃烧热:指1mol化合物完全燃烧生成二氧化碳和 水所放出的能量,其大小反映了分子能量的高低。
1
3
环己烷椅式构象:无角张力,也无扭转张力, 是无张力环。
2)船式构象
扭转张力
H 1 H 4 2 3 H H H 5 6 H H H
H H
室温下,环己烷的各构象异构体中,椅式构象为优势构象, 在异构体中最高占99.9%。
椅型构象和船型构象可以互相转变。船型环己 烷比椅型能量高30kJ· -1,常温下平衡体系主要以 mol 稳定的椅型构象存在。
H CH 3 CH 3 H
CH3 CH3
顺-1,4-二甲 基环己烷 若用构象式可表示为:
CH3 CH3
CH3
反-1,4-二甲 基环己烷
H3C
CH3
CH3
顺-1,4-二甲基环己烷
反-1,4-二甲基环己烷
(七) 脂环烃的主要来源和制法
脂环烃主要来源于石油。 (1)芳香族化合物催化氢化
OH
。 Ni,150~200 C + 3H 2 1.5MPa
(1)工业来源和制法
环戊二烯主要存在于煤焦油分馏苯的头馏分和石油馏分热 裂解的C5馏分中。目前工业上是利用分离C5馏分获得。
+
℃002~
100℃
实验室是通过二聚环戊二烯加热裂解的方法来制 备纯的环戊二烯的。
介绍 甾族化合物
甾族化合物的结构特征是包含一个四环稠合的碳环骨架, CH3 同时还有三个侧链。
2
2
4
CH3
8 CHCH5 6 3 6 5
3 CH2 4
2,8-二甲基-1-乙基二环[3.2.1]辛烷
(2) 螺环烷烃
共用一个碳原子的双环化合物, 共用碳原子称为螺原子。
按照“小环—螺原子—大环”的顺序编号,并使不 饱和键或取代基的位次尽可能小。
7 6 5 4 3 2 1
螺[2.4]庚烷
螺[5.5]十一烷
0.25nm
5 6 3 4 2
H 5 H H 3 H 4 H H H 6 H H 2 H
0.18nm
1
4 5 6 1
3
H 1 H
2
H H 4 H 5 H 3 H H 6 H 2 H H
H 1 H H
船型分子中 存在扭转张 力和氢原子 之间的非键 张力
在椅式构象中,环己烷中的碳氢键可分为两种类型,
每个碳原子上有一个a键和一个e键,在环中上下交替 排列。 a
R
甾环结构
1 2 3
NaI,乙醇
OH
(2) 分子内关环 (Wurtz反应)
Br
Br
Br + Zn
Cl + 2Na
,80%
二 恶烷 回流,78%~94%
+
ZnBr2
+
。 30 C 100%
NaCl + NaBr
(3) 其它方法
+
CHO
CHO
(八) 环戊二烯
1,3-环戊二烯简称环戊二烯。是具有特殊臭味的无色液体, 沸点41~42℃,相对密度0.805。
多取代的环己烷,一般取代基处于e键最多的构象最 稳定。例如杀虫剂六六六的最稳定构象是β-异构体 而不是γ-异构体:
Cl Cl
Cl
Cl
Cl
Cl
Cl Cl Cl Cl Cl Cl
γ-异构体(高活性)
β-异构体(低活性)
(六) 脂环化合物的顺反异构
当环上连有有两个或两个以上取代基时, 产生顺反异构。
H H
7 1 2 4 3 5 6
1 7 CH2
2
CH
CH2
8 CH2 3 CH2
CH2 CH
6 5
CH2
4
2-甲基双环[2.2.1]-2-庚烯,
双环[3.2.1]辛烷
5
1 6 7 5 3 2
4 3 CH3 2
6 1
7
CH3 CH3
4
7,7-二甲基二环[2.2.1]庚烷
CH2CH3 1
7 1
7 3
3,7,7-三甲基二环[4.1.0]庚烷
CH3
6 5 4 3 1 CH3 2 CH3
