高中化学试卷 物质的量计算
高中化学 物质的量浓度计算练习题

物质的量浓度计算一、选择题(每小题有一个或两个正确选项符合题意)1、标准状况下,a L HCl气体溶于1000g水中,得到的盐酸的密度为bg·cm—3,则该盐酸的物质的量浓度为A、a / 22.4摩·升—1B、ab / 22.4摩·升—1C、ab / (22400 + 36.5a )摩·升—1D、1000ab / (22400 + 36.5a )摩·升—12、 100毫升0.3摩·升—1的硫酸钠溶液和50毫升0.2摩·升—1的硫酸铝溶液混合后,溶液中硫酸根的物质的量浓度为A、0.20摩·升—1B、0.25摩·升—1C、0.40摩·升—1D、0.50摩·升—13、密度为d g·cm—3的溶液V毫升,含有式量为M的溶质mg,其物质的量浓度为c摩·升—1,质量分数为W%,下列表示式不正确的是A、c = 1000m / VMB、m=dV W/100C、d= cM/10WD、W%= (cM/1000d)%4、 VmLAl2(SO4)3溶液中含有a g Al3+,取出V/4 mL溶液,加水稀释到4V mL,则稀释后溶液中SO42—的物质的量浓度为A、125 a / 9V摩·升—1B、125 a / 18V摩·升—1C、125 a / 36V摩·升—1D、125 a / 54V摩·升—15、 0.5L 1摩·升—1FeCl3溶液与0.2 L 1摩·升—1的KC1溶液中,Cl—的浓度比为A、15:2B、1:1C、3:1D、1:36、有一未知浓度的硫酸溶液25mL,在加入0.5摩·升—1的Ba (NO3)2溶液25mL后,改加NaOH 溶液,结果用去1.0摩·升—1NaOH溶液50mL恰好完全反应,则硫酸的物质的量浓度为A、0.5摩·升—1B、1.0摩·升—1C、1.5摩·升—1D、2.0摩·升—17、实验室里需用480mL0.1摩·升—1的硫酸铜溶液,现选取容量瓶进行配制,以下操作正确的是A、称取7.68g无水硫酸铜,加入500毫升水B、称取12.0g胆矾配成500毫升溶液C、称取8.0g无水硫酸铜,加入500毫升水D、称取12.5g胆矾配成500毫升溶液8、已知25%的氨水的密度为0.91 g·cm—3,5%氨水的密度为0.98 g·cm—3,若将上述两溶液等体积混合,所得氨水的溶液的质量分数为A、等于15%B、大于15%C、小于15%D、无法确定二、填空题9、某温度下,22%的硝酸钠溶液150毫升,加100克水稀释后浓度为14%,原溶液的物质的量浓度为_________ 。
(完整版)高一化学物质的量计算题

化学练习: 班级___________姓名___________1。
如果a g 某气体中含有的分子数为b ,则c g 该气体在标准状况下的体积是( )(式中N A 为阿伏加德罗常数的值) A. A cN ab 4.22L B 。
A aN bc 4.22L C 。
AbN ac 4.22L D. A acN b 4.22L 2.N A 为阿伏加德罗常数的值,下列有关说法正确的是( )A. 标准状况下,相同体积的氢气与水所含的分子数目相同B. 标准状况下,22.4L 以任意比混合的氢气、二氧化碳的混合气体所含的分子数为N A 的数值C. 常温常压下,铁与盐酸发生置换反应,生成22。
4L 氢气,则参加反应的铁原子的个数为N A 的数值D. 标准状况下,22。
4L He 所含核外电子数为4 N A 的数值3。
从2 L 物质的量浓度为1 mol ·L 1-的NaOH 溶液中取出100mL 溶液,下面关于这100mL 溶液的叙述错误的是( )A 。
物质的量浓度为0.1 mol ·L 1- B. 物质的量浓度为1 mol ·L 1-C. 含4g 氢氧化钠D. 含0.1 mol 氢氧化钠4。
下列说法中正确的是( )A. 阿伏加德罗常数约等于6。
02×1023mol 1-B. 一摩氧约含6。
02×1023个氧原子C. 摩尔是表示物质的质量的单位 D 。
12g 12C 含有的碳原子数就是6.02×10235 。
下列说法正确的是( )A. 在常温下,常压下,11.2L N 2含有的分子数为0.5 N AB. 标准状况下,22。
4L H 2和O 2的混合物所含分子数为N AC. 标准状况下,18g H 2O 的体积是22.4LD. 1 mol SO 2的体积是22。
4L6 . 对相同状况下的12C 18O 和14N 2两种气体,下列说法正确的是( )A 。
高中化学 物质的量怎么算

物质的量定义:物质的量是表示物质所含微粒数(N)(如:分子,原子等)与阿伏加德罗常数(NA)之比,即n=N/NA。
它是把微观粒子与宏观可称量物质联系起来的一种物理量。
其表示物质所含粒子数目的多少。
公式:物质的量=物质所含微粒数目/阿伏加德罗常数,用符号表示:n =N/N A阿伏加德罗常数N A:把6.02×1023mol-1叫作阿伏加德罗常数。
物质的量是国际单位制中7个基本物理量之一。
7个基本的物理量分别为:长度(单位:m)、质量(单位:kg)、时间(单位:s)、电流强度(单位:A)、发光强度(单位:cd)、温度(单位:K)、物质的量(单位:mol)。
它和“长度”,“质量”,“时间”等概念一样,是一个物理量的整体名词。
其符号为n,单位为摩尔(mol),简称摩。
物质的量计算公式溶质的物质的量=溶质的物质的量浓度x溶液的体积n=cv物质的量=微粒数/阿伏伽德罗常数(n=N/Na)物质的量=物质的质量/物质的摩尔质量(n=m/M)物质的量=气体的体积/气体的摩尔体积(n=V/Vm)误区提醒阿伏加德罗定律只适用气体,对固体、液体物质不适用。
只有温度、压强、体积都相同的气体,其分子数才相同。
气体摩尔体积是阿伏加德罗定律的具体体现。
使用摩尔作单位时,应该用化学式符号指明粒子种类,而不能用名称。
否则,概念模糊,意义不清。
知识网络:基本公式:物质的量与微粒个数的关系: n=(2) 物质的量与质量的关系: n= M=m=M·n(3) 气体物质的量与体积的关系:n= n=(标准状况) Vm = V=(4) 物质的量浓度:c= n=c·V(5) 溶液物质的量浓度与质量分数的关系: c =(密度的单位:g/cm3 ) n=(6) 溶液稀释: c1V1=c2V2物质的量的相关知识和概念:物质的量:是表示大量粒子集体的一个物理量,符号为n,单位是摩尔(mol)。
摩尔:是物质的量的单位;国际上规定, 1摩尔粒子集体所含的粒子数与0.012 kg C中所含的碳原子数相同,约为6.02×1023阿伏加德罗常数:1摩尔的任何粒子的粒子数,即1摩尔粒子数的准确值,用符号NA表示,NA的近似值为6.02×1023mol-1。
高考化学物质的量综合经典题

高考化学物质的量综合经典题一、高中化学物质的量1.在实验室里,用足量的浓盐酸与一定量的高锰酸钾反应(不加热),来制取氯气。
反应:2KMnO 4+16HCl=2KCl+2MnCl 2+5Cl 2↑+8H 2O(1)“双线桥法”标出电子转移情况________ 。
(2)若生成2.24L 标准状况时的氯气,请计算(写出必要的计算过程):①理论上需要多少克KMnO 4参加反应?________。
②被氧化的HCl 的物质的量为多少?________。
【答案】 6.32g 0.2 mol【解析】【分析】(1)根据元素化合价升降数目等于反应过程中电子转移数目分析,标出电子转移情况;(2)先计算Cl 2的物质的量,然后根据方程式中KMnO 4、HCl 与Cl 2之间的反应转化关系计算。
【详解】(1)在该反应中,Mn 元素化合价由反应前KMnO 4中的+7价变为反应后MnCl 2中的+2价,化合价降低,得到5个电子,Cl 元素化合价由反应前HCl 中的-1价变为反应后Cl 2中的0价,化合价升高,失去2个电子,电子得失最小公倍数是10,所以KMnO 4、MnCl 2前的系数是2,HCl 前的系数是10,Cl 2前的系数是5,根据原子守恒,KCl 的系数是2,这样反应中有6个Cl 原子未参加氧化还原反应,所有Cl 原子都是由HCl 提供,因此HCl 前的系数为10+6=16,结合H 原子反应前后相等,可知H 2O 的系数是8,用“双线桥”表示电子转移为:;(2)在标准状态下, 2.24LCl 2的物质的量n(Cl 2)=m V 2.24L V 22.4L /mol=0.1mol 。
①根据反应的化学方程式可知:生成0.1molCl 2时,参与反应的KMnO 4的物质的量为0.1mol×25=0.04mol ,则参与反应的KMnO 4的质量m(KMnO 4)=0.04mol×158g/mol=6.32g ; ②由反应化学方程式可知,HCl 被氧化后生成Cl 2,因此根据Cl 元素守恒可知:被氧化的HCl 的物质的量n(HCl)氧化=0.1mol×2=0.2mol 。
人教版高中化学物质的量计算专项练习题(含答案解析)

人教版高中化学物质的量计算专项练习题一、选择题1.下列说法正确的是.下列说法正确的是( ( ( )A .同温、同压下,相同质量的气体都占有相同的体积.同温、同压下,相同质量的气体都占有相同的体积B .同温、同压下,相同体积的气体都含有相同数目的分子.同温、同压下,相同体积的气体都含有相同数目的分子C .在标准状况下,.在标准状况下,1 mol 1 mol任何物质的体积均约是22.4 L D .1 mol 某气体的体积约为22.4 L ,该气体所处的状况一定是标准状况,该气体所处的状况一定是标准状况,该气体所处的状况一定是标准状况 【答案】【答案】B B【解析】根据阿伏伽德罗定律可知;同温、同压、同体积的任何气体都具有相同的粒子数,“三同定一同”,数,“三同定一同”,B B 项正确。
项正确。
A A 项,质量相同的不同气体的物质的量不一定相同,错误;水在标准状况下不是气体,体积也不为22.4 L ,故C 项错误;项错误;1 1 mol 某气体若处于高温、高压或低温、低压的情况下,气体体积也可能约为22.4 L ,故,故D 项错误。
项错误。
2.N A 代表阿伏加德罗常数,下列说法正确的是代表阿伏加德罗常数,下列说法正确的是( ( ( )A .2.3 g Na 变成Na +时,失去的电子数为0.2N AB .0.2N A 个H 2SO 4与19.6 g H 3PO 4含有相同的氧原子数含有相同的氧原子数C .28 g N 2所含的原子数为N AD .N A 个O 2与N A 个H 2的质量之比为8:18:1【答案】【答案】B B【解析】【解析】Na Na +为+为+11价,价,2.3 2.3 g Na 为0.1 mol mol,失去的电子数为,失去的电子数为0.1N A ,A 项错误;项错误;19.6 19.6 g H 3PO 4即为0.2 mol ,含有,含有0.2N A 个H 3PO 4,等物质的量的H 2SO 4与H 3PO 4含有相同的氧原子数,数,B B 正确;正确;28 g N 28 g N 2即1 mol(28 g÷28 g·mol-1=1 mol),应含,应含2N A 个N ,C 错误;N A 个O 2的物质的量为1 mol mol,,其质量为32 g ,N A 个H 2的质量为2 g ,则二者质量之比为16:116:1,,D 错误。
高一化学必修一物质的量计算题

高一化学必修一物质的量计算题高一化学必修一物质的量计算题如下:一、选择题1.在标准状况下,烧瓶内充满HCl气体,将此烧瓶倒扣在盛水的水槽内,当液面上升到烧瓶容积的时,此时烧瓶内溶液的物质的量浓度为()A.0.74mol/LB.0.045mol/LC.0.037mol/LD.0.025mol/L规律:烧瓶中充有任何溶于水的气体,当气体溶于水后,其溶液的物质的量浓度皆是mol/L或0.045mol/L。
(无论该气体是否充满容器;无论是否混有不反应、且不溶于水的气体。
)若烧瓶容积为VL,即mol,若气体全部溶于水,溶液体积为VL,相除得到mol/L;若液面上升到烧瓶容积的时,气体的物质的量为mol×,溶液的体积也是VL,相除依然是mol/L。
2.用mg10%的NaOH溶液,蒸发掉4g水后,余下溶液10mL,溶质的质量分数为15%,浓缩后碱液的物质的量浓度是()A.1.8mol/LB.2.3mol/LC.3mol/LD.4.4mol/L3.将硫酸钾、硫酸铝、硫酸钾铝三种盐混合溶于硫酸酸化的水中,测得c()=0.105mol/L,c(Al3+)=0.055mol/L,溶液的pH=2.0(假设溶液中H2SO4完全电离为H+和),则c(K+)为()A.0.045mol/LB.0.035mol/LC.0.055mol/LD.0.040mol/L4.由2mol/L磷酸溶液和2mol/L磷酸溶液各50mL组成的混合溶液的物质的量浓度是()A.1mol/LB.2mol/LC.3mol/LD.4mol/L5.AL硫酸铝溶液中,含有Bmol铝离子,则此溶液的物质的量浓度是()A.mol/LB.mol/LC.mol/LD.mol/L6.配制500mL0.1mol/L硫酸铜溶液,需用胆矾()A.8.00gB.16.0gC.25.0gD.12.5g7.在100mL0.1mol/LNaOH的溶液中,所含NaOH的质量是()A.40gB.4gC.0.4gD.0.04g8.将等体积的氯化铝溶液和氢氧化钾溶液混合,所得沉淀物中含铝元素的物质的量与反应之后混合溶液中含铝元素的物质的量相等。
高考化学物质的量综合经典题含详细答案

高考化学物质的量综合经典题含详细答案一、高中化学物质的量1.(1)有相同物质的量的 H2O 和 H2SO4,其质量之比为_____,氢原子个数比为_____,氧原子个数比为_____。
(2)把 3.06 g 铝和镁的混合物粉末放入 100 mL 盐酸中,恰好完全反应,并得到标准状况下 3.36 L H2。
计算:①该合金中铝的物质的量为_____。
②该合金中镁的质量为_________。
③反应后溶液中 Cl﹣的物质的量浓度为__________(假定反应体积仍为 100 mL)。
(3)由 CO2与 CO 组成的混和气体对 H2的相对密度为 20,则混和气体中 CO2的体积分数为_____; CO 的质量分数为_____。
【答案】9:49 1:1 1:4 0.06 mol 1.44 g 3.0 mol·L-1 75% 17.5%【解析】【分析】【详解】(1)n (H2O)= n (H2SO4) ,m (H2O):m (H2SO4)= n (H2O)×18:n (H2SO4)×98= 9:49;N H(H2O) :N H(H2SO4)= n (H2O)×2:n (H2SO4)×2=1:1; N O(H2O) :N O(H2SO4)= n (H2O)×1:n (H2SO4)×4=1:4;(2)设镁的物质的量为xmol,铝的物质的量为ymol,二者混合物的质量为3.06=24x+27y;根据化学反应的计量系数比:Mg~2HCl~H2,2Al~6HCl~3H2,氢气的体积标准状况下3.36 L,n (H2)=0.15mol,列式x+1.5y=0.15,解方程x=0.06 mol,y=0.06 mol,故该合金中铝的物质的量为0.06 mol,该合金中镁的质量为0.06×24=1.44g,反应后溶液中Cl¯(盐酸恰好反应完全,溶液中溶质只有氯化镁和氯化铝)的物质的量=0.06×2+0.06×3=0.3mol,溶液体积100mL,Cl¯的物质的量浓度c=nV=3.0 mol·L-1;(3)由CO2与CO组成的混和气体对H2的相对密度为20,密度之比等于摩尔质量之比,则混合气体的平均摩尔质量为40g/mol,设1mol混合气体中有xmol CO,CO2ymol,故x+y=1,28x+44y=40,则x =0.25mol,y =0.75mol,同温同压,气体体积之比等于物质的量之比,则混和气体中CO2的体积分数为75%,CO的质量分数=0.25×28/40=17.5%2.纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。
高考化学物质的量的综合题试题及答案解析
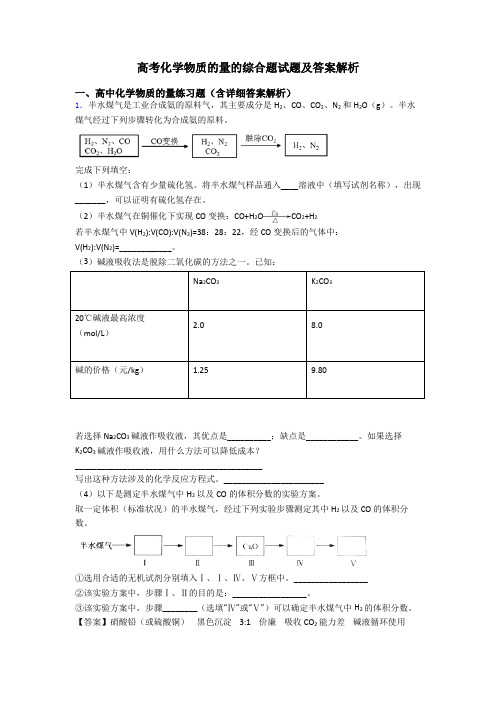
高考化学物质的量的综合题试题及答案解析一、高中化学物质的量练习题(含详细答案解析)1.半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2和H2O(g)。
半水煤气经过下列步骤转化为合成氨的原料。
完成下列填空:(1)半水煤气含有少量硫化氢。
将半水煤气样品通入____溶液中(填写试剂名称),出现_______,可以证明有硫化氢存在。
(2)半水煤气在铜催化下实现CO变换:CO+H2O CO2+H2若半水煤气中V(H2):V(CO):V(N2)=38:28:22,经CO变换后的气体中:V(H2):V(N2)=____________。
(3)碱液吸收法是脱除二氧化碳的方法之一。
已知:Na2CO3K2CO320℃碱液最高浓度(mol/L)2.08.0碱的价格(元/kg) 1.259.80若选择Na2CO3碱液作吸收液,其优点是__________;缺点是____________。
如果选择K2CO3碱液作吸收液,用什么方法可以降低成本?___________________________________________写出这种方法涉及的化学反应方程式。
_______________________(4)以下是测定半水煤气中H2以及CO的体积分数的实验方案。
取一定体积(标准状况)的半水煤气,经过下列实验步骤测定其中H2以及CO的体积分数。
①选用合适的无机试剂分别填入Ⅰ、Ⅰ、Ⅳ、Ⅴ方框中。
_________________②该实验方案中,步骤Ⅰ、Ⅱ的目的是:_________________。
③该实验方案中,步骤________(选填“Ⅳ”或“Ⅴ”)可以确定半水煤气中H2的体积分数。
【答案】硝酸铅(或硫酸铜)黑色沉淀 3:1 价廉吸收CO2能力差碱液循环使用2KHCO3→K2CO3+CO2↑+H2O除去半水煤气中的CO2(包括H2S)和H2O IV【解析】【分析】【详解】(1)硫化氢能与重金属生成沉淀,所以将半水煤气样品通入硝酸铅(或硫酸铜)溶液中,出现黑色沉淀可以证明有硫化氢存在。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2017年9月10日高中化学试卷
1、在100mL的混合液中,硝酸和硫酸的物质的量浓度分别是0.3mol•L﹣1、0.15mol•L﹣1,向该混合液中加入2.56g铜粉,加热,待充分反应后,所得溶液中铜离子的物质的量浓度是()
A、0.15 mol•L﹣1
B、0.225 mol•L﹣1
C、0.30 mol•L﹣1
D、0.45 mol•L﹣1
2、在100mL某混合溶液中,c(HNO3)=0.2mol•L﹣1,c(H2SO4)=0.1mol•L﹣1,向其中加入1.92g Cu 粉,微热充分反应后溶液中的c(Cu2+)为()
A、0.15 mol•L﹣1
B、0.3 mol•L﹣1
C、0.225 mol•L﹣1
D、无法计算
3、相对分子质量为M的气态化合物vL(标准状况),溶于mg水中,得到质量分数为w的溶液,物质的量浓度为cmol•L﹣1,密度为ρg•c m﹣3,则下列说法不正确的是()
A、相对分子质量M=
B、物质的量浓度c=
C、质量分数w=
D、溶液密度ρ=
4、设N A为阿伏伽德罗常数的值,下列叙述正确的是()
A、标准状态下,33.6L三氧化硫中含有硫原子的数目为1.5 N A
B、12g石墨烯(单层石墨)中含有六元环的个数为0.5 N A
C、50mL18.4mol•L﹣1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46 N A
D、标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1 N A
5、将50g质量分数为ω1,物质的量浓度为C1的浓硫酸沿玻璃棒加入到VmL水中,稀释后得到质量分数为ω2,物质的量浓度为C2的稀溶液.下列说法中正确的是()
A、若C1=2C2,则ω1<2ω2,V<50Ml
B、若C1=2C2,则ω1<2ω2,V>50mL
C、若ω1=2ω2,则C1<2C2,V=50mL
D、若ω1=2ω2,则C1>2C2,V<50Ml
6、下列图象表达正确的是()
A、浓硫酸的稀释
B、过量的盐酸与等量的锌粉反应
C、氢气与氧气反应中的能量变化
D、微粒电子数
7、将3.20g Cu跟50.0mL10.0mol•L﹣1的HNO3充分反应,还原产物有NO和NO2,若反应后溶液中有xmol H+,则此时溶液中含NO3﹣的物质的量为()
A、mol
B、(x+0.1)mol
C、2x mol
D、0.1x mol
8、使用容量瓶配置溶液时,由于操作不当会引起误差,下列情况会使所配溶液浓度偏低的是()
①用天平称量时所用砝码生锈②用量筒量取所需浓溶液时,仰视刻度
③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,俯视容量瓶的刻度线⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线.
A、②⑤
B、②③⑥
C、①⑤⑥
D、③⑥
9、已知20℃时,饱和NaCl溶液的密度为ρg/cm3,物质的量浓度为c mol/L,则下列说法中不正确的是()
A、温度低于20℃时,饱和NaCl溶液的浓度小于c mol/L
B、此溶液中NaCl的质量分数为
C、20℃时,密度小于ρg/cm3的NaCl溶液是不饱和溶液
D、20℃时,饱和NaCl溶液的溶解度
10、设N A为阿伏加德罗常数的值,下列叙述正确的是()
A、在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,则转移4 N A个电子
B、16g甲基正离子(13CH3+)所含中子数为7N A
C、10.0 mL 18mol/L的浓硫酸中氢离子数为0.36 N A
D、标准状况下,1mol SO3含有的分子数为N A
11、设N A为阿伏加德罗常数的值.下列说法正确的是()
A、标准状况下,2.24 Cl2完全反应生成FeCl3或CuCl2,转移的电子数都为0.2N A
B、18g D2O中含有的电子数为10 N A
C、pH=12的氨水中含有NH4+的数目为0.01 N A
D、28g 由乙烯和CO组成的混合物中含有的原子总数为3N A
12、(2017•浙江)设N A为阿伏伽德罗常数的值,下列说法正确的是()
A、标准状况下,2.24 L乙醇中碳氢键的数目为0.5 N A
B、1 L 0.1 mol•L﹣1硫酸钠溶液中含有的氧原子数为0.4 N A
C、0.1 mol KI与0.1 mol FeCl3在溶液中反应转移的电子数为0.1 N A
D、0.1 mol乙烯与乙醇的混合物完全燃烧所消耗的氧分子数为0.3 N A
13、(2017•海南)N A为阿伏伽德罗常数的值。
下列叙述错误的是( )
A、1 mol 乙烯分子中含有的碳氢键数为4N A
B、1 mol 甲烷完全燃烧转移的电子数为8N A
C、1 L 0.1 mol·L−1的乙酸溶液中含H+的数量为0.1N A
D、1 mol 的CO和N2混合气体中含有的质子数为14N A
14、物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)2.3g 乙醇含有________个H原子,所含共价键的物质的量________,其中所含官能团羟基的电子数为________.
(2)某条件下,8g氧气所占的体积为6L,则在该条件下的气体摩尔体积为________.
(3)100mL硫酸铝溶液中C(Al3+)=0.20mol/L(不考虑水解因素),则其中n(SO42﹣)=________.
(4)在9.5g某二价金属的氯化物中含有0.2mol Cl﹣,此氯化物的摩尔质量为________.
(5)6.72L CO(标准状况)与一定量的Fe2O3恰好完全反应(生成Fe与CO2)后,生成Fe的质量为________ g,转移的电子数目为________.。
