第八章芳烃
合集下载
c8-芳烃

+
E
+
E
1.卤化反应(Halogenation)
◇试剂(卤化剂):Cl2,Br2 ◇催化剂:Fe屑或FeX3 ◇亲电试剂:X+
.. .X . .. .. X. .. .
+
Fe X3
Lewis酸 (缺电 子)
X
. X . Fe X3
络合 物
X
+
+
FeX4
-
◇例:
+ +
C l2
FeCl3 55~60℃ FeB r3 55~60℃
R
O R C X, AlCl3
烷基化反应
Friedel-Crafts 反应 (傅-克反应)
R
O C
酰基化反应
四、苯环上取代反应的定位规律
1.定位规律
CH3 NO2
◇比较三者的硝化反应:
混酸 50~60℃ 98%
NO2
CH3 NO2 CH3 C H3
混酸 30℃ 邻硝基甲苯 58%
CH3
NO2
间硝基甲苯 4%
R
C OAlCl2
◇历程:
H
+
+
R
C
O
+
-H
+
CO R
CO R
AlCl3
C R
l O...Al C 3
产物芳酮与催化剂形成络合物,使 部分AlCl 3 失去催化活性,故AlCl 3 应过量
稀酸处理,AlCl 3 水解
C R
O
游离芳酮
◇例:
设CH3 COCl为1mol AlCl3 (>1mol) 通常为:1.1~1.5
有机化学课件-第八章芳烃

CH3CH2COCl AlCl3
O
Zn-Hg HCl
练习题 8.6
2.芳烃的化学反应
第 八 章 芳 烃
单取代苯的亲电取代反应定位规律: 取代基对反应速率的影响: 苯环上已经存在的取代基会对苯环上继续发生的亲电取代反应 速度产生影响。以苯环为基准: 使亲电取代反应活性提高(供电子)的基团称为活化基团; 使亲电取代反应活性降低(吸电子)的基团称为钝化基团; 旧取代基对新入取代基位置的影响: 苯环上已有的取代基会对第二个取代基引入的位置产生影响; 主要使新取代基进入邻位或对位的称为“邻对位定位基”; 主要使新取代基进入间位的称为“间位定位基”; 常见活化钝化基团和定位取代基见书248页表8-2 练习题 8.7
1.芳烃的分类和命名
第 八 章 芳 烃
当苯环上有俩不同取代基,按照下列顺序决定哪个取代基和苯 环一起作为母体:羧基-COOH > 醛基-CHO > 羟基-OH > 烯基 -C=C-或炔基 > 氨基-NH2 > 烷氧基-OR > 烷基-R > 卤素-X > 硝基-NO2 > 亚硝基-NO 当苯环上有三取代基时,先选出母体官能团,并把它编号为1 ,其他的官能团按编号最小原则顺时针或逆时针沿苯环编号, 书写官能团时依然按照取代基次序原则先后书写; 了解联苯的编号与命名; 了解萘的编号和α位β位; 练习题 8.1 8.2
① ② ③
卤代烃制备小节 可由醇与卤化氢、卤化磷或氯化亚砜反应将羟基转变为卤; 可由烷烃卤代,烯烃α位卤代,苯环卤化铁催化取代; 氟或碘代烷,可以氯、溴代烷置换而来;
2.芳烃的化学反应
第 八 章 芳 烃
苯磺酸的钠盐与碱共熔,可转化为酚的钠盐,经酸化后得酚。
O
Zn-Hg HCl
练习题 8.6
2.芳烃的化学反应
第 八 章 芳 烃
单取代苯的亲电取代反应定位规律: 取代基对反应速率的影响: 苯环上已经存在的取代基会对苯环上继续发生的亲电取代反应 速度产生影响。以苯环为基准: 使亲电取代反应活性提高(供电子)的基团称为活化基团; 使亲电取代反应活性降低(吸电子)的基团称为钝化基团; 旧取代基对新入取代基位置的影响: 苯环上已有的取代基会对第二个取代基引入的位置产生影响; 主要使新取代基进入邻位或对位的称为“邻对位定位基”; 主要使新取代基进入间位的称为“间位定位基”; 常见活化钝化基团和定位取代基见书248页表8-2 练习题 8.7
1.芳烃的分类和命名
第 八 章 芳 烃
当苯环上有俩不同取代基,按照下列顺序决定哪个取代基和苯 环一起作为母体:羧基-COOH > 醛基-CHO > 羟基-OH > 烯基 -C=C-或炔基 > 氨基-NH2 > 烷氧基-OR > 烷基-R > 卤素-X > 硝基-NO2 > 亚硝基-NO 当苯环上有三取代基时,先选出母体官能团,并把它编号为1 ,其他的官能团按编号最小原则顺时针或逆时针沿苯环编号, 书写官能团时依然按照取代基次序原则先后书写; 了解联苯的编号与命名; 了解萘的编号和α位β位; 练习题 8.1 8.2
① ② ③
卤代烃制备小节 可由醇与卤化氢、卤化磷或氯化亚砜反应将羟基转变为卤; 可由烷烃卤代,烯烃α位卤代,苯环卤化铁催化取代; 氟或碘代烷,可以氯、溴代烷置换而来;
2.芳烃的化学反应
第 八 章 芳 烃
苯磺酸的钠盐与碱共熔,可转化为酚的钠盐,经酸化后得酚。
第八章 芳烃

OH NH 2 COOH COOH Cl NO 2 Cl SO3H HO NO 2 NH 2 OCH 3
对氯苯酚
对氨基苯磺酸
间硝基苯甲酸
3-硝基-5-羟基 苯甲酸
2-甲氧基-6氯苯胺
9
第二节 苯及同系物的结构
一、苯的结构
仪器测得: 苯 分 子 中 12 个 原 子 共 平 面 。 所 有 的 C-C 键 长 为 0.140nm,所有的C-H键长为0.108nm,键角∠CCH及 ∠CCC均为120º 。
第八章
芳烃
Aromatic Hydrocarbons
1
芳烃( aromatic hydrocarbons )——芳香族碳氢化合物。 含有苯环的一大类C、H化合物。 “芳香”二字的含义: 过去:天然产物中许多有香味的物质分子中都含有苯环。芳
香二字的来由最初是指从天然树脂(香精油)中提取而得、
具有芳香气的物质。 现在:Hóckel 4n+2规则、以及特殊的化性。不一定具有香 味,也不一定含有苯环结构。 芳香性——易进行离子型取代反应,不易加成、氧化,并具有 特殊的稳定性。 芳香族化合物——具有芳香性的一大类有机化合物
6
记忆方法: 羧基、磺酸、酯、酰卤、酰胺、腈、醛基、酮基、醇羟基、 酚、巯、炔、烯、氨基、烷氧基、烷基、卤素、硝基。
7
(2)二元取代苯的命名
取代基的位置用邻、间、对或1,2; 1,3; 1,4表示。 例如:
CH3 CH3
邻二甲苯 1,2-二甲苯
CH3 CH3
间二甲苯 1,3-二甲苯
CH3
CH3
对二甲苯 1,4-二甲苯
1,2,3,4-四甲苯
CH 3 H3C CH 3
1,2,3,5-四甲苯
对氯苯酚
对氨基苯磺酸
间硝基苯甲酸
3-硝基-5-羟基 苯甲酸
2-甲氧基-6氯苯胺
9
第二节 苯及同系物的结构
一、苯的结构
仪器测得: 苯 分 子 中 12 个 原 子 共 平 面 。 所 有 的 C-C 键 长 为 0.140nm,所有的C-H键长为0.108nm,键角∠CCH及 ∠CCC均为120º 。
第八章
芳烃
Aromatic Hydrocarbons
1
芳烃( aromatic hydrocarbons )——芳香族碳氢化合物。 含有苯环的一大类C、H化合物。 “芳香”二字的含义: 过去:天然产物中许多有香味的物质分子中都含有苯环。芳
香二字的来由最初是指从天然树脂(香精油)中提取而得、
具有芳香气的物质。 现在:Hóckel 4n+2规则、以及特殊的化性。不一定具有香 味,也不一定含有苯环结构。 芳香性——易进行离子型取代反应,不易加成、氧化,并具有 特殊的稳定性。 芳香族化合物——具有芳香性的一大类有机化合物
6
记忆方法: 羧基、磺酸、酯、酰卤、酰胺、腈、醛基、酮基、醇羟基、 酚、巯、炔、烯、氨基、烷氧基、烷基、卤素、硝基。
7
(2)二元取代苯的命名
取代基的位置用邻、间、对或1,2; 1,3; 1,4表示。 例如:
CH3 CH3
邻二甲苯 1,2-二甲苯
CH3 CH3
间二甲苯 1,3-二甲苯
CH3
CH3
对二甲苯 1,4-二甲苯
1,2,3,4-四甲苯
CH 3 H3C CH 3
1,2,3,5-四甲苯
第八章芳烃

C(CH3)3
30 62 7.5 79
12 8.5
甲苯衍生物硝化的实例分析
CH3
CH2Cl
CHCl 2
CCl3
58 38 4 54
32 14 43
23 34 29.2
6.8 64
CH2F
CF3
28
18 54 99
邻 活化
对
位
定
位 中等钝化
间位定位 强钝化
微弱钝化
碳链长短的影响
NO2 CH2NO2
2. 分子轨道理论
反键轨道
E 成键轨道
3. 共振论
Ⅰ 贡献大
Ⅱ
Ⅲ
Ⅳ 贡献小 键长、键角不等 的不等价结构
Ⅴ
键长,键角完全 相等的等价结构
(二)苯衍生物的同分异构、 命名和物理性质
苯(Benzene) 苯基(phenyl) 苄基(benzyl)
(phenyl methyl) 苯基 (Ph)(C6H5-)
CH3
甲苯 Toulene 例如:
CH3
苯乙烯 Styrene
3-乙基甲苯(3-ethyltoulene) 不叫做3-甲基乙苯
CH2CH3
物理性质
芳香烃不溶于水,但溶于有机溶 剂。一般芳香烃均比水轻。沸点随相 对分子质量升高而升高。熔点除与相 对分子质量有关外,还与结构有关, 通常对位异构体由于分子对称,熔点 较高。
F
Cl
Br
I
12 1 87 69
30 0.9 62
37 1.2 58
40 1.8
对位主要受共轭效应的影响
苯酚与乙酰苯胺的实例分析
OH
NHCOCH3
40 60 95
5
第八章 芳烃

ψ4
ψ6 ψ5 简并轨道 简并轨道
ψ2
ψ1
四)共振理论
ψ3
11
二、苯衍生物同分异构体和物理性质 一) 同分异构
CH3 Br NO2 CH3 CH3 CH3
CH3
二) 物理性质 IR:
C C H C ~3030cm 900~600cm 1600,1580,1500,1450cm 12
HNMR: δ6.5~8.0
二). 取代苯的定位效应
Z Z Z
40
40
20
41
供电子取代基对反应的影响:
OH HNO 3 H2SO 4
OH NO 2
OH
OH
+
+
NO 2 NO 2
experimental yield predicted yield
50 40
trace 40
50 20
42
吸电子取代基对反应的影响:
NO 2 HNO 3 H2SO 4 NO 2 NO 2 NO 2 NO 2
+
+
NO 2 NO 2
experimental yield predicted yield
trace 40
93 40
trace 20
43
邻对位和间位定位基对苯环活性的影响
邻对位定位基 对活性的 间位定位基 影响
-NH2(R) -OH
对活性的影响
强活化
+
-NO2
-CF3
-NR3
很强的钝化
强钝化 强钝化
27
R AlCl 3 + RX + HX
For example, benzene reacts with 2-chloropropane
ψ6 ψ5 简并轨道 简并轨道
ψ2
ψ1
四)共振理论
ψ3
11
二、苯衍生物同分异构体和物理性质 一) 同分异构
CH3 Br NO2 CH3 CH3 CH3
CH3
二) 物理性质 IR:
C C H C ~3030cm 900~600cm 1600,1580,1500,1450cm 12
HNMR: δ6.5~8.0
二). 取代苯的定位效应
Z Z Z
40
40
20
41
供电子取代基对反应的影响:
OH HNO 3 H2SO 4
OH NO 2
OH
OH
+
+
NO 2 NO 2
experimental yield predicted yield
50 40
trace 40
50 20
42
吸电子取代基对反应的影响:
NO 2 HNO 3 H2SO 4 NO 2 NO 2 NO 2 NO 2
+
+
NO 2 NO 2
experimental yield predicted yield
trace 40
93 40
trace 20
43
邻对位和间位定位基对苯环活性的影响
邻对位定位基 对活性的 间位定位基 影响
-NH2(R) -OH
对活性的影响
强活化
+
-NO2
-CF3
-NR3
很强的钝化
强钝化 强钝化
27
R AlCl 3 + RX + HX
For example, benzene reacts with 2-chloropropane
第八章 芳烃系列产品(8.1-8.2)
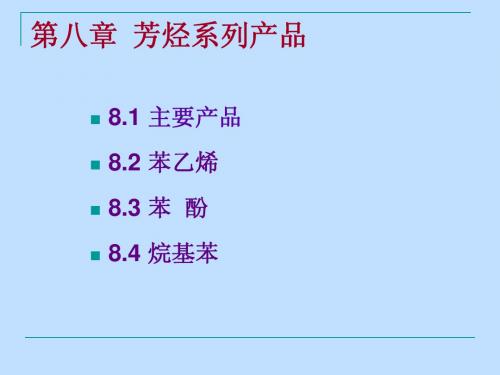
不凝气 冷凝 冷却 200℃ 新鲜丙烯 第一反应器 循 环 苯 加热 200~250℃ 3~4MPa 分离 燃料 放出部分冷 凝液(防止 惰物积累)
C6H5CH=CHC6H5+CH2=CH2 → 2C6H5CH=CH2
2Pb +O2→ 2PbO
② 甲苯和甲醇 →苯乙烯
目前尚处于研究阶段
cat 2C6H5CH3 +2CH3OH → C6H5C2H5 + C6H5CH=CH2
4. 乙烯与苯→苯乙烯
+2H2O +H2
CH=CH2
+
CH2=CH2
+
1/2 O2
High impact poly styrene Styrene Acrylonitrile(苯乙烯-丙烯腈) Acrylonitrile Butadiene Styrene(丙烯腈-丁二烯-苯乙烯) Styrene Butadiene Rubber(丁苯橡胶)
HIPS树脂
SAN树脂
ABS树脂
—用HCl中和 → 苯酚
3. 甲苯氧化法
甲苯在钴盐的作用下,用空气氧化生成苯甲酸,
再在铜cat作用下氧化脱酸成苯酚
C6H5 CH3 + 3/2 O2 Co 2+ 150℃-160℃ C6H5 COOH+ H2 O
氧化→苯甲酸
+1/2 O2
CuO-MgO 230℃-260℃
C6H5OH
+
CO2 氧化脱酸→苯酚
——异丙苯法生产苯酚简介
异丙苯法是目前世界上生产苯酚最主要的方法,其生产 能力约占世界苯酚总生产能力的90%。
C6H5CH=CHC6H5+CH2=CH2 → 2C6H5CH=CH2
2Pb +O2→ 2PbO
② 甲苯和甲醇 →苯乙烯
目前尚处于研究阶段
cat 2C6H5CH3 +2CH3OH → C6H5C2H5 + C6H5CH=CH2
4. 乙烯与苯→苯乙烯
+2H2O +H2
CH=CH2
+
CH2=CH2
+
1/2 O2
High impact poly styrene Styrene Acrylonitrile(苯乙烯-丙烯腈) Acrylonitrile Butadiene Styrene(丙烯腈-丁二烯-苯乙烯) Styrene Butadiene Rubber(丁苯橡胶)
HIPS树脂
SAN树脂
ABS树脂
—用HCl中和 → 苯酚
3. 甲苯氧化法
甲苯在钴盐的作用下,用空气氧化生成苯甲酸,
再在铜cat作用下氧化脱酸成苯酚
C6H5 CH3 + 3/2 O2 Co 2+ 150℃-160℃ C6H5 COOH+ H2 O
氧化→苯甲酸
+1/2 O2
CuO-MgO 230℃-260℃
C6H5OH
+
CO2 氧化脱酸→苯酚
——异丙苯法生产苯酚简介
异丙苯法是目前世界上生产苯酚最主要的方法,其生产 能力约占世界苯酚总生产能力的90%。
第8章 芳烃转化过程
前者适用于从宽馏分中分离苯、甲苯、二甲苯等。 后者适用了从芳烃含量高的炸馏分中分离纯度高的单一芳烃。
8.2 芳烃转化
各种芳烃组分中用途最广、需求量最大的是苯与对二甲苯,其 次是邻二甲苯。
8.2.1 芳烃的脱烷基化
芳烃的脱烷基化:烷基芳烃分子中与苯环直接相连的烷基,在一定的条件下 可以被脱去。 工业上主要应用于甲苯脱甲基制苯、甲基萘脱甲基制萘。
但其共同点是必须经蒸馏除去裂解汽油中C4馏分、部分C9芳烃与C9+馏分,
(2)裂解汽油加氢 裂解汽油加氢是目前普遍采用的精制方法。由于从裂解汽油中除去双烯烃、 单烯烃和氧、氮、硫等有机化合物的工艺条同,—般采用二段加氢精制工 艺。 第一段加氢的目的,将使易生胶的二烯烃加氢转化为单烯烃以及烯基芳烃转 化为芳烃。 这一段加氢在比较缓和的工艺条件下进行,以避免二烯烃聚合。 因此一段加氢多采用它(Pd/Al203)为催化剂,在低温(低于l00℃)液相下进行 选择性加氢。 一段加氢也有少数采用非贵金属镍钻、铂钨等催化剂,此类催化剂,其反 应温度一般要高于100℃,在这样温度下双烯烃难免在催化剂表面聚合,从 而降低催化剂活性,导致催化剂再生频繁。 裂解汽油经一段加氢后,其中二烯烃含量小于2%(以质量计); 第二段加氢目的,主要使单烯烃饱和并脱除硫、氧、氮等有机化合物。 这一段加氢精制,普遍采用非贵金属Co-Mo- Al203系列的催化剂,工艺技 术比较成熟。二段加氢在较高温度气相条件下进行。 二段加氢后,裂解汽油的溴值小于1,含硫质量分数小于2×10-6。
(2)重芳烃轻质化的Dctol工艺
8.1.2 芳烃馏分的分离
由催化重整相加氢精制裂解汽油得到的含芳烃馏分都是由芳烃 与非芳烃组成的混合物。 由于碳数相同的芳烃与非芳烃的沸点非常接近,有时还会形成 共沸物,用一般的蒸馏方法是难以将它们分离的。 为了满足对芳烃纯度的要求,目前工业上实际应用的主要是溶 剂萃取法和萃取蒸馏法。
8.2 芳烃转化
各种芳烃组分中用途最广、需求量最大的是苯与对二甲苯,其 次是邻二甲苯。
8.2.1 芳烃的脱烷基化
芳烃的脱烷基化:烷基芳烃分子中与苯环直接相连的烷基,在一定的条件下 可以被脱去。 工业上主要应用于甲苯脱甲基制苯、甲基萘脱甲基制萘。
但其共同点是必须经蒸馏除去裂解汽油中C4馏分、部分C9芳烃与C9+馏分,
(2)裂解汽油加氢 裂解汽油加氢是目前普遍采用的精制方法。由于从裂解汽油中除去双烯烃、 单烯烃和氧、氮、硫等有机化合物的工艺条同,—般采用二段加氢精制工 艺。 第一段加氢的目的,将使易生胶的二烯烃加氢转化为单烯烃以及烯基芳烃转 化为芳烃。 这一段加氢在比较缓和的工艺条件下进行,以避免二烯烃聚合。 因此一段加氢多采用它(Pd/Al203)为催化剂,在低温(低于l00℃)液相下进行 选择性加氢。 一段加氢也有少数采用非贵金属镍钻、铂钨等催化剂,此类催化剂,其反 应温度一般要高于100℃,在这样温度下双烯烃难免在催化剂表面聚合,从 而降低催化剂活性,导致催化剂再生频繁。 裂解汽油经一段加氢后,其中二烯烃含量小于2%(以质量计); 第二段加氢目的,主要使单烯烃饱和并脱除硫、氧、氮等有机化合物。 这一段加氢精制,普遍采用非贵金属Co-Mo- Al203系列的催化剂,工艺技 术比较成熟。二段加氢在较高温度气相条件下进行。 二段加氢后,裂解汽油的溴值小于1,含硫质量分数小于2×10-6。
(2)重芳烃轻质化的Dctol工艺
8.1.2 芳烃馏分的分离
由催化重整相加氢精制裂解汽油得到的含芳烃馏分都是由芳烃 与非芳烃组成的混合物。 由于碳数相同的芳烃与非芳烃的沸点非常接近,有时还会形成 共沸物,用一般的蒸馏方法是难以将它们分离的。 为了满足对芳烃纯度的要求,目前工业上实际应用的主要是溶 剂萃取法和萃取蒸馏法。
芳烃
烷基化历程
CH3CH2Cl + AlCl3
+
CH3CH2 AlCl4 CH2CH3 H CH(CH3)2
+
CH3CH2 AlCl4
H+
2019/2/7
烷基化的特点:
1) 可逆 2) 歧化 3) 重排 4) 速度控制和平衡控制
2019/2/7
1). 可逆:芳烃可以在催化条件下烷基化成为 烷基苯,烷基苯也可在同一催化剂存在下脱 烷基成为芳烃。 2). 歧化:多烷基化
2019/2/7
一、一取代苯的命名
a苯环为母体
甲苯,硝基苯,异丙苯,氯苯 取代基为烷基、硝基、卤素以苯为母体
b苯为取代基,官能团为母体
苯甲酸 苯胺 苯酚 苯甲醛
2019/2/7
单环芳烃的命名
苯环有不饱和基团; 带较长烷基或取代基复杂时; 分子中有多个苯环,以任何一个苯 环为母体命名都有困难时。
氢化热 120kJ/mol 208kJ/mol 离域能 120× 3-208=152(kJ/mol)
2019/2/7
四、苯分子结构的共振论解释 1. Resonance(共振的基本概念)
共振是经典结构的叠加组成共振杂化体, 经典结构叫作极限结构、共振结构
2019/2/7
书写共振式的规则
1共振式中原子的排列组合是相同的,不 同的是电子排列,PAI电子或未共用电子 对移动,弯箭头表示电子转移。 2共振式中成对电子数或未成对电子式应 相等。 3中性分子可表示为电荷分离式,但电子 转移与电负性一致。
硝基苯
发烟HNO3, 浓硫酸
间二硝基苯
CH3 + HNO3 O2N H2SO4 30。C NO2 CH3 CH3 NO2 + NO2
有机化学--第八章芳烃
Br+ + FeBr4-
Br+
3.磺化反应的机理
苯用浓硫酸磺化,反应很慢。若用发烟硫酸磺化, 在室温即可进行。故认为磺化试剂很可能是三氧化硫(也 有人认为是+SO3H)。在硫酸中也能产生三氧化硫:
SO3因为极化使硫原子显正性,通过硫原子进攻苯环。磺 化反应是可逆的。在浓硫酸中,磺化反应机理可能如下:
第八章 芳烃 芳香性
一般把苯及其衍生物总称为芳香族化合物。芳烃是 芳香族碳氢化合物的简称,亦称芳香烃。
芳烃按其结构可分为三类: 单环芳烃
芳烃 多环芳烃 稠环芳烃
①单环芳烃:分子中含有一个苯环的芳烃,称为单环芳烃。 例如:
②多环芳烃:分子中含有两个或两个以上独立苯环的芳烃, 称为多环芳烃。例如:
1
2
3
1.苯环上C—H伸缩振动 2.苯环的C=C伸缩振动 3.二取代苯C—H面外弯曲振动 (770~735)
8.4单环芳烃的化学性质
苯环平面的上下方有π电子云,与σ 键相比,平行重叠的π电子云结合较 疏松,因此在反应中苯环可充当一个电子源,与缺电子的亲电试剂发生反应, 类似于烯烃中π键的性质。但是苯环中π电子又有别于烯烃,π键共振形成的大 π键使苯环具有特殊的稳定性,反应中总是保持苯环的结构。苯的结构特点 决 定 苯 的 化 学 行 为 , 它 容 易 发 生 亲 电 取 代 反 应 ( elcctrophilic substulion reaction)而不是加成反应。
基本反应: 2RSH +0.5O2 Cat. RSSR + H2O
N
C
C
CN
N
N
Co
CN
N
C
C
N
酞菁钴
Br+
3.磺化反应的机理
苯用浓硫酸磺化,反应很慢。若用发烟硫酸磺化, 在室温即可进行。故认为磺化试剂很可能是三氧化硫(也 有人认为是+SO3H)。在硫酸中也能产生三氧化硫:
SO3因为极化使硫原子显正性,通过硫原子进攻苯环。磺 化反应是可逆的。在浓硫酸中,磺化反应机理可能如下:
第八章 芳烃 芳香性
一般把苯及其衍生物总称为芳香族化合物。芳烃是 芳香族碳氢化合物的简称,亦称芳香烃。
芳烃按其结构可分为三类: 单环芳烃
芳烃 多环芳烃 稠环芳烃
①单环芳烃:分子中含有一个苯环的芳烃,称为单环芳烃。 例如:
②多环芳烃:分子中含有两个或两个以上独立苯环的芳烃, 称为多环芳烃。例如:
1
2
3
1.苯环上C—H伸缩振动 2.苯环的C=C伸缩振动 3.二取代苯C—H面外弯曲振动 (770~735)
8.4单环芳烃的化学性质
苯环平面的上下方有π电子云,与σ 键相比,平行重叠的π电子云结合较 疏松,因此在反应中苯环可充当一个电子源,与缺电子的亲电试剂发生反应, 类似于烯烃中π键的性质。但是苯环中π电子又有别于烯烃,π键共振形成的大 π键使苯环具有特殊的稳定性,反应中总是保持苯环的结构。苯的结构特点 决 定 苯 的 化 学 行 为 , 它 容 易 发 生 亲 电 取 代 反 应 ( elcctrophilic substulion reaction)而不是加成反应。
基本反应: 2RSH +0.5O2 Cat. RSSR + H2O
N
C
C
CN
N
N
Co
CN
N
C
C
N
酞菁钴
第8章 芳烃
取代基相同时,合并称为多某基苯;取代基不同时,按硝基、卤、烷基顺 序列出。编号由烷基、卤素、硝基开始,循最短距离编向第二个取代基。 取代基的位臵也可以用邻( o-或1,2-)、间( m-或1,3-)、对( p-或 1,4-)表示。 例如:
CH3 CH3 CH3
邻二甲苯 (1, 2-二甲苯) (o-二甲苯)
+ Br2 FeBr3 Br + HBr H H Br Br
基于这些结果,1865年凯库勒(A. Kekulé )提出了苯的环状构造式。
H H C C H C C H C C H 简写为 H
苯的凯库勒式是19世纪有机化学的一个重大发 现,极大地促进了有机化学的发展。但凯库勒式 并不完美,例如,按凯库勒式1,2-二溴苯有两种 结构,但事实上只有一种。
–NO2、–X、–OR(烷氧基)、–R(烷基)、–NH2、–OH、–COR、 –CHO、–CN、–CONH2(酰胺)、–COX(酰卤)、–COOR(酯)、 –SO3H、–CO2H、–N+R3 例如
OH NH2 CO2H Cl Cl
对氯苯酚
NH2 OCH3
OH CO2H
SO3H
对氨基苯磺酸
NO2
间硝基苯甲酸 2-甲氧基-6-氯苯胺
第八章 芳 烃
第八章
芳 烃
芳烃,也叫芳香烃,指具有芳香性的环状不饱和碳氢化合物。 1825年M. Faraday从汽灯燃气冷凝液中分离出一种沸点为80℃的纯液 体化合物,元素分析表明其C/H为1:1。1834年E. Mitscherlich加热苯 甲酸合成了该化合物,用蒸气密度法测得其分子量为78,相应的分子式为 C6H6 。由于该化合物由安息香(benzoin)衍生而来,取名benzin,现称 benzene,苯。 19世纪发现了许多与苯有关、H/C比低、有芳香气味的化合物,这些化 合物与当时已知的脂肪(aliphatic)化合物具有显著不同的性质,如易进 行取代反应,而难进行加成和氧化反应等,因此称为芳香(aromatic)化 合物。 现代芳烃的概念是指具有芳香性的一类环状化合物,它们不一定具有香味, 也不一定含有苯环结构。芳香性一般指有特殊的稳定性、作为整体参与反应、 不饱和度高但不易发生加成和氧化反应而易发生取代反应等特性。
CH3 CH3 CH3
邻二甲苯 (1, 2-二甲苯) (o-二甲苯)
+ Br2 FeBr3 Br + HBr H H Br Br
基于这些结果,1865年凯库勒(A. Kekulé )提出了苯的环状构造式。
H H C C H C C H C C H 简写为 H
苯的凯库勒式是19世纪有机化学的一个重大发 现,极大地促进了有机化学的发展。但凯库勒式 并不完美,例如,按凯库勒式1,2-二溴苯有两种 结构,但事实上只有一种。
–NO2、–X、–OR(烷氧基)、–R(烷基)、–NH2、–OH、–COR、 –CHO、–CN、–CONH2(酰胺)、–COX(酰卤)、–COOR(酯)、 –SO3H、–CO2H、–N+R3 例如
OH NH2 CO2H Cl Cl
对氯苯酚
NH2 OCH3
OH CO2H
SO3H
对氨基苯磺酸
NO2
间硝基苯甲酸 2-甲氧基-6-氯苯胺
第八章 芳 烃
第八章
芳 烃
芳烃,也叫芳香烃,指具有芳香性的环状不饱和碳氢化合物。 1825年M. Faraday从汽灯燃气冷凝液中分离出一种沸点为80℃的纯液 体化合物,元素分析表明其C/H为1:1。1834年E. Mitscherlich加热苯 甲酸合成了该化合物,用蒸气密度法测得其分子量为78,相应的分子式为 C6H6 。由于该化合物由安息香(benzoin)衍生而来,取名benzin,现称 benzene,苯。 19世纪发现了许多与苯有关、H/C比低、有芳香气味的化合物,这些化 合物与当时已知的脂肪(aliphatic)化合物具有显著不同的性质,如易进 行取代反应,而难进行加成和氧化反应等,因此称为芳香(aromatic)化 合物。 现代芳烃的概念是指具有芳香性的一类环状化合物,它们不一定具有香味, 也不一定含有苯环结构。芳香性一般指有特殊的稳定性、作为整体参与反应、 不饱和度高但不易发生加成和氧化反应而易发生取代反应等特性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
I
+ I2 HNO 3
② 中间体碳正离子(苯鎓离子)远不及苯环稳定。 ③ 卤代要加催化剂,催化剂也可用Fe。 ④ 生成碳正离子(苯鎓离子)一步是决定反应速度的步骤。
14
⑤ 反应能线图
势 能
HX + FeX4
+ X2+ FeX3
从反应能线图也可 看出:生成碳正离 子(苯鎓离子)一步是 决定反应速度的步 骤。
重叠结果形成了一个闭合的、环状的大π键,形成的π电子 云像两个连续的面包圈,一个位于平面上面,一个位于平 面下面,经能量计算,这是一个很稳定的体系。
4
共振论解释苯分子的结构:
A
B
苯分子的结构是A和B的共振杂化体
通常用两种方法表示苯分子的结构:
强调π电子云的平均分布
注意:是A和B的共振杂化体
意义:苯的环状结构的提出,是芳香族化合物发展的一 个里程碑。
为了解释这些性质,1865年德国化学家凯库勒提出苯是
碳碳链首未相连的环状结构,环中三个单键,三个双键
相间。
H
H
H
H
H
H
苯的结构最早由奥地利化学家洛斯密 特(Loschmidt)提出(在1861年)
2
凯库勒结构不完善: ①.不能解释为什么苯分子的不饱和度为4,如此之大,却 不发生类似于烯烃和炔烃的加成反应。 ②.假定邻位两个氢被取代,但按此式应该有两种产物:
X X
X X
但实际上只有一种。 ③.由物理方法测定的苯分子中碳碳键长为0.139nm, 比正常
的碳碳单键(0.154nm)短, 比正常的碳碳双键长(0.134nm)
3
键长介于碳碳单键与碳碳双键之间,完全平均化,由凯 库勒结构式不能说明这一点。 分子轨道理论解释苯分子的结构:
C C
C
C C
C
C为SP2杂化 所有原子处于同一平面 分子中未杂化的6个P轨道侧面交 盖重叠形成6个分子轨道
注意:–X、–NO2、–NO等只作为取代基出现在命名中,分别称为 卤素、硝基、亚硝基。
10
例: COOH
NH 2 Cl
COOH
NH 2
4-氨基苯甲酸
CHO
NO 2
4-硝基-2-氯苯胺
NO 2
Cl
NO 2
4-硝基苯甲酸
CH 3
Cl
OCH 3
Cl
4-甲氧基苯甲醛 1-硝基-2, 4-二氯苯
Cl
2, 4-二氯甲苯
CH3 o-二甲苯 ortho
CH 3
1,3-二甲苯
间二甲苯
m-二甲苯
CH 3
meta
1,4-二甲苯 p-二甲苯
H3C
CH 3
对二甲苯 para
7
3. 结构复杂的化合物 以苯作为取代基:
CH 2OH
COOH
CH CH 2
苯甲醇
CH3CHCH 2 CH 3
苯甲酸
苯乙烯
CHCOOH CH 3
2-对异丁基苯基丙酸 2-(4-异丁基苯基)丙酸
110℃,5天
NO 2
CH 3
O2N
NO 2 CH 3
CH 3
浓 H2SO4 浓 HNO 3 30℃
NO 2
+
甲苯硝化比苯容易,为什么?
5
二. 苯衍生物的命名 (Nomenclature of Benzene Derivatives) 1. 基的命名 苯基 ph- phenyl
CH 3
对甲苯基
CH 2
苄基
Ar- Aryl-
芳基
6
2. 烷基取代的苯 以苯为母体:
CH 3
CH2CH 3
CH( CH 3)2
甲苯
乙苯
异丙苯
CH3 1,2-二甲苯 邻二甲苯
第八章
芳烃 (Aromatic hydrocarbon)
一. 苯的结构 二. 芳香烃化合物的命名 三. 苯环上的亲电取代反应 四. 苯环上取代反应的定位规律 五. 烷基苯的反应 六. 多环芳烃 七. 有手性芳烃 八. 卤代芳烃
九. 芳香性、休克尔(Huckel)规律
一. 苯的结构 (Structure of Benzene) 由元素分析,分子量测定,苯的分子式为:C6H6 性质:①. 易取代,不易加成 ②. 一取代物只有一种 ③. 邻二取代物只有一种
1. 卤化反应
例:
FeCl 3
+ Cl 2 25℃
Cl
+ HCl
12
机理:
FeBr3
+ Br2 △
Br
+ HBr
Br Br + FeBr3 慢
+ Br
Br Br FeBr3
H Br
Br + Br FeBr3
H Br
H Br
H Br
13
H Br
Br FeBr3
Br
+ Br H + FeBr3
注意:① 卤代通常用Cl2、Br2 氟代太剧烈,反应难于控制。碘代则用下列反应:
8
4. 苯环上有多个不同取代基的化合物
O
原则: R NH2 OH CHO 或 C
排在后面的基团为母体
SO3H
X NO2 只作取代基
①. 选母体,使母体编号为1,其他作为取代基 ②. 编号 ③. 较优基团后列出
例:
3 4
H2N
OH
2
COOH
1
4-氨基-2-羟基苯甲酸
COOH
9
补充:对于多官能化合物,选择哪一个官能团作为化合物母体的名称, 必须遵循如下的顺序原则:
H2SO4
+ HNO 3 50℃
NO 2
+ H2O
机理:HONO 2 + 2H2SO4
NO2 + H3 O + 2HS O4
ONO
+ NO2
H NO 2
H NO 2
H NO 2
H NO 2
H
NO 2
H NO 2
17
NO2 发烟H2SO4 浓 HNO 3 90℃
NO 2
NO 2
发烟 H2SO4 浓 HNO 3
优先顺序 基团
作官能团母体名
作取代基名
1
―COOH
羧酸
2பைடு நூலகம்
―SO3H
磺酸
3
―COOR
酯
4
―COX
酰卤
5
―CONH2
酰胺
6
―CN
腈
7
―CHO
醛
8
―C=O
酮
9
―OH
醇、酚
10
―NH2
胺
11
―OR
醚
12
―C≡C―
炔
13
―CH=CH―
烯
14
―R
烃
羧基 磺基 烃氧羰基 卤甲酰基 氨基甲酰基 氰基 甲酰基 酮基、氧代 羟基 氨基 烃氧基 炔基 烯基 烃基
X + HX + FeX3
反应进程
15
⑥ 若反应条件强烈可得二取代产物
Cl FeCl 3
+ Cl 2 △
Cl
Cl
Cl
+
Cl
CH 3
CH 3
CH 3
Cl
FeCl 3
+ Cl 2 室温
+
Cl
注意:甲苯氯代比氯苯容易,为什么? 上去基团的位置?
16
2. 硝化反应
苯在浓HNO3和浓H2SO4作用下生成硝基苯
11
三. 苯环上的亲电取代反应 (Electrophilic Substitution Reactions of Benzene)
根据苯环的结构,在苯环平面的上下,有π电子云,是富 电子基团,类似烯烃,所以可与缺电子的基团,即亲电试 剂发生反应。但与烯键有区别,在苯环中,由于形成了闭 合环状共轭大π键,使苯环稳定性提高,反应中总是苯环 结构保持不变。
+ I2 HNO 3
② 中间体碳正离子(苯鎓离子)远不及苯环稳定。 ③ 卤代要加催化剂,催化剂也可用Fe。 ④ 生成碳正离子(苯鎓离子)一步是决定反应速度的步骤。
14
⑤ 反应能线图
势 能
HX + FeX4
+ X2+ FeX3
从反应能线图也可 看出:生成碳正离 子(苯鎓离子)一步是 决定反应速度的步 骤。
重叠结果形成了一个闭合的、环状的大π键,形成的π电子 云像两个连续的面包圈,一个位于平面上面,一个位于平 面下面,经能量计算,这是一个很稳定的体系。
4
共振论解释苯分子的结构:
A
B
苯分子的结构是A和B的共振杂化体
通常用两种方法表示苯分子的结构:
强调π电子云的平均分布
注意:是A和B的共振杂化体
意义:苯的环状结构的提出,是芳香族化合物发展的一 个里程碑。
为了解释这些性质,1865年德国化学家凯库勒提出苯是
碳碳链首未相连的环状结构,环中三个单键,三个双键
相间。
H
H
H
H
H
H
苯的结构最早由奥地利化学家洛斯密 特(Loschmidt)提出(在1861年)
2
凯库勒结构不完善: ①.不能解释为什么苯分子的不饱和度为4,如此之大,却 不发生类似于烯烃和炔烃的加成反应。 ②.假定邻位两个氢被取代,但按此式应该有两种产物:
X X
X X
但实际上只有一种。 ③.由物理方法测定的苯分子中碳碳键长为0.139nm, 比正常
的碳碳单键(0.154nm)短, 比正常的碳碳双键长(0.134nm)
3
键长介于碳碳单键与碳碳双键之间,完全平均化,由凯 库勒结构式不能说明这一点。 分子轨道理论解释苯分子的结构:
C C
C
C C
C
C为SP2杂化 所有原子处于同一平面 分子中未杂化的6个P轨道侧面交 盖重叠形成6个分子轨道
注意:–X、–NO2、–NO等只作为取代基出现在命名中,分别称为 卤素、硝基、亚硝基。
10
例: COOH
NH 2 Cl
COOH
NH 2
4-氨基苯甲酸
CHO
NO 2
4-硝基-2-氯苯胺
NO 2
Cl
NO 2
4-硝基苯甲酸
CH 3
Cl
OCH 3
Cl
4-甲氧基苯甲醛 1-硝基-2, 4-二氯苯
Cl
2, 4-二氯甲苯
CH3 o-二甲苯 ortho
CH 3
1,3-二甲苯
间二甲苯
m-二甲苯
CH 3
meta
1,4-二甲苯 p-二甲苯
H3C
CH 3
对二甲苯 para
7
3. 结构复杂的化合物 以苯作为取代基:
CH 2OH
COOH
CH CH 2
苯甲醇
CH3CHCH 2 CH 3
苯甲酸
苯乙烯
CHCOOH CH 3
2-对异丁基苯基丙酸 2-(4-异丁基苯基)丙酸
110℃,5天
NO 2
CH 3
O2N
NO 2 CH 3
CH 3
浓 H2SO4 浓 HNO 3 30℃
NO 2
+
甲苯硝化比苯容易,为什么?
5
二. 苯衍生物的命名 (Nomenclature of Benzene Derivatives) 1. 基的命名 苯基 ph- phenyl
CH 3
对甲苯基
CH 2
苄基
Ar- Aryl-
芳基
6
2. 烷基取代的苯 以苯为母体:
CH 3
CH2CH 3
CH( CH 3)2
甲苯
乙苯
异丙苯
CH3 1,2-二甲苯 邻二甲苯
第八章
芳烃 (Aromatic hydrocarbon)
一. 苯的结构 二. 芳香烃化合物的命名 三. 苯环上的亲电取代反应 四. 苯环上取代反应的定位规律 五. 烷基苯的反应 六. 多环芳烃 七. 有手性芳烃 八. 卤代芳烃
九. 芳香性、休克尔(Huckel)规律
一. 苯的结构 (Structure of Benzene) 由元素分析,分子量测定,苯的分子式为:C6H6 性质:①. 易取代,不易加成 ②. 一取代物只有一种 ③. 邻二取代物只有一种
1. 卤化反应
例:
FeCl 3
+ Cl 2 25℃
Cl
+ HCl
12
机理:
FeBr3
+ Br2 △
Br
+ HBr
Br Br + FeBr3 慢
+ Br
Br Br FeBr3
H Br
Br + Br FeBr3
H Br
H Br
H Br
13
H Br
Br FeBr3
Br
+ Br H + FeBr3
注意:① 卤代通常用Cl2、Br2 氟代太剧烈,反应难于控制。碘代则用下列反应:
8
4. 苯环上有多个不同取代基的化合物
O
原则: R NH2 OH CHO 或 C
排在后面的基团为母体
SO3H
X NO2 只作取代基
①. 选母体,使母体编号为1,其他作为取代基 ②. 编号 ③. 较优基团后列出
例:
3 4
H2N
OH
2
COOH
1
4-氨基-2-羟基苯甲酸
COOH
9
补充:对于多官能化合物,选择哪一个官能团作为化合物母体的名称, 必须遵循如下的顺序原则:
H2SO4
+ HNO 3 50℃
NO 2
+ H2O
机理:HONO 2 + 2H2SO4
NO2 + H3 O + 2HS O4
ONO
+ NO2
H NO 2
H NO 2
H NO 2
H NO 2
H
NO 2
H NO 2
17
NO2 发烟H2SO4 浓 HNO 3 90℃
NO 2
NO 2
发烟 H2SO4 浓 HNO 3
优先顺序 基团
作官能团母体名
作取代基名
1
―COOH
羧酸
2பைடு நூலகம்
―SO3H
磺酸
3
―COOR
酯
4
―COX
酰卤
5
―CONH2
酰胺
6
―CN
腈
7
―CHO
醛
8
―C=O
酮
9
―OH
醇、酚
10
―NH2
胺
11
―OR
醚
12
―C≡C―
炔
13
―CH=CH―
烯
14
―R
烃
羧基 磺基 烃氧羰基 卤甲酰基 氨基甲酰基 氰基 甲酰基 酮基、氧代 羟基 氨基 烃氧基 炔基 烯基 烃基
X + HX + FeX3
反应进程
15
⑥ 若反应条件强烈可得二取代产物
Cl FeCl 3
+ Cl 2 △
Cl
Cl
Cl
+
Cl
CH 3
CH 3
CH 3
Cl
FeCl 3
+ Cl 2 室温
+
Cl
注意:甲苯氯代比氯苯容易,为什么? 上去基团的位置?
16
2. 硝化反应
苯在浓HNO3和浓H2SO4作用下生成硝基苯
11
三. 苯环上的亲电取代反应 (Electrophilic Substitution Reactions of Benzene)
根据苯环的结构,在苯环平面的上下,有π电子云,是富 电子基团,类似烯烃,所以可与缺电子的基团,即亲电试 剂发生反应。但与烯键有区别,在苯环中,由于形成了闭 合环状共轭大π键,使苯环稳定性提高,反应中总是苯环 结构保持不变。
