最新高考化学双向细目表
高中化学必修二双向细目表
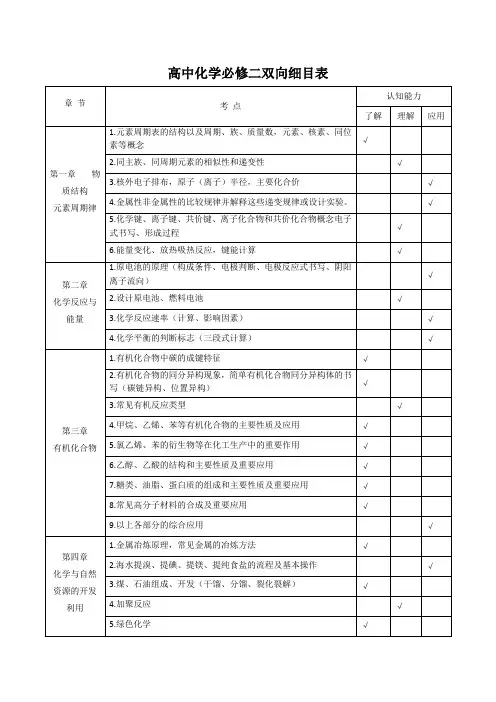
3.常见有机反应类型
√
4.甲烷、乙烯、苯等有机化合物的主要性质及应用
√
5.氯乙烯、苯的衍生物等在化工生产中的重要作用
√
6.乙醇、乙酸的结构和主要性质及重要应用
√
7.糖类、油脂、蛋白质的组成和主要性质及重要应用
√
8.常见高分子材料的合成及重要应用
√
9.以上各部分的综合应用
√
第四章化学与自然资源的开发利用
√
6.能量变化、放热吸热反应,键能计算
√
第二章化学反应与能量
1.原电池的原理(构成条件、电极判断、电极反应式书写、阴阳离子流向)
√
2.设计原电池、燃料电池
√
3.化学反应速率(计算、影响因素)
√
4.化学平衡的判断标志(三段式计算)
√
第三章有机化合物
1.有机化合物中碳的成键特征
√
2.有机化合物的同分异构现象,简单有机化合物同分异构体的书写(碳链异构、位置异构)
高中化学必修二双向细目表
理解
应用
第一章物质结构元素周期律
1.元素周期表的结构以及周期、族、质量数,元素、核素、同位素等概念
√
2.同主族、同周期元素的相似性和递变性
√
3.核外电子排布,原子(离子)半径,主要化合价
√
4.金属性非金属性的比较规律并解释这些递变规律或设计实验。
√
5.化学键、离子键、共价键、离子化合物和共价化合物概念电子式书写、形成过程
1.金属冶炼原理,常见金属的冶炼方法
√
2.海水提溴、提碘、提镁、提纯食盐的流程及基本操作
√
3.煤、石油组成、开发(干馏、分馏、裂化裂解)
√
4.加聚反应
√
5.绿色化学
√
高中化学双向细目表
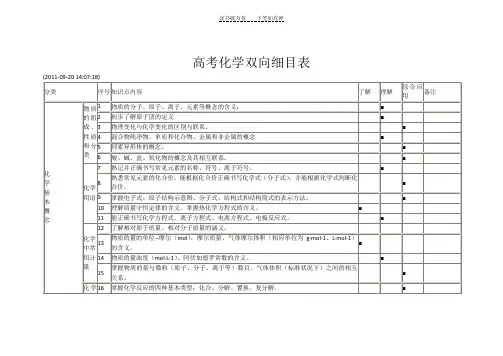
59
了解常见盐类的性质和用途。
■
60
了解常见化肥的基本性质。
■
61
了解硫、氮、碳的氧化物对大气的污染及其防止。
■
62
初步了解氟氯烃、含磷洗涤剂及二氧化硅粉尘对环境及人类健康的影响。
■
63
初步了解一些生活用水的净化及污水处理的基本原理。
■
有
机
化
学
基
础
64
理解基团、官能团的概念;识别结构式(结构简式)中的基团和官能团
■
75
了解有机物的主要来源,了解石油化工、煤化工、农副产品化工、资源综合利用及污染和环保的概念
■
76
了解在生活、生产中常见有机物的性质和用途
■
化
学
实
验
77
常见化学仪器的主要用途、使用方法,包括玻璃仪器的洗涤
■
78
能绘制和识别典型的实验仪器装置图
■
79
常见试剂的化学性质及其保存方法
■
80
化学实验的基本操作(药品取用,天平使用,仪器连接,气密性检查,物质的加热、过滤、蒸发,试纸的使用,容量瓶使用,萃取、分液、蒸馏等)
■
42
理解电解原理。了解铜的电解精练、镀铜、氯碱工业反应原理。
■
元
素
及
其
化
合
物
常
见
金
属
元
素
的
性
质
43
了解金属钠的物理性质,掌握钠和镁化学性质。
■
44
从原子的核外电子排布,理解ⅠA、ⅡA族元素(单质、化合物)的相似性和递变性。
■
45
以氢氧化钠为例,了解重要的碱的性质和用途。了解钠的重要化合物。
最新新课程实验区高考化学试题知识点归纳及能力双向细目表
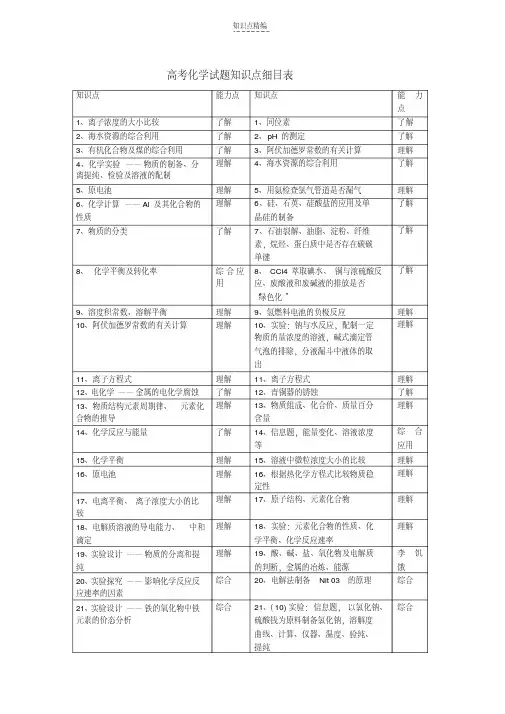
了解 了解 了解
7、同分异构体
8、有机物、无机物除杂
9、同位素、核素、质量数、质子 数、中子数、电子数
综合
25、( 10) 工业制硫酸,平衡常数、
理解
平衡转化率、尾气吸收、化学方程
式、制备 FeS04
26、《有机化学基础》 :信息题
综合
26、( 12) 信息题,羟基磷灰石的制
综合
备,化学方程式、龋齿原因等
综合
27、 (9) 信息题,克矽平的合成,
综合
原子利用率、双键及烃基的性质、
元素守恒、化学方程式
《化学与技术》
26、石油的裂化
了解
26、合成洗涤剂
了解
27、普钙磷肥
了解
27、生铁炼钢
了解
28、联合制碱法 29、金属的电化学腐蚀探究
理解 综合
28、离子交换技术
理解
29、“氨碱法”、 “联合制碱法”、 综合
知识点精编
知识点 7、实验安全 8、有机物分子空间结构 9、乙醇 、乙酸的性质
化学方程式、原子利用率 高考化学试题双向细目表
11、离子方程式 12、电化学 —— 金属的电化学腐蚀 13、物质结构元素周期律、 元素化 合物的推导 14、化学反应与能量
15、化学平衡 16、原电池
17、电离平衡、 离子浓度大小的比 较 18、电解质溶液的导电能力、 中和 滴定 19、实验设计 —— 物质的分离和提 纯 20、实验探究 —— 影响化学反应反 应速率的因素 21、实验设计 —— 铁的氧化物中铁 元素的价态分析
了解 了解
14、( 9)原电池原理 15、( 10)有机:根据元素含量确定 分子式、醇、化学方程式、结构简 式、产率
最新高考化学双向细目表

最新高考化学双向细目表分类序知识点内容近三年高考再现号化学基本概念物质的组成、性质和分类1物质的分子、原子、离子、元素等概念的含义;17 18 193物理变化与化学变化的区别与联系。
28盐类反应中的基础涉及84混合物纯净物、单质和化合物、金属和非金属的概念5 同素异形体的概念。
6酸、碱、盐、氧化物的概念及其相互联系。
化学用语7熟记并正确书写常见元素的名称、符号、离子符号。
熟悉常见元素的化合价。
能根据化合价正确书写化学式(分子式),并能根据化学式判断化合价。
8,综合化合价,共价键主要考C族元素27,综合元素周期律68熟悉常见元素的化合价。
能根据化合价正确书写化学式(分子式),并能根据化学式判断化合价。
掌握电子式、原子结构示意图、分子式、结构式和结构简式的表示方法。
能正确书写化学方程式、离子方程式、电离方程式、电极反应式。
化学中常用计量12了解相对原子质量、相对分子质量的含义。
11,综合原子结构中等6,氧化还原涉及简单13物质的量的单位--摩尔(mol),摩尔质量、气体摩尔体积(相应单位为g·mol-1、L·mol-1)。
14 物质的量浓度(mol·L-1)、阿伏加德罗常数。
15 掌握物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)之间的相互关系。
化学反应与能量16掌握化学反应的四种基本类型:化合、分解、置换、复分解。
12氧化还原、物质的量、化学计算中等26题一问6,综合部份物质的量计算,主要得失电子守恒、部份氧化还原,中上13题氧化与离子综合10,得失电子守恒,方程式配平17理解氧化还应反应,了解氧化剂和还原剂等概念。
掌握重要氧化剂、还原剂之间的常见反应。
18能判断氧化还原反应中电子转移的方向和数目,并能配平反应方程式。
19了解化学反应中的能量变化,吸热反应、放热反应、反应热、燃烧热和中和热及新能源的开发等概念。
26,热方程,反应热7分11热化学书写反应热,中等7热化学书写反应热,中等溶液20 了解溶液的含义8涉及21了解溶液的组成,理解溶液中溶质的质量分数的概念。
新高考化学命题双向细目表
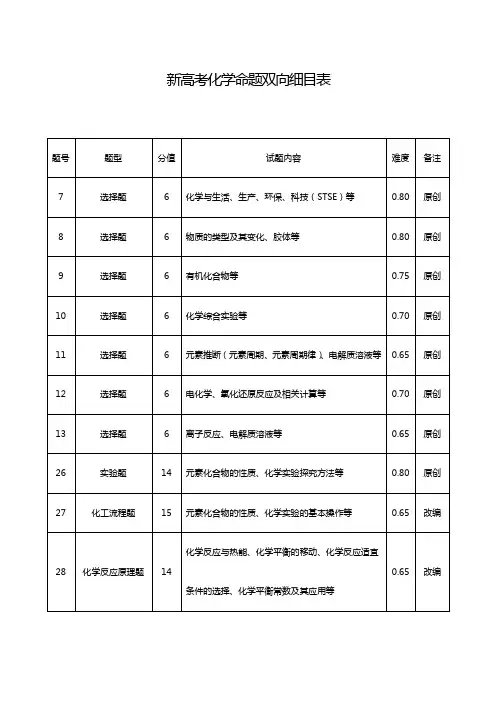
题号
题型
分值
试题内容
难度
备注
7
选择题
6
化学与生活、生产、环保、科技(STSE)等
0.80
原创
8
选择题
6
物质的类型及其变化、胶体等
0.80
原创
9
选择题
6
有机化合物等
0.75
原创
10
选择题
6
化学综合实验等
0.70
原创
11
选择题
6
元素推断(元素周期、元素周期律)、电解质溶液等
0.65
原创
12
选择题
6
电化学、氧化还原反应及相关计算等
0.70
原创
13
选择题
6
离子反应、电解质溶液等
0.65
原创
26
实验题
14
元素化合物的性质、化学实验探究方法等
0.80
原创
27
化工流程题
15
元素化合物的性质、化学实验的基本操作等
0.65
改编
28
化学反应原理题
14
化学反应与热能、化学平衡的移动、化学反应适宜条件的选择、化学平衡常数及其应用等
0.65
改编
35
二选一:结构
15
选择性必修3:物质结构与性质
0.70
改编
36
二选一:有机
15
选择性必修5:有机化学基础
0.70原创Biblioteka 命题思想达成
目标
优良率
及格率
平均分
20%
65%
65~75
本卷基于本届高三化学学科的复习进度和学生现有的知识、能力水平命制。侧重考查已经复习过的元素化合物知识、化学基本理论,考虑到知识、能力考查的覆盖面并与高考试卷逐步接轨,试卷中也有相当未复习的知识内容。全卷编写力求以学生为本,关注学生知识、能力水平,注意保护学生学习积极性;立意新颖,有思想性和时代特色;内容实在,重点考查重点和主干;形式多样,信息给予有文字、表格、图示、图像等,力求图文茂。
高中化学双向细目表
7、掌握乙酸的分子结构和化学性质,了解乙酸的用途、制法等
√
第四节
基本营养物质
1、油脂的组成、结构、重要性质和用途,酯和油脂的联系和区别
√
2、油脂的应用,肥皂和硝化甘油等日常生活中的知识
√
3、掌握糖类的主要代表物的组成和性质,了解淀粉、纤维素的组成和性质
√
4、掌握蛋白质的基本性质,认识蛋白质是生命现象最基本的物质基础
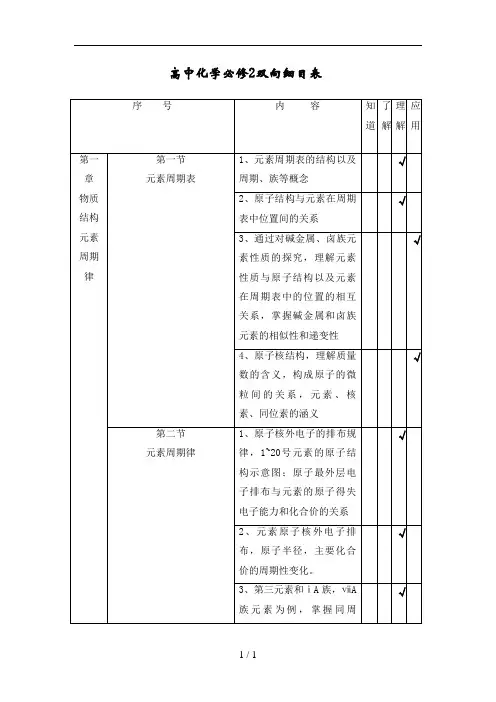
高中化学必修2双向细目表
序 号
内 容
知道
了解
理解
应用
第一章
物质结构元素周期律
第一节
元素周期表
1、元素周期表的结构以及周期、族等概念
√
2、原子结构与元素在周期表中位置间的关系
√
3、通过对碱金属、卤族元素性质的探究,理解元素性质与原子结构以及元素在周期表中的位置的相互关系,掌握碱金属和卤族元素的相似性和递变性
√
2、甲烷的组成和物理性质,掌握甲烷的正四面体结构和化学性质
√
3、烷烃的物理性质及其性质的变化规律,烷烃的结构、性质和烷烃的命名方法
√
4、取代反应,同分异构现象和同分异构体
√
第二节
来自石油和煤的两种基本化工原料
1、石油的分馏及其产品和用途,石油的裂化和裂解
√
2、煤的干馏和综合利用
√
3、煤、石油的组成和石油产品、煤干馏产品的广泛用途
第一节
化学能与热能
1、断裂化学键要吸收能量,生成化学键要放出能量
√
2、化学能和热能是相互转化的,并且符合能量守恒
√
3、什么是吸热反应和放热反应,并通过实验亲身体验放热反应和吸热反应,记住常接触的化学反应中哪些是放热反应,哪些是吸热反应。
高一化学必修双向细目表
高一化学必修双向细目表1. 化学基础知识- 原子结构和元素周期表- 化学键和化合物的分类- 化学反应和化学方程式- 酸碱中和和中性化学反应- 物质的状态变化和相变- 化学量和化学计算- 元素周期表中的主要元素和其特性- 元素的周期性和趋势- 物质的分子结构和化学键的类型2. 化学实验技能- 实验室安全和实验室设备的使用- 常用实验方法和仪器的操作- 实验数据的记录和处理- 实验结果的分析和解释- 实验原理和实验设计3. 化学反应与能量变化- 化学反应的能量变化- 燃烧反应和氧化还原反应- 酸碱中和反应和热化学方程式- 粒子间的引力作用和化学反应的速率- 化学反应的平衡和平衡常数- 溶液中的溶解度和溶液的浓度4. 化学物质的构成与结构- 元素和化合物的构成- 原子和分子的结构- 组成物质的化学键- 元素周期表中元素的结构特性- 金属和非金属元素的性质- 化合物的分子结构和性质- 傅里叶光谱和分子结构分析5. 化学周期律与离子反应- 元素周期表和周期律规律- 同一周期和同一族的元素特性- 阴离子与阳离子的结构和特性- 离子反应的性质和反应方程式- 酸碱反应和生成离子的化学方程式- 离子溶液中的电离反应和电导率6. 环境与持续发展化学- 化学物质对环境的影响- 大气污染和水污染的原因和防治- 可持续发展和绿色化学的概念- 环境友好的化学产品和过程- 生物质资源的利用和能源转化- 化学垃圾处理和废物回收利用的方法7. 高分子物质与生物化学- 高分子物质的结构和性质- 聚合反应与高分子合成- 塑料和纤维的生产和应用- 生物大分子的结构和功能- 生物有机物的合成和代谢- 酶的催化作用和生物化学反应以上是高一化学必修双向细目表的主要内容。
这份文档包含了学习该科目所需的基础知识、实验技能以及各个单元的重点内容。
希望能对你的学习和备考有所帮助。
2023届高考化学知识点双向细目表——化学基本概念和基础理论
44 化学反应的可逆性及化学平衡的建立。
化学反应速
45
化学平衡的特征。
率 和化学平
46
化学平衡常数的含义,能够用化学平衡常数进行简单计算。
衡
外界条件(浓度、温度、压强、催化剂等)对反应速率和化学平
47 衡的影响,能用相关理论
解释其一般规律。
化 学 反 应 速 率 和 化 学 平 衡 的 调 控 在 生 活 、生 产 和 科 学 研 究 领 域 48
38 写出电极反应和电池反应方程式。
39 常见电源的种类及其工作原理。
金 属 发 生 电 化 学 腐 蚀 的 原 因 、金 属 腐 蚀 的 危 害 以 及 防 止 金 属 腐 40
蚀的措施。
41 化学反应速率的概念、反应速率的定量表示方法。
42 能正确计算化学反应的转化率(α)。
43 反应活化能的概念,催化剂的重要作用。
25
知识点内容
分子、原子、离子、原子团等概念的含义; 物理变化与化学变化的区别与联系。 混合物和纯净物、单质和化合物、金属和非金属的概念 酸、碱、盐、氧化物的概念及其相互联系。 熟记并正确书写常见元素的名称、符号、离子符号。 熟 悉 常 见 元 素 的 化 合 价 。能 根 据 化 合 价 正 确 书 写 化 学 式( 分 子 式),或根据化学式判断 化合价。 原 子 结 构 示 意 图 、电 子 式 、分 子 式 、结 构 式 和 结 构 简 式 的 表 示 方法。 相对原子质量、相对分子质量的定义,并能进行有关计算。 能正确书写化学方程式、离子方程式,并能进行有关计算。 质量守恒定律。 物 质 的 量 (n) 及 其 单 位 摩 尔 (mol) 、摩 尔 质 量 (M) 、气 体 摩 尔 体 积 (Vm)、物质的量浓度(c)、 阿伏加德罗常数(NA)的含义。 能根据微粒(原子、分子、离子等)物质的量、数目、气体体 积(标准状况下)之间的 相互关系进行有关计算。 溶液的含义。 溶解度、饱和溶液的概念。 溶液浓度的表示方法。 溶 液 中 溶 质 的 质 量 分 数 和 物 质 的 量 浓 度 的 概 念 ,并 能 进 行 有 关 计算。 配制一定溶质质量分数溶液和物质的量浓度溶液的方法。 胶体是一种常见的分散系。溶液和胶体的区别。 元素、核素和同位素的含义。 原子构成。原子序数、核电荷数、质子数、中子数、核外电子 数以及它们之间的相互关 系。 原子核外电子排布规律。 元素周期律的实质。 元素周期表(长式)的结构(周期、族)及其应用。 以第 3 周期为例,掌握同一周期内元素性质的递变规律与原子 结构的关系 以 IA 和ⅦA 族为例,掌握同一主族元素性质递变规律与原子 结构的关系。
新课标考题双向细目表
Ⅰ
基因工程的原理及技术
Ⅱ
40(1、2)
基因工程的应用
Ⅱ
蛋白质工程
Ⅰ
植物的组织培养
Ⅱ
40(1、3)
动物的细胞培养与体细胞克隆
Ⅰ
细胞融合与单克隆抗体
Ⅱ
40
动物胚胎发育的基本过程与胚胎工程的理论基础
Ⅰ
40(2)
胚胎干细胞的移植
Ⅰ
40(3)
胚胎工程的应用
Ⅱ
转基因生物的安全性
Ⅰ
生物武器对人类的威胁
Ⅰ
生物技术中的伦理问题
Ⅰ
40(1、4)
简述生态工程的原理
Ⅱ
40(3)
生态工程的实例
Ⅰ
选修1、微生物的利用
生物技术在食品加工及其他方面的应用
探究实验
29
30
合计
67+19+16=102点
备注:1、★表示非选择题及选做题,不标的为选择题。
2、数字为题号,字母为能力类别(A:理解能力;B:实验与探究能力;C:获取信息的能力;D:综合运用能力)
附表1、考题双向细目表
知识内容
考纲要求
13
市1
附1
三1
蛋白质的结构和功能
Ⅱ
核酸的结构和功能
Ⅱ
糖类的种类和作用
Ⅱ
29(1)
脂质的种类和作用
Ⅱ
水和无机盐的作用
Ⅰ
细胞学说的建立过程
Ⅰ
1C
1A
多种多样的细胞
Ⅱ
细胞膜系统的结构和功能
Ⅱ
2AD
2
主要细胞器的结构和功能
Ⅱ
1D
细胞核的结构和功能
Ⅱ
高中化学双向细目表
高中化学双向细目表高考化学双向细目表分类序号知识点内容1 物质的组成、性质和分类2 化学基本概念3 物质的分子、原子、离子、元素等概念的含义;初步了解原子团的定义4 物理变化与化学变化的区别与联系5 混合物、纯净物、单质和化合物、金属和非金属的概念6 同素异形体的概念7 酸、碱、盐、氧化物的概念及其相互联系8 熟记并正确书写常见元素的名称、符号、离子符号9 熟悉常见元素的化合价;能根据化合价正确书写化学式(分子式),并能根据化学式判断化合价10 掌握电子式、原子结构示意图、分子式、结构式和结构简式的表示方法;理解质量守恒定律的含义;掌握热化学方程式的含义11 能正确书写化学方程式、离子方程式、电离方程式、电极反应式12 了解相对原子质量、相对分子质量的涵义13 掌握物质的量的单位--摩尔(mol),摩尔质量、气体摩尔体积(相应单位为g·mol-1、L·mol-1)的含义14 物质的量浓度(mol·L-1)、阿伏加德罗常数的含义15 掌握物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)之间的相互关系16 掌握化学反应的四种基本类型:化合、分解、置换、复分解17 理解氧化还原反应,了解氧化剂和还原剂等概念;掌握重要氧化剂、还原剂之间的常见反应18 能判断氧化还原反应中电子转移的方向和数目,并能配平反应方程式19 了解化学反应中的能量变化,吸热反应、放热反应、反应热、燃烧热和中和热及新能源的开发等概念20 了解溶液的涵义21 了解溶液的组成,理解溶质的质量分数的概念22 了解饱和溶液、不饱和溶液的概念;了解溶解度的概念;了解温度对溶解度的影响及溶解度曲线23 初步了解结晶、结晶水、结晶水合物、风化、潮解的概念24 了解胶体的概念及其重要性质和应用25 了解原子的组成及同位素的概念26 掌握原子序数、核电荷数、质子数、中子数、核外电子数,以及质量数与质子数、中子数之间的相互关系注:综合应用部分不在此表中列出。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
8涉及27题15分综合化学平衡及速率,难度中上
33
了解化学反应的可逆性。理解化学平衡的含义及其与反应速率之间的联系。
34
理解勒沙特列原理的含义。理解浓度、温度、压强等条件对化学平衡移动的影响。
35
以合成氨工业生产为例,用化学反应速率和化学平衡的观点理解工业生产的条件。
最新高考化学双向细目表
分类
序号
知 识 点 内 容
近三年高考再现
化
学
基
本
概
念
物质的组成、性质和分类
1
物质的分子、原子、离子、元素等概念的含义;
17
18
19
3
物理变化与化学变化的区别与联系。
28盐类反应中的基础涉及
8
4
混合物纯净物、单质和化合物、金属和非金属的概念
5
同素异形体的概念。
6
酸、碱、盐、氧化物的概念及其相互联系。
39
了解水的电离、溶液pH等概念。
7,选择,6分,中等
10综合电离,
8涉及,
40
了解强酸强碱中和滴定的原理。
9,选择,6分,
13离子反应量变关系
41
理解盐类水解的原理。了解盐溶液的酸碱性。
10综合电离水解
中上难度
8涉及
42
理解原电池原理。初步了解化学电源。了解化学腐蚀与电化学腐蚀及一般防腐蚀方法。
10主要电解综合原电池
元素周期律和周期表
30
掌握元素周期律的实质,了解元素周期表(长式)的结构(周期、族)及其应用。
27.
9题涉及
12题综合周期律、表
31
以第3周期为例,掌握同一周期内元素性质(如:原子半径、化合价、单质及化合物性质)的递变规律与原子结构的关系;以I A 和ⅦA 族为例,掌握同一主族内元素性质递变规律与原子结构的关系。
电
解
质
溶
液
36
了解电解质和非电解质、强电解质和弱电解质的概念。
28题,共13分,综合离子反应,盐类反应,实验方案,离子检验
8,涉及离子反应量变关系
10题涉及29题15分多半,综合元素化合物知识
6,方程式书写,中下9综合反应速率图象29电解综合运用15分,涉及实验方案
37
理解离子反应的概念。
38
理解电解质的电离平衡概念。
11综合同位素,物质的量计算,中等
9题,综合元素周期表,中等
27
以第1,2,3周期的元素为例,了解原子核外电子排布规律。
28
理解离子键、共价键的含义。理解极性键和非极性键。了解极性分子和非极性分子。了解分子间作用力。初步了解氢键。
29
了解几种晶体类型(离子晶体、原子晶体、分子晶体、金属晶体)及其性质。
8,选择,6分,,简单27,综合元素化合物15分
28元素周期律和元素化合物知识共15分难度中等及中上
ቤተ መጻሕፍቲ ባይዱ化学反应速率
化学平衡
32
了解化学反应速率的概念,反应速率的表示方法,理解外界条件(浓度、温度、压强、催化剂等)对反应速率的影响。
13,综合考化学速率及平衡6分,中等以上难度
26,第三问速率及平衡,中上4分
化学
中常
用计
量
12
了解相对原子质量、相对分子质量的含义。
11,综合原子结构
中等
6,氧化还原涉及
简单
13
物质的量的单位--摩尔(mol),摩尔质量、气体摩尔体积(相应单位为g·mol-1、L·mol-1)。
14
物质的量浓度(mol·L-1)、阿伏加德罗常数。
15
掌握物质的量与微粒(原子、分子、离子等)数目、气体体积(标准状况下)之间的相互关系。
化学反应与能量
16
掌握化学反应的四种基本类型:化合、分解、置换、复分解。
12氧化还原、物质的量、化学计算
中等26题一问
6,综合部份物质的量计算,主要得失电子守恒、部份氧化还原,中上13题氧化与离子综合
10,得失电子守恒,方程式配平
17
理解氧化还应反应,了解氧化剂和还原剂等概念。掌握重要氧化剂、还原剂之间的常见反应。
54
从原子的核外电子排布,理解卤族元素(单质、化合物)的相似性和递变性。
55
掌握氯气的化学性质,了解几种重要的含卤素化合物的性质和用途。
56
了解这些元素(如:H,O,S,N,P,C,Si)的单质及某些氧化物、氢化物的性质。
57
以Na2O2为例,了解过氧化物的性质。
58
掌握硫酸、硝酸的化学性质。
59
以硫酸为列,了解化工生产化学反应原理的确定。初步了解原料与能源的合理利用、"三废处理"与环境保护以及生产过程中的综合经济效益问题。
43
理解电解原理。了解铜的电解精练、镀铜、氯碱工业等反应原理。
10,选择,6分,
元
素
及
其
化
合
物
常
见
金
属
元
素
的
性
质
44
了解金属钠的物理性质,掌握钠和镁化学性质。
45
从原子的核外电子排布,理解ⅠA 、ⅡA族元素(单质、化合物)的相似性和递变性。
46
以氢氧化钠为例,了解重要的碱的性质和用途。了解钠的重要化合物。
18
能判断氧化还原反应中电子转移的方向和数目,并能配平反应方程式。
19
了解化学反应中的能量变化,吸热反应、放热反应、反应热、燃烧热和中和热及新能源的开发等概念。
26,热方程,反应热7分
11热化学书写反应热,中等
7热化学书写反应热,中等
溶液
20
了解溶液的含义
8涉及
21
了解溶液的组成,理解溶液中溶质的质量分数的概念。
化学
用语
7
熟记并正确书写常见元素的名称、符号、离子符号。熟悉常见元素的化合价。能根据化合价正确书写化学式(分子式),并能根据化学式判断化合价。
8,综合化合价,共价键主要考C族元素27,综合元素周期律
6
8
熟悉常见元素的化合价。能根据化合价正确书写化学式(分子式),并能根据化学式判断化合价。掌握电子式、原子结构示意图、分子式、结构式和结构简式的表示方法。能正确书写化学方程式、离子方程式、电离方程式、电极反应式。
22
了解饱和溶液、不饱和溶液的概念。了解溶解度的概念。了解温度对溶解度的影响及溶解度曲线。
23
初步了解结晶、结晶水、结晶水合物、风化、潮解的概念。
24
了解胶体的概念及其重要性质和应用。
7,综合胶体性质及应用,中等
化
学
基
本
理
论
物
质
结
构
25
了解原子的组成及同位素的概念。
26
理解原子序数、核电荷数、质子数、中子数、核外电子数,以及质量数与质子数、中子数之间的相互关系
47
了解金属的通性,金属冶炼的一般原理。初步了解金属的回收和资源保护。
48
掌握Fe和Al的化学性质。
49
掌握常见金属的活动顺序。
50
以Fe(Ⅱ)Fe(Ⅲ)的相互转化为例,了解变价金属元素的氧化还原性。
51
了解铝的重要化合物。
52
初步了解合金的概念。
常
见
非
金
属
元
素
的
性
质
53
以氯为例,了解卤族元素的物理性质和化学性质。
