大输液生产工艺规程
大输液制备工艺流程

大输液制备工艺流程英文回答:Process Flow of Large Volume Intravenous Fluid Preparation.1. Raw Material Inspection and Preparation.Inspect raw materials (e.g., purified water, electrolytes, drugs) for quality and compliance with specifications.Prepare purified water and electrolyte solutions according to established formulas.2. Mixing and Filtration.Mix raw materials in a sterile environment using automated or manual blending equipment.Filter the mixed solution through a 0.2 micronfilter to remove particles and microorganisms.3. Heat Disinfection (Optional)。
Heat the filtered solution to a temperature of 121°C for 15 minutes to achieve sterilization. This step is optional for solutions containing heat-sensitive drugs.4. Filling and Sealing.Fill sterile containers (e.g., bottles, bags) with the prepared solution using aseptic techniques.Seal containers securely to prevent contamination.5. Inspection and Testing.Visually inspect containers for anomalies (e.g., cracks, leaks).Perform sterility testing and chemical analysis toensure product quality and safety.6. Labeling and Packaging.Label containers clearly with product information (e.g., composition, dosage, expiration date).Package containers in sealed boxes or crates for storage and distribution.中文回答:大输液制备工艺流程。
500mL大输液车间生产工艺

500mL大输液车间生产工艺目录1 前言..............................................................................1.1 输液剂概念(1)1.1.1 输液剂的定义 (1)1.1.2 输液剂的特点 (1)1.1.3 输液剂的质量要求 (1)1.1.4 输液剂的应用 (2)1.2 输液剂生产工艺 (2)1.3 设计任务 (2)1.3.1 设计药品 (2)1.3.2 设计任务简介 (3)2 右旋糖酐70葡萄糖注射液简介 (3)2.1 处方组成 (3)2.2 药理作用 (4)3 工艺流程设计 (4)3.1 工艺流程简图 (5)3.2 工艺流程论证 (7)4 工艺计算 (13)4.1 计算基准 (13)4.2 物料衡算 (13)5 定型设备选择 (14)5.1 选择设备型号、规格、数量 (14)5.1.1 BSY50/500型玻璃瓶大输液生产线 (14)5.1.2 QG180型启盖机 (15)5.1.3 QJW6型外洗机 (15)5.1.4 QJB24(16)型超声波洗瓶机 (16)5.1.5 GFA1型灌封机 (16)5.1.6 上瓶机、卸瓶机、灯检机、贴签机 (17)6 车间GMP设计要求 (20)6.1 GMP简述 (20)6.2 车间GMP设计要求 (20)6.2.1 大输液生产车间设计一般性要求 (21)7 车间工艺设计 (21)7.1 生产工艺流程图 (21)8 结束语 (22)参考文献 (23)1 前言1.1 输液剂概述1.1.1 输液剂的定义输液(infusion solution)是通过静脉滴注输入体内的大剂量(一次给药在100mL以上)注射液。
它不仅可以补充必要的营养、热能和水分,以维持体内水、盐(电解质〕的平衡,而且对改善血液循环,防止和治疗休克,调节酸碱平衡,稀释和排泄毒素,经静脉滴注给药等均有重要作用。
大容量注射液生产工艺规程

制药有限公司大容量注射液生产工艺规程颁发单位:GMP办公室工艺规程批准程序目录1. 剂型、规格 (3)2. 生产工艺流程 (3)3. 操作过程及工艺条件 (4)4.质量控制要点 (6)5.设备一览表、主要设备生产能力 (7)6.工艺过程中的SOP (7)7.中间产品的控制 (8)8.验证工作要点 (8)9.工艺卫生和环境卫生 (10)10.劳动组织及岗位定员 (10)一、制剂类型:最终灭菌大容量注射液,100ml规格,西林瓶包装。
二、流程图:大容量注射剂工艺流程图三、操作过程及工艺条件1 生产前的检查与确认1.1 是否还留有前批生产的产品或物料,是否已清洁并取得“清场合格证”。
1.2 检查确认生产现场的机器设备和器具是否已清洁并准备完毕挂上“合格”标示。
1.3 所使用原辅料是否准备齐全。
是否有质量检验报告单,合格品才能使用。
1.4 检查工艺用水是否新鲜制备,贮存不得超过24小时。
1.5 检查确认与生产品种相适应的批生产指令、配套文件及有关记录是否已准备齐全。
1.6 检查确认生产场所的温度是否在规定范围内(18-26℃,相对湿度在30%-65%)。
2 洗瓶、塞、铝盖2.1理瓶:根据“批生产指令”准备所需的清洁盘、领取必须的西林瓶。
在理瓶室将西林瓶的合格品摆满瓶盘。
2.2清洗:把西林瓶放在不锈钢传送链条上,开动洗瓶机,定时检查安瓿的清洁度:目检1000ml注射用水无可见异物,抽50支,毛、块≤2%。
洗瓶岗位按清场SOP进行清场,并填写生产记录。
2.3 理塞、铝盖:根据《生产指令》准备所需的丁基胶塞和铝盖,分别、依次放入多功能胶塞漂洗机。
2.4清洗:将丁基胶塞放入多功能漂洗机后,加入纯化水,开动机器进行清洗,清洗后捞出、沥干。
排除纯化水后再加入注射用水清洗,捞出、沥干。
将铝盖放入多功能漂洗机后,加入纯化水,开动机器清洗,清洗后捞出、沥干。
排除纯化水后再加入注射用水清洗,捞出、沥干。
清洗过后,按岗位清场操作规程进行清场,填写清场合格证,并填写生产记录。
大输液生产流程简介

9
生产流程控制
05 关键工序-灌装岗位:
1、灌装机原理: 称重式液体灌装机(碘克沙醇注射液):在线逐瓶对灌装前空瓶进行称量清零,而
后根据设定的灌装重量逐瓶灌装至设定重量(品种密度×拟灌装平均装量)。
生产前确认关键项目:
装量、可见异物。
a
灌装岗位质 量要点01
可见异物控制是大容量注射剂 的重要检测项目之一。目
设备仪表校验 温度仪表和验证用仪
表
微生物挑战试 验
证明灭菌柜的灭菌程序是可行的,需 采用灭菌生物指示剂来判断灭菌柜灭 菌效果。根据颜色判断灭菌效果.
6
生产流程控制
03
关键工序-配制岗位:
7、 →
→
8、
配制质量要点(过滤器) 药液过滤器每天生产前后进 行完整性测试; 药液循环前应开启管道上脱 炭过滤器排气嘴进行适当排气, 应保证药液注满壳体; 药液输送时需要监测除菌过 滤器上下游压差,防止滤芯受 到高压破坏。
配制岗位质量要点(SIP) SIP程序结束后通入除
大输液生产流程简介
生产流程控制
01 工艺流程图:
浓配
稀配
上瓶
粗洗
精洗
灌装
轧盖
灭菌
注:
蓝色一般区
黄色C级区 绿色A/C级区
合格
灯检
包装
不合格
销毁
入库
2
生产流程控制
02 关键工序-称量岗位:
01 防止混淆措施 先称辅料后称原料,先称液体物料后称固体物料,先称晶 体物料,后称粉末物料,称一料、清一料,及时张贴物料 标识,称量工具专用。 02 防止交叉污染 房间现对于工艺走廊呈负压、称量间采用负压式称量罩 捕尘(确认流型、监控压差和风速)。
大容量输液制剂的生产工艺
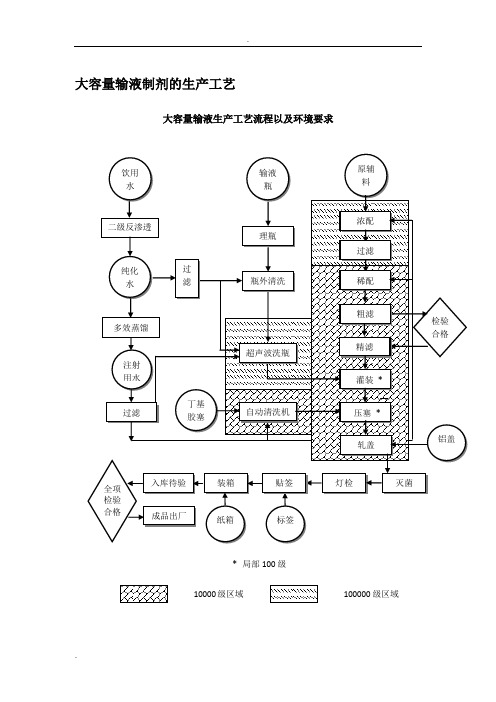
大容量输液制剂的生产工艺大容量输液生产工艺流程以及环境要求大容量输液认证检查要点大输液又名可灭菌大容量注射剂,是指将配制好的药液灌入大于50 ml的输液瓶或袋内,加塞、加盖、密封后用蒸汽热压灭菌而制备的灭菌注射剂。
1、机构与人员a)主管生产和质量管理的企业负责人、生产管理和质量管理部门负责人均应具有医药或相关专业大专以上学历,并具有药品生产和质量管理经验,并履行其职责。
b)企业负责人和各级管理人员应定期接受药品管理法律法规培训。
c)质量检验、生产、维修保养、清洁人员应定期进行卫生和微生物学基础知识、洁净作业等方面的培训和考核,并具有实际操作技能。
2、厂房设施的管理要点及检查重点a)洁净区:我国《药品生产质量管理规范》对最终灭菌的无菌药品生产厂房洁净度级别的要求是:浓配或采用密闭系统的稀配应在100000级洁净区内进行;稀配、滤过、灌封、直接接触药品的包装材料的最终处理等操作应在10000级洁净区内进行;物料、中间品应经过物流缓冲间或传递柜进、出洁净区。
称量配料间如产尘应与洁净走廊呈相对负压,必要时设捕尘设施。
中国药典规定:微生物限度检查、无菌检查应在100级或10000级背景下的局部100级区内进行,并与生产区分开。
微生物限度检查与无菌检查用的实验室和空气净化系统最好彼此分开,以尽可能减少对无菌检查的干扰。
b)空气净化系统应能确保洁净区的洁净度级别、温湿度、压差等符合生产工艺要求并经过验证。
初效、中效过滤器应明确清洗/更换周期,高效过滤器应定期检测其完整性,如有泄漏或阻塞应及时更换。
空气净化系统应每天24小时运行,停用后再次运行应进行清洁、消毒并经过再验证,符合要求的方可开始生产。
c)与产品直接接触的压缩空气、氮气、二氧化碳等辅助设施这些气体因与产品直接接触,不得对产品带来污染。
应对系统进行验证。
PQ测试项目包括洁净度级别、含水量、含油量等。
d)注射用水(WFI)系统以纯化水为原水,经多效蒸馏制得。
大输液生产工艺

大输液生产工艺大输液是指用于输液治疗的药物溶液,主要用于静脉注射。
大输液的生产工艺是指将药物原料经过一系列的加工和处理,制成符合药品质量标准的药物溶液的过程。
大输液的生产工艺一般包括以下步骤。
首先,进行原材料准备。
根据配方要求,准备药物原料、辅料和溶剂等。
药物原料主要是指需要进行溶解或混合的药物成分,辅料主要是为了调节药物制剂的各种性质,如稳定性、pH值等。
溶剂主要是用于溶解药物和辅料的介质,常见的有注射用水。
其次,进行溶解和混合。
将药物原料和辅料按照一定比例加入溶剂中,通过搅拌和加热等方式将其溶解和混合均匀。
这一步骤的目的是将药物和辅料充分溶解在溶剂中,使其形成均匀的药物溶液。
然后,进行过滤和灭菌。
将溶解和混合好的药物溶液进行过滤,去除其中的杂质和微生物。
过滤一般采用微孔滤器或膜滤器等器械,通过筛网或膜孔来阻挡杂质和微生物。
过滤后的药物溶液还需要进行灭菌处理,常见的方法有热灭菌和无菌过滤等。
接着,进行包装和质量检验。
将经过过滤和灭菌处理的药物溶液按照一定规格装入适宜的容器中,如注射瓶、袋装等。
装瓶前需要进行质量检验,包括外观检查、标志和标签的贴附和打印等。
质量检验的目的是确保药物溶液的质量符合规定标准。
最后,进行包装成品的包装和储存。
将装瓶好的药物溶液进行密封和包装,以确保其在储存和运输过程中不受外界环境的影响。
包装常采用塑料袋、纸箱等包材,包装成品应符合药品包装和储存的要求,如密封性、防水性等。
以上就是大输液的生产工艺的主要步骤。
通过上述工艺步骤,可制得符合药品质量标准的药物溶液,以满足临床治疗的需要。
在整个生产工艺中,需严格按照药品生产的标准操作,确保药物的质量和安全性。
大容量输液制剂地生产实用工艺
标准文档大容量输液制剂的生产工艺大容量输液生产工艺流程以及环境要求局部100级10000级区域 wwmwxx 100000级区域 理瓶1 1 L 瓶外j 清洗1 原辅 输液 饮用料水 瓶 浓配二级反渗透 过滤 过 纯化稀配 滤水 粗滤 检验 多效蒸馏 合格精滤 超声波洗瓶 注射用水 灌装基自动清洗机 过滤 压塞胶塞 轧盖灭菌 入库待验 装箱 贴签 灯检 全项检验合格 成品出厂 标签纸箱 k\sx\* 上大容量输液认证检查要点大输液又名可灭菌大容量注射剂,是指将配制好的药液灌入大于50ml的输液瓶或袋,加塞、加盖、密封后用蒸汽热压灭菌而制备的灭菌注射剂。
1、机构与人员a)主管生产和质量管理的企业负责人、生产管理和质量管理部门负责人均应具有医药或相关专业大专以上学历,并具有药品生产和质量管理经验,并履行其职责。
b)企业负责人和各级管理人员应定期接受药品管理法律法规培训。
c)质量检验、生产、维修保养、清洁人员应定期进行卫生和微生物学基础知识、洁净作业等方面的培训和考核,并具有实际操作技2、厂房设施的管理要点及检查重点a)洁净区:我国《药品生产质量管理规》对最终灭菌的无菌药品生产厂房洁净度级别的要:浓配或采用密闭系统的稀配应在100000级洁净区进行;稀配、滤过、灌封、直接接触药品的包装材料的最终处理等操作应在10000级洁净区进行;物料、中间品应经过物流缓冲间或传递柜进、出洁净区。
称量配料间如产尘应与洁净走廊呈相对负压,必要时设捕尘设施。
中国药典规定:微生物限度检查、无菌检查应在100级或10000 级背景下的局部100级区进行,并与生产区分开。
微生物限度检查与无菌检查用的实验室和空气净化系统最好彼此分开,以尽可能减少对无菌检查的干扰。
b)空气净化系统应能确保洁净区的洁净度级别、温湿度、压差等符合生产工艺要求并经过验证。
初效、中效过滤器应明确清洗/更换周期,高效过滤器应定期检测其完整性,如有泄漏或阻塞应及时更换。
大输液生产工艺质量控制要点
大输液生产工艺质量控制要点-------------制备注射用水一.用于蒸馏器1)水源:去离子水2)冷却水:洁净的软水(即生活用水)二.蒸馏水质量检查1)生产时:每台每隔2小时检查氯化物,酸碱度,易氧化物的铵盐2)贮藏时:每星期全项检查一次三.蒸馏水贮藏条件1)容器:不锈钢罐或搪瓷罐2)温度:80摄氏度以下3)时间: 不超过12小时-------------洗输液瓶一.常水冲洗1)温度: 60摄氏度~70摄氏度2)压力: 不低于9.81×10Pa3)时间: 不低于三秒4)次数: 2~3次二.精洗1)次数: 2~3 次2)压力: 不低于9.81×Pa3)时间: 不少于3秒4)末道滤材: 0.8~1.2um微孔滤膜5)蒸馏水澄明度: 200ml容量瓶不得有可见异物-------------配液一.浓配1)活性炭用量: 0.02%(g/ml)2)煮沸时间: 10~15min3)药液浓度不低于50%二.稀配1)活性炭用量0.01%(g/ml)2)药液温度: 40~60摄氏度质量检查:1)含量:97.5%~102.5%2)PH: 应符合规定三.滤材1)炭脱: 砂棒或钛合金制成的滤棒2)初滤: 垂熔玻璃滤器3)精滤: 0.8~1.2um 微孔滤膜四.微孔滤膜1)磨砂棒灯检: 均无亮点2)起泡点试验: 合格五.无菌要求配料间空气菌落数: 9cm培养皿,暴露空间30minih 小于15个六.药液温度控制: 含盐品种: 40~50摄氏度七.药液温度控制: 含糖品种: 50~60摄氏度-------------洗涤纶薄膜质量要求1)乙醇浓度: 95%2)浸泡时间: 大于8小时3)加盐煮沸: 100摄氏度. 30min,消除静电效应4)漂洗水澄明度: 200ml容量瓶仅允许有微量白点-------------洗涤橡皮塞一.NaOH1)浓度: 1%(g/ml)2)温度: 100摄氏度3)时间: 30分钟二.HCl1)浓度: 1%(g/ml)2)室内温度15~25摄氏度浸泡3)时间30分钟三.洗胶塞水澄明度检查: 200ml容量瓶检查允许微量白点-------------灌装一.药液澄明度: 200ml容量瓶检查应无异物二.容量1)500ml : 500~510ml2)250ml : 250~255ml三.药渡稀释到灌装时间: 不超过4小时四.空气菌落数: 9cm培养皿,暴露空间30min<10个-------------轧盖质量检查: 不松动, 不缩皮, 不切皮.-------------灭菌一.从灌装到灭菌的时间: 不超过45分钟二.温度: 不低于112~115摄氏度三.压力: 不低于6.34×10000Pa四.时间: 不低于30分钟五.灭菌升温时间: 10~15分钟六.测温点: 不低于2 个-------------灯检一.视力检查: 1)次数2次/年二.结果: 远近视力大于0.9三.被检药液温度室温四.时间不低于4秒/瓶输液生产工艺质量控制要点。
大输液的生产工艺
大输液的生产工艺大输液是一种经静脉注射或输液器直接输入人体血液中的补充药物、营养液的治疗方式。
大输液的生产工艺主要包括原料准备、混合配制、质量控制和包装消毒等环节。
首先,原料准备是大输液生产的第一步。
常见大输液的原料有氯化钠、葡萄糖、氯化钾等,这些原料需通过检验合格的药品厂家供应。
在原料准备过程中,需要按照生产配方和计量要求准确称取原料,并对其进行检验,确保原料的质量符合标准。
其次,混合配制是大输液生产的关键环节。
混合配制的目的是将各种原料精确配比,并通过搅拌混合使之均匀稳定。
混合配制过程中,需严格按照生产工艺要求,根据不同的产品类型和配方进行操作,并遵守无菌操作规范,保证产品的无菌性。
配制完成后,还需一定的时间进行质量控制样品的检验,确保产品的成品质量达到标准。
接下来是质量控制环节。
质量控制是大输液生产过程中的重要环节,它包括两方面内容:一方面是对原料和各个加工步骤进行监控,确保每个环节的操作符合标准,防止产品受到污染;另一方面是对成品进行检验,包括外观、pH值、药物浓度、微生物检验等,以确保成品的质量符合标准。
对于不合格产品,需要进行追溯和调查,并进行相应的处理措施,以保证产品的质量和安全性。
最后,是包装消毒环节。
大输液的包装消毒是为了保持产品的无菌性,防止细菌侵入并污染产品。
通常采用无菌灌装技术,即将配制好的大输液灌装到无菌袋中,封口后进行高温高压灭菌处理,确保产品的长期无菌状态,并防止细菌污染。
在大输液的生产过程中,还需严格遵守相关的GMP(药品生产质量管理规范)和药品生产许可证要求,确保产品的质量和安全性。
同时,生产过程中需加强设备和人员的培训,定期进行设备的维护和保养,保证生产设备的正常运行,提高生产效率和产品质量。
总之,大输液的生产工艺包括原料准备、混合配制、质量控制和包装消毒等环节,需要严格按照生产工艺要求和GMP规范进行操作,以确保产品的质量和安全性。
此外,还需加强设备和人员的培训,定期进行设备的维护和保养,保证生产设备的正常运行,提高生产效率和产品质量。
软袋大输液的生产工艺
软袋大输液的生产工艺软袋大输液是一种常用的医疗器械,用于将药物或营养液输送到人体血液中。
它的生产工艺是一个复杂而精细的过程,需要严格的质量控制和高度的生产技术。
本文将从原料准备、药物配制、包装灭菌等方面介绍软袋大输液的生产工艺。
软袋大输液的生产工艺需要准备一系列的原料。
其中,主要原料包括药品、溶剂、滤器、软袋等。
药品是输液的主要成分,需要根据不同的药物和剂量进行准确配制。
溶剂用于溶解药物,并确保药液的稳定性。
滤器用于过滤药液,去除杂质和微生物。
软袋是输液的容器,需要符合一系列的标准,如无毒、无菌、耐压等。
药物配制是软袋大输液生产工艺的关键步骤。
药物配制需要在无菌条件下进行,以确保药液的纯净性和安全性。
首先,将准备好的药品和溶剂按照一定的比例加入到配制容器中。
然后,通过搅拌、混合等方式使药物充分溶解和均匀分布。
在整个过程中,需要严格控制温度、pH值等参数,以确保药物的质量和稳定性。
接下来是软袋的制备和包装。
软袋的制备需要使用特殊的材料和设备。
首先,将药物配制好的溶液通过一系列的管道输送到软袋中。
软袋具有一定的弹性和耐压性,可以容纳一定的药液容量。
然后,使用高温高压的方法将软袋进行密封,确保药液的无菌性和安全性。
最后,对软袋进行外观检查和质量检测,确保软袋的完整性和符合标准。
最后是灭菌和包装。
灭菌是软袋大输液生产工艺中非常重要的一步。
灭菌的目的是杀灭软袋和药液中可能存在的微生物,确保药液的无菌性。
常用的灭菌方法包括高温高压灭菌、辐射灭菌等。
在灭菌之后,软袋需要经过一系列的包装流程,如贴标、装箱等,最终成品可以出厂。
软袋大输液的生产工艺需要严格控制每个环节,确保药液的质量和安全性。
在整个生产过程中,需要严格遵守相关的法律法规和标准要求,如GMP、ISO等。
此外,注重员工的培训和技术支持,提高生产效率和质量。
软袋大输液的生产工艺是一个复杂而精细的过程,需要严格的质量控制和高度的生产技术。
通过合理的原料准备、药物配制、包装灭菌等步骤,可以生产出质量稳定、安全可靠的软袋大输液产品,为医疗事业提供良好的支持。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
大输液生产工艺规程
大输液生产工艺规程
大输液生产工艺规程
输液工序关键质控要点
输液工序关键质检要点
十、半成品质量标准(指标)、成品及原辅料质量标准依据
输液半成品质量标准(指标)
原辅料及成品质量标准依据品名质量标准依据
葡萄糖中国药典95年版二部Р.845 氯化钠中国药典95年版二部Р.945 氯化钾中国药典95年版二部Р.947 氯化钙中国药典95年版二部Р.943 甘露醇中国药典95年版二部Р.85 甲硝唑中国药典95年版二部Р.152 各种氨基酸日本味之素质量标准(92版)
大输液生产工艺规程
大输液生产工艺规程
大输液生产工艺规程
大输液生产工艺规程。
