铝原子簇
(必考题)初中化学九年级上册第三单元《物质构成的奥秘》测试题(答案解析)(1)

一、选择题1.(0分)[ID:131850]原子簇是若干原子的聚集体,有望开发成新材料,某铝原子簇由13个铝原子构成其最外层电子数的总和为40时相对稳定,下图为铝原子的结构示意图,则该稳定铝原子簇的微粒符号是A.Al3+B.13Al3+C.13Al-D.Al13-2.(0分)[ID:131848]作为相对原子质量标准的1个碳原子的质量是1.993×10-26kg.现有27g金属铝,则这些金属铝中含有铝原子的个数有A.5.02×1025B.6.02×1023C.6.02×1026D.5.02×10223.(0分)[ID:131835]关于如图所示实验有以下说法,其中正确的说法组合是()①该实验用到了对比的方法②该实验能证明分子在不断地运动③该实验能证明分子运动的快慢与温度有关④片刻后可观察到试管A中溶液变红⑤加热后氨分子的能量升高⑥加热后氨分子的质量变小A.①②③④⑤⑥B.①③④⑥C.②③④⑤D.①②③⑤4.(0分)[ID:131833]下列变化能证明分子可以再分的是()A.酒精挥发B.冰雪融化C.玻璃破碎D.过氧化氢分解5.(0分)[ID:131828]下列各组元素中,元素符号的大写字母完全相同的一组是()A.镁、锰、锌B.铝、银、汞C.氖、钠、硅D.氯、钙、铜6.(0分)[ID:131819]亚硒酸钠可用于提升人体免疫力。
下图是硒元素在元素周期表中的部分信息及原子结构示意图。
有关说法正确的是()A.硒原子易得电子B.硒是一种金属元素C.硒原子的质量为78.96g D.硒原子核内中子数为347.(0分)[ID:131818]纽约大学的科学家最近研制出有“双腿”、能在盘子里“散步”的机器人,它是由26个氨基酸结合而成的多肽分子。
下列说法中正确的是()A.这种机器人是一种分子B.我们已可以用肉眼直接看到这种分子“散步”C.分子本身是不会运动的,其“散步”一定是在人的推动下进行的D.这种分子的组成是混合物8.(0分)[ID:131800]我国成功发射的“北斗三号”卫星采用了高性能的“铷原子钟”和“氢原子钟”。
最新人教版九年级全一册化学下册水平测试试卷

19.(10分)欲证明“CO2与NaOH发生了化学反 应”,某化学兴趣小组进行以下探究实验(
实验装置中夹持仪器已略去)。
【实验1】按如图SM-5甲所示装置进行实验。
(1)实验前U形管两端液面相平,将NaOH溶液滴入试管中,恢复到室温后
,U形管中的液面左__高__右__低____。据此,甲同学得出“CO2与NaOH发生了化学 反应”的结论。
返回目录
解:设参加反应的CaCl2的质量为x。 CaCl2+Na2CO3 == CaCO3↓+2NaCl(1分) 111 106
x 40 g×26.5%(1分)
(1分) x=11.1 g(1分)
该溶液中CaCl2的质量分数为
×100%=18.5%(1分)
答:该溶液中CaCl2的质量分数为18.5%。(设和答共1分)
返回目录
9.下列各项是人体中几种体液的正常pH,其中酸性最强的是( )A A.胃液(0.9~1.5) B.唾液(6.6~7.1) C.胆汁(7.1~7.3) D.血液(7.35~7.45)
返回目录
10.下列实验操作能达到实验目的的是( B )
选项
实验目的
实验操作
A 检验某未知溶液是否为碱溶液
测量溶液的pH
复杂的化学变化,最后生成了易被农作物吸收的硝酸盐。雷雨
给庄稼施加了( C )
A.钾肥
B.磷肥
C.氮肥
D.复合肥
返回目录
12.某同学的妈妈因病手术,医生嘱咐要增加摄入蛋白质类食物 以利于伤口愈合。则他为妈妈准备的以下食物中,最有利于伤 口愈合的是( B ) A.苹果、香蕉 B.牛奶、鸡蛋 C.巧克力、橙汁 D.面包、饼干
C.压强减小,气体的溶解度增大 D.温度升高,气体的溶解度减小
日照市人教版初中化学九年级第三章物质构成的奥秘经典习题(含答案解析)

考试范围:xxx;满分:***分;考试时间:100分钟;命题人:xxx 学校:__________ 姓名:__________ 班级:__________ 考号:__________一、选择题1.原子簇是若干原子的聚集体,有望开发成新材料,某铝原子簇由13个铝原子构成其最外层电子数的总和为40时相对稳定,下图为铝原子的结构示意图,则该稳定铝原子簇的微粒符号是A.Al3+B.13Al3+C.13Al-D.Al13-2.关于如图所示实验有以下说法,其中正确的说法组合是()①该实验用到了对比的方法②该实验能证明分子在不断地运动③该实验能证明分子运动的快慢与温度有关④片刻后可观察到试管A中溶液变红⑤加热后氨分子的能量升高⑥加热后氨分子的质量变小A.①②③④⑤⑥B.①③④⑥C.②③④⑤D.①②③⑤3.下列变化能证明分子可以再分的是()A.酒精挥发B.冰雪融化C.玻璃破碎D.过氧化氢分解4.下列说法正确的是()A.钠原子失去一个电子就变成稀有气体元素氖的原子B.氯原子得到一个电子后,就变成了与氩原子核外电子排布相同的阴离子C.两种离子,核外电子排布相同,化学性质一定相同D.原子最外层电子数少于4个的元素,一定是金属元素5.事物的宏观表象是由其微观性质决定的。
下列事实及对这些事实的解释中,二者不相符的是()A.成熟的菠萝会散发出浓浓的香味,说明分子在不断地运动B.湿衣服晾在太阳晒着的地方干得快,说明分子的运动速率与温度有关C.50mL水和50mL酒精混合后总体积小于100mL,说明分子间有间隔D.水沸腾时能掀开壶盖,说明分子的大小随温度升高而增大6.下列根据粒子结构示意图归纳出的信息正确的是()A.①②两种元素化学性质相似B.只有③④具有相对稳定结构C.③④都属于阴离子D.②③属于同种元素的不同种粒子7.下图为某粒子的结构示意图,下列有关该粒子的说法中错误的是A.质子数为12B.有2个电子层C.该粒子是原子D.属于相对稳定结构8.下列装置或操作能达到实验目的的是( )A.准确读出液体体积B.探究分子运动C.空气中氧气含量测定D.氧气的验满9.能量的改变会引起分子运动的速率发生改变。
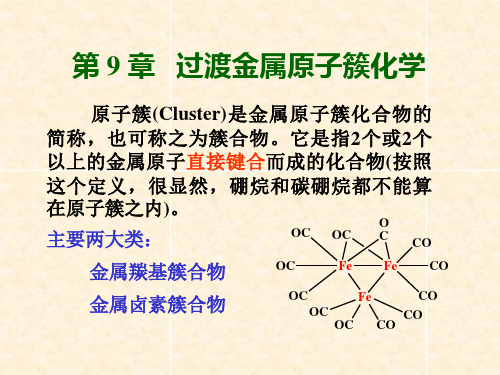
第9章 过渡金属原子簇化学
合起来; • 一般重金属元素形成原子簇的倾向更大一些。 • 一个配位体常常能和两个或两个以上金属原子成键,对金属原 子起桥连作用。
若干化合物中的 M—M 化学键 键 级 4.0 3.5 3.0 2.5 1.0 电 子 组 态 σ2π4δ2 σ2π4δ2 δ*1 σ2π4δ2 δ*2 σ2π4δ2δ*2 π*1 σ2π4δ2 δ*2 π*1 实 例
以Re2C182-为例: 2 Re3+=2×(7-3)=8,8 C1-=16,4 M-M=8, 总电子数=32, 平均每个Re为16e。 然而,对于Mo6C184+, Mo612+=6×6-12=24,8C1-=16, 总数=40, 每个Mo为40/6, 这很难用18或16电子规则描述。 其结构见右下。 其中六个钼原子构成一个八面 体,在八面体的每个面上方有一个 氯原子。因此, Cl-离子应为面桥基 配位, Mo6C184+应写作Mo6(3-C1)84+。 如果把8个Cl-取掉,则剩下Mo612+, 其价电子数为6×6-12=24,共12 对,而八面体共12条边,正好足够 沿着八面体的每个边形成一条Mo- Mo键,这一点可能是很有意义的。
③ 在羰基簇中,金属的 d 轨道大多参与形成 d→反 馈键,因而羰基簇的金属与金属间大都为单键,很少有多 重键。而在卤素簇中,金属的 d 轨道多用来参与形成金属 之间的多重键,只有少数用来参与同配体形成键。如 Re2C182-; ④ 中心原子的氧化态一般比羰基化合物高, d 轨道紧 缩(如果氧化数低, 卤素负离子的配位将使负电荷累积, 相 反,如果氧化数高, 则可中和这些负电荷), 不易参与生成d →反馈键; ⑤ 由于卤素不能易用*轨道从金属移走负电荷,所以 中心金属的负电荷累积造成大多数卤素簇合物不遵守18电 子规则。
(必考题)初中化学九年级上册第三单元《物质构成的奥秘》测试(答案解析)(8)

一、选择题1.(0分)[ID:131850]原子簇是若干原子的聚集体,有望开发成新材料,某铝原子簇由13个铝原子构成其最外层电子数的总和为40时相对稳定,下图为铝原子的结构示意图,则该稳定铝原子簇的微粒符号是A.Al3+B.13Al3+C.13Al-D.Al13-2.(0分)[ID:131843]已知硫原子核内质子数和中子数都是氧原子核内质子数和中子数的两倍,又知氧原子核外电子数与核内中子数相等,由此得出结论:在二氧化硫分子中,①电子数等于核内质子数;②硫元素与氧元素的质量比为1:1;③电子数等于核内中子数;④质子数等于中子数。
以上结论正确的是()A.①②B.②③④C.①②③D.①②③④3.(0分)[ID:131842]下列结构示意图表示阴离子的是A.B.C.D.4.(0分)[ID:131812]根据如图粒子结构示意图,有关说法正确的是A.属于同一种元素B.都是同一种粒子C.都显电性D.都达到了稳定结构5.(0分)[ID:131809]如图所示的是氧原子结构示意图和硫元素在元素周期表中的信息。
下列说法正确的是A.氧原子核外有6个电子B.硫属于金属元素C.硫原子的相对原子质量为32.06gD.一个硫原子有16个质子6.(0分)[ID:131802]下列对分子、原子、离子的认识,正确的是A.质子数相同的微粒一定属于同种元素B.镁原子的质子数大于镁离子的质子数C.分子可分,原子不可再分D.分子、原子、离子都可以直接构成物质7.(0分)[ID:131799]分别分解高锰酸钾、氯酸钾、过氧化氢三种物质,都可以制得氧气。
这说明三种物质的组成中都含有A.氧气B.氧分子C.氧化物D.氧元素8.(0分)[ID:131791]某元素R的原子序数为m,能够形成核外有x个电子的R n-离子,则下列关系正确的是A.m=nB.m=n+xC.m=n-xD.m=x-n9.(0分)[ID:131786]已知A-、B2-、C+、D2+、E3+五种简单离子的核外电子数相等,则它们对应的核电荷数由大到小的顺序是A.A>B>C>D>E B.B>A>C>D>EC.C>D>E>A>B D.E>D>C>A>B10.(0分)[ID:131768]元素观是化学的重要观念。
北京第二中学分校九年级化学上册第三单元《物质构成的奥秘》(含答案)

一、选择题1.原子簇是若干原子的聚集体,有望开发成新材料,某铝原子簇由13个铝原子构成其最外层电子数的总和为40时相对稳定,下图为铝原子的结构示意图,则该稳定铝原子簇的微粒符号是A.Al3+B.13Al3+C.13Al-D.Al13-D解析:D铝原子最外层电子数是3,其最外层电子数的总和为40时相对稳定,说明该稳定铝原子簇Al。
带1个单位负电荷,微粒符号可以表示为-13故选:D。
2.下列说法正确的是①高锰酸钾加热完全分解后剩余的固体是纯净物;②能保持氧气化学性质的最小粒子是2O;③蒸馏水不宜养鱼,因为蒸馏水中几乎不含氧分子;④铪、钨两种元素原子的本质不同是核内质子数目不同⑤已知M2-核外有x个电子,其相对原子质量为a,则该粒子含有的中子数为a-x+2;⑥质量相同的Na、Mg、Al、Ca四种金属,含原子数最少的是Mg。
A.①②B.③④C.③④⑤D.③⑤⑥C解析:C①高锰酸钾加热完全分解生成锰酸钾、二氧化锰和氧气,则高锰酸钾加热完全分解后剩余的固体是锰酸钾和二氧化锰,属于混合物,不符合题意;②氧气由氧气分子构成,则能保持氧气化学性质的最小粒子是O2,2O表示的是两个氧原子,不符合题意;③蒸馏水不宜养鱼,因为蒸馏水中几乎不含氧气,故几乎不含氧分子,符合题意;④元素是质子数相同的一类原子的总称,铪、钨两种元素原子的本质不同是核内质子数不同,符合题意;⑤在原子中,相对原子质量≈质子数+中子数,M2-核外有x个电子,是得到2个电子形成的,该粒子中质子数=x-2,因为相对原子质量为a,所以该粒子中含有的中子数为:()x x-+,符合题意;a--2=a2⑥Na、Mg、Al、Ca相对原子质量逐渐增大,相对原子质量越大,等质量物质含原子个数越少,因此质量相同的Na、Mg、Al、Ca四种金属,含原子数最少的是Ca,不符合题意。
故选C。
3.作为相对原子质量标准的1个碳原子的质量是1.993×10-26kg.现有27g金属铝,则这些金属铝中含有铝原子的个数有A .5.02×1025 B .6.02×1023 C .6.02×1026 D .5.02×1022B 解析:B根据相对原子质量的定义可知,相对原子质量和原子的实际质量成正比,碳的相对原子质量是12,铝的相对原子质量是27,1个碳原子的质量是1.993×10-26kg 。
2020年江苏苏州中考化学试题(含答案)

2020年江苏苏州中考化学试题可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Mg-24 Cl-35.5选择题(共40分)一、单项选择题(包括20小题、每题2分,共40分。
每题只有一个选项符合题意。
)1.“垃圾分类工作就是新时尚”。
废旧报纸应投入的垃圾箱是A.B.C.D.2.下列物质属于氧化物的是A.O3B. SO3C .NaOHD.K2 SO43.下列变化属于化学变化的是A.干冰升华B.衣服晾干C.冰雪融化D.食物腐败4.下列物质由离子构成的是A.铜B.水C.氯化钠D.氖气5.四氯化钛(TiCl4)可用于冶炼金属钛。
四氯化钛中钛元素的化合价为A.+4B.-4C.0D.-16.下列实验操作图示正确的是A.加热液体B.测定pHC.滴加液体D.检查气密性7.下列常见材料中,属于合成材料的是 A.陶瓷 B.焊锡 C.塑料 D.钢筋混凝土8.下列有关化学用语表示正确的是 A.五氧化二磷:P2O5 B.银元素:AG C.2个镁离子:2Mg +2D.8个硫原子:S 89.工业用反应324222NaHCO =Na CO H +O CO +↑来制备纯碱,该反应属于 A.分解反应 B.化合反应 C.置换反应 D.复分解反应10.下列有关氧气的说法中,不正确的是 A.氧气可供给呼吸B.鱼类能在水中生存,说明氧气易溶于水C.植物的光合作用是空气中氧气的主要来源D.焊接或切割金属时使用纯氧代替空气以获得更高的温度 11.某净水装置如右图所示。
下列说法正确的是A.该装置能对水进行杀菌消毒B.该装置能除去水中的颜色和异味C.硬水经过该装置后可转化为软水D.自来水经过该装置后可得蒸馏水 12.下列指定反应的化学方程式正确的是 A.镁条燃烧:2Mg+O Mg 点燃 B.铜绿分解:2232Cu (OH)CO 2CuO CO +↑C.氨水中和硫酸:3424422NH H O H SO NH SO H O ⋅+=+D.酒精完全燃烧:26222C H O+3O CO +3H O 2点燃13.利用右图所示实验装置模拟工业炼铁。
原子簇的概念

原子簇的概念
原子簇,也被称为金属簇合物或金属原子簇,是化学中的一个重要概念。
它指的是由两个或更多的金属原子通过共享电子形成的多个金属-金属键合的分子或离子。
这些原子簇通常具有特定的几何形状和电子结构,在化学反应中表现出独特的性质和行为。
原子簇的形成是由于金属原子之间存在强的金属-金属相互作用,这种相互作用使得金属原子之间共享电子,形成多个金属-金属键。
这些键合方式可以是桥键、面内和面外配位等。
原子簇的大小可以从二聚体到包含数十个甚至数百个金属原子的庞大簇合物。
原子簇在化学反应中具有重要的应用。
由于其独特的几何形状和电子结构,原子簇可以作为催化剂、反应中间体或反应底物参与到各种化学反应中。
例如,在烯烃复分解反应中,RuCl2(CO)2(PPh3)2这样的二茂铁二氯化钌催化剂可以通过与烯烃的配位和插入反应,促进烯烃的分解和重组。
此外,原子簇在材料科学领域也有广泛的应用。
由于其独特的结构和性质,原子簇可以作为功能材料、磁性材料、光电子材料等。
例如,Fe3S4是一种具有磁性的原子簇,可以用作磁记录材料;又如,Pt3Ni4是一种具有催化活性的原子簇,可以用于催化氢化反应。
在研究原子簇的过程中,科学家们通过合成、表征和反应等方法来探索其性质和行为。
随着科学技术的发展,原子簇的研究和应用将更加广泛和深入,其在化学、材料科学、能源科学等领域的应用前景也将更加广阔。
总之,原子簇是化学中的重要概念,它涉及到金属原子的键合方式和性质。
原子簇的研究不仅有助于理解化学反应的本质和机制,而且有助于发现新的功能材料和催化剂,推动科学技术的发展。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
铝原子簇摘要原子簇是现今化学研究的热点之一。
简要介绍了原子簇的概念,并详细介绍了铝原子簇中的Al13、Al14的结构、性质,以及铝碘化物原子簇的稳定性规律。
最后介绍了研究铝原子簇的意义。
关键词原子簇铝原子簇超原子凝胶模型Science 上发表了2篇美国宾夕法尼亚州大学教授A.Welford Castleman等关于铝原子簇(clusters of aluminum atoms)研究的文章[1,2],引起了广泛的兴趣和关注。
原子簇(cluster)是当今化学比较活跃的研究领域,涉及的内容非常广泛和丰富,取得了许多引人注目的研究成果。
最为人们所熟悉的原子簇可能就是足球烯(C60)。
了解原子簇,不仅能了解当前科技的发展与科学家们进行的探索,还能帮助人们在介观的角度上认识自然。
在20世纪80年代以前,人们对物质系统的研究可分为宏观和微观2个层次。
约在20世纪80年代中期,人们提出了介观这一概念,并将尺度介于宏观和微观之间的体系称为介观体系。
为了研究的方便,人们又把介观体系细分为亚微米体系(0.1 μm~1 μm)、纳米体系(1 nm~100 nm)和原子簇(典型尺寸<1 nm)[3]。
原子簇从其大小上看,是介于原子分子和纳米体系之间的。
原子簇化学是无机化学、物理化学、结构化学和金属化学相互交叉衍生出的一门边缘学科。
进入20世纪90年代,它与纳米科学技术、介观物理相结合,成为一门迅速发展的新型交叉科学。
铝原子簇是该领域的研究热点之一。
1 原子簇1.1 原子簇是什么原子簇是由几个乃至几百个原子以化学键结合在一起的聚集体,是一种特殊的物质状态[4]。
也有学者认为:原子簇是由几个乃至几千个原子或分子(国际上多数定义原子数在10~10 5范围)通过一定的物理或化学结合力组成的相对稳定的微观和亚微观聚集体[5]。
原子簇的名称是F.A. Cotton 于1966年首次提出的[6]。
1982年,徐光宪建议将原子簇化合物定义为:以3个或3个以上的有限原子直接键合组成多面体或缺顶多面体骨架为特征的分子或离子[7]。
目前的一些文献中常将原子簇和原子簇化合物均称为原子簇[8]。
原子簇按照原子间的化学键和是否带有电荷可分为:离子型原子簇、共价型原子簇、类离子型原子簇等。
按照构成原子簇的微粒进行分类,可分为惰性元素原子簇、金属卤化物原子簇以及金属原子簇等。
相对早期的研究曾发现,若要Hg、Ca、Zn等金属保持金属的导电、有光泽等特性至少需要13个原子结合在一起形成原子簇[9];固氮酶中的活性中心铁钼辅因子是一种Mo—Fe—S原子簇,而参与传递储存电子的则是Fe4S4原子簇;半导体器件尺寸的不断缩小,引起人们对硅原子簇性质的研究兴趣;C60的出现更进一步激起了人们研究原子簇的热情,而Al13、Al14原子簇的研究成果则在实验设计和量子力学计算方面达到了前所未有的高度。
原子簇研究的基本内容包括:原子簇几何结构和稳定性的规律;原子簇是如何由原子或分子发展而成的;在此发展过程中,原子簇的结构和性质如何变化;尺寸较小的原子簇,每增加1个原子,原子簇的结构就会变化,当变化到什么程度(尺寸多大)时,变成大块固体的结构;表面修饰及载体对原子簇特性的影响;原子簇的应用等方面。
1.2 金属原子簇研究的理论模型之一凝胶模型金属原子簇的研究是原子簇研究的重要组成部分。
人们提出了很多理论来解释金属原子簇的稳定性,其中应用较广泛的是凝胶模型。
该模型将金属原子簇看作一个整体,其中原子核和内层电子相当于一个球形的、带正电荷的核,外围是价电子形成的壳层,结构与原子很相似。
与原子不同的是,稳定的金属原子簇的电子排布是2、8、18、20、40……。
这些原子簇被称为“幻数原子簇”(magic cluster)。
具有稳定价电子数的“幻数原子簇”就可以被看作“超原子(superatom)”,因为它们是多个原子的集合体,同时又具有像单个原子一样形成化合物的能力[10]。
Castleman研究小组的研究在一定程度上证实和完善了凝胶模型。
1989年,他们研究了氧气与铝原子簇离子(即获得了1个额外电子的铝原子簇)的反应,观察到氧气会从某些铝原子簇离子中夺走铝原子,直到原子簇化为乌有。
当用多种不同大小的铝原子簇离子做实验时,质谱分析发现生成了含铝原子数分别为13、23、37的原子簇离子,说明这些原子簇离子不与氧气反应,是稳定的[11],而Al13的价电子数恰好是40个。
2 铝原子簇Castleman研究小组长期从事铝原子簇的研究,在实验数据的获得和理论计算方面做了高水平的工作,使铝原子簇研究在揭示Al13具有超卤素性质、Al14性质类似碱土金属和铝原子簇的稳定性和结构研究等方面有了重大的突破。
2.1 Al13表现出超卤素性质3 研究意义和前景3.1 制造纳米材料纳米科技研究的技术路线可分为“自上而下”和“自下而上”2种方式。
“自上而下”是指通过微加工或固态技术,不断在尺寸上将人类创造的功能产品微型化,而“自下而上”是指以原子、分子为基本单元,根据人们的意愿进行设计和组装,从而构筑成具有特定功能的产品.利用原子簇研究成果,人们可以将原子簇作为建筑板块或积木,搭建出各种具有特定性质的纳米材料。
这种制造纳米材料的方式是自下而上的方式。
长期以来人们习惯于通过“自上而下”的方式来制作纳米材料,即将大颗粒变为小颗粒。
预计“自上而下”的方式将会受到瓶颈限制,因此,“自下而上”的制作方式将愈来愈受到重视。
以原子、分子为起点,去设计制造具有特殊功能的产品是纳米科技的最终目的之一。
3.2 制造有效的固体燃料添加剂纯铝粉燃烧时能放出大量的热,但是它的化学性质太活泼,在没有燃烧前就已被氧化。
Castleman认为解决办法就是利用惰性的Al13[12]。
他计划将铝原子簇离子与易燃的有机物料结合,这样的话,燃料就会非常稳定。
当燃烧开始,铝原子簇离子失去额外电子回复中性后,燃料就会充分燃烧。
3.3 将元素周期表扩展成为一个三维立体结构20世纪80年代,加州理工学院的Thomas Upton发现,6个铝原子组成的原子簇能催化氢的裂解,催化方式与钌大致相同。
钌在化工上经常被用作催化剂。
现在,人们又发现中性的Al13原子簇和卤素性质相似,并且像一个介于碘和溴之间的卤素。
而Al14原子簇又类似碱土金属。
这样看来,一种元素的原子簇完全有可能表现出另一种元素的性质。
于是人们设想若将这些原子簇按性质递变规律排列在现有周期表的第三维上,就可能产生一个三维的周期表,在这个周期表中,新增的并不是元素,而是原子簇。
这无疑是十分大胆而又诱人的设想。
参考文献[1]Bergeron D E,Roach P J,Castleman Jr A W , et al . science, 2005,307:231-235[2]Bergeron D E,Castleman Jr A W, et al . Science, 2004,304:84-87[3]赖珍荃,周斌,王珏.自然杂志,1998,20(5):259-262[4]/support/frm/chenguozhenlansun.htm.原子簇离子的激光产生与研究.2006-2-8[5]王广厚.团簇物理学.上海:上海科学技术出版社,2003:1-3[6]胡英.物理化学参考.北京:高等教育出版社.2003[7]徐光宪.高等学校化学学报,1996,3(专刊):114,转引自[6][8]唐敖庆,李前树.原子簇的结构规则和化学键.济南:山东科学技术出版社,1998,转引自[6][9]http://www.chemie.hu-berlin.de/agrad/index.html.Research Area.2006-2-8[10]Leuchtner R E,Harms A C,Castleman Jr A W.J.Chem.Phys.,1989,91,:2753-2754[11]/alert/Castleman3-2004.Research Reveals Halogen Characteristics of Cluster of Metal Atoms.2005-10-25[12]/superatom.htm.A new kind of alchemy.2006-2-8[13]Rao B K,Jena P.J.Chem.Phys.,1999,111:1890-1904Aluminium ClustersMA Hongjia LI Ling(College of Chemistry and Environmental Science of Nanjing Normal University,Jiangsu Province,210097 )AbstractCluster is one of the hot research fields in chemistry nowadays. In thispaper, the concept of cluster is introduced. Moreover, the structures and properties of Al 13 and Al 14 as well as the stability rules of aluminium iodide clusters are introduced. Finally, the significance of aluminium clusters research is given.Keywords cluster, aluminium clusters, superatom, jellium model“本文中所涉及到的图表、注解、公式等内容请以PDF格式阅读原文”。
