光催化与光电催化第三章
光催化反应原理简介及应用

光催化反应原理简介及应用光催化反应是一种利用光能激发催化剂表面电子,从而促进化学反应进行的反应过程。
光催化反应的原理是利用光能激发催化剂表面的电子,将其提升至更高能级,形成活性中心,从而促进化学反应的进行。
光催化反应通常涉及光生电化学过程和表面催化反应过程。
在光生电化学过程中,光能被吸收后,产生电子-空穴对,并参与化学反应。
在表面催化反应过程中,催化剂表面的活性中心与吸附的物质发生反应,促进化学反应的进行。
光催化反应在环境保护、能源利用和化学合成等方面有着广泛的应用。
在环境保护方面,光催化反应可用于废水处理和空气净化。
通过光催化反应,可以将水中的有机物、重金属和其他污染物高效地转化为无害的物质。
此外,光催化反应还可以利用太阳能将二氧化碳转化为有用的化学品,从而减少大气中的二氧化碳含量,减缓全球变暖的进程。
在能源利用方面,光催化反应可用于光解水制氢和光催化CO2还原制备燃料等领域。
光解水制氢是一种利用太阳能将水分解为氢气和氧气的过程,可以用于储能和清洁能源生产。
光催化CO2还原可以利用太阳能将二氧化碳转化为甲烷等燃料,有助于解决能源和环境问题。
在化学合成方面,光催化反应可以用于有机合成和药物合成。
光催化反应可以实现在温和条件下进行多种化学反应,从而提高合成效率并减少副产物的生成,具有重要的应用价值。
除了上述应用外,光催化反应在电化学、光电子器件和材料科学等领域也有着重要的应用。
光催化反应可以用于制备催化剂、光催化剂、光电催化剂和光催化电极,可用于制备水解制氢、光催化解污染物和光催化CO2还原等器件。
此外,光催化反应还可以用于表面修饰、光催化涂层和光催化材料等方面。
这些应用有助于提高能源利用效率、提高新能源和新材料的研发水平,具有重要的科学和应用价值。
总之,光催化反应具有重要的科学价值和应用前景。
光催化反应的原理和应用将为环境保护、能源利用和化学合成等领域带来新的技术突破和发展机遇。
光催化反应的深入研究和应用将为人类社会的可持续发展作出重要贡献。
光催化与光电催化
分 辨 率 0.1nm 放 大 倍 数 80~100万倍。
水热合成系列钙钛矿DyMnO3和DyFeO3
熔融盐法制备钙钛矿材料EDS分析
特征X射线:当样品原子的内层电子被入射电子激发或电离时,原子就会处于能 量较高的激发状态,此时外层电子将向内层跃迁以填补内层电子的空缺,从而使 具有特征能量的X射线释放出来。
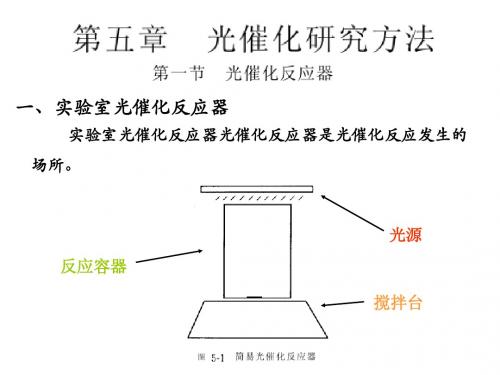
自然光源
自然光源为太阳光,一般将反应器设计成平板型光催 化反应器和聚光式光催化反应器等类型。
2. 催化剂的存在方式
选择催化剂的存在方式也是光催化反应器中的重要因素之一。 悬浆态 悬浆体反应器 负载型 催化剂的存在方式 固定态 固定床反应器 薄膜型 填充型 流化态 流化床反应器
一定程度上 实现光催化 剂使用后的 回收和重复 利用。
而携带流过此固定相的流体称为流动相。
色谱法因具有分离性能高、灵敏度高和分析速度快等特点, 已经成为现代仪器分析方法中应用最为广泛的一种方法,也在光催
化研究中得到广泛应用。
气相色谱法是采用气体(载气)作为流动相的一种 色谱方法,色谱仪通常由载气系统、进样系统、分离系
统、检测系统和记录与数据处理系统等部分构成。
射时,在溶液中急剧衰减。因此,只有溶液表面 的那层能够利用光源,效率较低。 第二 不能避免溶质与溶剂的挥发损失。如果被降解的对
象(溶质)是具有一定挥发性的有机物,则在反应
过程中会有挥发损失,程度与有机物的挥发性大小 有关。如果光源的功率较大,还会导致溶剂发热而 蒸发损失,使得反应结果存在较大误差。
圆柱形光催化反应器的优点:
(a) Transmission electron microscopy (TEM) image of La0.5Ba0.5MnO3 nanocubes。 (b) ( b) High-resolution TEM image of a 30-nmLa0.7Ba0.3MnO3nanocube along with a selected area diffraction pattern shown inthe inset.
光化学基础(课堂PPT)

.
25
➢ 有机分子吸收紫外和可见光后,一个电子就从原来较低 能量的轨道被激发到原来空着的反键轨道上,被吸收的光 子能量用于增加一个电子的能量,通常称为电子跃迁。
➢ 有机分子电子跃迁的方式(见图1.4): π→π*、 n →π*、n →σ*、σ→σ*
➢ 有机化合物中能够吸收紫外或可见光的基团称为生色团。
能量小于或等于1eV。
红外光作用于分子,只能引起分子转动能级 与振动能级的改变,从而发生光的吸收,产生红 外吸收光谱。
紫外和可见光作用于分子,可使分子的电子 能级(包括转动能级和振动能级)发生改变,产生 可见—紫外吸收光谱。
.
20
光对分子的作用
2、分子对光的吸收 ❖ 分子吸收光的本质:
是在光辐射的作用下,物质分子的能态发生了 改变,即分子的转动、振动或电子能级发生变化, 由低能态被激发至高能态,这种变化是量子化的。 ❖ 能态之间的能量差必须等于光子的能量:
❖ 量子产率:光化学反应的效率通常用量子产率()来表示,其 定义为:
分解或生成的分子数 吸收的光量子数
2)初级光化学过程与次级光化学过程
.
41
3)初级光化学过程的主要类型
在对流层中发生不同类型的初级光化学过程,但是对于气相 主要类型有:
(a)光解。一个分子吸收一个光量子的辐射能时,如果所吸收 的能量等于或多于键的离解能,则发生键的断裂,产生原子或 自由基。例如:
.
22
evH
H
F= C
( 可忽略)
磁 矢 量
分子内的电子 。
v sec
F=e
电矢量
传播矢量
。
C=3 10 18 A/sec
图1.2 光对分子. 作用示意图
光催化原理

光催化原理
光催化原理是指利用光能激发催化剂表面的电子,使催化剂具有更强的催化活性的过程。
在光催化反应中,光能作为外界能量来源,可以激发催化剂表面的电子从基态跃迁到高能级,形成活性物种。
这些活性物种可以与待催化物质发生反应,并加速催化反应的进行。
光催化反应主要涉及催化剂、光源和反应物三个要素。
其中,催化剂是实现光催化的核心,是光催化反应能否发生和催化效果的关键。
光催化剂一般由半导体材料或含有过渡金属的化合物构成,具有良好的光催化性能。
当催化剂暴露在光源下时,其表面会吸收光的能量,产生电子-空穴对。
这些电子-空穴对
能够参与氧化还原反应,从而产生活性物种。
光催化反应中的光源通常为紫外线或可见光,其能量可以激发催化剂表面的电子。
不同波长的光源对应的激发能量不同,因此选择合适波长的光源对于光催化反应的进行是至关重要的。
在光催化反应中,反应物分子与光催化剂表面形成接触后,活性物种能够在光催化剂表面发生反应。
这些活性物种可以有氧化还原活性的电子或提供氢、氧等活性基团的化学物质。
光催化反应可以加速原本需要高能消耗的化学反应,实现高效率、高选择性的催化反应。
总的来说,光催化原理是通过利用光能激发催化剂表面的电子,形成活性物种,促进催化反应的进行。
这种原理在环境净化、能源转换、有机合成等领域有着广泛的应用前景。
半导体光催化基础第三章光催化原理

二、光催化反应类型
1. 敏化光反应: 起始光激发发生在催化剂表面吸附的分子上,该分子再与基态催化剂本底反应的过程。分为两种情况: (1)绝缘体(或非光活性半导体),固体不参与光诱导电子过程;(2)半导体具有合适能级,半导体基底与被吸附物之间存在很强的电子相互作用,固体参与光诱导电子动力学过程.
第一规则:(Grottus-Draper规则,1818),只有被物质吸收的光才能有效地引发物质的光化学变化;
第二规则:量子活化规则(Stark,1908;Einstein,1912)在光化学反应初期过程中活化一个分子吸收的光,称为1光量子。因此,这时的量子收率总和必须等于1。
01
光催化反应:A B
02
上式表明,光催化反应仍是仅有光()或仅用具有催化功能的K都不能使其进行,只有在光和催化剂同时存在时才能进行的反应。
03
例:H2O H2 + O2。
04
n-型半导体吸收λ=400nm的光形成电子空穴对,这样生成的电子将水还原成氢,而空穴则可将水氧化成氧。而在无TiO2情况下,水必须吸收波长小于165nm的所谓真空紫外光后才能使其电子状态激发到可以断键的程度。
光催化原理
单击此处添加正文,文字是您思想的提炼,为了演示发布的良好效果,请言简意赅地阐述您的观点。
01
多相光催化研究始于1972年,藤岛昭和本多健一在n-型半导体TiO2电极上发现了水的光电催化分解作用。 光催化反应与光催化剂 催化反应:A B 反应的驱动力只是热能,只限于热力学上可进行的反应。 光催化反应:A B 光能( )被直接用于实现化学反应的基元作用。 克服反应势垒所需的能量: 反应粒子(分子、离子)的激发过程中提供;
半导体光电催化技术.

半导体光电催化第一章1.原子轨道相互交迭情况原子钟的电子分布在内外层电子轨道上,每一层轨道对应确定的能量。
当原子相互接近并形成晶体时,不同原子的内外壳层。
电子轨道之间就有一定的交迭,相邻原子最外层轨道交迭最多,内层轨道交迭最少。
当原子组成晶体后,由于原子轨道的交迭,电子不再完全局限在某一个原子钟,它可以转移到相邻原子上去,而且可以从邻近的原子轨移到更远的原子上去,以致任何一个电子可以在整个晶体中以一个原子转移到另一个原子,不再属于某个原子所有,这即晶体中的电子共有化运动。
2.用能级的形式解释能带禁带:在相邻两个能带之间的区域中,不存在电子占有的能级,将这两个能带间的区域称为禁带。
每个能带和禁带的宽度是由各种晶体的具体原子结构和晶体结构所决定的。
禁带宽度为零点几到几个电子伏。
由于可得出①同一晶体的某个能带,其宽度一定,这是因为能带宽度主要取决于电子轨道的交迭程度。
对同一晶体,原子间距是常数,所以各轨道的交迭程度一定。
②同一晶体的不同能带,上面的宽,下面的窄。
这是因为上面的能带与原子的外层轨道相对应,外层轨道交迭多,能带就宽,内层轨道交迭少,能带就窄。
由此可见,能带的宽窄实际上反映了电子共有化的自由程度。
3.满带:能带全部被电子填满。
内层电子轨道对应的能带。
零带:能带中可占据能级全部是空的。
价带:价电子所处的能带,最高电子占有能带。
(HDMO),可能是全部填满或部分填满。
导带:最低空能带(LLIMO)4.能带对不同材料的解释(对导体,半导体电导率的差别)按电阻来分:金属导体p<10-6Ω·m绝缘体p>107Ω·m半导体10-6<p<107Ω·m对于导体来说:导带与价带之间不存在禁带,而半导体的导带与价带之间存在一禁带宽度,绝缘体的禁带宽度更大一些,因此导体,半导体和绝缘体的电阻率逐渐增大。
☆能使半导体中自由电子浓度增加的杂质称为“施主”型杂质☆相应的主要依靠电子导电的半导体称为电子半导体或n型半导体☆能使半导体空穴浓度增加的杂质叫做“受主”型杂质☆主要依靠空穴导电的半导体则叫做空穴半导体或P型半导体5.本征半导体和本征激发(杂质激发对结构的影响)半导体按导电机制分为:本征半导体,和非本征半导体(掺杂半导体)本征半导体:晶体结构完整而不含杂质的半导体称本征半导体,半导体晶格中不存在自由运动的电子,电子都被束缚在原子核周围。
光催化与光电催化

光催化与光电催化
光催化与光电催化都是通过光照下催化剂对化学物质进行反应的方法,但其具体机理和应用有所不同。
光催化是指通过光照下催化剂促进化学反应的方法,此时光的能量被吸收后转化为催化活性位点的能量,使得反应物在较低的温度和压力下发生化学反应。
光催化广泛应用于环境保护、水处理、空气净化、有机合成等领域。
光催化反应的典型例子是可见光下二氧化钛催化氧化有机物。
在此反应中,二氧化钛表面吸收光能后,经历一系列复杂的物理化学过程,生成具有氧化性的电子空穴对,这些电子空穴对可以将水分子氧化为具有氧化性的自由基,从而促进有机物的氧化反应。
相比之下,光电催化则是光电转换和光化学反应相结合的过程。
在此过程中,外加电场和有机化合物的光催化剂共同作用,将光能转换为电能和化学能,实现光电催化反应。
光电催化的应用非常广泛,涵盖了太阳能电池、光电催化分解水为氢气、光电阴极、光电催化二氧化碳还原等多个领域。
光电催化反应时间短、效率高,能够在不需要外界供应的条件下实现化学反应,有望成为一种能源的替代技术。
总之,光催化和光电催化分别是光化学反应和光电转换与光化学反应的两种光化学反应形式,其在环境净化、能源转化和有机合成等领域都有广泛的应用前景。
半导体光催化基础第三章光催化剂

3.7.1 利用有机染料作敏化剂
将类似叶绿素分子结构的有机光敏染料(如
金属卟啉化合物,金属酞菁化合物,联吡啶 衍生物等),有机耦合在宽带的半导体材料 上以扩展对可见光的采集范围,提高太阳能 利用效率的方法,称作有机光敏染料敏化 。
染料敏化纳晶半导体电极PEC电池的工作原理
工作原理:染料分子S受可见光激 发成为激发态分子S*,S*再释放 出一个电子并注入半导体的导带而 被氧化为S+(1),光注入的电子 通过半导体体相和背接触势垒 (4),再经外电路及负载流入对 电极后,将溶液中的氧还对中继物 (redox relay)R+还原为R(5), R再将S+还原为S(6),如此反复 循环,电流则通过负载对外输出电 能。S*注入的导带电子亦可转移到 半导体表面直接将S+还原为S(2) 或将R+还原为R(3)。以上电荷 转移过程中,(1)为快步骤,(2) (3)为逆反应,(4)为慢步骤, 后面三个步骤决定着电池的光电转 换效率。
窄禁带半导体敏化
选择合适的能级匹配时,他们内部的pn结有助于光生电子空穴的有效分离。两种半导体在能级位置上的差异,是组成 复合半导体的前提,也是实现电荷转移过程的关键因素。
3.7.3 杂质掺杂敏化剂
利用杂质掺杂实现宽禁带半导体吸收光谱的扩展, 早在70年代光解水研究中就已提出 。
杂质掺杂敏化
掺杂元素对纳米 TiO2 吸收光谱 的影响 (1)Rh(2)V(3)Fe (4)Cu(5)Ni(6)Cd
3.6 光催化剂
光催化研究的核心在于对于指定反应如何
开发出一个高效、稳定、廉价的优良的光 催化剂 。 目前,催化剂的制备“艺术”,仍然停留 在经验或半经验的水平 。
3.6.1 光催化设计的一般原则
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
由图中可以看出,在大于387nm的光子辐射下,激发能
虽不足以激发复合光催化剂中的,但却可以激发CdS,使其
发生电子跃迁。光激发产生的空穴留在CdS的价带,电子则 跃迁到TiO 2 的导带上。这种电子从CdS 向TiO 2 的迁移不仅 大大扩宽了TiO 2 的光谱响应范围,而且有效地减少了光生 电子 空穴的复合概率,提高了光催化剂的量子效率。 TiO2与适量具有发达孔结构和较大比表面积的绝缘体复 合,载体能够从溶液中吸附大量有机分子为TiO2提供高浓度 反应环境,增加光生空穴和自由基与有机分子碰撞概率,提
高光催化效率。
离子掺杂
离子掺杂是利用物理或化学方法,将离子引入到TiO2
晶格结构内部,从而在其晶格中引入新电荷、形成缺陷或
改变晶格类型,影响光生电子和空穴的运动状况、调整其 分布状态或者改变TiO2的能带结构,最终导致TiO2的光催 化活性发生改变。 过渡金属离子 稀土金属离子 无机官能团离子以及其他离子
大多数实验证明,在一定范围内TiO2 的催化效率是随
着投加量的增加而增加的。但是当投加量高于某一值后其
催化效率不仅不会再提高,而且会有稍降的趋势。TiO2较为 理想的投加范围为0.5%-2%。
表明随着热处理温度增加,催化剂颗粒尺寸逐 渐变大,800℃出现,有锐钛矿向金红石的相变。
第四节 光催化氧化环境净化技术存在问题
相转移法(空气吹脱和吸附)
物理方法
环境净化技术
化学方法
过滤法(膜分离技术)
燃烧法
பைடு நூலகம்
传统环境净化技术: 物理法:只是通过物理作用将污染物富集并转移,易造成二次 污染; 化学法:装置复杂且耗能,而且存在燃烧不完全而生成有毒有 害中间产物的问题。
光催化氧化技术特点:
• 光催化过程是通过化学氧化的方法,把有机污染 物矿化分解为水、二氧化碳和无毒害的无机酸;
影响TiO2光催化反应的动力学因素
主要是载流子的产生和捕获效率,只有抑制电子和空 穴的复合,才能使光生载流子更有效地引发光催化反应。 在催化剂表面吸附的作为捕获剂的底物浓度或作为 载流子势阱的催化剂表面基团密度对催化剂的活性非常 重要。其他还有光照强度、催化剂用量、底物浓度等。
水中悬浮的金属氧化物TiO2,由于其表面离子的配位不饱和, 在水溶液中与水配位,水发生离解吸附而生成羟基化表面。
离子掺杂修饰TiO2
其中以金属离子掺杂为主
金属离子掺杂在光催化反应的作用特点与效果
吸 光 性 能
电 荷 扩 散
表 面 反 应
粒 径 和 晶 型
离子 掺杂
小离子 Li
大离子 稀土元素
稀土间隙红移:
在有催化剂参与的反应体系中, 光催化剂失活都 是一个非常普遍的现象。 一、
在光催化反应中,
TiO2 的表面性质,进而改善其光催化活性。 • 金属和TiO2 形成的空间电荷层中,金属表面将获得多 余的负电荷,TiO2表面上负电荷完全消失,从而大大提高
光生电子输运到吸附氧的速率。
• 金属-TiO2 界面上形成能俘获电子的浅势阱Schottky
能垒进一步抑制光生电子和空穴的复合。
贵金属沉积改性研究中Pt的改性效果最好,但成本较
吸附在金属氧化物表面羟基和水分子通过俘获光致空穴,形
成表面键合的羟基自由基。 有机物的吸附也可以直接或间 接地俘获电子和空穴。
光催化反应中有机物和羟基自由基之间可能发生的反应:
光催化氧化实验的光源多为中压汞灯,其他的还有高 压汞灯、低压汞灯和氙灯等光源的强度也是一个重要的影
响因素。相关实验证实应用大功率光源更合算。
第七、高浓度废水透光率。 第八、有机污染物降解中间产物的复杂性。
第九、工业化成本较高。
研究表明,通过对半导体材料沉积贵金属或 其他金属氧化物、硫化物,掺杂无机离子,光敏
化以及表面还原处理等方法引入杂质或缺陷,有
助于改善TiO2的光吸收,提高稳态光降解量子效
率及光催化效能。
贵金属修饰TiO2 是通过改变体系中的电子分布,影响
• 光催化氧化是一种室温深度氧化技术,在环境温 度就能将有机物分解,且反应装置简单。
光催化氧化技术实际应用中存在的不足方面
第一、量子效率偏低,单纯TiO2光催化剂的光生电子-空穴
对的再复合率高,光催化性能不突出。
第二、反应机制缺乏必要验证手段。 第三、TiO2选择吸附性能差, 极大地降低了光催化反应的 速率和选择性。 第四、光谱响应范围窄,对太阳能的有效利用率低。 第五、光催化剂粉末的分散问题。
高。Ag改性相对毒性较小,成本较低。
因此,Ag沉积改性制备高活性Ag/TiO2将是未来提高 TiO2活性的重要方向之一。
复合半导体
半导体复合本质上是另一种粒子对TiO2的修饰。
复合方式
复合半导体容易地调节半导体的带隙和光谱吸收范 围;半导体微粒的光吸收为带边型,有利于太阳光的有 效采集;通过粒子的表面改性可增加其光稳定性。
