金银花中绿原酸和黄酮的同时提取分离工艺研究
金银花中绿原酸提取方法的研究

2 方 法
2 . 1 金银花提取 工艺的比较 2 . 1 . 1 水 煎煮 法 取 金银 花 3 0 g + l O倍 量水 一 煎 煮 3
取金银 花 2 0 g + l O倍 量 乙醇一
1 . 8 7 a r g 置2 5 m L容 量瓶 中 ,加 5 0 %甲醇使溶解 并稀释
裹5 验 证 试 验 结 果
参 考 文 献
川 盂 日增 。 石建平 . 等。 金银花 中绿原酸的提取工艺及抗 菌
2 0 0 8 。 l 1 ( 8 ) : 9 4 2 — 9 4 3 .
【 3 】 张春华, 严云良. 医药数理统计( 第 l 版) 【 ^ = I 】 . 北京: 科学出
中圈分类号 : R 2 8 4 . 2 文献标识码 : A
S t u d y o n Ex t r a c t i o n o f Ch l o r o g e n i c Ac i d i n F l o s Lo n i c e r a e
W ANG Ya n g - q i u, HE Mi a o
2 . 1 . 2 乙醇 回流提 取
回流提取 3 次, l h / 次一合并提取液一减压浓缩至 l: 1 的浸膏 。 2 . 1 . 3 酸 醇 回 流提 取 取 金银 花 2 0 g + 1 0倍 量 乙 醇 ( p H 4 ) 一 回流提取 3次 , l h /果 与 分 析
3 . 1 提取工艺 比较
通过 3 种 提取 工艺 比较 , 水 提结果偏低 , 此法不 可 行; 醇提 和酸 醇提法绿原 酸转移率较高 , 二 者差别不大 ( 表2 ) 。 考虑实验简便 , 故选择醇提金银花 , 制定 因素水 平表 , 做正交试验 优选最佳工艺 。
金银花中提取分离总黄酮的工艺研究

文章标题:金银花中提取分离总黄酮的工艺研究导言1. 金银花是一种常见的中草药材,广泛用于食品和药物制备中。
2. 其中的总黄酮具有抗氧化、抗炎和抗肿瘤等多种药理作用,因此对其提取分离的工艺研究具有重要意义。
工艺研究方法1. 传统提取方法:水煎、醇提等2. 现代提取方法:超声波提取、微波提取等3. 不同提取方法的优缺点比较1) 传统提取方法:操作简单,成本低,但提取效率低,环境污染严重2) 现代提取方法:提取效率高,操作简便,但设备成本较高提取工艺优化1. 提取溶剂的选择1) 水、乙醇、丙酮等2. 提取温度和时间的优化1) 不同温度下提取总黄酮的效果对比2) 不同提取时间下提取总黄酮的效果对比3. 提取压力和超声波功率的优化1) 不同压力下提取总黄酮的效果对比2) 不同超声波功率下提取总黄酮的效果对比分离工艺研究1. 薄层色谱法2. 高效液相色谱法3. 分离效果比较1) 薄层色谱法的分离效果2) 高效液相色谱法的分离效果4. 最佳分离工艺的确定总结与回顾1. 金银花中提取分离总黄酮的工艺研究是一项复杂但具有重要意义的工作。
2. 通过对不同提取和分离工艺的研究,可以找到最适合的方法来提取和分离金银花中的总黄酮。
3. 未来的研究方向可以集中在提高提取效率、降低成本、减少环境污染等方面。
个人观点和理解在提取分离总黄酮的工艺研究中,我认为现代提取方法具有更大的发展潜力,可以提高提取效率、减少操作时间和成本,并减少对环境的影响。
分离工艺研究也需要不断优化,以提高总黄酮的纯度和稳定性。
希望未来相关研究能够更加深入,为金银花的应用提供更多可能性。
结语通过对金银花中提取分离总黄酮的工艺研究,我们可以更好地利用这一中草药材,并发掘其更多的药理价值。
这项工作的持续深入研究将为中药制药行业带来更多的创新和发展。
提取总黄酮的过程中,首先需要选择合适的提取溶剂。
在传统方法中,水和醇是常用的提取溶剂,它们操作简单,成本低,但提取效率相对较低。
金银花中绿原酸提取工艺研究
第5期刘金磊,等:金银花中绿原酸提取工艺研究-5 -金银花中绿原酸提取工艺研究刘金磊,邓皮凯,邓仕英(长江大学工程技术学院,湖北荆州434020)摘要:绿原酸作为金银花中的主要 成分,具有高 抗氧化、抗病毒、保肝利胆等功效,在医化工和食 有广泛的应用。
金银花为原料, 醇提法 ,探讨了 、、料液比、 、 浓及 pH 值 素对绿原酸 影响, 了 金银花中绿原酸的最:以70%的乙醇,料比为1 : 25,控制pH 值为6,60 < , 60 min 。
关键词:金银花;绿原酸;提中图分类号:TQ460.7文献标识码:A 文章编号:1008-021X ( 2021) 05-0005-02金银花作 见的植物,具有清热解毒,疏散风 功效,广泛用于中药制剂、抗病毒、降血脂等。
其中最主要的有效 成分为绿原酸,是 抗氧化剂,是重要 质,具有抗菌、抗病毒、保肝利胆、抗氧化等功效,在临床 中有重要作用。
近年来,从金银花中 绿原酸受到广泛关注”勺。
,绿原酸方法主要有:酶 法、超声波法、水醇 !法*4*。
王 [5]方 金银花中绿原酸,探讨了最 工艺;[6] 水热法对绿原酸进, 响分析法优化了 。
通过醇提法,对金银花中的绿原酸 ,探了 素对绿原酸影响, 过程中,影响 量 素 了分析。
1实验部分15实验材料与仪器金银花,无水乙醇(AR )、甲醇(AR )、丙酮(AR )、 酸 (AR )、氢氧化纳(AR )、绿原酸 (98%)、723分光光度计、DZTW -电子 、 、真空泵、 瓶、 烧瓶璃仪器。
15实验过程1.2.1 标准曲线的绘制6 mg 绿原酸,加 量80%的乙醇 解后,定容到50 mL 容量瓶的刻度线,静 备用。
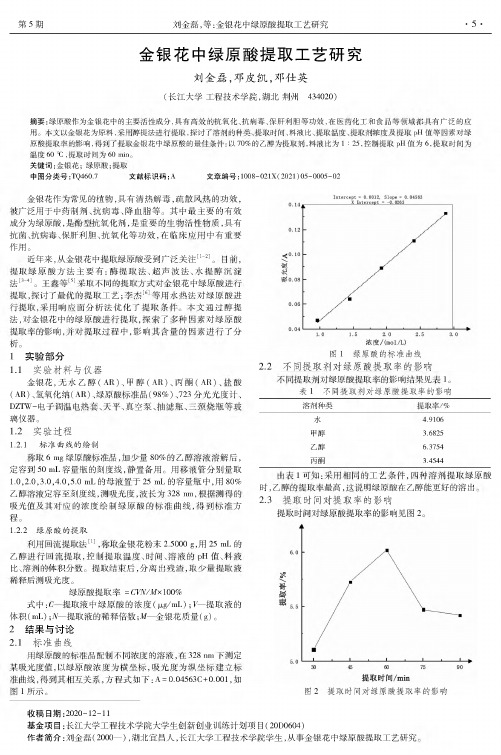
用移 管分别量取 1.0,2.0,3.0,4.0,55) mL 的母 于 25 mL 的容量瓶中,用 80%乙醇 定容至刻度线,测光度, 328 nm , 测吸光值及 浓度绘制绿原酸 曲线, 方程。
1.2.2绿原酸的提取回 法⑴, 金银花粉末2.5000 g ,用25 mL 的乙醇 回 ,控制 、 、 pH 值、料比、 体积分数。
HPLC法检测金银花中的绿原酸和黄酮类物质的研究

3.4、 3.4、样品的测定
表3
木犀草素 66.76 绿原酸 1345.91
样品的含量测定( g/g 样品的含量测定(µg/g )
芦丁 17.65 阿魏酸 33.65 新绿源酸 59.85
四、结论
本实验研究建立了用高效液相色谱法同时测定金银花中 的五种物质, 的五种物质,采用乙醇提取法和超声波萃取对金银花粗粉进 行了预处理。实验结果表明,采用80%乙醇浸泡和超声波萃取 行了预处理。实验结果表明,采用80%乙醇浸泡和超声波萃取 80% 能够有效的提取金银花中的五种有效成分,样品中的绿原酸 能够有效的提取金银花中的五种有效成分, 含量最高,五种组分的加标回收率为93.3%-98.9%, 含量最高,五种组分的加标回收率为93.3%-98.9%,相对标准 93.3% 偏差RSD≤3.02%。该方法提取率高,操作简单,重复性好, 偏差RSD≤3.02%。该方法提取率高,操作简单,重复性好, RSD≤3.02% 可同时分析金银花中的有机酸和黄酮类成分等有效成分, 可同时分析金银花中的有机酸和黄酮类成分等有效成分,改 变了把有机酸和黄酮类等分开的传统方法, 变了把有机酸和黄酮类等分开的传统方法,同时也提高了金 银花中的有效成分的提取率。
2.2、 2.2、样品的预处理
准确称取金银花粗粉5.064g, 准确称取金银花粗粉5.064g,置具塞锥形 5.064g 瓶中,准确加入80%乙醇50ml,浸泡24h, 瓶中,准确加入80%乙醇50ml,浸泡24h,转移 80%乙醇50ml 24h 至容量瓶中,然后在通风橱中超声波萃取 至容量瓶中, 30min,抽滤,合并滤液,再在60° 30min,抽滤,合并滤液,再在60°C下旋转蒸 60 发浓缩,并用石油醚脱脂, 0.45 m微孔滤膜。 发浓缩,并用石油醚脱脂,过0.45µm微孔滤膜。
金银花中绿原酸和黄酮的同时提取分离工艺研究

将金银花原料在 2.1 节优化的工艺条件下提取,得 绿原酸和总黄酮的浓缩液。选择聚酰胺为吸附剂,选 择不同体积分数的乙醇(1 0 %、5 0 %、9 0 %)作为洗脱 剂,通过柱层析梯度连续洗脱,得到绿原酸、水溶 性黄酮和脂溶性黄酮 3 个不同类型的洗脱物。测定结 果见图 3。
mAU
350 300 250 200 150 100
1.3.1 紫外分光光度法
1.3.1.1 芦丁标准溶液的配制
收稿日期:2009-06-11 基金项目:国家自然科学基金项目(20565003);宁夏大学科学研究基金项目(ZR200706) 作者简介:郝凤霞(1978 -),女,讲师,硕士,主要从事天然产物开发研究。E-mail:hfx220@
1 材料与方法
1.1 材料与试剂 金银花采自宁夏银川市合木公司。 甲醇、磷酸、9 5 % 乙醇、氢氧化钠、硝酸铝为
分析纯 天津市科密欧化学试剂有限公司;绿原酸、 芦丁对照品 中国药品生物制品鉴定所;实验室用水为 自制蒸馏水。 1.2 仪器与设备
Agilent 1100 高效液相色谱仪 美国 Agilent 公司; UV-2450 紫外 - 可见分光光度计 日本岛津公司;AL204 型电子天平 梅特勒 - 托力多仪器有限公司;101A-1E 型电热鼓风干燥箱 上海实验仪器厂有限公司;TDL802B 型台式离心机 上海安亭科学仪器厂;KQ-250DE 型 数控超声波清洗器 昆山市超声仪器有限公司;SHBⅢ型循环水式多用真空泵 郑州长城科工贸有限公司。 1.3 方法
450
500
550
600
波长(nm)
图 1 芦丁络合物吸收光谱
Fig.1 Absorption spectrum of rutin complex
金银花黄酮活性成分分离纯化与生物学效应研究

金银花黄酮活性成分分离纯化与生物学效应研究金银花为常用的传统中草药,功能清热解毒,临床上主要治疗细菌感染、感冒等症。
现代药理研究显示金银花中主要化学成分有黄酮类、有机酸类、苷类及挥发油等。
其中苷类中三萜皂苷类成分主要与金银花保肝利胆作用有关,而以绿原酸为主的有机酸类化合物和挥发油被认为与其抗菌活性相关。
但金银花黄酮是其组成中仍未经充分药理学研究的成分,其相关的生物学活性研究甚少。
对其它植物药黄酮的研究提示,该类成分多具有抗菌和抗氧化作用,因此本研究在国家自然科学基金的支持下,对金银花中黄酮类物质进行分离纯化,并考察其生物学效应,为说明金银花发挥药理作用的机制奠定实验基础。
第一部分金银花总黄酮的分离纯化及抑菌活性考察一、实验方法:1.金银花总黄酮的提取金银花总黄酮以醇提法提取,并采用均匀设计对提取条件进行优化。
2.金银花总黄酮初步分离及抑菌活性考察金银花总黄酮浸膏以DM130型大孔吸附树脂柱采用不同浓度乙醇(0,20%,40%,60%)梯度洗脱进行初步分离,对获得的分离组分按A、B、C等依序命名。
微量稀释法考察各分离组分对金黄色葡萄球菌(n=7)、肺炎克雷伯菌(n=5)、大肠杆菌(n=6)、铜绿假单胞菌(n=4)等细菌的MIC值。
3.金银花黄酮组分分离纯化及抑菌活性考察对方法2中分离所得且体外抑菌活性较好的黄酮组分采用制备型HPLC分离制备,对制备组分按A1、A2、 (1)B2等依序命名,并采用微量稀释法考察各制备组份对金黄色葡萄球菌(n=7)、肺炎克雷伯菌(n=5)、大肠杆菌(n=6)、铜绿假单胞菌(n=4)等细菌体外抑菌活性。
4.金银花黄酮抑菌活性成分结构鉴定对方法3中制备所得且体外抑菌活性较好组分采用HPLC分离提纯,并对纯化分离所得纯度较高单一成分进行LC-MS、1H NMR、13C NMR等鉴定。
二、实验结果:1.金银花总黄酮醇提法最佳提取工艺为:在10g金银花粉末(60目)中加入10倍体积50%乙醇溶液于90℃条件下提取1h。
金银花中绿原酸提取的研究前景和应用概述

金银花中绿原酸提取的研究前景和应用概述作者:赵御锜于方园来源:《食品安全导刊·下旬刊》2019年第02期摘要:绿原酸是金银花中的一种主要提取物。
常用的提取方法有聚酰胺柱层析法、石硫醇法、水提醇析法等。
本文介绍了绿原酸的生理活性及应用。
关键词:绿原酸;抗菌;应用金银花为忍冬科植物忍冬的干燥花蕾或者初开的花,呈棒状,上粗下细,略弯曲,长2~3 cm,表面黄白色或绿白色。
绿原酸是其主要有效成分,广泛存在于植物中,以金银花、杜仲中的含量较高,具有广泛的药理作用。
1 绿原酸的提取绿原酸半水合物为针状结晶(水)。
110 ℃变为无水化合物,熔点208 ℃,25 ℃水中溶解度为4%,热水中溶解度更大。
易溶于乙醇及丙酮,极微溶于醋酸乙酯。
绿原酸是由咖啡酸与奎尼酸生成的缩酚酸,是植物体在有氧呼吸过程中经莽草酸途径产生的一种苯丙素类化合物。
绿原酸分子结构中有酯键、不饱和双键及多元酚三个不稳定部分的特殊结构,可以用乙醇等极性溶剂提取。
提取时不能在高温强光下进行,绿原酸通常存放置于棕色瓶、冰箱冷藏下条件保存[1]。
1.1 聚酰胺柱层析法蔡鹰等人用此法研究过分离总黄酮[2],称取金银花加入10倍量70%的乙醇冷凝回流,再用两次8倍量回流两次,过滤,合并滤液,然后浓缩滤液或者用旋蒸仪旋干滤液至无醇味得到金银花浓缩液,用聚酰胺装柱常压下用乙醇作为洗脱剂收集流分,与标准品对照合并相同流分旋干及为绿原酸。
此方法得到的绿原酸纯度较高。
1.2 硅胶吸附法金银花粉末用乙醇索氏回流4小时,得到残渣和滤液(粗提液),60 ℃进行减压浓缩进行干燥得到粗体物在1∶1硅胶拌样得到提取物。
将拌好的混合样上硅胶柱,用乙酸乙酯、甲醇、水按不同比例洗脱得到含绿原酸的洗脱液。
在氯仿—甲醇梯度进行洗脱得到绿原酸。
1.3 其他方法石硫醇法和水提醇析法也常见。
高海谦曾用酸沉淀法与石硫醇法对比提取黄岑甙[3],将提取液濃缩用石灰乳调节pH,过滤沉淀物加入乙醇再用浓硫酸调节pH,再过滤滤液用氢氧化钠中和,过滤浓缩干燥得含量一般在20%左右绿原酸粗品[4]。
金银花中绿原酸的提取与分离

现代分离技术实验安排一、实验说明1、本课程实验为一次性综合大实验,采取分班进行,每班实验必须在连续两天内完成,各组的实验安排均为周六和周日的上午8点到晚上的8点。
每次实验1个班,每个实验由两个人共同完成,即两人一组,每组一套实验仪器和一张实验台。
每班的班长负责实验室的卫生和安全。
2、课程考核方法采用实验考察形式进行,每人只安排一次实验机会,过期不补,希望各位同学能够按时参加。
若有冲突,学生之间可相互对调。
3、进入实验室后,各组同学首先按照仪器清单检查仪器的数量和完好情况。
若有仪器短缺或破损等问题,请在上课后20分钟内与实验室工作人员及时联系,并要求实验人员进行补充或更换。
4、实验结束后,各组同学应对照仪器清单检查,分别洗净后交实验人员验收。
如有损坏或缺少,应按规定缴纳赔偿金。
因此,希望同学们爱惜仪器,认真操作。
实验期间,应注意保持实验室台面、地面和水槽的卫生,尤其是自己的工作区域。
同时应注意实验室的财产安全和自身安全,不可在实验室喧哗吵闹。
二、实验内容题目:金银花中绿原酸的提取与分离学习内容:固体中有效成分的提取(索氏法)技术;减压浓缩(旋转蒸发)技术;硅胶吸附柱层析;硅胶吸附TLC技术;薄层色谱对产品纯度检测金银花为忍冬科忍冬属植物忍冬及同属多种植物的干燥花蕾,它是一种“药食同源”的绿色植物,是临床常用的中药之一。
具有清热解毒、凉风散热、抗病毒、保肝利胆的功能,主治痈肿疗疮、喉痹、丹毒、热血毒痢、风热感冒、瘟病发热、急性支气管炎、肺炎、腮腺炎、胆道感染、关节炎等,能改善放、化疗所致的白细胞降低,有“中药中的青霉素”的美誉。
另外,金银花还被广泛地应用于保健品、化妆品、卷烟、食品等行业。
近代研究一般认为金银花的主要生物活性有效成分为绿原酸类化合物,并且常以绿原酸含量的高低来评价金银花质量的优劣。
绿原酸结构式HO HOOO2'3'4'5'6'8'9'OHHO OH OHO 1234567'1'三、实验方案 四、方法1、TLC 板的制备与活化在干净的研钵内加入约6g 硅胶GF254,在轻轻研磨的同时缓慢加入15ml 0.5%羧甲基纤维素钠水溶液。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Abstract:Chlorogenic acid and flavonoids were simultaneously extracted by ethanol with the aid of ultrasonic treatment from Flos lonicerae and then isolated by polyamide column chromatography. Results showed that three products (A, B and C) were
原 K2 13.85 9.25 11.53 12.53
酸 K3 5.00 9.86 9.17 10.44
直 k1 3.58 3.49 2.96 2.20
观 k2 4.62 3.08 3.84 4.17
分 k3 1.67 3.29 3.06 3.48
析 R 2.95 0.41 0.88 1.97
K1 27.35 19.95 19.2 14.22 黄 K2 25.89 16.1 20.66 23.06 酮 K3 6.93 24.12 20.31 22.89 直 k1 9.12 6.65 6.4 4.74 观 k2 8.63 5.37 6.89 7.69 分 k3 2.31 8.04 6.77 7.63 析 R 7.77 2.67 0.49 2.95
试验号 A
B
C
D 绿原酸得率(%) 总黄酮得率(%)
11
1
1
1
2.37
6.85
21
2
2
2
4.82
9.00
31
3
3
3
3.54
11.5
42
1
2
3
5.57
9.74
52
2
3
1
3.10
5.45
62
3
1
2
5.18
10.7
73
1
3
2
2.53
3.36
83
2
1
3
1.33
1.65
93
3
2
1
1.14
1.92
绿 K1 10.73 10.47 8.88 6.61
1 材料与方法
1.1 材料与试剂 金银花采自宁夏银川市合木公司。 甲醇、磷酸、9 5 % 乙醇、氢氧化钠、硝酸铝为
分析纯 天津市科密欧化学试剂有限公司;绿原酸、 芦丁对照品 中国药品生物制品鉴定所;实验室用水为 自制蒸馏水。 1.2 仪器与设备
Agilent 1100 高效液相色谱仪 美国 Agilent 公司; UV-2450 紫外 - 可见分光光度计 日本岛津公司;AL204 型电子天平 梅特勒 - 托力多仪器有限公司;101A-1E 型电热鼓风干燥箱 上海实验仪器厂有限公司;TDL802B 型台式离心机 上海安亭科学仪器厂;KQ-250DE 型 数控超声波清洗器 昆山市超声仪器有限公司;SHBⅢ型循环水式多用真空泵 郑州长城科工贸有限公司。 1.3 方法
C 时间(min) 10 30 50
D 次数 1 2 3
采用乙醇超声波法提取,考察了乙醇体积分数、 料液比、提取时间、提取次数这 4 个主要因素对绿原 酸和黄酮得率的影响,并采用正交试验法 L9(34)对主要 影响因素进行了优化,正交试验结果及分析见表 1~4。
※工艺技术
食品科学
2009, Vol. 30, No. 20 213
由表 2~4 直观分析及方差分析结果可知,综合考 虑绿原酸和总黄酮得率,得出最佳的提取工艺条件: 70% 的乙醇体积分数、料液比为 1:8、超声时间 30min、 超声温度为 3 0 ℃、超声提取两次。
表 2 正交试验结果表 L9(34) Table 2 Results of L9(34) orthogonal array design experiments
槲皮素和木犀草素:色谱柱为 Zorbax-C18 柱(250mm × 4.6mm,5μm);流动相:甲醇 -0.02% 磷酸(50:50, V / V );流速:1 . 0 m l / m i n ;检测波长:3 5 0 n m ;柱温: 3 0 ℃;进样量:1 0 . 0μl 。
1.3.2.2 对照品溶液的制备 绿原酸:精密称取绿原酸对照品 0.001g,用 50%
1.3.2.3 标准曲线的绘制 绿原酸:精密吸取绿原酸对照品溶液 0、1.0、3.0、
5.0、7.0、9.0、10.0ml 于 10ml 容量瓶中,用 50% 甲醇 定容至刻度,作峰面积 - 绿原酸浓度标准曲线,得直 线回归方程为 y = 14270x,R2 = 0.9997;绿原酸在 0~ 0.02mg/ml 范围内呈良好的线性关系。
甲醇溶解,转移至 50ml 容量瓶中,定容至刻度,摇匀, 配制成 0.02mg/ml 的绿原酸对照品溶液。
槲皮素和木犀草素:准确称取槲皮素对照品 0.030g, 用甲醇溶解并定容于 50ml 容量瓶,配制成 0.60mg/ml 的 溶液。取该溶液 1.00ml 用甲醇稀释并定容至 10ml,即 得浓度为 0.06mg/ml 的槲皮素对照品溶液。以相同的方 法制备浓度为 0.057mg/ml 的木犀草素的对照品溶液。
2 结果与分析
2.1 金银花中绿原酸和总黄酮的提取工艺研究
表 1 正交试验因素水平表 Table 1 Factors and levels in L9(34) orthogonal array design
水平 1 2 3
A乙醇体积分数(%) 70 50 95
B 料液比(m/V) 1:12 1:5 1:8
※工艺技术
食品科学
2009, Vol. 30, No. 20 211
金银花中绿原酸和黄酮的同时提取分离 工艺研究
郝凤霞,杨敏丽
(宁夏大学能源化工重点实验室,宁夏 银川 750021)
摘 要:采用乙醇超声波法提取,聚酰胺柱层析法分离的方法对金银花中的绿原酸和黄酮进行提取分离。结果表 明:聚酰胺柱层析法分离、梯度洗脱得到绿原酸、水溶性黄酮和脂溶性黄酮 3 个不同产品 A、B 和 C,其中 A 绿 原酸含量为 68.2%,得率为 1.34%;B 黄酮含量 95%,得率为 1.12%;C 中槲皮素和木犀草素含量分别为 7.5%、 16.9%,得率为 0.11%。 关键词:金银花;绿原酸;黄酮;槲皮素;木犀草素
1.3.1 紫外分光光度法
1.3.1.1 芦丁标准溶液的配制
收稿日期:2009-06-11 基金项目:国家自然科学基金项目(20565003);宁夏大学科学研究基金项目(ZR200706) 作者简介:郝凤霞(1978 -),女,讲师,硕士,主要从事天然产物开发研究。E-mail:hfx220@
槲皮素和木犀草素:取槲皮素对照品溶液和木犀草 素对照品溶液,分别用甲醇稀释,得一系列不同质量 浓度的对照品溶液后进样,以对照品溶液的浓度 C (μg / ml)为横坐标,峰面积 Y 为纵坐标,得槲皮素和木犀草 素的对照品溶液的回归方程分别为:Y=19.12C - 0.6778, R2 = 0.9999 和 Y= 47.20C + 120.2,R2 = 0.9999,它们分 别在 4.0~20μg/ml 和 3.8~19μg/ml 范围内呈良好的线性 关系。
212 2009, Vol. 30, No. 20
食品科学
※工艺技术
准确称取芦丁标品 0.0050g,用 95% 乙醇溶解,并 完全溶解后转入 25ml 容量瓶中,用 95% 乙醇定容,配 成 0.20mg/ml 的芦丁标准溶液。
1.3.1.2 标准曲线的绘制
1.2
0.9
吸光率
0.6
0.3
0
400
obtained from column chromatography with gradient elution, which were identified to be chlorogenic acid, soluble flavonoid and
lipid-soluble flavonoid, respectively. The chlorogenic acid content in product A was 68.2% with a yield of 1.34%; the
1.3.1.3 绿原酸和总黄酮得率的计算
浓缩液中绿原酸浓度×浓缩液体积 绿原酸得率(%)= ———————————————× 100
金银花质量
浓缩液中黄酮浓度×浓缩液体积 总黄酮得率(%)= ———————————————× 100
金银花质量
1.3.2 高效液相色谱法 1.3.2.1 色谱条件
绿原酸:色谱柱:Zorbax SB -C18 柱(250 mm × 4.6mm,5μm);流动相:0.4% 磷酸 - 乙腈(87:13,V/V); 流速:1.0ml/min;检测波长:327nm;柱温:2 0 ℃; 进 样 量:5 μl 。
吸光度
1
A=1.157C+0.014
0.8
R2=0.9988
0.6
0.4
0.2
0
0
0.2 0.4 0.6 0.8
1
浓度(mg/ml)
图 2 芦丁工作曲线 Fig.2 Standard curve of rutin
在最大吸收波长 505nm 处,分别测定不同浓度的络 合物,绘制标准曲线(图 2),得到芦丁浓度 C 与吸光 度 A 关系曲线的回归方程式:A=1 .15 7C +0 .01 4,R2= 0.9988。
50 0
0
2.634
2.5
5
7.5
时间(min)
a.绿原酸对照品
mAU
350 300 250 200 150 100
50 0
0
9.200
2.5 5 7.5 10 12.5 15 时间(min)
