重要有机化学反应类型归纳
高中化学十二种有机反应类型

高中化学十二种有机反应类型本文将介绍高中化学中的十二种有机反应类型。
这些反应类型涵盖了烃、醇、醛、酸、酯等常见有机化合物之间的基本转化。
了解这些反应对于学习有机化学至关重要。
一、烷烃的取代反应烷烃在光照或高温条件下,可以与氯气、溴蒸气等发生取代反应。
例如,甲烷与氯气在光照条件下反应,生成一氯甲烷和氯化氢。
二、烯烃的加成反应烯烃在催化作用下,可以与氢气、卤素等发生加成反应。
例如,乙烯与氢气在催化作用下反应,生成乙烷。
三、炔烃的加成反应炔烃在催化作用下,可以与氢气、卤素等发生加成反应。
例如,乙炔与氢气在催化作用下反应,生成乙烯和氢气。
四、醇的氧化反应醇可以在催化作用下,被氧化成醛或酮。
例如,乙醇在催化作用下被氧化成乙醛。
五、醛的氧化反应醛可以在催化作用下,被氧化成酸。
例如,乙醛在催化作用下被氧化成乙酸。
六、醛的还原反应醛可以在催化作用下,被还原成醇。
例如,乙醛在催化作用下被还原成乙醇。
七、酯的合成反应酯可以通过酸和醇的酯化反应生成。
例如,乙酸和乙醇在浓硫酸和加热条件下反应,生成乙酸乙酯和水。
八、酯的水解反应酯可以在水溶液中,发生水解反应生成酸和醇。
例如,乙酸乙酯在酸性条件下水解生成乙酸和乙醇。
九、酰胺的合成反应酰胺可以通过氨和羧酸或酸酐反应生成。
例如,氨和乙酸在浓硫酸和加热条件下反应,生成乙酸铵(酰胺)。
十、酮的双分子亲核取代反应酮可以在强碱条件下,发生双分子亲核取代反应生成烯烃和卤代烃。
例如,环己酮在强碱条件下反应,生成乙烯酮和卤代烃。
十一、羧酸的氧化反应羧酸可以在氧化剂作用下,被氧化生成过氧化物。
例如,乙酸在氧化剂作用下被氧化成过氧乙酸。
十二、环氧化合物的开环反应环氧化合物可以在酸或碱的作用下,发生开环反应生成醇或醚。
例如,环氧乙烷在酸性条件下开环生成乙醇。
以上是高中化学中常见的十二种有机反应类型。
这些反应为有机化合物之间的转化提供了基础理论依据。
在学习有机化学的过程中,掌握这些基本反应类型对于理解有机化合物的性质和合成具有重要意义。
有机物主要反应类型归纳

有机物主要反应类型归纳
有机物的主要反应类型可以归纳如下:
1. 取代反应:取代反应是有机化学中最常见的反应类型之一。
它涉及到一个原子或官能团被其他原子或官能团取代的过程。
例如,卤代烃可以和氢氧化钠反应形成醇,醛或酮可以通过醛缩反应形成酯或胺。
2. 加成反应:加成反应是指两个或多个分子中的原子或官能团结合在一起形成一个新分子的过程。
例如,烯烃可以和溴反应产生溴代烷烃,烯烃可以和水加成生成醇。
3. 消除反应:消除反应是指一个分子中的两个官能团通过消除一个小分子(通常是水、氨等)从而结合在一起形成一个新分子的过程。
例如,醇可以通过脱水反应形成烯烃,醇可以和酸反应形成醚。
4. 缩合反应:缩合反应是指两个或多个分子合成一个较大的分子的过程。
例如,酮或醛可以和胺反应形成Schiff碱,酮或醛可以和醇反应形成醚。
5. 氧化还原反应:氧化还原反应是指有机物中的电子转移过程。
氧化是指失去电子,而还原是指获得电子。
例如,醇可以被氧化为酮或羧酸,醛可以被还原为醇。
这些是有机物主要的反应类型,但并不是全部。
有机化学中还存在许多其他特定的反应类型,如重排反应、环化反应等。
有机化学反应理解和记忆方法
与卤素单质的加成反 应与:卤代烃的加成反应: 与水的加成反应:
碳碳双键加成反应 碳碳三键加成反应
醛基加成反应 苯环加成反应
和卤素单质及卤化氢加成:
CH2≡CH2 + 2Br2
CHBr2-CHBr2
浓H2SO4 50~60℃
—NO2 + H2O 苯的硝化
+ HO–SO3H 浓H2SO4
—SO3H+ H2O 苯的磺化
甲基和羟基对苯环起着活化的作用, 使得连有甲基或羟基的苯环发生取代 更容易
CH3
CH3
+ 3HNO3浓H2SO4 O2N— —NO2 + 3H2O
OH
OH
Br
Br
TNT的制取
NO2
–O– + H2O –COO– + H2O –CONH– + H2O
关于乳酸:
CH3CHCOOH OH
O —[ OCHC—] n
CH3
CH3
CH O
O
C
C
O
O CH
CH3
酚醛树脂
OCHH3
OH
浓盐酸
n + nHCHO
[
CH2–]+n nH2O
浓盐酸
nC6H5OH+ nHCHO
— [C6H3OHCH2—]n
提示: CH3—CH=CH—R
CH2Br—CH=CH—R
请填写下列空白: (1)A中所含官能团是____________ (名称)。 (2)B、H结构简式为__________、__________。 (3)写出下列反应方程式(有机物用结构简式表示) D→C_________________________________; E→F(只写①条件下的反应)______________。 ⑷F的加聚产物的结构简式为____________。
高考化学有机反应类型总结

高考化学有机反应类型总结
高考化学中的有机反应类型是化学考试中的重要考点,也是学生需要掌握的重要知识点。
以下是对高考化学有机反应类型的总结:
一、取代反应
取代反应是有机化学中最常见的反应类型之一,它涉及到有机物分子中的原子或基团被其他原子或基团所取代。
例如,甲烷与氯气在光照条件下发生取代反应,生成氯代甲烷和氯化氢。
二、加成反应
加成反应是烯烃和炔烃与氢气、卤素或卤化氢等发生反应,生成饱和烃或卤代烃的反应。
例如,乙烯与氢气发生加成反应,生成乙烷。
三、消去反应
消去反应是有机化学中另一种常见的反应类型,它涉及到有机物分子中的羟基或卤素原子与相邻的碳原子上的氢原子结合,生成不饱和键的反应。
例如,乙醇发生消去反应,生成乙烯。
四、酯化反应
酯化反应是有机酸和醇发生反应,生成酯和水的反应。
例如,乙酸和乙醇发生酯化反应,生成乙酸乙酯和水。
五、水解反应
水解反应是有机酸或酯等在水中发生分解的反应。
例如,乙酸乙酯在酸性条件下发生水解反应,生成乙酸和乙醇。
六、氧化还原反应
氧化还原反应是有机化学中涉及电子转移的反应,包括氧化和还原两个过程。
例如,烯烃与臭氧发生氧化还原反应,生成醛或酮。
以上是对高考化学有机反应类型的总结,学生需要掌握每种反应类型的概念、原理和实例,以便能够正确理解和应用这些知识。
同时,学生还需要注意不同反应类型之间的联系和区别,以便能够更好地掌握有机化学的知识体系。
有机化学重要的有机反应及类型

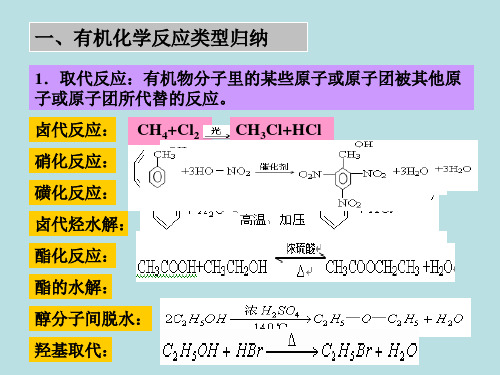
重要的有机反应及类型 1.取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应叫取代反应。
(1)酯化反应:醇、酸(包括有机羧酸和无机含氧酸)(2)水解反应:卤代烃、酯、油脂、糖、蛋白质;水解条件应区分清楚。
如:卤代烃—强碱的水溶液;糖—强酸溶液;酯—无机酸或碱(碱性条件水解反应趋于完全);油脂—无机酸或碱(碱性条件水解反应趋于完全);蛋白质—酸、碱、酶。
C 2H 5Cl+H 2O ∆−−→−NaOH C 2H 5OH+HClCH 3COOC 2H 5+H 2O −−−→−无机酸或碱CH 3COOH+C 2H 5OH (3)硝化反应:苯、苯的同系物、苯酚(4)卤代反应:烷烃、苯,苯的同系物,苯酚、醇、饱和卤代烃等。
特点:每取代一个氢原子,消耗一个卤素分子,同时生成一个卤化氢分子。
2.加成反应:有机物分子里不饱和碳原子与其他原子或原子团直接结合生成新化合物的反应叫加成反应。
如烯烃与卤素、卤化氢或氢气、水的反应;炔烃与卤素、卤化氢或氢气的反应;苯与氢气的反应等。
3.氧化反应(1)与O 2反应①点燃:有机物燃烧的反应都是氧化反应. ②催化氧化:如:醇→醛(属去氢氧化反应);醛→羧酸(属加氧氧化反应)2C 2H 2+5O 2−−−−→−点燃4CO 2+2H 2O 2CH 3CH 2OH+O 2℃网550−−→−Ag 2CH 3CHO+2H 2O 2CH 3CHO+O 2℃~锰盐7565−−→− (2)使酸性高锰酸钾溶液褪色的反应在有机物中如:R —CH=CH 2、R—CCH 、 ROH (醇羟基)、R—CHO 、苯的同系物等都能使酸性高锰酸钾溶液褪色,发生的反应都属氧化反应。
(3)银镜反应和使Cu(OH)2转变成Cu 2O 的反应实质上都是有机物分子中的醛基(-CHO )加氧转变为羧基(—COOH )的反应.因此凡是含有醛基的物质均可发生上述反应(碱性条件).例如:含醛基的物质:醛、甲酸(HCOOH )、甲酸酯(HCOOR )、甲酸盐、葡萄糖、麦芽糖 。
有机化学反应类型总结

有机化学反应类型总结1.亲电取代反应:亲电取代反应是有机化学中最常见的一类反应类型。
在这类反应中,一个亲电试剂攻击另一个有机化合物,取代其中一个官能团形成新的化学键。
经典的亲电取代反应包括醛和酮的取代、烯烃芳基取代和亲核取代反应等。
2.脱羧反应:脱羧反应是有机酸分子中羧基(COOH)被去除的反应。
这类反应可以通过酸催化、碱催化或酶催化来实现。
脱羧反应通常伴随着羧基碳骨架的重排或改变。
3.加成反应:加成反应是指在有机化合物中加入一个新的官能团的反应。
加成反应可以根据加成试剂的类型和形式来进行分类。
常见的加成反应包括醛酮加成、烯烃加成、亚硫酸盐加成等。
4.消除反应:消除反应是指有机化合物中一个或多个官能团被去除的反应。
消除反应的产物是由消失的官能团之间的化学键形成的。
常见的消除反应包括醇酯消除、烯烃消除和卤代烷消除等。
5. 重排反应:重排反应是指有机化合物中化学键的重新排列以形成新的分子结构的反应。
重排反应常常伴随着官能团的迁移和碳骨架的重构。
常见的有机重排反应包括烯烃重排、醇烷重排、Wagner-Meerwein重排等。
6.氧化还原反应:氧化还原反应是指有机化合物中的氧化态和还原态之间的转变。
在氧化还原反应中,氧化剂会接受电子,并使有机化合物的氧化态增加,而还原剂会提供电子,并使有机化合物的还原态增加。
通过以上的总结,我们可以看到有机化学反应涵盖了各种形式的化学变化。
熟练掌握这些反应类型,并了解其机理和应用范围,对于有机化学研究和合成有机化合物都具有重要的意义。
有机化学反应类型分类总结
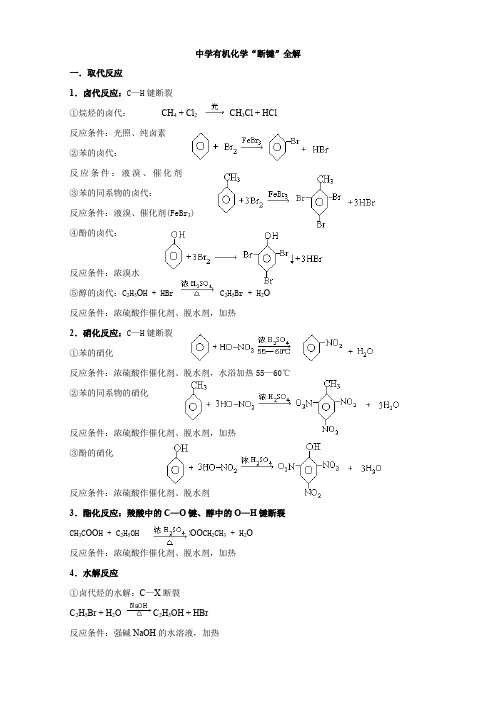
中学有机化学“断键”全解一.取代反应1.卤代反应:C—H键断裂①烷烃的卤代:CH4 + Cl2CH3Cl + HCl反应条件:光照、纯卤素②苯的卤代:反应条件:液溴、催化剂(FeBr3) ③苯的同系物的卤代:反应条件:液溴、催化剂(FeBr3)④酚的卤代:反应条件:浓溴水⑤醇的卤代:C2H5O H + HBr C2H5Br + H2O反应条件:浓硫酸作催化剂、脱水剂,加热2.硝化反应:C—H键断裂①苯的硝化反应条件:浓硫酸作催化剂、脱水剂,水浴加热55—60℃②苯的同系物的硝化反应条件:浓硫酸作催化剂、脱水剂,加热③酚的硝化反应条件:浓硫酸作催化剂、脱水剂3.酯化反应:羧酸中的C—O键、醇中的O—H键断裂CH3C OO H + C2H5OH CH3C OO CH2CH3 + H2O反应条件:浓硫酸作催化剂、脱水剂,加热4.水解反应①卤代烃的水解:C—X断裂C2H5Br + H2O C2H5OH + HBr反应条件:强碱NaOH的水溶液,加热②酯的水解:C—O键断裂反应条件:稀硫酸作催化剂,水浴加热70—80℃③蛋白质的水解:酰氨键中C—N键断裂5.醇与醇分子间脱水:醇分子中的的C—O键与另一醇分子中与羟基相连碳原子上的C—H键发生断裂2 CH3CH2OH CH3CH2OCH2CH3 + H2O反应条件:浓硫酸作催化剂、脱水剂,加热140℃6.置换反应:①醇的置换反应:O—H键断裂2 CH3CH2OH + 2 Na →2CH3CH2ONa + H2↑反应条件:活泼金属(K、Ca、Na、Mg、Al、Li等)②酚的置换反应:O—H键断裂反应条件:活泼金属(K、Ca、Na、Mg、Al、Li等),熔化的苯酚③羧酸的置换反应:O—H键断裂2CH3COOH + Zn →(CH3COO)2Zn + H2↑反应条件:氢以前的活泼金属7.羧酸盐的脱羧反应:C—C键断裂CH3C OO Na + Na O H CH4↑+ Na2CO3反应条件:羧酸盐无水,加热8.复分解反应:C—H键断裂①中和反应:R COOH + NaOH → R COONa + H2O②羧基的检验:R COOH + NaHCO3→ R COONa + H2O + CO2↑二.加成反应1.烯烃的加成反应:断裂中的一个键①与水的加成:CH2=CH2 + H2O CH3CH2OH②与卤素的加成:CH2=CH2 + Br2 →CH2BrCH2Br③与卤代烃的加成:CH2=CH2 + HCl CH3CH2Cl④与氢气的加成:CH2=CH2 + H2CH3CH32.炔烃:断裂中的一个键或二个键①与水的加成:②与卤素的加成:③与卤代烃的加成:④与氢气的加成:3.苯及苯的同系物的加成:断裂苯环上的特殊化学键4.醛的加成:断裂碳氧双键中的一个键三.消去反应:1.醇的消去反应:羟基与碳相连的C—O键及与羟基所在碳原子相邻的碳上的C—H键断裂CH3CH2OH CH2==CH2↑+ H2O反应条件:浓硫酸作催化剂、脱水剂,加热170℃2.卤代烃的消去反应:卤代烃C—X键及与卤素原子所在碳原子相邻的碳上的C—H键断裂CH3CH2Cl + NaOH CH2==CH2↑+ NaCl + H2O反应条件:强碱NaOH的醇溶液,加热四.氧化反应:1.剧烈氧化(有机物的燃烧):断裂分子中所有化学键CH3CH2OH + 3O22CO2 +3 H2O2.控制氧化①醇的催化氧化:醇羟基上的C—H键及与羟基所在碳原子相邻的碳上的C—H键断裂2 CH3CH2OH + O22CH3CHO + H2O②醛的催化氧化:断裂醛基上的C—H键2R—CHO + O2RCOO H③醛的银镜反应:断裂醛基上的C—H键R—CHO + 2Ag(NH3)2OH RCOONH4 + 3NH3 +2Ag↓+H2O反应条件:现配的银氨溶液,水浴加热④醛与新制的Cu(OH)2反应:断裂醛基上的C—H键R—CHO +2Cu(O H)2 RCOOH + Cu2O↓+ 2H2O反应条件:新配的Cu(O H)2悬浊液,加热⑤苯的同系物与酸性KMnO4反应:断裂苯环侧链上的C—H、C—C键⑥烯烃的催化氧化:断裂中的一个键断裂CH2=CH2 +O2CH3CHO⑦丁烷的催化氧化:C—C断裂CH3CH2 CH2CH3 + 5O2 4 CH3COOH + 2 H2O五、聚合反应:1.加聚反应:断裂中的一个键断裂①烯烃的加聚:②卤烯烃的加聚:③不饱和羧酸的加聚:2.缩聚反应:①酚醛缩聚:酚羟基上的C—H与醛基上的C==O键断裂②氨基酸缩聚:羧基中C—O键与氨基中N—H键断裂③脂化缩聚:醇羟基上的O—H与羧基上的C—O键断裂六、分解与裂化、裂解1.分解反应①甲烷的分解:断裂C—H键反应条件:隔绝空气,加热到1000—1500℃②烯烃的臭氧分解:中的二个键全断裂③炔烃的臭氧分解:中的三个键全断裂2.裂化与裂解:C—C键断裂CH3CH2 CH2CH3 C2H4 + C2H6七、颜色反应酚遇Fe3+显蓝色:酚羟基上的O—H键断裂。
有机化学反应类型分类总结

有机化学反应类型一.取代反应1.卤代反应:C—H键断裂①烷烃的卤代:CH4 + Cl2CH3Cl + HCl反应条件:光照、纯卤素②苯的卤代:反应条件:液溴、催化剂(FeBr3) ③苯的同系物的卤代:反应条件:液溴、催化剂(FeBr3)④酚的卤代:反应条件:浓溴水⑤醇的卤代:C2H5O H + HBr C2H5Br + H2O反应条件:浓硫酸作催化剂、脱水剂,加热2.硝化反应:C—H键断裂①苯的硝化反应条件:浓硫酸作催化剂、脱水剂,水浴加热55—60℃②苯的同系物的硝化反应条件:浓硫酸作催化剂、脱水剂,加热③酚的硝化反应条件:浓硫酸作催化剂、脱水剂3.酯化反应:羧酸中的C—O键、醇中的O—H键断裂CH3C OO H + C2H5OH CH3C OO CH2CH3 + H2O反应条件:浓硫酸作催化剂、脱水剂,加热4.水解反应①卤代烃的水解:C—X断裂C2H5Br + H2O C2H5OH + HBr反应条件:强碱NaOH的水溶液,加热②酯的水解:C—O键断裂反应条件:稀硫酸作催化剂,水浴加热70—80℃③蛋白质的水解:酰氨键中C—N键断裂5.醇与醇分子间脱水:醇分子中的的C—O键与另一醇分子中与羟基相连碳原子上的C—H键发生断裂2 CH3CH2OH CH3CH2OCH2CH3 + H2O反应条件:浓硫酸作催化剂、脱水剂,加热140℃6.置换反应:①醇的置换反应:O—H键断裂2 CH3CH2OH + 2 Na →2CH3CH2ONa + H2↑反应条件:活泼金属(K、Ca、Na、Mg、Al、Li等)②酚的置换反应:O—H键断裂反应条件:活泼金属(K、Ca、Na、Mg、Al、Li等),熔化的苯酚③羧酸的置换反应:O—H键断裂2CH3COOH + Zn →(CH3COO)2Zn + H2↑反应条件:氢以前的活泼金属7.羧酸盐的脱羧反应:C—C键断裂(了解)CH3C OO Na + Na O H CH4↑+ Na2CO3反应条件:羧酸盐无水,加热8.复分解反应:C—H键断裂①中和反应:R COOH + NaOH → R COONa + H2O②羧基的检验:R COOH + NaHCO3→ R COONa + H2O + CO2↑二.加成反应1.烯烃的加成反应:断裂中的一个键①与水的加成:CH2=CH2 + H2O CH3CH2OH②与卤素的加成:CH2=CH2 + Br2 →CH2BrCH2Br③与卤代烃的加成:CH2=CH2 + HCl CH3CH2Cl④与氢气的加成:CH2=CH2 + H2CH3CH32.炔烃:断裂中的一个键或二个键①与水的加成:②与卤素的加成:③与卤代烃的加成:④与氢气的加成:3.苯及苯的同系物的加成:断裂苯环上的特殊化学键4.醛的加成:断裂碳氧双键中的一个键三.消去反应:1.醇的消去反应:羟基与碳相连的C—O键及与羟基所在碳原子相邻的碳上的C—H键断裂CH3CH2OH CH2==CH2↑+ H2O反应条件:浓硫酸作催化剂、脱水剂,加热170℃2.卤代烃的消去反应:卤代烃C—X键及与卤素原子所在碳原子相邻的碳上的C—H键断裂CHCH2Cl + NaOH CH2==CH2↑+ NaCl + H2O反应条件:强碱NaOH的醇溶液,加热四.氧化反应:1.剧烈氧化(有机物的燃烧):断裂分子中所有化学键CH3CH2OH + 3O22CO2 +3 H2O2.控制氧化①醇的催化氧化:醇羟基上的C—H键及与羟基所在碳原子相邻的碳上的C—H键断裂2 CH3CH2OH + O22CH3CHO + H2O②醛的催化氧化:断裂醛基上的C—H键2R—CHO + O2RCOO H③醛的银镜反应:断裂醛基上的C—H键R—CHO + 2Ag(NH3)2OH RCOONH4 + 3NH3 +2Ag↓+H2O反应条件:现配的银氨溶液,水浴加热④醛与新制的Cu(OH)2反应:断裂醛基上的C—H键R—CHO +2Cu(O H)2 RCOOH + Cu2O↓+ 2H2O反应条件:新配的Cu(O H)2悬浊液,加热⑤苯的同系物与酸性KMnO4反应:断裂苯环侧链上的C—H、C—C键五、聚合反应:1.加聚反应:断裂中的一个键断裂①烯烃的加聚:②卤烯烃的加聚:③不饱和羧酸的加聚:六、分解与裂化、裂解(了解)1.分解反应①甲烷的分解:断裂C—H键反应条件:隔绝空气,加热到1000—1500℃2.裂化与裂解:C—C键断裂CH3CH2 CH2CH3 C2H4 + C2H6七、颜色反应酚遇Fe3+显蓝色:酚羟基上的O—H键断裂。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一. 教学内容:
专题一重要有机化学反应类型
1. 取代反应
①定义:有机分子里的某些原子或原子团被其它原子或原子团所代替的反应叫取代反应。
②能发生取代反应的物质:、苯、、苯酚、甲苯
③典型反应
2. 加成反应
①定义:有机分子里不饱和的碳原子跟其它原子或原子团直接结合生成别的物质。
加成反应是不饱和键(主要为,)重要性质。
②能发生加成反应的物质有:烯烃、炔烃、苯环、醛、酮、油脂等。
③典型反应
(水溶液)(溴水褪色)
(制取塑料用)
(1,2加成)
(1,4加成)
(工业制乙醇)
3. 加聚反应
①本质:通过自身加成反应形成高分子化合物。
特征:生成物只有高分子化合物,且其组成与单体相同,如聚乙烯与乙烯的比相同。
②能发生加聚反应的物质有:乙烯、丙烯、1,3—丁二烯、异戊二烯、氯乙烯等。
③典型反应
塑料
天然橡胶
4. 缩聚反应
①定义:单体间通过缩合反应而生成高分子化合物,同时还生成小分子(如水、氨等)
的反应。
②特征:有小分子生成,所以高分子化合物的组成与单体不同。
③能发生缩聚反应的物质:苯酚与甲醛;葡萄糖,氨基酸,乙二醇与乙二酸等。
④典型反应
(的确良)
5. 消去反应
①定义:从一个有机分子中脱去一个小分子(如水、卤化氢等分子),而生成不饱和
(双键或叁键)化合物的反应。
②能发生消去反应的物质:某些醇和卤代烃。
③典型反应
6. 脱水反应
①本质与类型:脱水反应是含羟基的化合物非常可能具有的性质,通常是两个羟基之间可脱去一分子水,也可以是一个羟基与另一个非羟基氢结合脱去一分子水。
脱水可以在一个分子内进行,也可在分子之间进行。
②能脱水的物质有:醇、羧酸、蔗糖、氨基酸、无机含氧酸等。
③典型反应
(乙酸酐)
()()
()
(三磷酸)
7. 酯化反应
①定义:醇跟酸起作用、生成酯和水的反应。
其本质是脱水(酸脱—,醇脱—)。
②能发生酯化反应的物质:羧酸和醇、无机含氧酸和醇、糖与酸等。
③典型反应
(硝酸乙酯)
(葡萄糖乙酸酯)
8. 水解反应
①反应特征:有水参加反应,有机物分解成较小的分子,常为可逆反应。
②能够水解的有机化合物:卤代烃、酯、油脂、二糖、多糖(淀粉、纤维素)、蛋白质等。
③典型反应
(皂化反应)(蔗糖)(葡萄糖)(果糖)
9. 氧化反应
(1)含义:有机物去氢或加氧的反应。
(2)三种类型:
①在空气中或氧气中燃烧。
绝大多数有机物(除等外)都能燃烧,燃烧产物取决于的量是否充足。
若足量,产物为和,若氧气不足,产物是和。
燃烧时火焰的明亮程度、黑烟的多少与分子中含碳量有关,含碳量越高、火焰越明亮、黑烟越多。
例如乙醇、乙烷、乙炔的燃烧。
最容易完全燃烧,火焰也不明亮(淡蓝色)且无烟的是,最不容易完全燃烧,火焰很明亮且有黑烟的是。
②在催化剂存在时被氧气氧化,即有机物的局部被控制氧化,在有机合成工业上有重要意义。
例如:
(工业制乙醛)
(工业制乙酸)
③有机物被某些非的氧化剂氧化。
<1> 能被酸性(紫色)氧化,使其褪色的物质有:烯烃、炔烃、二烯烃、油脂(含)、、、、、葡萄糖等。
<2> 能被银氨溶液或新制备的悬浊液氧化的有机物为含醛的物质:
(一)指出的箭头,表明该物质的化学性质。
例如,乙醇出来6个箭头,即乙醇有6条化学性质。
(二)指入的箭头,表明生成该物质的方法。
例如:有5个箭头指向乙醇,即合成乙醇的途径可有5种。
1.
2.
3.
4.
5.
6.
7.
8.
9.
10 .
11.
12.
13.
14.
15.
16.
17.
18.
19.
20.
21.
22.
23.
24.
25.
26.
27. (紫色溶液)
28.
29.
30.
31. +
32.
33.
34.
35.
36.
37.
38.
39.
40.。
