分析化学hf络合滴定法
络合滴定法学习要点

络合滴定法学习要点1、络合滴定ABC2、络合滴定的条件是什么?3、络合滴定曲线是怎样绘制的?4、络合滴定曲线有什么意义和用途?5、络合滴定突跃如何计算?6、络合滴定误差如何计算?1、络合滴定ABC络合滴定法又叫配位滴定法,是以生成金属络合物为滴定反应基础的容量分析,通常教材中介绍的络合滴定是指以EDTA滴定M(或M滴定EDTA)的反应体系。
络合滴定受到pH值(EDTA酸效应和M的水解效应)、共存的其他络合剂L(M的络合效应)、共存的其他金属离子N(争夺EDTA,对EDTA 的共存离子效应)的四重影响。
分析化学中将各种影响用副反应系数α来表示,计算出各自的α值,再与绝对稳定常数K合并,构成条件稳定常数K’MY,或lgK’MY。
引入条件稳定常数后,原来简单溶液的EDTA-M络合平衡的平衡定律表达式就可替换成用M总浓度M’和EDTA总浓度Y’及MY总浓度MY’(一般情况下忽略MY的副反应)表示的化学平衡定律。
各项副反应系数的定义式和计算式如下:(1)酸效应系数(影响EDTA,使EDTA质子化,降低[Y]浓度):6Y(H)1[Y']1[H ][Y]H ii i αβ+===+∑其中:6EDTA [Y']=[Y]+[HY]+......[H Y]=c(M ’中不含MY 项,络合滴定中必须考虑,可以查表)(2)络合效应系数(影响M ,L 与M 络合,降低[M]浓度):M(L)1[M']1[L][M]n ii i αβ===+∑ 其中:n [M']=[M]+[ML]+......[M L](Y ’中不含MY 项,络合滴定中比较常见的影响,重点)(3)水解效应系数(影响M ,生成羟基络离子,降低[M]浓度):M(OH)1[M']1[OH][M]n ii i αβ===+∑ 其中:n [M']=[M]+[MOH]+......[M OH](不含MY 项,该效应相当于OH 对M 的络合效应,滴定条件下一般可以忽略)(4)共存离子效应系数(对EDTA ):''Y(H)NY NY [Y']1[N]1[N ][Y]K K α==+=+ 其中:[Y']=[Y]+[NY](Y ’中不含MY 项,络合滴定中考虑共存金属离子干扰及消除时要用到,通过加入一种掩蔽剂进去,使干扰的N 生成稳定络离子,就不再干扰M 的滴定了。
分析化学 络合平衡和络合滴定法(2)

最低酸度
金属离子的水解酸度-避免生成氢氧化物沉淀 对 M(OH)n
[OH-]=
n
Ksp [M]
例 0.02mol/LZn2+ Zn(OH)2 Ksp=10-15.3
可求得:pH≤7.2
? 可在pH10的氨性缓冲液中用Zn2+标定EDTA 最佳酸度 金属指示剂也有酸效应,与pH有关 pMep=pMsp 时的pH ?
络合掩蔽注意事项:
1. 不干扰待测离子: 如pH10测定Ca2+、Mg2+, 用F-掩蔽Al3+, 则 CaF2 ↓、MgF2 ↓
2. 掩蔽剂与干扰离子络合稳定:
3. 合适pH F-, pH>4; CN-, pH>10)
b 沉淀掩蔽法
加沉淀剂,降低[N]
例:Ca2+ Mg2+混合溶液中Ca2+的测定 lgKCaY=10.7, lgKMgY=8.7
b 单一金属离子滴定的适宜pH范围
最高酸度
csp=0.01mol· L-1, lgKMY≥8 lgKMY= lgKMY-lg Y(H)≥8, (不考虑 M) 有 lgαY(H) ≤lgK(MY) - 8 对应的pH即为pH低,
例如: KBiY=27.9 lgY(H)≤19.9 pH≥0.7 KZnY=16.5 lgY(H)≤8.5 pH≥4.0 KMgY=8.7 lgY(H)≤0.7 pH≥9.7
6.4 络合滴定基本原理
络合滴定曲线:溶液pM随滴定分数(a)变化的曲线 在络合滴定中,随着EDTA滴定剂的不断加入,被滴定 金属离子的浓度不断减少, 以被测金属 离子浓度的负对数pM(pM=-lg[M])对 加入滴定剂体积作图,可得络合滴定曲 线即pM~V曲线。 见书P186
分析化学hf络合滴定法分析

M+Y
MY
主反应
H+
HY
H+
H+
H2Y
H+ H6Y
酸效应引起的副反应
EDTA的酸效应系数
Y(H)
Y' Y
H 6Y 2
H5Y Y 4
Y 4
Y(H)
1
Y
,Y
H 6
Ka1Ka2 Ka6 H 5 Ka1 Ka1Ka2Ka3Ka4Ka5Ka6
EDTA与金属离子形成的配合物的特点:
1. 配位能力强,络合广泛。
2. 配比比较简单,多为1:1
3. 配合物大多带电荷,水溶性较好。
4. 配合物的颜色主要决定于金属离子的颜色。 即无色的金属离子与EDTA络合,则形成无色的 螯合物,有色的金属离子与EDTA络合物时,一 股则形成颜色更深的螯合物。
三、配合物的稳定常数(形成常数)
常以 H4Y 表示. (1)结构式:
EDTA(乙二胺四乙酸)结构 H
-
OOCH2C H+ N CH2 CH2
HOOCH2C
H
-
H+ CH2COO N
CH2COOH
两个氨氮 四个羧氧
双极离子
四元酸 H4Y
+ 2 H+
H6Y2+ 六元酸
(2)EDTA的溶解性: 溶解度 0.02g/100mL (22°C) 710-4mol/L
Ag++Ag[(CN)2]-= Ag[Ag(CN)2]↓
一、配位滴定的反应必须具备下列条件:
(一)形成的配合物要相当稳定,K形≥108, 否则不易得到明显的滴定终点。
(二)在一定反应条件下,配合数必须固定 (即只形成一种配位数的配合物)。
络合平衡和络合滴定法剖析
● ● ●
H6Y
Y
酸效应系数 Y(H):
[Y]
Y(H)= [Y] =
[Y]+[HY]+[H2Y]+…+[H6Y] [Y]
=
1
Y
=
[Y]+[Y][H+]1+[Y][H+]22+…+[Y][H+]66
[Y]
=(1+1[H+]+2[H+]2+…+6[H+]6)
[Y] =
[Y]
Y(H)
Y(H) ≥1
EDTA的酸效应系数曲线
Ka1=
[H+][H5Y]
[H6Y]
Ka2=
[H+][H4Y] [H5Y]
= 10 = 10
Ka3=
[H+][H3Y] [H4Y]
= 10
Ka4=
[H+][H2Y] [H3Y]
Ka5= Ka6=
[H+][HY] [H2Y]
[H+][Y] [HY]
= 10 = 10 = 10
M-EDTA螯合物的立体构型
lgY(H)
lg Y(H)~pH图
共存离子效应系数 Y(N)
[Y]
[Y]+[NY]
Y(N)= [Y] =
[Y]
= 1+ KNY[N]
多种共存离子
[Y]
Y(N)= [Y]
=
[Y]+[N1Y]+[N2Y]+…+[NnY] [Y]
= 1+KN1Y[N1]+KN2Y[N2]+…+KNnY[Nn]
高等教育版《分析化学》第五章 络合滴定法

1.络合剂常含有两个或两个以上的配位原子,称之为多齿
(基)配体,与金属离子形成具有环状结构的螯合物;
2. 螯合物稳定很强,络合反应的完全程度很高; 3.控制一定的条件,其络合比是可以固定的。 因此,可以满足滴定分析对化学反应的要求,可作滴定剂、 掩蔽剂等。
在络合滴定法中,广泛使用的一类螯合剂为氨羧络合剂,
金属离子一般生成颜色更深的螯合物;
第五章
络合滴定法
分析化学
Analytical Chemistry
EDTA与常见金属离子配合物的稳定常数:
第五章
络合滴定法
分析化学
Analytical Chemistry
有色 EDTA 螯合物 螯合物 CoY CrYCr(OH)Y
2
颜色 紫红 深紫
螯合物 Fe(OH)Y FeY
无机络合物特点:
1.络合剂大多数只含有一个原子(单齿配体),与金属离 子分级络合,各配体之间无联系; 2.络合物稳定性差; 3.各级形成常数彼此相差不大,产物无固定组成。 因此绝大多数无机络合剂不可以用作滴定剂。 (可作掩蔽剂、辅助络合剂和指示剂等)
第五章 络合滴定法 有机络合物的特点:
分析化学
Analytical Chemistry
例:某溶液含有EDTA、Pb2+和(1) Ca2+,(2) Mg2+, 浓度均为0.01mol·L-1。在pH=5.0时,对于EDTA与 Pb2+的主反应,计算两种情况下的α Y和lgα Y值。
K P bY 1 0
18.04
, K C aY 1 0
10.7
, K M gY 1 0
8.7
第五章
22-
颜色 褐(pH=6) 黄 紫红 蓝绿
络合滴定法

]
4.9 1010
金属离子-EDTA络合物的稳定常数
(20oC ,I =0.1mol/L)
lgK
lgK
lgK
lgK
Na+ 1.66 Mg2+ 8.79 Fe2+ 14.32 Hg2+ 21.7
Ca2+ 10.69
La3+ 15.50 Th4+ 23.2 Al3+ 16.3 Fe3+ 25.1
Zn2+ 16.50 Bi3+ 27.8
按分布分数δ定义,得到:
M
[M ] CM
[M
[M ]
n
](1 i
[L
]i
)
1
1
n
i
[L
]i
i 1
i 1
ML
[ML ] C M [M
1[M ][L ]
n
](1 i [L
]i
)
1
1[L ]
n
i [L
]i
i 1
i 1
●●●
ML n
[ML n CM
]
[M
n [M ][L
n
](1 i
]n [L
]i
)
β3H = 1/ Ka6 Ka5 Ka4
…
β6H = 1/Ka6Ka5Ka4Ka3Ka2Ka1
EDTA离解常数和质子化常数
离解 常数
Ka1 10-0.9
Ka2 10-1.6
Ka3
Ka4
Ka5
10-2.0 10-2.67 10-6.16
Ka6 10-10.26
逐级质 子化常
数
K1 1010.26
络合滴定法

-
NH+-CH2-CH2-NH+
CHCHOOCH2COOH
OOCH2C
在酸性溶液中,2个羧基再结合2个H+,形成六元酸形式,H6Y2+:
HOOCH2C HOOCH2C
NH -CH2-CH2-NH
+
+
CHCHOOH CH2COOH
分析化学课件
概
述
基本原理
滴定条件选择
应用与示例
习
题
EDTA为白色粉末,在水中溶解度很小;室温下EDTA溶于
分析化学课件
概
述
基本原理
滴定条件选择
应用与示例
习
题
例: 计算pH=2和5时的lgKZnY 值。
解:查表得:
lgKZnY =16.50
pH=2时,lgY(H)=13.79 pH=5时,lgY(H)=6.45
查附表得: pH=2时和pH=5时 , lgZn(OH)=0 所以 pH=2时,lgKZnY =lgKZnY -lg Y(H)
应用与示例
习
题
例: 计算pH=11,[NH3]=0.1mol/L时的Zn 解:已知Zn(NH3)42的lg1~lg4 :2.27、4.61、7.01、9.06 则 Zn(NH3)=1+102.2710-1+104.6110-2+107.0110-3+109.0610-4 • =105.10 而pH=11时,lgZn(OH)=5.4 所以 Zn=Zn(NH3)+Zn(OH)-1 =105.1 +105.4-1105.6
[Y] [Y] [HY] [H2 Y] [H6 Y] [NY] Y [Y] [Y] [Y] [HY] [H2 Y] [H6 Y] [NY] [Y]- [Y] [Y]
【分析化学】络合滴定法

O C O C CH2 O
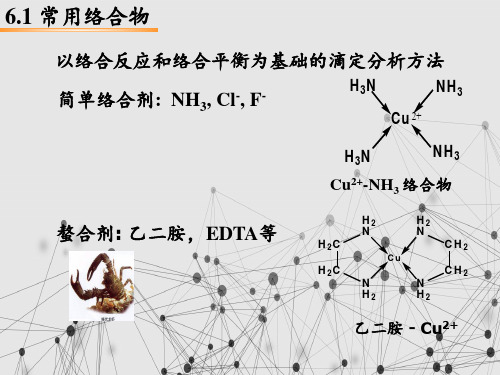
分析化学中的络合物
简单配体络合物 螯合物
O
多核络合物
Cu(NH3 ) 2 4
H2C H2C N O C O
C
O CH2 CH2 Ca O N CH2
[(H2O)4Fe
OH OH
Fe(H2O)4]4+
O C O C CH2 O
简单配体络合物:中心离子和单齿配体(只含有一个配位原子的配体)所 形成,也称为简单络合物。简单络合物不稳定。与多元酸相类似,简单络 合物是逐级形成的。如:Cu2+与单基配位体NH3的反应: Cu2+ + NH3 === Cu(NH3)2+ K1=104.18 Cu(NH3)2+ + NH3 === Cu(NH3)22+ K2=103.48 Cu(NH3)22+ + NH3 === Cu(NH3)32+ K3=102.87 Cu(NH3)32+ + NH3 === Cu(NH3)42+ K4=102.11 正是因为这一性质限制了简单络合物在滴定分析中的应用,仅作为掩蔽剂 、显色剂和指示剂,而作为滴定剂的只有以CN-为络合剂的氰量法和以Hg2 +为中心离子的汞量法具有一些实际意义。 如:①以AgNO3标准溶液测定氰化物,反应如下: 2CN-+Ag+===[Ag(CN)2]- 此反应的累积稳定常数,相当稳定。当滴定到计量点时,稍过量的Ag+ 与Ag(CN)2-结合生成白色AgCN沉淀,使溶液变浑浊而指示终点。 Ag++Ag(CN)2-===2AgCN↓(白色) ②以Hg2+溶液作滴定剂,二苯胺基脲作指示剂,滴定Cl-,反应如下: Hg2++2Cl-===HgCl2 生成的HgCl2是解离度很小的络合物,称为拟盐或假盐。过量的汞盐与指示 剂形成兰紫色的螯合物以指示终点的到达。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
二.配位剂的分类 1. 无机配位剂 用于配位滴定分析的限制: (1)许多无机配合物不够稳定 (2)在配位过程中存在逐级配位现象 氰量法(CN-): 测 Ag+, Ni2+ 汞量法(Hg2+): 测 Cl-, SCN2. 有机配位剂 特点(1)配合比固定;(2)稳定
氨羧络合剂,是一类含有氨基二乙酸
✓ 注:[Y’] ——EDTA 与 N 配合物平衡浓度 和参与配位的Y4-平衡浓度之和
[Y] ——参与配位反应的Y4-的平衡浓度
➢ 结论: Y (N ) ,[Y ] 副反应越严重
3. Y的总副反应系数[同时考虑酸效应和共存离子效应]
Y
[Y '] [Y ]
[H 6Y 2 ] [H5Y ] [Y 4 ] [NY ] [Y 4 ]
EDTA与金属离子形成的配合物的特点:
1. 配位能力强,络合广泛。
2. 配比比较简单,多为1:1
3. 配合物大多带电荷,水溶性较好。
4. 配合物的颜色主要决定于金属离子的颜色。 即无色的金属离子与EDTA络合,则形成无色的 螯合物,有色的金属离子与EDTA络合物时,一 股则形成颜色更深的螯合物。
三、配合物的稳定常数(形成常数)
M+Y
MY
稳定常数
➢ 讨论:
K MY
MY M Y
K
稳=
K
1
不稳
KMY↑大,配合物稳定性↑高,配合反应↑完全
续前2、MLn型配合物的累积稳定常数
ML
M+L
ML
一级稳定常数 K1 M L
ML + L
ML2
二级稳定常数
K2
ML2
ML L
MLn-1 + L
M Ln
n级稳定常数 Kn
▪ L多指NH3-NH4CL缓冲溶液,辐助配位剂,掩蔽剂,OH-
L OH M (L) M (OH)
➢ 结论: [L] , M(L),副反应程度 高
2、水解效应及副反应系数M(OH)
同理有
M(OH)的定义:
[M] [M]+[M(OH)]+[M(OH)2] + … +[M(OH)n]
M(OH) =
基团的有机化合物。其分子中含有氨氮和羧 氧两种络合能力很强的络合原子,可以和许 多金属离子形成环状结构的络合物。
在配位滴定中常遇到的氨羧络合剂有以下几种:
(一)氨三乙酸
(二)乙二胺四乙酸
(三)环己烷二胺四乙酸 (四)乙二胺四丙酸
(五)乙二醇二乙醚二胺四乙酸
(六)三乙四胺六乙酸
应用有机络合剂(多基配位体)的配位滴定方法,
M+Y
MY
主反应
H+
HY
H+
H+
H2Y
H+ H6Y
酸效应引起的副反应
EDTA的酸效应系数
Y(H)
Y' Y
H 6Y 2
H 5Y Y 4
Y 4
Y(H)
1
Y
,Y
H
6
Ka1Ka2 Ka6
H
5
K a1
Ka1Ka2 Ka3Ka4 Ka5Ka6
Y(H )
H 6
H
5
Ag++Ag[(CN)2]-= Ag[Ag(CN)2]↓
一、配位滴定的反应必须具备下列条件:
(一)形成的配合物要相当稳定,K形≥108, 否则不易得到明显的滴定终点。
(二)在一定反应条件下,配合数必须固定 (即只形成一种配位数的配合物)。
(三)反应速度要快。 (四)要有适当的方法确定滴定的计量点。
已成为广泛应用的滴定分析方法之一。目前应用最
为 广 泛 的 有 机 络 合 剂 是 乙 二 胺 四 乙 酸 (Ethytlene
Diamine Tetraacetic Acid 简称 EDTA)。
§5-2
EDTA与金属离子的配合物 及其稳定性
一、EDTA的一般性质
乙二胺四乙酸 简称:EDTA或EDTA酸
Na2H2Y·2H2O 也简称EDTA 溶解度 11.1g/100mL (22°C)
0.3mol/L
(3). EDTA各种型体的分布
各型体浓度取决于溶液pH值 pH < 1 强酸性溶液 → H6Y2+ pH 2.67~6.16 → 主要H2Y2-
pH > 10.26碱性溶液 → Y4-
EDTA只在pH≥12时几乎完全以Y4–形式存在
pH Y(H) ;pH 12 Y (H ) 1,配合物稳定
2. 共存离子效应:由于其他金属离子存在使 EDTA主反应配位能力降低的现象。
其大小用Y(N)来衡量。
M+Y
MY
主反应
N NY
干扰离子效应引起的副反应
共存离子(干扰离子)效应系数
Y (N)
Y ' Y
Y
NY Y
1
K NY
N
aMY
KMY =
=
aM aY
未参加反应的
[ MY] [M][Y]
[M´] = [M]+[ML]+[ML2] + … +[M(OH)]+[M(OH)2]… [Y´] = [Y]+[HY]+[H2Y] + … +[H6Y]+[NY]
形成配合物的总量 [MY´] = [MY]+[MHY]+[M(OH)Y]
K a1
Ka1Ka2 Ka3Ka4 Ka5Ka6
Ka1Ka2 Ka3Ka4 Ka5Ka6
1 H
H 6
Ka6
K a6 Ka5 Ka4 Ka3Ka2 Ka1
✓ 注:[Y’]——EDTA所有未与M 配位的七种型体总浓度 [Y] ——EDTA能与 M 配位的Y4-型体平衡浓度
➢ 结论:pH ,[H ] Y (H ) ,[Y 4 ] 副反应越严重
ML
MLn MLn1 L
一级累积稳定常数 1 K1 M L
二级累积稳定常数
2
K1 K2
ML2
M L2
总累积稳定常数
n
K1 K2 Kn
MLn
M Ln
注:各级累计常数将各级 [MLi]和 [M ]及 [L]联系起来
§5-3 外界条件对EDTA与金属离子配 合物稳定性的影响
常以 H4Y 表示. (1)结构式:
EDTA(乙二胺四乙酸)结构 H
-
OOCH2C H+ N CH2 CH2
HOOCH2C
H
-
H+ CH2COO NCH来自COOH两个氨氮 四个羧氧
双极离子
四元酸 H4Y
+ 2 H+
H6Y2+ 六元酸
(2)EDTA的溶解性: 溶解度 0.02g/100mL (22°C) 710-4mol/L
=
[M]
[M]
= 1+1[OH]+ 2[OH]2+…+ n[OH]n
lgM(OH)可在附录中查得 M = M(L) + M(OH) -1 M(L) + M(OH)
3. 金属离子的总副反应系数
溶液中同时存在两种配位剂:L,A
M的配位副反应1 M + L
ML
M的配位副反应2 M + A
MA
M
M M
6H = K1H K2H K3H K4H K5H K6H = ka6 ka5 ka4 ka3 ka2 ka1
[Y]+1H[H+][Y]+ 2H[H+]2[Y]+…+ 6H[H+]6[Y] Y(H)=
[Y]
= 1+1H[H+]+ 2H[H+]2+…+ 6H[H+]6
1 K MHY
H
MY' MY M (OH)Y
MY(OH) MY
MY
1 K M (OH)Y
OH
二、条件稳定常数(表观稳定常数,有效稳定常数)
配位反应
M+Y
MY
副反应系数 M Y
MY
稳定常数
[MY ] KMY [M ][Y ]
条件稳定常数
K
' MY
[MY '] [M '][Y ']
第五章 配位滴定法
§5-1 概 述
利用形成配合物的反应进行滴定分析的方 法,称为配位滴定法。
例如,用AgNO3标准溶液滴定氰化物时,反应 如下:
Ag+十2CN-=Ag[(CN)2]-
K形=1021
当 滴 定 达 到 计 量 点 时 , 稍 过 量 的 Ag+ 就 与
Ag[(CN)2]- 反 应 生 成 白 色 的 Ag[Ag(CN)2] 沉 淀 , 使 溶 液变浑浊,而指示终点。
[H
6Y
2
]
[H5Y ] [Y 4 ]
[Y
4
]
[
NY ] [Y [Y 4 ]
4
]
[Y [Y
4 4
] ]
Y Y(H) Y(N) 1
例1 :在pH=1.5的溶液中,含 有浓度均为0.010mol/L的EDTA、 Fe3+及Ca2+,计算Y(Ca)、 Y
例2:某溶液中含有Pb2+和Ca2+ , 浓度均为0.010mol/L,在pH=5.0 时用EDTA标液滴定Pb2+ ,计算
[MY´]
= K´MY [M´] [Y´]
二.各种副反应系数的计算
Y(H) 1. Y的副反应及副反应系数的计算Y{
Y(N) (1)酸效应及酸效应系数Y(H)
