苯、甲苯、乙苯的定性分析及其混合物的定量分析
苯、甲苯、乙苯混合物的分离和定量分析

1.实验目的1.1掌握气相色谱分离多组分混合物的方法。
1.2练习用归一化法测量混合物中各组分的含量。
2.实验原理 2.1气相色谱仪结构2.2混合物分离:色谱峰的确定在确定的固定相和色谱条件下,每种物质都有一定的保留时间t R ,因此在相同的条件下,分别测定纯物质和混合物各物质的保留值,将二者进行比较,即可确定样品中各组分的种类。
2.3定量分析:色谱定量归一化法 %100%/⨯=∑iii ii i f A f A Wi A :峰面积 i f :校正因子(苯:0.780,甲苯:0.794,乙苯:0.818)气相色谱图 3.实验仪器与试剂气相色谱仪 热导池检测器 色谱柱微量注射器 固定相:15%邻苯二甲酸二壬酯 102白色载体60~80目 载气N 2 丙酮苯(AR )甲苯(AR )乙苯(AR )苯、甲苯、乙苯混合样品(体积比为1:1:1) 4.实验过程4.1开通载气N 2瓶阀门,打开气相色谱仪开关,2min 左右后启动电脑和软件。
4.2设置参数: 进样口温度:180℃ 色谱柱温度:100℃ 检测器温度:200℃ 4.3纯试剂色谱仪器稳定后,用10L μ微量注射器分别注射2L μ苯、甲苯、乙苯的纯试剂,分别得到苯、甲苯、乙苯的纯试剂的气相色谱图。
4.4混合物分析在相同条件下,用微量注射器注射2L μ混合物样品,得到混合物的气相色谱图。
(每次注射前均用丙酮洗涤,滤纸擦干,并用所注射试剂进行润洗)。
4.5结束实验后要把设定的各项温度降到50℃以下,关闭软件和电脑,关掉气相色谱仪和载气阀。
5.实验数据处理 5.1纯试剂的色谱5.2混合物分析(混合物气相色谱图见附页) 6.实验总结与思考6.1气相色谱法:是利用气体作为流动相的一种色谱分析方法,根据不同组分在色谱柱两相中的分配能力不同而达到分离的目的。
6.2与液相色谱相比气相色谱法的特点:6.2.1优点:气相色谱中的物质在气体中传递速度快,气态样品中各组分与固定相作用次数多,而且可供选择的固定液相种类多,因而选择性好、分离效能高、分析速度快;具有多种检测器可供选择,灵敏度较好。
气相色谱分析混合样品中的苯和甲苯

气相色谱分析混合样品中的苯和甲苯气相色谱(Gas chromatography,GC)是一种常用的分析方法,可以用于分离和检测混合物中的化合物。
在气相色谱分析中,样品通过气相进样器进入气相色谱柱,然后由携带气体推动,在柱内固定相的作用下,进行分离。
本文将介绍气相色谱分析混合样品中的苯和甲苯的方法。
1.实验材料和设备-气相色谱仪:包括气源、进样系统、柱温控制系统和检测器等组成。
-色谱柱:根据待分析物的性质选择合适的柱类型,如非极性柱(例如,HP-5、DB-5)。
-气瓶:用于提供分离所需的携带气体,常用的是氮气。
-样品溶剂:例如甲醇、乙醇等。
-样品:包含苯和甲苯的混合物。
2.实验步骤2.1准备实验仪器-将色谱柱安装到气相色谱仪上,并确保柱端口密封良好。
-将气瓶连接到气相色谱仪的携带气体入口。
-打开仪器电源,开启仪器。
2.2系统预热-调节气相色谱仪的柱温,通常设置在柱的上限温度附近,以确保样品可以有效地沿着柱进行分离。
-让气相色谱仪预热至稳定的温度,通常需要较长的时间(20分钟以上)。
2.3准备样品-将苯和甲苯溶解在合适的溶剂中,通常选择不溶于气相色谱柱固定相的溶剂。
-将样品溶液密封保存,以免溶剂挥发。
2.4样品进样-打开气相色谱仪的进样系统,设置进样量和进样速度。
-将待分析样品的适量溶液通过气相进样器进入气相色谱柱。
2.5分离和检测-通过气源提供的携带气体,将样品沿柱进行分离。
-在柱的一端设置检测器,检测被分离物质的信号。
-根据样品特征峰的保留时间和峰面积,进行定性和定量分析。
3.结果解析-根据样品色谱图中苯和甲苯的保留时间和峰面积,可以确定它们是否存在于样品中。
-通过比较待测样品中目标化合物的峰面积与已知浓度标准曲线的峰面积,可以定量分析它们的浓度。
4.结论和注意事项-气相色谱分离和检测的结果应该根据已知标准进行定性和定量分析,以确保准确性和可靠性。
-在实验中,应注意柱温、进样量和检测器参数的设置,以获得较好的分离和检测效果。
高效液相色谱测定混合样品中苯和甲苯
实验项目:高效液相色谱测定混合样品中苯和甲苯试验【实验题目】高效液相色谱测定混合样品中苯和甲苯【实验目的】1、掌握高效液相色谱定性和定量分析的原理及方法2、了解高效液相色谱的构造、原理及操作技术【实验原理】高效液相色谱由储液器,泵、进样器、色谱柱、检测器、记录仪等几部分组成,储液器中的流动相被高压泵打入系统,样品溶液经进样器进入流动相,被流动相载入色谱柱内,由于样品溶液中的各组分在两相中具有不同的分配系数,在两相中作相对运动是,经过反复多次的吸附-解吸的分配过程,各组分在移动速度上产生较大的差别,被分离成单个组分依次从柱内流出,通过检测器时,样品浓度被转换成电信号传送到记录仪。
【仪器和试剂】主要仪器:高效液相色谱HPLC-20A T ,10μL 微量注射器1支试剂:苯标准溶液,甲苯标准溶液,苯、甲苯标准溶液0.2μL/mL ,2μL/mL ,4μL /mL ,10μL/mL ,色谱醇,甲醇【实验内容与步骤】1.调好最佳色谱条件,控制流速为1ml/min 。
柱温30℃,检测波长254nm 。
2.优化条件用微量注射器注射60%甲醇和水的混合溶液,记录保留时间;如保留时间过长,增大甲醇与水的混合比例到80%,记录保留时间;如保留时间过长,继续增大甲醇与水的混合比例到85%,记录保留时间,直至保留时间小于5min 。
3.苯、甲苯定性分析在最佳条件下,用微量注射器分别进样4μL 试样,4μL 苯标液和4μL 甲苯的标液(注射器用甲醇润洗3~5遍)观察其记录保留时间,确定苯和甲苯的峰。
4.苯、甲苯定量分析在最佳条件下,用微量注射器分别进样0.2μL/mL 、2μL/mL 、4μL/mL 、10μL/mL 的标液各4μL 。
观察记录保留时间和峰面积。
根据峰面积在工作曲线上查出苯和甲苯待侧液的浓度,并计算试样中苯和甲苯的含量。
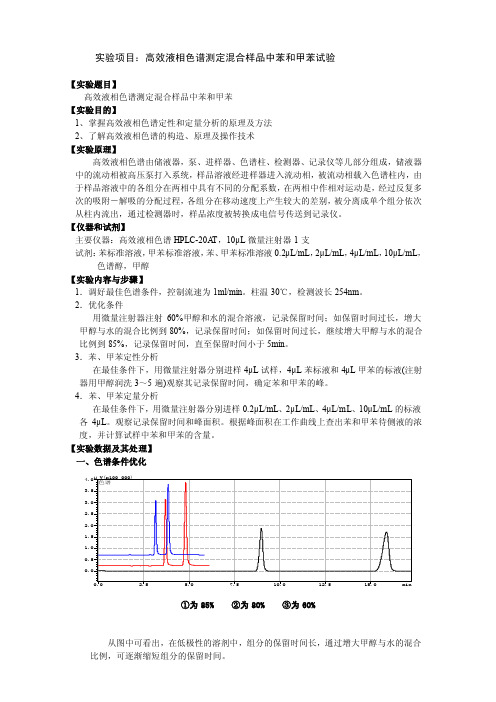
【实验数据及其处理】 一、色谱条件优化0.02.55.07.510.012.515.0min0.00.51.01.52.02.53.03.54.0μV(x100,000)色谱①为85% ②为80% ③为60%从图中可看出,在低极性的溶剂中,组分的保留时间长,通过增大甲醇与水的混合比例,可逐渐缩短组分的保留时间。
实验二 利用高效液相色谱测定混合样品中苯和甲苯

三、操作步骤
1、最佳分离条件的选择 启动仪器,先注入5微升的甲醇流动相,
观察检测器当峰斜率小于1000是,设定流动 相甲醇含量为60%,注入5微升的苯与甲苯混 合液,观察检测器显示的两峰的保留时间及 分离效果。双峰显示完毕后,改变流动相甲 醇含量为80%,观察检测器显示的两峰保留 时间及分离效果。
1.色谱条件优化
2.00μ色V(x谱100,000)
1.75 1.50 1.25 1.00 0.75 0.50 0.25 0.00
0.0
2.5
5.0
7.5
10.0
12.5
15.0
17.5
min
由上图可知,当甲醇的含量为85%时,能将两者分 开,且时间较短,因此可选甲醇含量为85%作为实验 条件。
2.苯、甲苯定性分析
Y = aX + b a = 264149.7 b = 98330.34 R^2 = 0.9978541 R = 0.9989265
甲苯
浓度
在最佳分离条件下,用10μL微量注射器, 分别注射5.0μL苯、甲苯的标准溶液,观 察记录保留时间,确定苯和甲苯的峰
10.0μ色V(x谱10,000)
9.0
8.0
7.0
甲苯
6.0
苯
5.0
4.0
3.0
2.0
1.0
0.0
-1.0
0.0
0.5
1.0
1.5
2.0
2.5
3.0
3.5
min
样品 保留时间
苯 3.177
苯、甲苯混合标准溶液浓度分别为:1 ul/ml, 2 ul/ml,5 ul/ml, 10 ul/ml。
气相色谱法分析混合样品中苯和甲苯实验报告(华南师范大学)

⽓相⾊谱法分析混合样品中苯和甲苯实验报告(华南师范⼤学)实验报告学⽣姓名学号专业化学(师范)年级班级课程名称仪器分析实验实验项⽬⽓相⾊谱分析混合样品中苯和甲苯实验类型□验证□设计□综合实验时间2020 年10 ⽉7 ⽇指导⽼师朱⽴才实验评分⼀、实验⽬的1.了解⽓相⾊谱仪的基本结构及掌握分离分析的基本原理2.了解氢⽕焰离⼦化检测器的检测原理3.了解影响分离效果的因素4.掌握定性、定量分析与测定⼆、实验原理1.⽓相⾊谱分离是利⽤试样中各组分在⾊谱柱中的⽓相和固定相间的分配系数不同⽽分离的。
当汽化后的试样被载⽓带⼊⾊谱柱运⾏时,组分就在其中的两相中进⾏反复多次的分配,由于固定相各个组分的吸附或溶解能⼒不同(即保留作⽤不同),因此各组分在⾊谱柱中的运⾏速度就不同,经过⼀定的柱长后,使彼此分离,顺序离开⾊谱柱进⼊检测器。
检测器将各组分的浓度或质量的变化转换成⼀定的电信号,经过放⼤后在记录仪上记录下来。
即得到描绘各组分⾊谱峰的⾊谱图。
根据保留时间和峰⾼或峰⾯积,便可进⾏定性定量的分析。
2.⽓相⾊谱基本结构供⽓系统:⽓源、⽓体净化、流速控制及测量进样系统:进样器、⽓化室分离系统:⾊谱柱及控温装置检测系统:检测器、控制电源及控温装置记录系统:放⼤器、记录仪或数据处理机3.氢⽕焰离⼦化检测器(FID)选择性检测器,是典型的破坏性、质量型检测器,是以氢⽓和空⽓燃烧⽣成的⽕焰为能源,当含碳有机物进⼊以氢⽓和氧⽓燃烧的⽕焰,在⾼温下产⽣化学电离,⽣成的离⼦在外加电场的作⽤下,形成离⼦流,根据离⼦流产⽣的电信号强度,检测被⾊谱柱分理出的组分。
三、仪器与试剂1.仪器⽓相⾊谱仪;氢⽓发⽣器;空⽓发⽣器;微量注射器10µL2.试剂B1苯(正⼰烷);C1甲苯(正⼰烷);苯、甲苯(正⼰烷)未知液;A1苯、甲苯(正⼰烷)标准液0.2µL/mL;A2苯、甲苯(正⼰烷)标准液2.0µL/ mL;A3苯、甲苯(正⼰烷)标准液4.0µL/ mL;A4苯、甲苯(正⼰烷)标准液10.0µL/ mL四、实验内容与步骤1.最佳分离条件:进样⼝温度:250℃;进样⽅式:分流(50:1);进样量:1µL;恒流模式;柱流量:1.0mL/min;升温程序:50℃(2min)→20℃/min→150℃(0.5min);检测器(FID)温度:250C;尾吹⽓流量:30mL/min;氢⽓流量:30mL/min;空⽓流量:300mL/min2.苯、甲苯定性分析在最佳的分离条件下,⽤10µL微量注射器,分别注射4.0µL的B1,C1标准溶液(重复进样3次),观察保留时间,确定苯和甲苯的峰。
苯、甲苯、乙苯混合物的分离与定性分析

苯、甲苯、乙苯混合物的分离与定量分析一.实验目的1.了解气相色谱仪的基本结构及操作步骤。
2.掌握气相色谱法分离多组分混合物的方法。
3.练习用归一化法定量测定混合物中各组分的含量二.实验原理1.气相色谱:气相色谱法是指用气体作为流动相的色谱法,主要是利用物质的沸点、极性及吸附性质的差异来实现混合物的分离。
待分析样品在汽化室汽化后被惰性气体(即载气:氮气)带入色谱柱,柱内含有固定相(邻苯二甲酸二壬酯)。
由于样品中各组分的沸点、极性或吸附性能不同,每种组分都倾向于在流动相和固定相之间形成分配或吸附平衡。
气相色谱主要由五部分组成:气路系统、进样系统、分离系统、温控系统、检测记录系统。
其中的分离系统和检测系统是仪器的核心。
(1-载气钢瓶;2-减压阀;3-净化干燥管;4-针形阀;5-流量计;6-压力表;7-进样口;8-色谱柱;9-热导检测器;10-放大器;11-温度控制器;12-记录仪)苯、甲苯、乙苯的沸点依次增高,所以汽化时苯先达到沸点汽化,甲苯、乙苯再依次汽化,故苯的保留时间最短,甲苯、乙苯的保留时间依次增长,故可以通过保留时间对混合物进行定性分析。
根据三者峰面积的不同则可以进行定量分析。
2.归一化法:若试样中含有n 个组分,且各组分均能洗出色谱峰,则其中某个组分的质量可按下式计算:三.实验仪器与试剂 Agilent Technologies 6890N 气相色谱仪热导池检测器微量注射器(1μL )苯(分析纯)甲苯(分析纯)乙苯(分析纯)丙酮(色谱纯)四.实验步骤1.取10支点样管,分别放两份丙酮、苯、甲苯、乙苯。
按照体积比苯:甲苯:乙苯=1:1:1配制两份混合液并摇匀。
(一份用于洗涤进样器,一份用于进样,防止污染试剂)2.自右向左打开仪器。
○1开气瓶时,先开减压阀,再开总阀,最后将减压阀调制0.5MPa 。
100)(100%1''21⨯⋅⋅=⨯+++=∑=n i i i i i ni i A f A f m m m m c○2开气相色谱仪,自检4-5min。
苯系物的分析
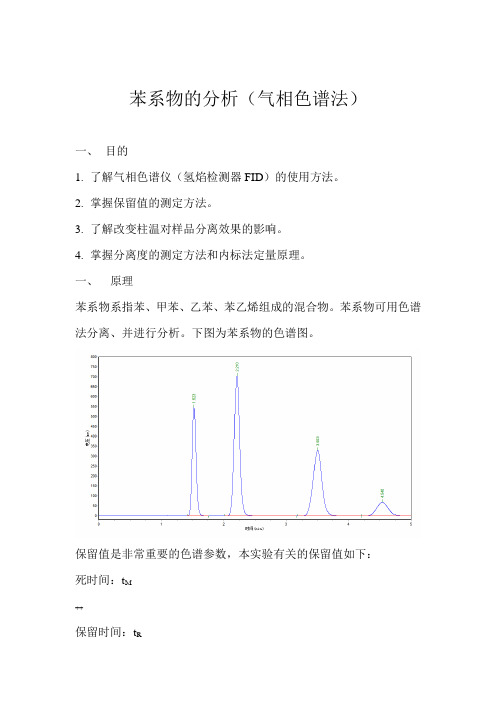
42.107225393.6721995986.87599.2652
混合物1
峰号保留时间峰高峰面积含量
10.940164832.016620187.31324.8665
21.215126205.609602062.62524.1398
31.69095220.805599251.43824.0271
21.50773556.453370126.00018.9160
32.08219617.906142608.7817.2883
42.54818056.539156139.8597.9798
3-1
峰号保留时间峰高峰面积含量
11.165297244.8441270635.62559.7502
21.50786255.570399224.65618.7731
10.94813687.00070874.7974.0158
21.190272253.5001684603.87595.4503
31.648562.0006378.2000.3614
42.007288.5003045.1750.1725
乙基苯1
峰号保留时间峰高峰面积含量
10.9231942.6925459.9920.3493
1-2
峰号保留时间峰高峰面积含量
11.165282513.5311273661.37569.4037
21.50775126.172384926.50020.9752
32.09010224.17279721.0554.3441
42.54810423.60096840.8595.2770
2-1
峰号保留时间峰高峰面积含量
液相色谱分析混合样品中的苯和甲苯

液相色谱分析混合样品中的苯和甲苯华南师范大学实验报告课程名称仪器分析实验实验项目液相色谱分析混合样品中的苯和甲苯实验类型□验证□设计□综合实验时间 2010 年 3 月 31 日实验指导老师实验评分一、实验目的1.掌握高效液相色谱定性和定量分析的原理及方法;2.了解高效液相色谱的构造、原理及操作技术。
二、实验原理高效液相色谱由储液器,泵、进样器、色谱柱、检测器、记录仪等几部分组成。
储液器中的流动相被高压泵打入系统,样品溶液经进样器进入流动相,被流动相载入色谱柱内。
由于样品溶液中的各组分在两相中具有不同的分配系数,在两相中作相对运动是,经过反复多次的吸附-解吸的分配过程,各组分在移动速度上产生较大的差别,被分离成单个组分依次从柱内流出,通过检测器时,样品浓度被转换成电信号传送到记录仪,记录成数据。
液相色谱的定性依据是保留时间的相对性,通常相对误差不能大于5%。
定量参数常常采用峰高、峰面积、相对峰高、相对峰面积等。
定量方法通常采用外标法、内标法和面积归一化法。
外标法为标准物质标准溶液制定标准曲线法;内标法为在标准溶液、样品溶液中加入内标物质,以相对峰高、相对面积对标准物质的浓度制定标准曲线;面积归一化法假定所有出峰物质的吸光系数相同,计算某物质的峰面积占所有峰面积的百分比。
三、仪器与试剂:1.仪器:SCL-10A vp紫外可见双波长检测器;SPD-M10A vp柱温箱;LC-10AT高效液相色谱仪;10μL微量注射器2.试剂:2μL/mL苯标液;2μL/mL甲苯标液;0.2μL/mL、2μL/mL、4μL/mL、10μL/mL的苯与甲苯的混合标准溶液;甲醇溶液;待测试样溶液四、实验内容与步骤:1.选择合适的流动相配比,优化色谱条件设置有关参数:控制流速为1mL/min。
柱温30℃,检测波长354nm。
设置流动相配比(甲醇:水=1:1),用10μL微量注射器注射5μL的10μL/mL苯与甲苯的混合标准溶液进行测定,观察其分离度和出峰时间。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1 实验目的
1.1 了解气相色谱仪的基本结构及基本操作。
1.2 掌握气相色谱法分离多组分混合物的方法。
1.3 练习用归一化法定量测定混合物中各组分的含量。
2 实验原理
2.1 气相色谱法
流动相为气体(称为载气);按固定相的不同又分为:气固色谱和气液色谱。
2.1.1 气相色谱法的特点:
(1)分离效率高:复杂混合物,有机同系物、异构体。
手性异构体。
(2)灵敏度高:可以检测出μg.g-1(10-6)级甚至ng.g-1(10-9)级的物质量.
(3)分析速度快:一般在几分钟或几十分钟内可以完成一个试样的分析。
(4)应用范围广:适用于沸点低于400℃的各种有机或无机试样的分析。
不足之处:
(1)不适用于高沸点、难挥发、热不稳定物质的分析。
(2)被分离组分的定性较为困难。
2.1.2 气相色谱流程
注:1-载气钢瓶;2-减压阀;3-净化干燥管;4-针形阀;5-流量计;6-压力表;7-进样口;8-色谱柱;9-热导检测器;10-放大器;11-温度控制器;12-记录仪。
(1)载气系统:包括气源、净化干燥管和载气流速控制;
(2)进样系统:进样器及气化室;
(3)色谱柱:填充柱(填充固定相)或毛细管柱(内壁涂有固定液);
(4)检测器:可连接各种检测器,以热导检测器或氢火焰检测器最为常见;
(5)记录系统:放大器、记录仪或数据处理仪;
(6)温度控制系统:柱室、气化室的温度控制。
2.2 内标法
在一定试样中加入一定量的内标物,根据待测组分和内标物的峰面积及物质量计算待测物质质量的方法。
内标物要满足以下要求:
(1)试样中不含有该物质;
(2)与被测组分性质比较接近;
(3)不与试样发生化学反应;
(4)出峰位置应位于被测组分附近,且无组分峰影响。
试样配制:准确称取一定量的试样W ,加入一定量内标物m S 。
计算式:
内标法的特点:
(1)内标法的准确性较高,操作条件和进样量的稍许变动对定量结果的影响不大。
(2)每个试样的分析,都要进行两次称量,不适合大批量试样的快速分析。
(3)若将内标法中的试样取样量和内标物加入量固定,则:
2.3 归一化法
若试样中含有n 个组分,且各组分均能洗出色谱峰,则其中某个组分的质量可按下式计算。
3 主要仪器及试剂 3.1 主要仪器
气相色谱仪,热导池检测器,微量注射器(10mL ),色谱柱(2 m ×5 mm ) 3.2 主要试剂
氮气,苯,甲苯,乙苯 4 实验步骤
4.1 打开电脑主机,再打开气相色谱的模块,启动工作站并初始化仪器。
4.2 开机调试,按下列参考色谱条件将仪器调至所需工作状态。
气化室温度:150℃; 柱温:110 ℃; 检测器温度: 200 ℃
4.3 运行程序,清洗色谱柱,直至基线平稳,然后进样,进行测定。
4.4 开始测定
4.4.1 定性测定
仪器稳定后,用1.0μL 注射器分别进0.8μL 苯、甲苯和乙苯,记录保留时间。
4.4.2 定量测定
用1.0μL 注射器分别进0.8μL 苯、甲苯和乙苯的混合物,记录色谱图。
5 数据处理 5.1 实验数据
5.2.2 定量测定
Peak1: 保留时间=2.006min;峰面积=106.01720 Peak2: 保留时间=2.186min;峰面积=73.44507
S s i
i s i S
s i
i s i A f A f m m A f A f m m '
''';==100
100100%'''
'⨯⋅=⨯=⨯=S
s i
i s S s i i s i i A f A f W m W A f A f m W m c 常数⨯=
S
i
i A A c %
Peak3: 保留时间=2.490min;峰面积=74.97932
5.2 数据处理
四次实验结果对比可知,混合物的色谱图中Peak1是苯的峰, Peak2是甲苯的峰, Peak3时乙苯的峰。
重量校正因子的文献值为:苯:0.780,甲苯:0.794,乙苯:0.818。
混合物中各组分的含量分别为:
m
苯
=0.780×106.01720=82.69
m
甲苯
=0.794×73.44507=58.32
m
乙苯
=0.818×74.97932=61.33
S总= 82.69+58.32+61.33=202.34
各组分所占百分比分别为:
α(苯)=82.69
202.34
×100%=40.86%
α(甲苯)=58.32
×100%=28.83%
α(乙苯)=61.33
202.34
×100%=30.31%
6 实验结果与讨论
6.1 实验结果
6.2
6.2.1 进样器要充分洗涤,否则会有杂质,导致用归一化法求含量时会有较大误差。
本次实验中疑似混合样中混有少量丙酮,因为每一次测得的色谱图中都会出现一个很小很小的杂质峰。
6.2.2 3、进样时动作应迅速,进样速度和按下START键的速度应一致,否则会使峰形变化。
6.2.3 进样量如果不准,不会影响归一化法的分析结果,因为无论量的多少,溶液的组成成分都不会改变。
6.2.4 本次实验仪器较稳定,进样速度较快,故得出的谱图中峰较窄、尖锐,达到了较好的分离效果,实验较成功。
