2015版纯化水微生物限度检查记录
纯化水微生物限度检查记录
RF-08-099 A/0
第 1 页 共 1 页
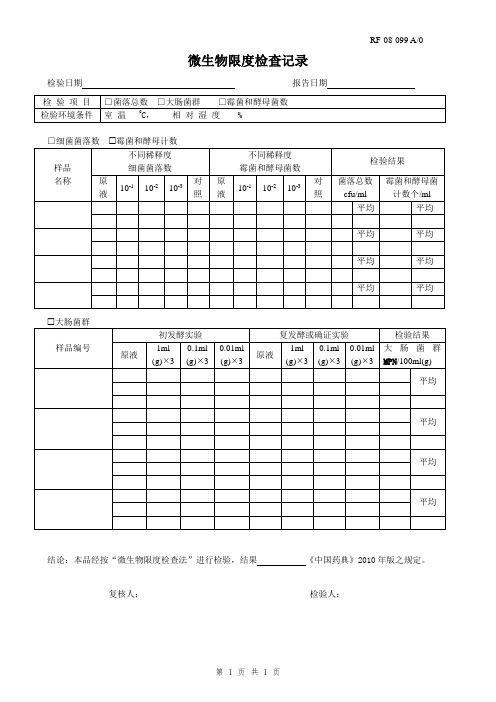
微生物限度检查记录
检验日期 报告日期 检 验 项 目
□菌落总数 □大肠菌群 □霉菌和酵母菌数
检验环境条件 室 温 0
C , 相 对 湿 度 %
□细菌菌落数 霉菌和酵母计数 样品 名称 不同稀释度 细菌菌落数
不同稀释度 霉菌和酵母菌数 检验结果
原液 10-1 10-2 10-3 对照 原液
10-1 10-2 10-3 对照
菌落总数cfu/ml 霉菌和酵母菌计数个/ml
平均 平均 平均 平均 平均 平均
平均
平均
大肠菌群
样品编号 初发酵实验
复发酵或确证实验 检验结果
原液
1ml (g) 3 0.1ml (g) 3 0.01ml (g) 3 原液 1ml (g) 3 0.1ml (g) 3 0.01ml (g) 3 大肠菌群MPN /100ml(g)
平均
平均
平均
平均
结论:本品经按“微生物限度检查法”进行检验,结果 《中国药典》2010年版之规定。
复核人: 检验人:。
《中国药典》2015版 纯化水

纯化水ChunhuashuiPurified Water本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
【性状】本品为无色的澄清液体;无臭。
【检査】酸碱度取本品1 0ml,加甲基红指示液2 滴,不得显红色;另取1 0m l,加溴麝香草酚蓝指示液5 滴,不得显蓝色。
硝酸盐取本品5m l置试管中,于冰浴中冷却,加10%氣化钾溶液0. 4 m l与0. 1%二苯胺硫酸溶液0. 1ml,摇匀,缓缓滴加硫酸5m l,摇勻,将试管于50T:水浴中放置1 5分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0. 163g,加水溶解并稀释至100ml,摇匀,精密量取lm l ,加水稀释成100ml,再精密量取1 0m l,加水稀释成100ml,摇匀,即得(每lm l相当于1吨N 0 3)]0 . 3m l,加无硝酸盐的水4. 7m l,用同一方法处理后纯化水的颜色比较,不得更深(0. 000 006% ) 。
亚硝酸盐取本品1 0m l,置纳氏管中,加对氨基苯磺酰胺的稀盐酸溶液(1 — 1 0 0 ) lm l与盐酸萘乙二胺溶液(0. 1 -l00Uml,产生的粉红色,与标准亚硝酸盐溶液[取亚硝酸钠0. 750g(按干燥品计算),加水溶解,稀释至100ml,摇匀,精密量取1m l,加水稀释成100ml,摇匀,再精密量取1ml,加水稀释成50m l,摇勻,即得(每lm l相当于1叫NO2) ]0 . 2m l,加无亚硝酸盐的水9. 8m l,用同一方法处理后的颜色比较,不得更深(0. 000 002% ) 。
氨取本品5 0m l ,加碱性碘化汞钾试液2m l ,放置1 5分钟;如显色,与氣化铵溶液(取氣化铵31. 5m g ,加无氨水适量使溶解并稀释成1000ml) 1. 5m l ,加无氨水4 8m l与碱性碘化汞钾试液2m l制成的对照液比较,不得更深(0_ 000 03% ) 。
2015版中国药典纯化水微生物限度检测方法验证方案
1. 审批起草人签名:审核人签名:批准人签名:2. 目录1.审批 (1)2.目录 (2)3.目的 (3)4.范围 (3)5.职责 (3)6.执行程序 (4)7.描述 (4)8.方法验证 (4)8.1.人员培训 (4)8.2.文件确认 (5)8.3.仪器确认 (5)8.4.供试品确认 (6)8.5.培养基及缓冲液确认 (6)8.6.菌种确认 (7)8.7.培养基 (7)8.8.菌种:枯草芽孢杆菌、铜绿假单胞菌。
(7)8.9.供试品制备 (8)8.10.试验结果 (9)8.11.验证结果分析与评价 (10)9.偏差处理 (10)10.变更控制 (10)11.附件日志 (11)12.再验证 (11)13.参考书目 (11)14.修订历史 (12)3. 目的纯化水微生物限度检查采用薄膜过滤法,验证该方法适用于纯化水中需氧菌总数的测定。
4. 范围本验证方案适用于上海XXXX有限公司QC实验室,对纯化水微生物限度检查方法(薄膜过滤法)适用性的验证。
5. 职责5.1. 验证小组组成:5.2. 验证小组组长负责5.2.1. 组织起草或审核验证方案及变更申请;5.2.2. 对验证小组成员进行培训;5.2.3. 验证方案的组织实施;5.2.4. 对验证过程中的记录审核,保证其真实性、可靠性和完整性;5.2.5. 组织验证报告的起草、汇总并参与对其进行审核及验证周期的拟定。
5.3. QA参与人员负责5.3.1. 审核验证方案、报告及报告中出现的偏差、变更;5.3.2. 参与验证方案的实施及评价;5.3.3. 对验证方案及报告进行编号并纳入验证文件系统且归档。
5.4. QC参与人员负责5.4.1. 起草验证方案;5.4.2. 已经批准的验证方案的具体实施;5.4.3. 收集测试数据,应评估数据并对测试数据做出评论;5.4.4. 参与偏差调查、变更申请等;5.4.5. 起草验证报告。
6. 执行程序6.1. 一旦方案被批准和发布,组长对本验证小组人员进行本方案的培训;6.2. 所有用于测试的仪器/仪表都必须经过校验/验证后才能用于测试;6.3. 验证小组负责核查所有完成的测试结果和附件的完整性;6.4. 测试完成后,由组长及相关部门做出确认结论。
制药用水微生物限度检验方法学确认2015.11

制药用水-微生物限度检验方法学确认目录一、引言1、概述2、验证的目的二、验证方法合格标准三、主要材料确认1、仪器设备确认2、辅助材料确认3、人员确认4、商品培养基及灭菌培养基确认5、菌种及菌液的制备四、样品制备1、稀释液2、供试液制备3、操作方法五、方法验证1、需氧菌总数的计数方法验证2、计算菌回收率公式六、验证结果及评价七、再验证周期八、验证结论批准一、引言1、概述:根据《中国药典》2015年版三部通则“1105 非无菌产品微生物限度检查:微生物计数法”(以下简称《药典》)的要求,对内控标准中有“微生物限度”检查项的产品进行该项验证。
根据《中国药典》2015年版三部纯化水进行方法学确认。
2、验证目的:确保药品微生物限度检查实验的准确性,在建立药品的微生物限度检查法时,应进行需氧菌总数计数方法的验证,以确认所采用的方法适合于该样品的需氧菌总数的测定。
二、验证方法合格标准1.前提条件:培养基适用性实验应符合规定,即:被检R2A培养基上菌落平均数与对照培养基上菌落平均数比值应为0.5~2,且菌落形态大小应与对照培养基上的菌落一致。
2.计数方法适用性试验:在3次独立的平行试验中,若试验组的菌回收率(试验组的平均菌落数减去供试品对照组的平均菌落数的值与菌液对照组的平均菌落数的比值)均在0.5~2范围内,照该供试液制备方法和计数法测定供试品的需氧菌总数。
三、主要材料确认1、仪器、设备确认检查结果:检查人:复核人:日期:2、辅助材料确认2.1移液器、接种环、酒精灯、记号笔、酒精棉球、试管架、试管、玻璃平皿、止血钳等2.2需灭菌物品见《微生物限度检查法验证记录》2.3一次性无菌用具见下表检查结果:检查人:复核人:日期:3、人员确认化验员经设备操作、微生物检验技术和实验室生物安全等方面的培训,考核合格后上岗。
4、商品培养基及灭菌培养基4.1 所用培养基均不得有结块、吸潮、异味、颜色发生改变等现象。
培养基检查结果,如下检查结果:检查人:复核人:日期:4.2已灭菌培养基的检查结果及结论见《微生物限度检查法验证记录》。
《中国药典》2015药典纯化水标准

中国药典2015年版溶液的澄清度与颜色取本品,加水制成每lml中约含阿魏酸钠20m g的溶液,溶液应澄清无色;如显浑浊,与1号池度标准液(通则0902第一法)比较,不得更浓;如显色,与黄色或黄绿色3号标准比色液(通则0901第一法)比较,不得更深。
有关物质避光操作。
取本品,加流动相溶解并稀释制成每l m l中约含0. 7m g的溶液,作为供试品溶液;精密量取lm l,置200m l量瓶中,用流动相稀释至刻度,摇勻,作为对照溶液。
照阿魏酸钠有关物质项下的方法测定。
供试品溶液的色谱图中如有杂质峰,各杂质峰面积的和不得大于对照溶液的主峰面积(0.5%)。
水分取本品,照水分测定法(通则0832第一法1)测定,含水分应为13.0%〜16.0%(供无菌粉末用)或应不超过3.0%(供无菌冻干品用)。
热原取本品,加灭菌注射用水制成每l m l中含阿魏酸钠5m g的溶液,依法检查(通则1142),剂量按家兔体重每l k g 缓慢注射3m l,应符合规定。
无菌照阿魏酸钠项下的方法检査,应符合规定。
其他应符合注射剂项下有关的各项规定(通则0102)。
【含置测定】避光操作。
取装量差异项下的内容物约0.15g,精密称定,加冰醋酸20m l使阿魏酸钠溶解,照阿魏酸钠项下的方法,自“加醋酐3m l”起,依法测定。
每l m l高氣酸滴定液(0.lm o l/L)相当于25.22mg的C10H9N a04•2H20。
【类别】同阿魏酸钠。
【规格】(1)0. lg(2)0. 3g【贮藏】遮光,密封保存。
纯化水ChunhuashuiPurified WaterH2018.02本品为饮用水经蒸馏法、离子交换法、反渗透法或其他适宜的方法制得的制药用水,不含任何添加剂。
【性状】本品为无色的澄清液体;无臭。
【检査】酸碱度取本品10m l,加甲基红指示液2滴,不得显红色;另取10m l,加溴麝香草酚蓝指示液5滴,不得显蓝色。
硝酸盐取本品5m l置试管中,于冰浴中冷却,加10%氣化钾溶液0.4m l与0.1%二苯胺硫酸溶液0.1m l,摇匀,缓缓滴加硫酸5m l,摇勻,将试管于50T:水浴中放置15分钟,溶液产生的蓝色与标准硝酸盐溶液[取硝酸钾0.163g,加水溶解并稀释至100m l,摇匀,精密量取l m l,加水稀释成100m l,再精密量取10m l,加水稀释成100m l,摇匀,即得(每l m l相当于1吨N03)]0.3m l,加无硝酸盐的水4.7m l,用同一方法处理后纯化水的颜色比较,不得更深(0.000006%)。
微生物限度检验记录表 2015版药典

阴性对照
菌落数(cfu)
平皿
1∶1
1∶10
1∶102
1
2
平均
样品编号
平皿编号
各稀释度菌落数
阴性对照
菌落数(cfu)
平皿
1∶1
1∶10
1∶102
1
2
平均
标准规定
纯化水需氧菌总数不超过100cfu/mL
注射用水需氧菌总数不过超过10cfu/100ml
结论
微生物限度□符合□不符合标准要求。
审核:复核:检验-01-0
使用编号
微生物限度检验记录
样品名称:□纯化水□注射用水取样日期:
取样数量:样品编号:
培养开始时间:月日结束培养时间:月日
R2A琼脂培养基批号:培养温度:℃
样品编号
平皿编号
各稀释度菌落数
阴性对照
菌落数(cfu)
平皿
1∶1
1∶10
1∶102
1
2
平均
样品编号
平皿编号
2015年版微生物限度检验操作规程.
青岛**有限公司文件目的建立微生物限度检查操作规程,规范操作,保证结果的准确性。
范围成品、辅料、内包装袋及纯化水的检验。
责任品管部微生物限度检验人员内容概述:本检验操作规程依据中国药典2015年版四部《通则1105 非无菌产品微生物限度检查:微生物计数法》和《通则1106 非无菌产品微生物限度检查:控制菌检查法》进行检查。
微生物计数法一、计数方法1.微生物计数法系用于能在有氧条件下生长的嗜温细菌和真菌的计数。
2、计数方法本法包括平皿法、薄膜过滤法。
3、计数培养基适用性检查和供试品计数方法适用性检查供试品微生物计数中所使用的培养基应进行适用性检查。
供试品的微生物计数方法应进行方法适用性试验,以确定采用的方法适合于该产品的微生物计数。
4、菌种及菌液的制备4.1试验用菌株的传代次数不得超过5代(从菌种保藏中心获得的干燥菌种为第0袋),并采用适宜的菌种保藏技术进行保藏。
计数培养基适用性检查和计数方法适用性试验见表1。
4.2菌液制备按表1规定培养各试验菌株。
取金黄色葡萄球菌、铜绿假单胞菌、枯草芽孢杆菌、白色念珠菌的新鲜培养物,用PH7.0无菌氯化钠-蛋白胨缓冲液或0.9%无菌氯化钠溶液制成适宜浓度的菌悬液;取黑曲霉的新鲜培养物加入3-5ml含0.05%(ml/ml)聚山梨酯80的PH7.0无菌氯化钠-蛋白胨缓冲液或0.9%无菌氯化钠溶液,将孢子洗脱。
采用适宜的方法吸出孢子悬液至无菌试管中,用含0.05%(ml/ml)聚山梨酯80的PH7.0无菌氯化钠-蛋白胨缓冲液或0.9%无菌氯化钠溶液制成适宜浓度的黑曲霉孢子悬液。
菌液制备后若在室温下放置,应在2小时内使用;若保存在2-8℃,可在24小时内使用。
黑曲霉孢子悬液可保存在2-8℃,在验证过的贮存期内使用。
表1 试验菌液的制备和使用4.3阴性对照为确认试验条件是否符合要求,应进行对照试验,阴性对照试验应无菌生长。
4.4培养基适用性检查按照表1规定,接种不大于100cfu的菌液至胰酪大豆胨液体培养基或胰酪大豆胨琼脂培养基平板或沙氏葡萄糖琼脂培养基平板,置规定的条件下培养。
微生物限度记录2015
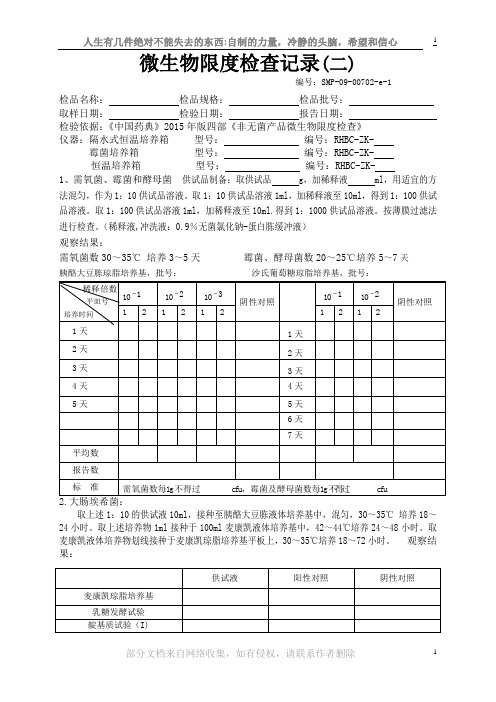
微生物限度检查记录(二)编号:SMP-09-00702-e-1检品名称:检品规格:检品批号:取样日期:检验日期:报告日期:检验依据:《中国药典》2015年版四部《非无菌产品微生物限度检查》仪器:隔水式恒温培养箱型号:编号:RHBC-ZK- 霉菌培养箱型号:编号:RHBC-ZK-恒温培养箱型号:编号:RHBC-ZK-1、需氧菌、霉菌和酵母菌供试品制备:取供试品 g,加稀释液 ml,用适宜的方法混匀,作为1:10供试品溶液。
取1:10供试品溶液1ml,加稀释液至10ml,得到1:100供试品溶液。
取1:100供试品溶液1ml,加稀释液至10ml.得到1:1000供试品溶液。
按薄膜过滤法进行检查。
(稀释液,冲洗液:0.9%无菌氯化钠-蛋白胨缓冲液)观察结果:需氧菌数30~35℃培养3~5天霉菌、酵母菌数20~25℃培养5~7天胰酪大豆胨琼脂培养基,批号:沙氏葡萄糖琼脂培养基,批号:取上述1:10的供试液10ml,接种至胰酪大豆胨液体培养基中,混匀,30~35℃培养18~24小时。
取上述培养物1ml接种于100ml麦康凯液体培养基中,42~44℃培养24~48小时。
取麦康凯液体培养物划线接种于麦康凯琼脂培养基平板上,30~35℃培养18~72小时。
观察结果:取供试品,用胰酪大豆胨液体培养基作为稀释剂制成1:10供试液,混匀,在20~25℃培养约2小时。
取上述预培养物10ml接种至100ml肠道菌液体培养基中,30~35℃培养24~48小时后,划线接种于紫红胆盐葡萄糖琼脂培养基平板上,30~35℃培养18~24小时。
取相当于0.1g、0.01g和0.001g(或0.1ml、0.01ml和0.001ml)的供试品的预培养物接种至 ml的肠道菌液体培养基中,30~35℃培养24~48小时。
取上述培养物分别划线接种于紫红胆盐葡萄糖琼脂培养基平板上,30~35℃培养18~24小时。
观察结果:取供试品10g或10ml,直接接种到200ml胰酪大豆胨液体培养基中,混匀,30~35℃培养18~24小时。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
累计培养时间
年月日时
年月日时
h
培养
时间
/
取样点编号
阴性对照
24h
1
□长菌
□未长菌
2
48h
1
□长菌
□未长菌
2
72h
1
□长菌
□未长菌
2
菌数报告
CFU/ml
/
标准规定
需氧菌总数每1ml不得过100CFU。
项目结论
□符合规定
□不符合规定
□符合规定
□不符合规定
纯化水微生物限度检查记录
检验日期
年月日
报告日期
年月日
检验依据
《中国药典》2015年版二部、四部通则微生物检查法
需氧菌总数检查:取纯化水50ml,用薄膜过滤器(0.45±0.02um,50MM直径)过滤,减压抽干。取出滤膜,将滤膜放入制备好的R2A培养基平板上,在30~35℃培养3天,计数。
需氧菌阴性对照:取50ml已灭菌的纯化水按供试品同法处理,作为阴性对照。
□符合规定
□不符合规定
□符合规定
□不符合规定
□符合规定
□不符合规定
□符合规定
□不符合规定
/
检验人:复核人:
