盐酸莫西沙星氯化钠与3种注射液配伍的化学稳定性考察
盐酸莫西沙星氯化钠注射液与注射用丹参配伍的稳定性考察

图 2 混 合 液 中莫 西 沙 星 色 谱 图
2 10 0 ) 注 射 用 丹 参 ( 干 ) 哈 药 集 团 中 药 二 厂 生 产 , 0 0 39 ; 冻 ( 规
格 : . / , 号 :0 0 3 9 。 0 4g 支 批 2 10 2 )
流 动 相 为 甲醇 一水 一三 乙 胺 ( 1 . 0 2 8 9 : . 6 , 速 1 12 5 :0 .0 0 0 ) 流 m /m n, 外 检 测 波 长 为 2 9 m , 样 量 1 L 。 图 L i 紫 8 n 进 0 … 见
l ~2。
Hale Waihona Puke 喹 诺 酮 类 相 比 , 于 其结 构 中 引 入 了 8一甲氧 基 和 C一7位 上 由
同 时观 察 混 合 液 外 观 及 p H值 的 变化 。 结 果 盐 酸 莫 西 沙 星 氯 化 钠 注 射 液 与 注射 用 丹 参 混 合 后 , 8h内莫 西 沙 星 含 量
和 p 值 无 明显 变化 , 1h时 , 合 液 出现 白 色沉 淀 ,H值 及 盐 酸 莫 西 沙 星 含 量 均 有 所 下 降 。 结 论 盐 酸 莫 西 沙 星 H 但 混 p 氯 化钠 注 射 液 与 注射 用丹 参 配伍 在 室 温 下 性 质 不 稳 定 。 [ 键 词 ] 盐 酸 莫 西 沙 星 ; 参 冻 干 粉 ; 定 性 关 丹 稳 [ 图 分 类 号 ] R 6 . 中 992 [ 献标 识 码 ] B 文 [ 章 编 号 ] 10 文 0 8—84 (0 2 0 0 4 0 8 9 2 1 )6— 64— 2
型 酸度计( 海伟 业仪器厂 )T L3 上 ;T 2 0超 纯 水 器 ( 家 ) 盐 酸 厂 ;
沙星注射液在两种输液中的配伍稳定性

Results of recovery test of FLX(T/=5,z±S)
FS
XL
X RSD
/%/%
对企业药品微生物限度检查方法验证 资料的审核分析
罗书香 (贵州省黔南州药品检验所,贵州都匀5581)()【))
3结果 3.1 FLX与2种输液配伍稳定性实验模拟FLX临床用 药质量浓度[(o。2 g·(250 mL)1)],分别用FS和XL配制 质量浓度为0.8 g·I。1的样品。将两种样品分别置25,37℃ 恒温水浴中放置,于(),1,2,4,6 h各精密量取适量,稀释成8 mg·L1溶液,摇匀,依法测定峰面积。以零时FLX含量为 100%,计算各样品在不同温度、不同时间的相对百分含量, 结果见表2。 表2 FLX在2种输液中pH值及含量变化《挖=5)一 Tab 2 The results of pH determination and assay of FLX injection in two infusion(n=5)
[作者简介]熊建华,男,电话:0577—88059585,E-mail:Xjh0512@163.net
万方数据
·686·
中国医院药学杂志2007年第27பைடு நூலகம்第5期Chin Hosp Pharm J,2()07 May,Vol 27,No.05
表1 FLX在两种输液中的回收率(行=5,f±s)
,鬻,焉,瓣熏 Tab 1
海科学技术出版社,1999.63. [23中国药典.临床用药须知[S].2000:320. t-3]贾公孚,谢惠民主编.药物联用禁忌手册[M].第11版,北京:
中国协和医科大学出版社,2001:319-321. [4]迟丹恰,王大猷,李虹影,等.药师在药物警戒中的作用CJ3.中
盐酸莫西沙星氯化钠注射液与丹红注射液存在配伍禁忌

上 层 液 体 仍 为 深 黄 色 较 清 发 现 加入 的丹 红 注 射 液 越 多 , 生 的 絮状 物 及 沉 淀 越 多 。 产
用 于冠 心 病 、 心绞 痛 、 脑血 栓 的治 疗 。 述 药 物 在 临 床 中 应用 上
以 上 两 种 药 物 均 经 药 检 合 格 , 由 正 规 厂 商 生 产 。经 临 且
床 观 察 及 实 验 证 明 , 酸 莫 西 沙星 氯 化 钠 注 射 液 确 实 与 丹 红 盐
注 射 液 存 在 配 伍 反 应 。 因 此 , 示 临床 应 用 这 两 种 药 物 时 应 提 避 免 同 时使 用 , 病 情 需 要 同 时 使 用 , 使 用 生 理 盐 水 作 为 如 可 间 隔 液 冲洗 输 液 器 管 道 后 再 输入 。
【】 均艳 .医疗 事故 处 理 条 例 》 护 士 的影 响【 】 理 研 究 , 1刘 《 对 J. 护
2 0 ,6 1 ) 6 5 6 6 0 21 ( :7 — 7 . 1
[1 2 中华 人 民共 和 国 国务 院第 5 7号 .护 士 条 例 》MJ 京 : 1 《 [. 北 中
【 验荟萃 】 经
盐 酸莫西沙星氯化钠注射液 与丹红注射液存在配伍禁忌
韩甜甜
( 国人 民解 放 军 第 3 9医 院 干部 病 房 , 京 1 0 9 ) 中 0 北 0 0 1
【 关键词】 盐酸莫西沙星氯化钠注射液;丹红注射液;配伍禁忌
盐 酸 莫 西 沙 星 氯 化 钠 注 射 液 ( 品名 : 复 乐 )规 格 为 商 拜 ,
来盐酸莫西沙星氯化钠注射液的配伍禁忌

来盐酸莫西沙星氯化钠注射液的配伍禁忌盐酸莫西沙星氯化钠注射液(商品名:拜复乐),黄色澄明液体,规格250ml,是第4代新型8-甲氧基氟喹诺酮类抗菌药物,具有抗菌谱广、抗菌力强、体内分布广、体内药物浓度高、半衰期长、疗效好、不良反应小、与其他抗菌药物无交叉耐药性、几乎无光敏反应等优点。
临床上主要应用于治疗呼吸系统、泌尿生殖系统、皮肤系统等感染性疾病。
在近几年的临床用药过程中,笔者发现盐酸莫西沙星氯化钠注射液与多种药物之间存在配伍禁忌,经混合后,均出现白色浑浊现象或者有晶体析出。
为保证临床用药安全,本文查阅了国内相关文献,对其配伍禁忌进行综述,以供临床合理配伍药品参考,保证患者用药安全。
1 抗感染类药物1.1头孢菌素类与头孢哌酮钠他唑巴坦钠存在配伍禁忌。
有研究报道,头孢哌酮钠他唑巴坦钠组滴注完予更换盐酸莫西沙星氯化钠注射剂组液体5s后,茂菲氏滴管内出现白色浑浊,经摇晃不消失[1]。
1.2青霉素类与氟氯西林钠存在配伍禁忌。
有研究报道,将盐酸莫西沙星氯化钠注射剂与0.9%氯化钠注射液100ml+注射用氟氯西林钠联合应用,盐酸莫西沙星氯化钠注射剂更换注射用氟氯西林钠组液体时,输液管内立即出现乳白色浑浊及絮状物;将两种溶液直接混合,发现混合液立即变为乳白色浑浊液,轻摇晃后不溶解,放置30min后观察乳白色浑浊液未恢复澄清[2]。
1.3利福霉素与注射用利福霉素钠存在配伍禁忌。
有研究报道,将注射用利福霉素钠1.0g溶解于5%葡萄糖250ml,抽取2ml注射用利福霉素钠溶液,再抽取2ml 盐酸莫西沙星氯化钠注射剂,将两者混合,或更换两者顺序抽取,混合液均立即出现红色絮状混浊物,剧烈振荡后无变化[3]。
1.4米卡芬净钠与注射用米卡芬净钠存在配伍禁忌。
有研究报道,盐酸莫西沙星氯化钠注射剂输注完毕更换米卡芬净钠时,输液器内溶液呈现乳黄色混浊并有絮状物[4]。
1.5夫西地酸钠与注射用夫西地酸钠存在配伍禁忌。
有研究报道,用20ml 注射器分别抽取夫西地酸钠和莫西沙星注射液各5ml。
盐酸莫西沙星氯化钠注射液和止血药的配伍分析

盐酸莫西沙星氯化钠注射液和止血药的配伍分析【摘要】:目的:探究盐酸莫西沙星氯化钠注射液和止血药的配伍分析。
方法:临床上分别选择等吸收双波长消去法、紫外分光光度法,对基于25 ℃、37℃条件下,盐酸莫西沙星氯化钠注射液同共4种止血药物配伍情况,以及8 h 内莫西沙星含量进行分析,并对混合液pH值及外观变化实施观察。
结果:在8h时间中配伍液是透明的、浅黄色液体,无沉淀、气泡生成,无颜色转变。
配伍液的pH 值从 0~ 8 h无显著变化。
针对于莫西沙星的含量,于定波长处测定,结果显示其含量在配伍后8 h 内无显著变化。
在测定含量时,经紫外扫描各配伍液,结果显示在8h时间中,吸收曲线无显著变化,也没有新吸收峰出现。
结论:经同4种止血药配伍后8h中,盐酸莫西沙星氯化钠注射液含量与混合液性质较为稳定,但是仍需进一步探究4种止血药含量是否有影响。
【关键词】:止血药;莫西沙星;配伍盐酸莫西沙星氯化钠注射液中的主要成分包含盐酸莫西沙星,氢氧化钠、注射用水、氯化钠、盐酸等均是其辅料,此种药物作为第 4 代新型8-甲氧基氟,常用于对上下呼吸道感染的治疗[1]。
临床上常与止血药配伍,用于治疗和预防术后出血和感染情况,但是当前的临床上无较多关于配伍稳定性的研究。
基于此探究分析盐酸莫西沙星氯化钠注射液配伍止血药的稳定性,现将相关报道如下:1.材料1.1试药盐酸莫西沙星氯化钠注射液(国药准字H20130039,规格:20ml:400mg,南京优科制药有限公司)、维生素K1注射液(国药准字H11021167,1ml:10mg,山西晋新双鹤药业有限责任公司)、氨基己酸注射液(国药准字H21024268,20ml:4g)、酚磺乙胺注射液(国药准字H20040754,规格:100ml,四平巨能药业有限公司)、氨甲苯酸注射液(国药准字:H32024863,规格:5ml∶5mg,常州康普药业有限公司)。
1.2仪器选择美国奥立龙公司的CHN 828 型酸度计;上海天美科学仪器公司的UV -VIS 8500型分光光度计;上海嘉程仪器设备厂的JC303-3B 电热(隔水)培养箱。
常用中药注射剂与各类抗菌药物配伍稳定性研究

1 材料与方法 1.1 一般资料
选取本院20 0 9年11月—2011年11月期间的临床中药注射剂与 抗菌 药 物配 伍 用 药 情况的 报 告。 1.2 方法
组 成由执 业药师组 成的常用中药注 射剂和各 类 抗菌 药物配 伍 稳 定 性 观 察 小 组,对 本 院 这 段 时 间内中药注 射 剂和 抗菌 药 物 配 伍使 用 情况 进 行 调 查、研 究、总 结。 2 结果
行配伍 之 后,溶液在4 h内的吸收 度变化值均全 部>10 %,即使 溶 液在4 h内的澄明度并没有明显变化,但 是 还是不 建 议 进行联用 使 用。有资 料证明,中药鱼 腥草注 射 液在和临床常用的 抗菌 药物 进行配伍 后,其 不溶性微粒以及pH值等 会发生明显的变化,并已 经 确定中药 鱼 腥草 注 射 液和 头 孢 拉 定以及 头 孢噻 肟 进 行 联 合 配 伍 禁止使 用。 3.2 莪术油葡萄糖注射液和各类抗菌药的配伍
青霉素 青霉素钠 头孢唑林钠 头孢曲松 庆大霉素 庆大霉素 阿奇霉素 盐酸莫西沙星氯化钠 夫西地酸钠
出现pH值降低,有效 成分含量明显降低。 颜色变深,不溶性微粒
数量明显增加。 出现pH波动, 吸光度波动。 出现乳白色的液体
浑浊情况。 出现浑浊、沉淀。 颜色改变,莪术油的 含量发生下降。 连续静滴,出现沉淀
有报 道经临床实验 认为,发生沉淀的主要原因是发生了pH值 的降低。并经相关实验 证明,中药双黄连注射 液在和pH值较低的 抗菌 药 阿 米 卡星和庆 大 霉素 联 合 使 用时会出现明显的药 物 沉 淀, 在和 p H 值比 较 高的 抗菌 素头 孢 唑 林 共同 配 伍 时可以保 持 相 对 的 澄明。有报 道研 究中药双黄连和氧氟沙星、培氟沙星、环 丙沙星、 洛美沙星以及氟罗沙星等喹 诺酮类抗菌 药物进行配伍时,均发现 混 合后的不溶性 微粒 全 部 不符 合《中国药典》的相关 规 定,所以 不 容许直 接 进 行 配 伍使 用。 4 小结
盐酸莫西沙星氯化钠注射液与注射用丹参多酚酸盐存在配伍禁忌

盐酸莫西沙星氯化钠注射液与注射用丹参多酚酸盐存在配伍禁忌目的探讨盐酸莫西沙星氯化钠注射液与注射用丹参多酚酸盐存在配伍禁忌。
方法将盐酸莫西沙星氯化钠注射液与注射用丹参多酚酸盐进行配伍试验,观察盐酸莫西沙星氯化钠注射液与注射用丹参多酚酸盐的配伍试验结果。
结果盐酸莫西沙星氯化钠注射液与注射用丹参多酚酸盐混合后,立即出现絮状物及乳白色混浊,经过震荡以及久置后混浊不退,说明盐酸莫西沙星氯化钠注射液与注射用丹参多酚酸盐存在配伍禁忌。
结论盐酸莫西沙星氯化钠注射液与注射用丹参多酚酸盐存在配伍禁忌,要尽量避免两种药物的同时应用,如果必须联合应用,应在两药之间用0.9%氯化钠进行间隔。
标签:盐酸莫西沙星氯化钠注射液;注射用丹参多酚酸盐;配伍禁忌盐酸莫西沙星氯化钠注射液(商品名称:拜复乐)由拜耳医药保健股份公司生产是具有广谱活性和杀菌作用的8-甲氧基氟喹诺酮类抗菌药,为黄色的澄清液体,临床常用于成人(≥18岁)上呼吸道和下呼吸道感染,以及皮肤、软组织感染有良好的抗感染作用。
注射用丹参多酚酸盐(上海绿谷制药有限公司)为浅棕色疏松块状物,具有活血、化瘀、通脉作用,适用于胸部刺痛、绞痛的患者,或有心悸、冠心病、心绞痛等病症的人,它的药理作用机制是抑制血小板聚集和增加冠脉流量的作用,能明显改善人体血液流变的作用,它还可以可降低血液黏度,有效增加血液流量。
用于冠心病的稳定性心绞痛,可分级为Ⅰ、Ⅱ级,心绞痛症状表现为轻、中度,中医辨证为心血瘀阻证者,症见胸痛、胸闷、心悸。
以上2种药均为临床上常用的静脉滴注药物。
近期本科室收治1例冠心病以及上呼吸道感染的患者,就需要这两种药物同时使用,在临床治疗过程中,发现拜复乐注射液同注射用丹参多酚酸盐存在配伍禁忌。
现报道如下。
1资料与方法1.1一般资料患者,男,90岁。
诊断:①慢性阻塞性肺疾病,②冠心病。
2013年10月因慢性阻塞性肺疾病收入我科。
入院后,患者咳嗽、咳痰、喘气、双下肢浮肿、夜间不能平卧。
盐酸莫西沙星氯化钠与3种注射液配伍的化学稳定性考察
氯化 钾 、 塞 米 松 注 射 液 配 伍 使 用 , 此 , 者 模 拟 临床 处 地 为 笔 方 . 察 了盐 酸莫 西沙 星氯 化钠 与 维 生素 C 氯化 钾 、 塞米 考 、 地 松间 物 的配 伍稳 定 性 . 临床 使 用 盐 酸奠 西 沙 星 氯 化钠 与 药 为 维 生 素 C、 氯 化 钾 、 地 塞 米 松 配 伍 提 供 实 验 依 据 。
称 取盐 酸 莫 西沙 星 对 照 品适 量 , 盐 酸溶 液 ( . m l ) 用 0 1 o/ L 溶 解并 稀 释至 1 gIl即得盐 酸莫 西 沙星 对照 液 。 0 ,l T, 取 盐 酸莫 西沙 星对 照溶 液 ,维生 素 C注 射液 + 化钠 注 氯 射液 .氯 化钾 注射 液+ 氯化 钠 注射 液 ,地塞 米 松磷 酸 钠注 射 液+ 氯化钠 注 射 液 , 成适 当浓度 , 配 以盐 酸溶 液 ( . mo/ ) 01 l 为 L 空 白 . 别 于 2 0 4 O n 范 围 内扫描 , 分 0 ~ O m 结果 盐 酸莫 西 沙星 在 2 4n 处有 最大 吸收 。而 氯化 钠 、 生素 C 氯化 钾 、 塞 米 9 m 维 、 地 松磷 酸钠 注射 液 在该处 无 吸收 ,故选 择 2 4n 9 m为 测定 波 长
司 ) 。 1 . 2试 药
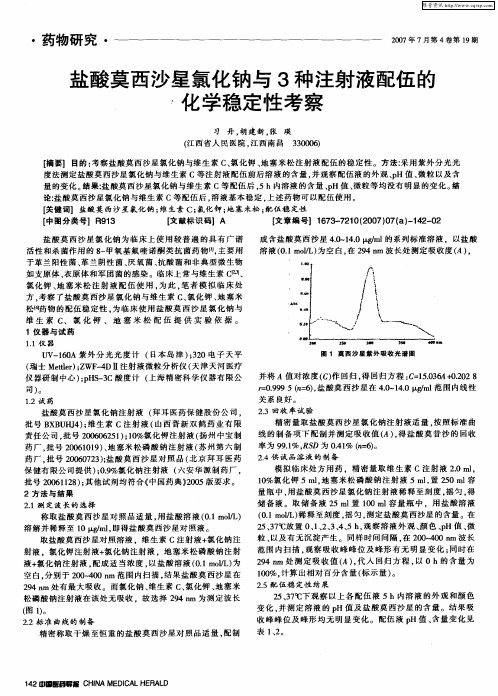
图 1 莫 西 沙 星 紫 外 吸收 光 谱 图
并 将 A值 对浓 度 ( ) 回归 , 回归 方程 := 5 3A o 0 C作 得 C 1. 6 + . 28 0 2 r09 95 = )盐 酸莫 西 沙 星在 40 1 . gm 范 围 内线性 - 9 = . 6 , .~ 40 ̄ / ]
1仪 器与 试药
23回 收 率 试 验 .
掌 ■ 瑚 嬲● 枷 ● 戚
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
盐酸莫西沙星氯化钠与3种注射液配伍的化学稳定性考察
目的:考察盐酸莫西沙星氯化钠与维生素C、氯化钾、地塞米松注射液配伍的稳定性。
方法:采用紫外分光光度法测定盐酸莫西沙星氯化钠与维生素C等注射液配伍前后溶液的含量,并观察配伍液的外观、pH值、微粒以及含量的变化。
结果:盐酸莫西沙星氯化钠与维生素C等配伍后,5 h内溶液的含量、pH值、微粒等均没有明显的变化。
结论:盐酸莫西沙星氯化钠与维生素C等配伍后,溶液基本稳定,上述药物可以配伍使用。
[关健词]盐酸莫西沙星氯化钠;维生素C;氯化钾;地塞米松;配伍稳定性
盐酸莫西沙星氯化钠为临床上使用较普遍的具有广谱活性和杀菌作用的8-甲氧基氟喹诺酮类抗菌药物[1],主要用于革兰阳性菌、革兰阴性菌、厌氧菌、抗酸菌和非典型微生物如支原体、衣原体和军团菌的感染。
临床上常与维生素C[2,3]、氯化钾、地塞米松注射液配伍使用,为此,笔者模拟临床处方,考察了盐酸莫西沙星氯化钠与维生素C、氯化钾、地塞米松[4]药物的配伍稳定性,为临床使用盐酸莫西沙星氯化钠与维生素C、氯化钾、地塞米松配伍提供实验依据。
1 仪器与试药
1.1 仪器
UV-160A紫外分光光度计(日本岛津);320电子天平(瑞士Mettler);ZWF-4D Ⅱ注射液微粒分析仪(天津天河医疗仪器研制中心);pHS-3C酸度计(上海精密科学仪器有限公司)。
1.2 试药
盐酸莫西沙星氯化钠注射液(拜耳医药保健股份公司,批号BXBUHJ4);维生素C注射液(山西晋新双鹤药业有限责任公司,批号200606251);10%氯化钾注射液(扬州中宝制药厂,批号20061019)、地塞米松磷酸钠注射液(苏州第六制药厂,批号20060723);盐酸莫西沙星对照品(北京拜耳医药保健有限公司提供);0.9%氯化钠注射液(六安华源制药厂,批号20061128);其他试剂均符合《中国药典》2005版要求。
2 方法与结果
2.1 测定波长的选择
称取盐酸莫西沙星对照品适量,用盐酸溶液(0.1 mol/L)溶解并稀释至10 μg/ml,即得盐酸莫西沙星对照液。
取盐酸莫西沙星对照溶液,维生素C注射液+氯化钠注射液,氯化钾注射液+氯化钠注射液,地塞米松磷酸钠注射液+氯化钠注射液,配成适当浓度,以盐
酸溶液(0.1 mol/L)为空白,分别于200~400 nm范围内扫描,结果盐酸莫西沙星在294 nm处有最大吸收。
而氯化钠、维生素C、氯化钾、地塞米松磷酸钠注射液在该处无吸收,故选择294 nm为测定波长(图1)。
2.2 标准曲线的制备
精密称取干燥至恒重的盐酸莫西沙星对照品适量,配制成含盐酸莫西沙星4.0~14.0 μg/ml的系列标准溶液,以盐酸溶液(0.1 mol/L)为空白,在294 nm波长处测定吸收度(A),并将A值对浓度(C)作回归,得回归方程:C=15.036A+0.202 8r=0.999 5 (n=6),盐酸莫西沙星在4.0~14.0 μg/ml范围内线性关系良好。
2.3 回收率试验
精密量取盐酸莫西沙星氯化钠注射液适量,按照标准曲线的制备项下配制并测定吸收值(A),得盐酸莫昔沙的回收率为99.1%,RSD为0.41% (n=6)。
2.4 供试品溶液的制备
模拟临床处方用药,精密量取维生素C注射液2.0 ml,10%氯化钾5 ml,地塞米松磷酸钠注射液5 ml,置250 ml容量瓶中,用盐酸莫西沙星氯化钠注射液稀释至刻度,摇匀,得储备液。
取储备液25 ml置100 ml容量瓶中,用盐酸溶液(0.1 mol/L)稀释至刻度,摇匀,测定盐酸莫西沙星的含量。
在25、37℃放置0、1、2、3、4、5 h,观察溶液外观、颜色、pH值、微粒、以及有无沉淀产生。
同样时间间隔,在200~400 nm波长范围内扫描,观察吸收峰峰位及峰形有无明显变化;同时在294 nm处测定吸收值(A),代入回归方程,以0 h的含量为100%,计算出相对百分含量(标示量)。
2.5 配伍稳定性结果
25、37℃下观察以上各配伍液5 h内溶液的外观和颜色变化,并测定溶液的pH值及盐酸莫西沙星的含量。
结果吸收峰峰位及峰形均无明显变化。
配伍液pH 值、含量变化见表1、2。
2.6 不溶性微粒的测定
测定维生素C等加入至盐酸莫西沙星氯化钠注射液后溶液的微粒变化(光阻法),结果见表3。
2.7 重现性试验
取同批样品6份,按样品测定项下所述方法测定,结果方法的重现性良好,RSD=0.43%(n=5)。
3 讨论
实验结果显示,盐酸莫西沙星与维生素C、氯化钾、地塞米松磷酸钠配伍时,在25、37℃下5 h内,溶液的稳定性随时间的变化,盐酸莫西沙星的含量有所下降,但都在合格范围内,配伍液外观、pH值以及微粒变化程度不大。
故盐酸莫西沙星与上述注射液可以配伍使用。
[参考文献]
[1]张英,赵志刚,张杰.莫西沙星——一种新的氟喹诺酮类药物[J].中国临床药理学杂志,2002,18(5):396.
[2]陈学军.培氟沙星与维生素C注射液配伍的化学稳定性考察[J].海峡药学,2003,15(2):20-21.
[3]李月红,李荣振.盐酸洛美沙星葡萄糖注射液与维生素C注射液配伍的稳定性分析[J].中国药物与临床,2004,4(7):558-559.
[4]郭英芳,肖克来提.盐洛美沙星注射液与2种药物配伍的稳定性[J].中国医院药学杂志,2000,20(1):57-58.
“本文中所涉及到的图表、注解、公式等内容请以PDF格式阅读原文”。
