化学平衡的移动条件
影响平衡的因素及移动的判断

化学平衡移动因素(1)化学平衡移动的判断当条件改变时,m生增加,表示平衡向右移动;m反增加,表示平衡向左移动。
判断原则:当υ正>υ逆,平衡向右移动;当υ正=υ逆,平衡不移动;当υ正<υ逆,平衡向左移动。
(2)外界条件对化学平衡的影响一、浓度:在其它条件不变时,增大任意反应物的浓度或减小任意生成物的浓度,平衡向正反应(右)方向移动;减小任意反应物的浓度或增大任意生成物的浓度,平衡向逆反应(左)方向移动。
注意:(1)指气体或溶液的浓度,增加固体或纯液体的量,平衡不移动。
例如在方程式2A(g)+B(s)中,增加或减少一部分B固体,平衡不移动(2)在溶液中进行的反应,如果整体稀释,反应物和生成物的浓度都减小,正逆速率都减小,但减小的程度不一样,总的结果是:整体稀释平衡向计量数增大的方向移动,整体浓缩平衡向计量数减小的方向移动,例如:例题:一定量混合气体在密闭容器中发生如下反应:xA(g)+yB(g) zC(g),达到平衡后测得A气体的浓度为0.5mol·L-1;当恒温下将密闭容器的容积扩大两倍并再次达到平衡时,测得A的浓度为0.3mol·L-1。
则下列叙述正确的是()A.平衡向右移动 B.x+y>z C.B的转化率提高 D.C的体积分数增加(3)由于增加一反应物的浓度,化学平衡向正反应方向移动,另一反应物的转化率要增大,生成物的浓度要增大。
但由于浓度增加引起平衡时反应混合物总的物质的量的增加,生成物的百分含量不一定会提高,该反应物的转化率往往会减少。
(4)浓度改变的图像t1图像1:增大某种反应物的浓度,平衡右移,υ正>υ逆,正逆速率都比原平衡增大,但在变化的瞬间由于生成物浓度不变υ逆与原平衡相等,大家在图像上可以看到υ逆的曲线与原平衡有接触点图像2:增大某种生成物的浓度,平衡左移,υ正<υ逆,正逆速率都比原平衡增大,但在变化的瞬间由于反应物浓度不变υ正与原平衡相等,大家在图像上可以看到υ正的曲线与原平衡有接触点图像3:减小某种生成物的浓度,平衡右移,υ正>υ逆,正逆速率都比原平衡减小图像4:减小某种反应物的浓度,平衡左移,υ正<υ逆,正逆速率都比原平衡减小二、压强:在其它条件不变时,增大平衡体系的压强,平衡向着气体体积缩小(分子数减小)的方向移动;减小平衡体系的压强,平衡向着气体体积增大(气体分子数增多)的方向移动。
影响化学平衡移动条件(公开课课件)PPT课件

生物体内酸碱平衡的调节也是一个化学平衡移动的过程,通过调节酸碱物质的 浓度和反应条件,维持生物体内酸碱平衡的状态。
Part
05
结论
化学平衡移动的重要性
化学平衡移动是化学反应中一个重要的概念,它影响着化学反应的速率和方向,对 于理解化学反应的本质和规律具有重要意义。
通过研究化学平衡移动,可以更好地控制化学反应的过程和结果,实现更加高效、 环保的化学工业生产。
利用化学平衡移动原理,通过控制大 气中的污染物浓度和反应条件,实现 大气污染物的转化和去除。
水处理
在水处理过程中,利用化学平衡移动 原理,将水中的有害物质转化为无害 物质,达到净化水质的目的。
生物体内的化学平衡移动
代谢平衡
生物体内的代谢过程是一个动态平衡的过程,通过化学平衡移动原理,维持生 物体内各种物质的平衡和稳定。
压力对化学平衡的影响
总结词
压力是影响化学平衡移动的另一 个重要因素。
详细描述
压力的变化会影响气体的分压, 进而影响化学平衡。增加压力, 平衡会向气体分子数少的方向移 动;减小压力,平衡会向气体分
子数多的方向移动。
实例
在反应2H2(g) + O2(g) → 2H2O(g)中,增加压力,平衡会
向生成H2O的方向移动。
随着计算能力的提升,未来可以通过 计算机模拟和计算来预测化学平衡移 动,为化学反应的设计和优化提供更 加科学和可靠的依据。
THANKS
感谢您的观看
催化剂对化学平衡的影响
总结词
催化剂虽然可以加快化学反应速 率,但对化学平衡的移动没有影
响。
详细描述
催化剂可以降低反应的活化能,从 而加快反应速率,但对化学平衡的 常数没有影响,因此不影响化学平 衡的移动。
影响化学平衡的条件及vt图
Chem is try!
例3: 反应 2NO2(g)
N2O4(g)
达平衡后增大压强,平衡如何移动?
【分析】P变化-﹥体积变化-﹥浓度变化 (气体系数之和大的方向,浓度变化更大,即速率变化更大!)
v
V正
V正 ′ V逆′
V逆
t
Chem is try!
对于反应前后气体总体积相等的反应,改变
压强对平衡无影响;
滴加NaOH溶液
增加C(反应物) 向正方向移动 滴加NaOH溶液
现象
改变因素 移动方向
产生红褐色沉淀,溶液红色变浅
减小C(反应物) 向逆方向移动
图像分析: •增加反应物的浓度, V正 瞬间增大, 而V逆不变,V正 > V逆
平衡向正反应方向移动,直到
速率-时间关系图:V”正 = V ”逆,最后建立新的化学平衡。
例:对如下平衡
A(气) + B (气)
2C (气) + D (固)
V正
V正’= V逆’ V正
V逆 0
t1 t2 t3
加压对化学平衡的影响
V正’ = V逆’
V逆 0
t1 t2 t3
减压对化学平衡的影响
Chem is try!
[注意] ①对于反应前后气体总体积相等的反应,改
变压强对平衡无影响;
增大压强,体积 减小,浓度同等程 度增大,颜色变深, 但平衡不移动.
实验目的:探究浓度变化对化学平衡的影响
实验原理:Cr2O72-+H2O
橙色
实验结果及现象:
步骤
滴加3-10滴浓H2SO4
2CrO42-+2H+
黄色
滴加10-20滴 6mol/LNaOH
第九讲-影响化学平衡移动的条件

练习4
•对于2A(g)+B(g) C(g)+3D(g)(正反应吸热)有 如下图所示的变化,图中Y轴可能表示: A、B物质的转化率 Y B、正反应的速率 C、平衡体系中的A% 300℃ D、平衡体系中的C%
200℃ 100℃
P
A、D
课堂练习
5.已建立化学平衡的某可逆反应,当改变条件 使化学平衡向正反应方向移动时,下列有关 叙述正确的是 B • ① 生成物的百分含量一定增加② 生成物的产 量一定增加③ 反应物的转化率一定增大④ 反 应物浓度一定降低⑤ 正反应速率一定大于逆 反应速率⑥ 使用了合适的催化剂 • A ① ② (B) ② ⑤ (C) ③ ⑤ (D) ④ ⑥
即:平衡移动的结果是减弱改变而不是抵消改变。
5、催化剂对化学平衡的影响 讨论:催化剂怎样改变v正和 v逆? 小结:同步、等倍数改变v正和 v逆
v
含量
v’正= v’逆
v正 = v逆
t t t1 t2
结论:催化剂不能使化学平衡发生移动; 不能改变反应混合物含量;但可以改变达 到平衡的时间
练习1
(2004年广东18).右下图曲线a表示 放热反应X(g)+Y(g) Z(g)+M(g)+N(s) 进行过程中X的转化率随时间变化的关 系。若要改变起始条件,使反应过程按 b曲线进行,可采取的措施是(C,D ) A.升高温度 B.加大X的投入量 C.加催化剂 D.减小体积
说明:
⑴、此原理只适用于已达平衡的体系 ⑵、平衡移动方向与条件改变方向相反,例如: 增大浓度,平衡移向减小这种浓度的方向;增大 压强,向减小压强方向移动。 ⑶、“减弱”的含义:平衡移动后结果变化的方 向不变,但程度减小。例如,增加反应物浓度平 衡移动后该反应物浓度仍增加,只是增加的程度 比没有平衡移动时要小。
高中化学平衡移动的超全知识点总结
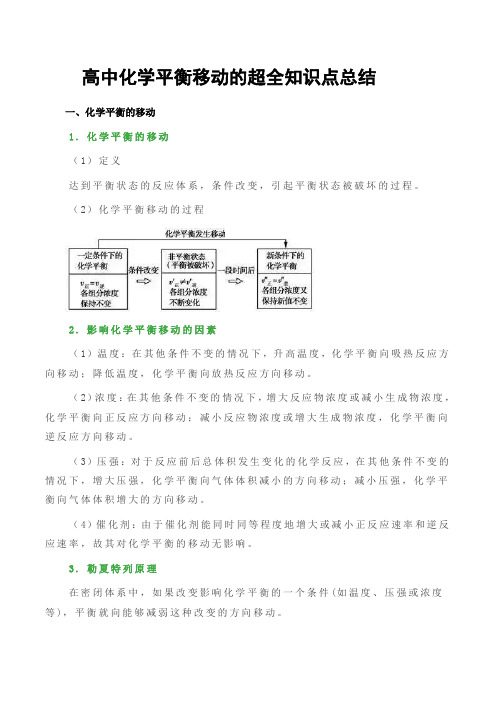
高中化学平衡移动的超全知识点总结一、化学平衡的移动1.化学平衡的移动(1)定义达到平衡状态的反应体系,条件改变,引起平衡状态被破坏的过程。
(2)化学平衡移动的过程2.影响化学平衡移动的因素(1)温度:在其他条件不变的情况下,升高温度,化学平衡向吸热反应方向移动;降低温度,化学平衡向放热反应方向移动。
(2)浓度:在其他条件不变的情况下,增大反应物浓度或减小生成物浓度,化学平衡向正反应方向移动;减小反应物浓度或增大生成物浓度,化学平衡向逆反应方向移动。
(3)压强:对于反应前后总体积发生变化的化学反应,在其他条件不变的情况下,增大压强,化学平衡向气体体积减小的方向移动;减小压强,化学平衡向气体体积增大的方向移动。
(4)催化剂:由于催化剂能同时同等程度地增大或减小正反应速率和逆反应速率,故其对化学平衡的移动无影响。
3.勒夏特列原理在密闭体系中,如果改变影响化学平衡的一个条件(如温度、压强或浓度等),平衡就向能够减弱这种改变的方向移动。
对于反应mA(g)+nB(g)pC(g)+qD(g),分析如下:2.浓度、压强和温度对平衡移动影响的几种特殊情况(1)改变固体或纯液体的量,对平衡无影响。
(2)当反应混合物中不存在气态物质时,压强的改变对平衡无影响。
(3)对于反应前后气体体积无变化的反应,如H2(g)+I2(g)2HI(g),压强的改变对平衡无影响。
但增大(或减小)压强会使各物质的浓度增大(或减小),混合气体的颜色变深(或浅)。
(4)恒容时,同等程度地改变反应混合物中各物质的浓度时,应视为压强的影响,增大(减小)浓度相当于增大(减小)压强。
(5)在恒容容器中,当改变其中一种气态物质的浓度时,必然会引起压强的改变,在判断平衡移动的方向和物质的转化率、体积分数变化时,应灵活分析浓度和压强对化学平衡的影响。
若用α表示物质的转化率,φ表示气体的体积分数,则:①对于A(g)+B(g)C(g)类反应,达到平衡后,保持温度、容积不变,加入一定量的A,则平衡向正反应方向移动,α(B)增大而α(A)减小,φ(B)减小而φ(A)增大。
高三化学 平衡移动 化学平衡的移动
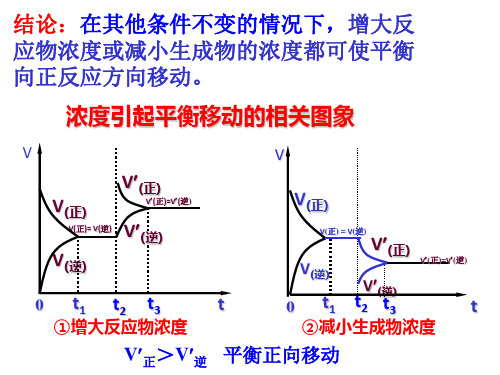
①此原理只适用于已达平衡的可逆反应 ②平衡移动方向与条件改变方向相反。 ③移动的结果只能是减弱外界条件的该 变量,但不能抵消。
练习1:反应 2 A(g) 2B(g) + C(g) △H >0 达平衡时,要使V正降低,A的浓度增大,应采取
的措施是( C )
A. 加压
B. 减压
C. 降温
D. 增大C的浓度
能否引起平衡移动?(① ③ )
①增大水蒸气浓度
②加入更多的碳
③增加H2浓度 改变条件后能使CO浓度有何变化?
强调:气体或溶液浓度的改变会引起反应速
率的变化,纯固体或纯液体用量的变化不会
引起反应速率改变,化学平衡不移动
压强对化学平衡的影响:
(1)结论
aA (g) + bB(g)
当 a+b=c+d
cC(g) + dD(g)
(2)若X为气体,增大压强,X的物质的量不变,则可知
Y是_气___体___, Z是__固__体___或液体
4、在密闭容器中进行下列反应
CO2(g)+C(s)
2CO(g)
达平衡后,改变条件,指定物的浓度及平衡如何变化:
(1)减小密闭容器体积,保持温度不变,则平
衡 逆向移动; c(CO2)
增大。
(2温)
Ⅰ、恒温恒容下,充入与反应无关的气体,气体的浓度保 持恒定,正逆反应速率不变,故平衡不移动。
Ⅱ、恒温恒压下,充入与反应无关的气体。平衡混合气体 的浓度减小,正逆反应速率均减小,故相当于减小压强。
2.恒温下, 反应aX(g) bY(g) + cZ(g),达到平 衡后, 把容器体积压缩到原来的一半且达到新
V逆
化学平衡移动规律总结

化学平衡移动规律总结化学反应是物质转化的过程,而化学平衡则是在反应物和生成物浓度达到一定比例时的状态。
化学平衡的移动规律是指在一定条件下,平衡位置如何随着外界条件的改变而发生变化的规律。
下面将从温度、压力、浓度和催化剂四个方面来总结化学平衡的移动规律。
一、温度影响在化学反应中,温度的改变会影响反应物和生成物的速率以及平衡位置。
根据Le Chatelier定律,当温度升高时,反应速率会增加。
对于吸热反应,升高温度会使平衡位置向右移动,生成物浓度增加;而对于放热反应,升高温度会使平衡位置向左移动,生成物浓度减少。
二、压力影响在气相反应中,压力的改变对平衡位置有一定影响。
根据Le Chatelier定律,当压力增加时,平衡位置会向反应物浓度较小的一侧移动,以减少压力。
对于反应物和生成物摩尔数相等的反应,压力的改变不会影响平衡位置。
而对于摩尔数不相等的反应,压力的增加会使平衡位置向摩尔数较小的一侧移动。
三、浓度影响在溶液中的反应中,溶液浓度的改变会导致平衡位置的移动。
根据Le Chatelier定律,当浓度增加时,平衡位置会向生成物浓度较小的一侧移动,以减少浓度差。
而当浓度减少时,平衡位置会向生成物浓度较大的一侧移动,以增加浓度差。
四、催化剂影响催化剂可以加速化学反应的速率,但不参与反应。
催化剂的加入不会改变平衡位置,因为它同样影响反应物和生成物的速率。
催化剂提供了一个更低的活化能路径,使反应更容易进行,但并不改变反应的平衡位置。
化学平衡的移动规律可以通过调节温度、压力和浓度来实现。
根据Le Chatelier定律,当这些条件发生改变时,平衡位置会向着减少影响的一侧移动,以达到新的平衡状态。
催化剂的加入可以提高反应速率,但不会改变平衡位置。
这些规律的理解和应用对于理解和控制化学反应过程具有重要意义。
化学平衡的移动,化学反应进行的方向

【重点内容】化学平衡的移动,化学反应进行的方向。
2【内容讲解】一、化学平衡的移动1、含义:可逆反应达到平衡状态后,反应条件(如浓度、压强、温度)改变,使正和逆不再相等,原平衡被破坏;一段时间后,在新的条件下,正、逆反应速率又重新相等,即V正'=V逆',此时达到了新的平衡状态,称为化学平衡的移动。
应注意:v正'≠v正,v逆'≠v逆。
2、影响因素:(1)浓度:其它条件不变时,增大反应物浓度或减小生成物浓度,平衡向正反应方向移动;增大生成物浓度或减小反应物浓度,平衡向逆反应方向移动。
在下列反应速率(v)对时间(t)的关系图象中,在t1时刻发生下述相应条件的变化,则正、逆反应速率的改变情况如图所示:①增大反应物浓度;②减小生成物浓度;③增大生成物浓度;④减小反应物浓度注:①由于纯固体或纯液体的浓度为常数,所以改变纯固体或纯液体的量,不影响化学反应速率,因此平衡不发生移动。
②增大(或减小)一种反应物A的浓度,可以使另一种反应物B的转化率增大(或减小),而反应物A的转化率减小(或增大)。
(2)压强:其它条件不变时,对于有气体参加的可逆反应,且反应前后气体分子数即气体体积数不相等,则当缩小体积以增大平衡混合物的压强时,平衡向气体体积数减小的方向移动;反之当增大体积来减小平衡混合物的压强时,平衡向气体体积数增大的方向移动;若反应前后气体分子数即气体体积数相等的可逆反应,达到平衡后改变压强,则平衡不移动。
对于反应mA(g)+nB(g)pC(g)+qD(g),在下列v-t图中,在t1时刻发生下述相应条件的变化,则正、逆反应速率的改变情况如图所示:①m +n >p +q,增大压强;②m +n >p +q,减小压强;③m +n <p +q,增大压强;④m +n <p +q,减小压强;⑤m +n =p +q,增大压强;⑥m +n =p +q,减小压强。
(3)温度:其它条件不变时,升高温度,平衡向吸热反应(△H>0)方向移动;降低温度,平衡向放热反应(△H<0)方向移动。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学平衡的移动条件
化学平衡是指当反应物和生成物在一定条件下达到动态平衡状态时,它们的浓度、压力或其他相关物态参数不再发生变化。
为了使化学反
应达到平衡状态,可以通过改变温度、压力、浓度和添加催化剂等手
段来移动平衡。
本文将讨论影响化学平衡移动的条件以及它们的作用
机理。
一、温度的影响
温度是影响化学平衡移动的重要因素之一。
根据利奥·香特列定律,当温度发生变化时,平衡反应的正向和逆向反应速率都会发生变化。
对于吸热反应(放热反应),升高温度会使平衡转向生成物一侧,而
降低温度则会偏向反应物一侧。
对于放热反应(吸热反应),情况相反。
以氨的合成反应为例:
N2(g) + 3H2(g) ⇌ 2NH3(g) + 92.4 kJ
该反应是一个放热反应,因此当温度升高时,反应向生成物一侧移动,生成氨的产率增加。
而当温度降低时,反应向反应物一侧移动,
生成氨的产率减少。
二、压力的影响
压力是影响化学平衡移动的另一个关键因素。
对于气体反应,改变
压力会对平衡产生影响。
根据洪特定律,当体积不变的情况下,提高
压力会使平衡转向摩尔数较少的一侧,而减小压力则会偏向摩尔数较
多的一侧。
以二氧化碳和一氧化碳反应生成一氧化碳和氧化碳的平衡反应为例:CO2(g) + CO(g) ⇌ 2CO(g)
该反应为气体反应,增加压力会使平衡向CO2和CO的生成物一侧
移动,生成CO的产率增加。
减小压力则会偏向反应物一侧,生成CO
的产率减少。
三、浓度的影响
浓度也是影响化学平衡移动的重要因素之一。
对于溶液反应,改变
物质的浓度会对平衡产生影响。
根据一般来说,增加浓度会使平衡转
向生成物一侧,而降低浓度则会偏向反应物一侧。
以还原铁离子为例:
Fe3+(aq) + SCN-(aq) ⇌ Fe(SCN)2+(aq)
该反应为溶液反应,增加铁离子或硫氰离子的浓度会使平衡向生成
配合物Fe(SCN)2+的一侧移动,生成铁离子配合物的产率增加。
减小
浓度则会偏向反应物一侧,生成铁离子配合物的产率减少。
四、催化剂的影响
催化剂是一种能够提高反应速率但不被反应消耗的物质。
它可以降
低反应物的活化能,从而加快反应达到平衡的速度。
催化剂对平衡位
置没有直接的影响,但可以使系统更快地达到平衡。
以硫酸铁为催化剂的硫酸与乙醇的酯化反应为例:
H2SO4 + C2H5OH ⇌ C2H5HSO4 + H2O
该反应需要硫酸作为催化剂,催化剂的存在可以加速反应速率,使系统更快达到平衡。
催化剂不改变平衡位置,只是加快反应的正向和逆向速率,使达到平衡的时间缩短。
综上所述,温度、压力、浓度和催化剂是影响化学平衡移动的关键条件。
通过控制这些条件的变化,可以调节化学平衡位置,实现对反应产物的控制。
在实际应用中,了解和掌握这些条件对于合理设计和优化化学反应过程具有重要意义。
