常见原子团符号
元素名称和符号
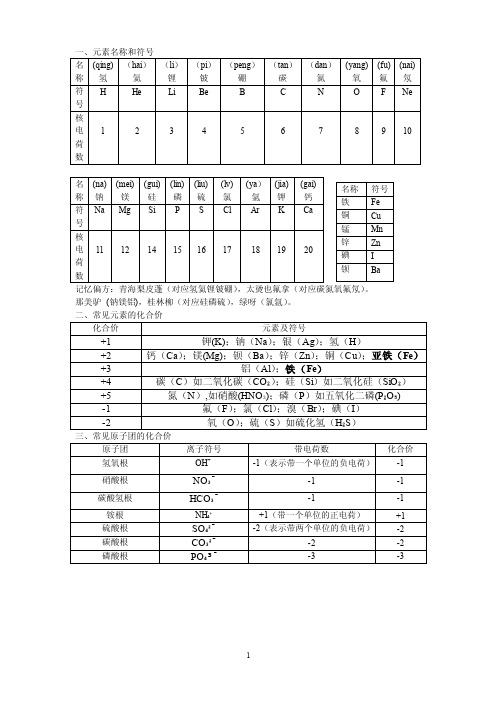
记忆偏方:青海梨皮蓬(对应氢氦锂铍硼),太烫也氟拿(对应碳氮氧氟氖)。
那美驴 (钠镁铝),桂林柳(对应硅磷硫),绿呀(氯氩)。
二、常见元素的化合价四、常见物质的名称和化学式(化学式可以表示物质的一个分子。
如化学式O₂也可表示为一个氧气分子;H₂O可表示为一个水分子)1、单质:金属单质、非金属固态单质(除碘外)、稀有气体的化学式由元素符号表示氧气O₂臭氧O₃氢气H₂氮气N₂氟气F₂溴水Br₂氯气Cl₂碘I₂磷P 硫磺S 碳C 铁Fe 镁Mg 铜Cu 铝Al 汞Hg 2、化合物氧化镁MgO 氧化铜CuO 四氧化三铁Fe₃O₄氧化铝Al₂O₃二氧化锰MnO₂氧化铁Fe₂O₃氧化汞HgO 氧化钙CaO 氧化锌ZnO 氧化钠Na₂O二氧化碳CO₂水H₂O 一氧化氮NO 二氧化氮NO₂三氧化硫SO₃一氧化碳CO 二氧化硫SO₂五氧化二磷P₂O₅双氧水H₂O₂盐酸HCl 硫酸H₂SO₄硝酸HNO₃碳酸H₂CO₃氢氧化钠NaOH 氢氧化钾KOH 氢氧化钡Ba(OH)₂氢氧化钙Ca(OH)₂氢氧化铝Al(OH)₃氢氧化铁Fe(OH)₃氢氧化亚铁Fe(OH)₂氢氧化锌Zn(OH)₂氢氧化铜Cu(OH)₂氢氧化镁Mg(OH)₂3、盐(由金属负离子和酸根离子组成的化合物)①钾盐:(金属离子为钾离子的盐)氯酸钾KClO₃;高锰酸钾KMnO₄;氯化钾KCl;硝酸钾KNO₃;硫酸钾K₂SO₄;碳酸钾K₂CO₃;磷酸钾K₃PO₄;硫化钾K₂S②钠盐(金属离子为钠离子的盐)氯化钠NaCl;硫酸钠Na₂SO₄;硝酸钠NaNO₃;碳酸钠Na₂CO₃; 硫化钠Na₂S; 碳酸氢钠NaOH;③银盐(金属离子为银离子的盐)氯化银AgCl;硝酸银AgNO₃;④铵盐(阳离子为铵根离子的盐)氯化铵NH₄Cl;硫酸铵(NH₄)₂SO₄;硝酸铵NH₄NO₃;碳酸铵(NH₄)₂CO₃;⑤钙盐(金属离子为钙离子的盐)氯化钙CaCl₂;硫酸钙CaSO₄;硝酸钙Ca(NO₃)₂;碳酸钙CaCO₃;磷酸钙Ca₃(PO₄)₂⑥锌盐(金属离子为锌离子的盐)氯化锌ZnCl₂;硫酸锌ZnSO₄;硝酸锌Zn(NO₃)₂碳酸锌ZnCO₃;⑦镁盐(金属离子为镁离子的盐)氯化镁MgCl₂;硫酸镁MgSO₄;硝酸镁Mg(NO₃)₂;碳酸镁MgCO₃;⑧钡盐(金属离子为钡离子的盐)氯化钡BaCl₂;硫酸钡BaSO₄;硝酸钡Ba(NO₃)₂;碳酸钡BaCO₃;⑨铜盐(金属离子为铜离子的盐)氯化铜CuCl₂;硫酸铜CuSO₄;硝酸铜Cu(NO₃)₂;碳酸铜CuCO₃⑩亚铁盐(金属离子为亚铁离子的盐)硫化亚铁FeCl₂;硫酸亚铁FeSO₄;硝酸亚铁Fe(NO₃)₂⑪铁盐(金属离子为铁离子的盐)氯化铁FeCl₃;硫酸铁Fe₂(SO₄)₃;硝酸铁Fe(NO₃)₃⑫铝盐(金属离子为铝离子的盐)氯化铝AlCl₃;硫酸铝Al₂(SO₄)₃;硝酸铝Al(NO₃)₃文案编辑词条B 添加义项?文案,原指放书的桌子,后来指在桌子上写字的人。
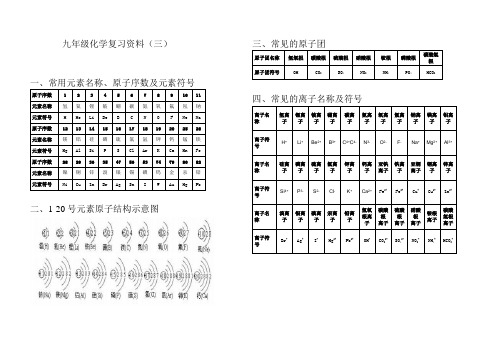
原子符号原子团
锂离子
铍离子
硼离子
碳离子
氮离子
氧离子
氟离子
钠离子
镁离子
铝离子
离子符号
H+
Li+
Be2+
B3+
C4+C4-
N3-
O2-
F-
Na+
Mg2+
Al3+
离子名称
硅离子
磷离子
硫离子
氯离子
钾离子
钙离子
亚铁离子
铁离子
亚铜离子
铜离子
锌离子
离子符号
Si4+
P3-
S2-
Cl-
K+
Ca2+
Fe2+
Fe3+
Cu+
Cu2+
28
29
30
35
47
50
74
79
80
82
元素名称
镍
铜
锌
溴
银
锡
碘
钨
金
汞
铅
元素符号
Ni
Cu
Zn
Br
Ag
Sn
I
W
Au
Hg
Pb
二、1-20号元素原子结构示意图
三、常见的原子团
原子团名称
氢氧根
碳酸根
硫酸根
硝酸根
铵根
磷酸根
碳酸氢根
原子团符号
OH
CO3
SO4
NO3
NH4
PO4
HCO3
四、常见的离子名称及符号
离子名称
Zn2+
离子名称
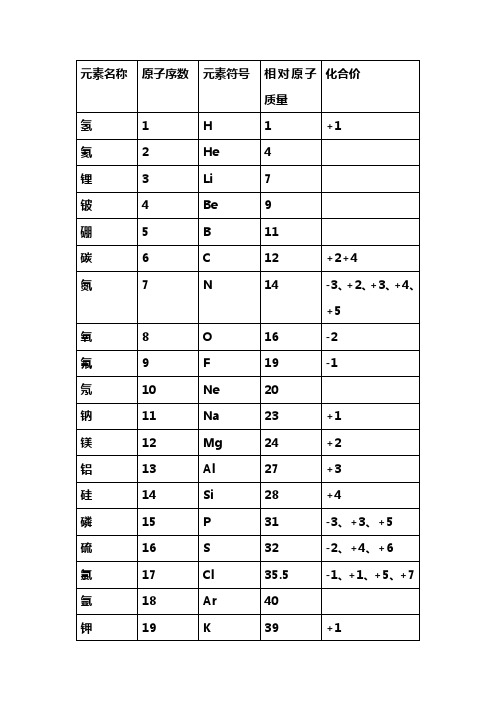
27种常见元素符号、原子质量和化合价一览表

+1
原子团化合价
原子团名称
原子团符号
原子团化合价
氢氧根
OH
-1
磷酸根
PO4
-3
氯酸根
ClO3
-1
硫酸根
SO4
-2
磷酸二氢根
H2PO4
-1
高锰酸根
MnO4
-1
碳酸根
CO3
-2
碳酸氢根
HCO3
-1
磷酸氢根
HPO4
-2
硝酸根
NO3
-1
磷酸根
PO4
-3
醋酸根
CH3COO
-1
亚硫酸根
SO3
-2
锰酸根
MnO4
-2
铵根
27种常见元素名称符号和相对原子质量一览表
名称
符号
相对原子质量
化合价
名称
符号
相对原子质量
化合价
名称
符号
相对原子质量
化合价
氢
H
1
+1
钠
Na
23
+1
锰
Mn
55
氦
He
4
镁
Mg
24
+2
鉄
Fe
56
+2 +3
铝
Al
27
+3
铜
Cu
63.5
+2 -1
碳
C
12
+2 +4
硅
Si
28
+4
锌
Zn
65
+2
氮
N
14
-3 +2 +4 +5
常见元素符号和原子团的化合价

初中化学常见元素符号H(氢)、He(氦)、Li(锂)、Be(铍)、B(硼)。
C(碳)、N(氮)、O(氧)、F(氟)、Ne(氖)。
Na(钠)、Mg(镁)、Al(铝)、Si(硅)、P(磷)。
S(硫)、Cl(氯)、Ar(氩)、K(钾)、Ca(钙)。
Mn(锰)、Fe (铁)、Cu(铜)、Zn(锌)、Br(溴)。
Ag(银)、I(碘)、Ba(钡)、Au(金)、Hg(汞).(写法:由一个字母组成的大写,由两个字母组成的第一个字母大写,第二个字母小写。
)常见元素和原子团的化合价:一价氢(H)氯(Cl)钾(K)钠(Na)银(Ag);二价钙(Ca)镁(Mg)钡(Ba)和锌(Zn);二、四、六、硫(S)二、四碳(C);三铝(Al)四硅(Si)五氮(N)磷(P);铁(Fe)有二、三要分清;莫忘单质都是零;负一硝酸(NO3-)氢氧(OH-)根;负二硫酸(SO42-)碳酸(CO32-)根;负三记住磷酸根(PO43-);正一价的是铵根(NH4+);要正确书写物质的化学式:一、要熟练记忆元素符号,二、书写化合物的化学式时,要熟练记忆常见元素和原子团的化合价,三、书写化合物的化学式要符合各元素正负化合价的代数和为零的原则,四、掌握书写化学式的一般方法化学式的一般写法是:(1)、单质的化学式除H2、O2、N2、F2、Cl2、Br2和I2七种单质为双原子分子外,其余单质(惰性气体、金属单质和固态非金属单质等)都是以元素符号表示其化学式。
(2)、化合物的化学式书写时一般规律是先读后写,后读先写;排好顺序,写好角号。
一般将显正价的元素或原子团写在左边,显负价的元素或原子团写在右边。
书写化学式的步骤:(1)定位:确定元素或原子团的顺序。
(2)标价:正确地在各元素或原子团的上方标出化合价。
(3)交叉约简:将化合价的绝对值交叉写在对方元素或原子团的右下方,能约简的要约为最简约数。
原子或原子团的个数为1时,通常1省去不写。
原子团在2个或2个以上时,应加上括号。
元素符号、化合价顺口溜及原子团符号

硅酸根SiO3 亚硫酸根SO3 锰酸根MnO4
磷酸根PO4
硅酸根离子SiO32- 亚硫酸根离子ቤተ መጻሕፍቲ ባይዱO32- 锰酸根离子MnO42-
磷酸根离子PO43-
化 化合价顺口溜 合 单 物 +1氢 钾钠银,另有+1是铵根; 质 氢氧根 价-1,还有氯酸根、硝酸根; 中 正 中 +2价 钡镁锌,钙是+2记在心; 负 氧是- 2 少不了,另有碳酸根,硫酸根; 元 化 加上硅酸根,亚硫酸根; 素 合 +3价的铝和金,-3价的磷酸根; 化 价 硅+4 钨+6, 变价元素不能丢; 合 总 价 +1、+2铜和汞,+2、+3铁元素; 代 -3、+3、+5磷, +2,+4碳和锡; 数 为 氯化物中氯-1,余选+1、+5、+7; 和 零 硫化物中硫-2, 余选+4和+6; 为 锰的变价也不少,+2,+4,+6,+7。 零
原子团名称及符号 铵根NH4 氢氧根OH 硝酸根NO3 氯酸根ClO3 碳酸氢根HCO3 高锰酸根MnO4 硫酸根SO4 碳酸根CO3
离子名称及符号 铵根离子NH4+ 氢氧根离子OH- 硝酸根离子NO3- 氯酸根离子ClO3- 碳酸氢根离子HCO3- 高锰酸根离子MnO4- 硫酸根离子SO42- 碳酸根离子CO32-
离子化合物

4、离子化合物常用命名方法:
①两种元素组成时,由后向前读作:×化× ②含氢氧根离子时,由后向前读作:氢氧化× ③含酸根离子时,由后向前读作: × 酸×
试写出下列符号的名称: ①K2O ②Ba(OH)2 ③CaF2 ④NH4NO3 ⑤Fe2(SO4)3 ⑥Na3PO4 ⑦CuSO4 ⑧BaCO3
三、元素、分子、原子、离子 与物质之间的关系
10.请写出符合要求的10个电子的微粒: 原子 ; 分子 ; 阳离子 ; 阴离子 ;
5、对于Mg、Mg2+两种粒子的判断正确的是 ①核电荷数相同②核外电子数相同③电子层 结构完全相同④相对原子质量几乎相同⑤属 于同种元素 A、①②⑤ B、②③⑤ C、③④⑤ D、①④⑤ 6、(南充市)用化学用语填空: (1)2个铵根离子 ; (2)硫酸根离子 (3)写出氯化铁的化学式 ; ;
7、已知X 、Y 、Z 、Q 均与Ar的核外电 子排布相同,且n<m,p>a,则下列说法正 确的是 A、m+n=p+a B、m+a=p+n C、Y的原子序数比X的大 D、Z的原子核外的电子数比Q的多 8.参考下列物质的微观结构图示,其中由阴, 阳离子构成的物质是
-
ClO33PO4
高锰酸根离子 MnO4-
锰酸根离子 MnO42- 亚硫酸根离子
SO3
2-
磷酸根离子
铵根离子
NH4+
5、离子符号表达的含义:
①表示一种离子 ②表示一个离子带有多少个单位的电荷 ③当符号前有具体的数字时只表示离子个数 写出下列离子符号表达的含义: ①Ca2+ ①表示钙离子 ②表示一个钙离子带两个单位的正电荷
2-
②2S
③表示两个硫离子
二、离子化合物 阴阳离子通过静电作用结 1、概念: 合而成的化合物
初中常见元素,原子团名称,化学式,化合价
35
Br
80
-1
氢氧根
OH
-1
硝酸根
NO3
-1
高锰酸根
MnO4
-1
氯酸根
ClO3
-1
硫酸根
SO4
-2
碳酸根
CO3
-2
铵根
NH4
+1
初中化学常见的原子团(根)及其化合价
根的名称
根的符号
常见化合价
常见化合物举例
铵根
NH4
+1
NH4Cl
硝酸根
NO3
-1
KNO3
氢氧根
OH
-1
NaOH
高锰酸根
MnO4
-1
KMnO4
32
-2、+4、+6
氯
17
Cl
35.5
-1、+1、+5、+7
氩
18
Ar
40
钾
19
K
39
+1
钙
20
Ca
40
+2
锰
25
Mn
55
+2、+4、+6、+7
铁
26
Fe
56
+2、+3
铜
29
Cu
63.5
+1、+2
锌
30
Zn
65
银
47
Ag
108
钡
56
Ba
137
铂
78
Pt
195
金
79
Au
197
汞
80
Hg
原子团化合价口诀及符号

原子团化合价口诀及符号咱们上学的时候,化学这门课里有个挺重要的知识点,就是原子团化合价。
这玩意儿要是弄不明白,那化学题可就难做喽!今天咱就好好聊聊原子团化合价的口诀还有符号。
先来说说原子团化合价口诀吧,“一价氢氯钾钠银,二价氧钙钡镁锌,三铝四硅五价磷,二三铁,二四碳,二四六硫都齐全,铜汞二价最常见。
单质零价永不变。
负一硝酸氢氧根,负二硫酸碳酸根,负三记住磷酸根,正一价的是铵根。
”这口诀是不是有点像绕口令?但你多念几遍,那效果可是杠杠的!我还记得我当年教学生的时候,有个小同学,叫明明。
这孩子啊,脑袋瓜挺灵,就是对这原子团化合价有点犯迷糊。
有一次做作业,明明错得那叫一个惨不忍睹。
我就把他叫到办公室,打算好好给他补补课。
我问明明:“孩子,这氢氧根化合价是多少来着?”明明眨巴着大眼睛,一脸迷茫地说:“老师,我好像给忘了。
”我又耐心地给他重复了一遍口诀,让他跟着我念。
然后我再问他:“这回记住没?”明明有点不太确定地点点头。
我拿出一道题,让他试着做做。
结果呢,这孩子还是做错了。
我这心里呀,又着急又无奈。
但还是耐着性子给他讲解:“明明啊,你看这个式子,氢氧根是负一价,这里有两个氢氧根,那化合价总共是多少呀?”明明皱着眉头想了半天,终于恍然大悟:“老师,我知道啦,是负二价!”从那以后,明明可下功夫了,天天嘴里都念叨着这口诀。
过了段时间,再做这类题的时候,明明做得又快又准。
咱们再来说说这原子团化合价的符号。
像硝酸根是 NO₃⁻,硫酸根是 SO₄²⁻,碳酸根是 CO₃²⁻,磷酸根是 PO₄³⁻,铵根是 NH₄⁺。
这些符号可都得记清楚了,不然写化学方程式的时候,一准出错。
比如说在写硫酸铜的化学式时,如果不知道硫酸根是 SO₄²⁻,铜是二价的 Cu²⁺,那可就没法写出正确的 CuSO₄啦。
学习原子团化合价这部分知识,得多做题,多练习。
就像明明那样,一开始迷糊没关系,只要肯下功夫,肯定能掌握好。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
常见原子团符号
原子团符号是一种使用一个简单的符号来表示原子、分子或其他物质的一种表示方法。
这有助于我们快速识别并记忆物质的名称,也有助于更好地理解化学反应,以及研究它们之间的关系。
原子团符号可以简便地表示原子的结构、元素之间的构成关系,甚至是化学反应式。
在原子团符号中,常见的符号主要有4类:
1.子分子符号:这一类符号是用来表示元素原子或分子的,例如氢原子符号H,水分子符号H2O。
一般情况下,元素原子符号都是它
们在元素周期表中的符号,分子符号则是原子符号前面加上分子中原子个数的数字。
2.子团符号:这类符号也是常见的,它们表示的是元素的一种化合物,例如氯离子的符号Cl-,氧化物的符号O2-。
这样的符号一般
也会有一个负号,用来表示它们的电荷数。
3.学式:一种用简单的符号表示原子、分子或其他物质的相互作用的方法。
这样的式子有助于理解化学反应本身,例如二氧化碳与氢气反应的反应式CO2 + 2H2 -> 2H2O。
4.他类型:用简单符号表示化学反应中复杂的过程,以便更容易理解,例如酸催化反应符号H+,离子水平符号[H+]等。
上面所说的几类符号,在日常的学习中可以说是一种必学的内容,无论是用来记忆化学基本知识,还是用于理解化学反应式,都是必不可少的。
还有,认识原子团符号也有助于在实验中进行识别,比如发
现一种元素,能够通过它的原子团符号迅速判断它是什么元素,从而有效地完成实验。
总而言之,原子团符号对化学知识的学习与研究有着重要的作用,准确、快速地认识和使用原子团符号,是有效学习化学知识的重要技能。
除了上述常见的原子团符号,在化学教学中可以学到更多的原子团符号,比如有机物的分子式,以及无机化合物中的氧化物、碱、盐等等,所以我们应该努力学习它们,使自己对化学更加熟悉。
