2.5 聚合反应动力学
聚合反应动力学
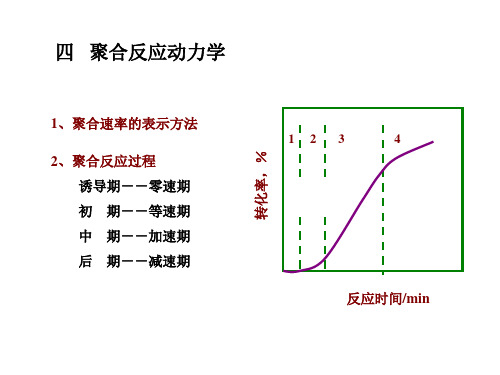
5、 聚合后期反应速率 、 6、 聚合类型 、
b
转化率 / %
各阶段总速率 = 正常聚合速率+加速反应贡献速率
c a
a. S型 b. 匀速聚合型 c. 前快后慢型
→ → →
低活性引发剂 中活性引发剂 高活性引发剂
时间 / min
相对分子质量(聚合度) 五 相对分子质量(聚合度)
思考: 思考:影响聚合度大小的主要因素
k
Rtr , x = ktr , x [M ⋅][ I ]
Rtr , s = ktr , s [ M ⋅][S ]
tr , s Mn • + S − X → MnX + S •
k
3、有链转移时的聚合度 、
Xn =
Rp − d [ M ] / dt − d [ M ] / dt = = d [ P ] / dt d [ P ]t / dt + d [ P ]tr / dt Rtc + R + ∑ R td tr 2
链增长
R M. + n M k
p i
双基终止
Mx x
.
+
M x
y
.
k k
tc td
Vtc = 2 k Vtd = 2 k
tc td
[M. ]
2
.] 2 [M
(2)聚合反应总速率 )
R p = - d [ M ]/ d t = V i2
+
( Vp1
+
Vp2
+
......
+
Vpn )
假设一: 假设一:自由基等活性
4、各种链转移反应 、
(1)向单体的链转移 ) 两条规律:自由基的活性起决定作用;活泼单体的自由基不活 泼而不易发生转移。不活泼单体的自由基活泼而容易发生转移。 典型例子:PVC (2)向引发剂的链转移 ) 偶氮类引发剂无转移,过氧类引发剂有诱导分解 (3)向溶剂的链转移 )
聚合物动力学及弛豫行为

聚合物动力学及弛豫行为聚合物是由许多重复单元组成的大分子,具有广泛的应用领域,包括材料科学、生物医学、能源等。
聚合物的动力学及弛豫行为对于了解其性质和应用具有重要意义。
聚合物的动力学研究主要集中在聚合过程中的反应速率和反应机制。
聚合反应是指将单体分子通过共价键连接起来形成聚合物的过程。
在聚合过程中,单体分子发生聚合反应,逐渐形成长链聚合物。
聚合反应的速率受多种因素影响,包括反应物浓度、温度、催化剂等。
聚合速率的研究可以帮助我们理解聚合反应的机理,并优化合成条件。
聚合物的弛豫行为是指聚合物在外界作用下的松弛过程。
聚合物在应力作用下会发生形变,当外力作用消失时,聚合物会恢复到原来的形态。
这种形变和恢复的过程称为弛豫。
聚合物的弛豫行为与其分子结构、分子量、交联程度等有关。
通过研究聚合物的弛豫行为,可以了解其物理性质,并为材料设计和应用提供指导。
聚合物动力学和弛豫行为的研究方法多种多样,包括实验方法和理论模型。
实验方法主要包括拉伸实验、动态力学分析、热分析等。
拉伸实验可以测量聚合物在不同应变下的力学性能,从而研究其弛豫行为。
动态力学分析可以通过振动试验测量聚合物的弹性模量、损耗模量等物理性质,进一步了解其弛豫行为。
热分析可以通过测量聚合物在不同温度下的热性能,揭示其分子结构和热弛豫行为。
理论模型的研究可以通过数学模型和计算模拟来解释聚合物动力学和弛豫行为。
数学模型主要基于聚合物的动力学方程和弛豫方程,通过求解这些方程,可以得到聚合物的动力学和弛豫行为的数值解。
计算模拟可以通过计算机模拟方法,建立聚合物分子的模型,模拟其动力学和弛豫行为。
这些模型和模拟方法可以帮助我们深入理解聚合物的行为,并指导实验设计和材料开发。
总结起来,聚合物动力学和弛豫行为对于了解聚合物的性质和应用具有重要意义。
通过实验和理论研究,我们可以揭示聚合物的动力学和弛豫行为的规律,并为材料设计和应用提供指导。
聚合物动力学和弛豫行为的研究将为未来的材料科学和技术发展提供重要支持。
自由基聚合动力学研究方法

自由基聚合动力学研究方法1引言聚合反应动力学的研究在理论上可以帮助我们了解聚合反应的机理,在工程上则能为反应器设计、聚合工艺条件的优化提供必要的依据,指导生产实践,因此具有重要的意义。
聚合反应动力学主要是研究聚合反应速率、聚合物分子量、聚合物的分子量分布和引发剂浓度、单体浓度、聚合反应温度之间的定量关系。
在共聚反应中共聚物的组成及其序列分布和引发剂浓度、单体配比、聚合温度间的关系也是研究的重点。
本文将从基于聚合反应机理的动力学模型、聚合动力学研究实验方法等方面介绍自由基聚合动力学的研究。
2自由基聚合动力学自由基聚合反应一般分为诱导期、聚合初期、聚合中期、聚合后期等几个阶段。
诱导期初级自由基为体系中存在的阻聚剂及一些杂质所消耗,没有聚合物形成,聚合速率为零。
如果能将体系产生阻聚作用的杂质完全去除,可以消除诱导期。
诱导期过后,单体开始正常聚合。
这一阶段的特点是聚合反应速率不随反应时间变化,为恒速聚合,称为聚合初期。
这一阶段的长短随单体种类和聚合方法而变,一般转化率在10~20%之间。
由于是恒速反应,利于微观动力学和反应机理的研究。
随着转化率的进一步提高,聚合反应速率逐步加大,出现自动加速现象,这种现象有时可以延续到转化率达50~70%,这一阶段称为聚合中期。
聚合中期后,单体浓度逐渐减少,聚合速率下降,为了提高转化率常需要延长反应时间。
这一阶段称为聚合后期。
聚合中期和聚合后期的聚合反应偏离了微观动力学,一般称为宏观动力学。
2.1自由基聚合微观动力学自由基聚合由链引发、链增长、链终止、链转移几个基元反应组成。
一般链转移反应对聚合反应速率影响较小,在研究自由基聚合微观动力学时,主要考虑前三个基元反应对聚合反应速率的贡献。
(1)自由基聚合的链引发反应由引发剂分解成初级自由基和初级自由基同单体加成形成单体自由基两步反应由于初级自由基的形成速率远小于单体自由基的形成速率,为控制反应速率的关键一步。
因此可以认为引发速率和单体浓度无关,仅取决于初级自由基的生成速率。
聚合反应工程基础_第四章

22
聚合反应工程
聚合反应速度分析 (间歇过程自由基均聚)
kd 引发剂引发 : I 2 R, rd 2kd [ I ] f ki R M P , ri ki [ R] [ M ] 1
链增长 : Pj M Pj 1 , rp k p [ M ] [ Pj ]
2013-10-7
4
聚合反应工程
本章主要内容
聚合反应速度的工程分析 连锁聚合反应的平均聚合度及聚合度分布 缩聚反应及非均相反应的工程分析 流动与混合对聚合度分布的影响
2013-10-7
5
聚合反应工程
聚合反应工程的目标
反应器流动模型 结合起来 建立统一的反应器模型 聚合反应动力学 预计所需质量和产量的聚合物。 现实情况: 高聚物流体一般是非牛顿流体,在流动过程还有物 态的变化。 对反应机理的认识; 对结构与性能的认识; 反应器影响反应结果的认识不深透。
平均分子量及聚合度分布可表征聚合物 性质,所以首先寻找,然后确定目标函数.
2013-10-7 12
聚合反应工程
自由基聚合反应动力学
• 自由基聚合微观动力学
研究聚合初期(通常转化率在5%~10%以下)聚合速率与 引发剂浓度、单体浓度、温度等参数间的定量关系。
说明:由于组成自由基聚合的三步主要基元反应: 链引发、链增长和链终止对总聚合速率均有所贡 献;链转移反应一般不影响聚合速率。 所以聚合反应总的动力学方程的建立过程为:首 先从自由基聚合反应的三个基元反应的动力学方 程推导出发,再依据等活性、长链和稳态三个基 本假设推导出总方程。
_
_
重均分子量 重均聚合度 重基分子量分布函数
2013-10-7
苯乙烯的原子转移自由基聚合(ATRP)——一个典型的“活性”

Univ. Chem. 2023, 38 (8), 225–231225收稿:2022-09-20;录用:2022-12-09;网络发表:2023-01-11 *通讯作者,Emails:********************(陶磊);********************(于莹)基金资助:自然科学基金(21971141);清华学堂创新人才培养计划;清华大学笃实专项(2022Z11DSZ026)•化学实验•doi: 10.3866/PKU.DXHX202209048苯乙烯的原子转移自由基聚合(ATRP)——一个典型的“活性”/可控自由基聚合实验何贤哲,于莹*,陶磊*清华大学化学系高分子化学与物理研究所,北京 100084摘要:我国理科院系的高分子化学实验教学内容主要集中于传统聚合方法,难以满足学科快速发展的现状和人才培养要求。
我们将苯乙烯的原子转移自由基聚合引入高分子化学实验教学,设计了一系列丰富的教学内容,包括实验操作、聚合过程监控和仪器表征等,旨在引导学生理解课堂知识,掌握从事高分子学科研究的基本实验技能。
通过结合前沿科研开展教学,提高学生的综合科研素养,为培养理科院系的高分子人才提供了全新的思路。
关键词:高分子化学;本科实验教学;原子转移自由基聚合 中图分类号:G64;O6Atom Transfer Radical Polymerization (ATRP) of Styrene: A Typical “Living”/Controlled Radical Polymerization ExperimentXianzhe He, Ying Yu *, Lei Tao *Institute of Polymer Chemistry & Physics, Department of Chemistry, Tsinghua University, Beijing 100084, China.Abstract: Experimental teaching of polymer chemistry in science colleges mainly focuses on traditional polymerization methods, making it difficult to meet the rapid development of polymer science and the requirements of student training. We introduced atom transfer radical polymerization into the experimental course of polymer chemistry and designed a series of contents, including experimental operation, polymerization process monitoring, and instrumental characterization, which are conducive for students to understand polymer research and master the basic skills of the field. We combined cutting-edge scientific research and experimental teaching to cultivate comprehensive scientific research literacy in students, providing new ideas for training students in science colleges.Key Words: Polymer chemistry; Undergraduate experimental teaching; Atom transfer radical polymerization1 引言1920年,德国科学家H. Staudinger 开创性地提出了高分子的概念,标志着高分子学科的建立[1]。
《聚合反应工程与设备》课程教学大纲

《聚合反应工程与设备》课程教学大纲英文名称:Polymerization Reaction Equipment课程类型:专业课课程要求:必修学时/学分:40/2.5适用专业:高分子材料与工程一、课程性质与任务聚合反应工程与设备课程是高分子材料与工程专业选修的专业课。
通过本课程的学习,掌握反应动力学和反应器设计与分析的知识和技能;掌握聚合反应工程分析方法,理解搅拌聚合釜内流体的流动与混合、传热;了解高聚物生产工艺设备的操作管理;掌握聚合反应器的特性及搅拌聚合釜放大设计方法。
培养和训练学生将所学过的基本理论和技能与聚合反应设备紧密结合在一起,形成有机地统一体,加强学生基础知识及专业基础知识在聚合物合成工程实践中的运用能力,从而提高学生分析和解决工程实践中的实际问题的能力。
同时对国内外聚合物生产设备和发展方向有所了解。
二、课程与其他课程的联系聚合反应工程与设备课程是高分子材料与工程专业的专业课,是在学生在学习了高等数学、物理化学、无机化学、有机化学、分析化学及化工原理等基础课程,掌握了高分子化学、高分子物理、聚合物近代仪器分析等专业基础知识之后,所学的关于聚合物合成的,具有工程实践指导意义的专业课。
学生在学习本课程之后,有助于对聚合物加工及应用的相关课程,如聚合物改性、聚合物加工原理及设备、高分子材料应用基础等课程内容的掌握和理解。
三、课程教学目标1.学习化学反应工程基础知识和基本理论知识,掌握化学反应动力学、化学反应器设计、反应器的热稳定性、停留时间分布等基本知识,了解化学反应工程研究的内容,具有分析、选用和设计化学反应器的能力;2.学习聚合反应工程分析的基础知识和基本理论知识,掌握聚合反应工程分析的方法、聚合反应器的选择及调控等基本知识,了解聚合反应工程研究的内容,具有分析、选用和设计聚合反应器的能力;3.掌握搅拌釜内流体的流动与混合对聚合物合成的影响及搅拌器设计基本知识,培养学生具有分析、选用和设计搅拌釜的能力;4.掌握聚合反应器的传热方式、计算方法及放大原理、方法,培养学生具有分析、放大聚合反应器的能力;5.培养学生的工程实践学习能力,使学生掌握典型聚合反应设备的选择、设计方法,获得实践技能的基本训练,具有运用标准、规范、手册、图册和查阅有关技术资料的能力;6.了解国内外聚合物生产设备和发展动向。
第2.5节 自由基聚合反应速率
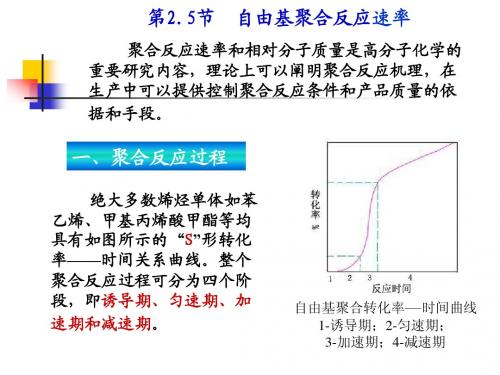
一、聚合反应过程
绝大多数烯烃单体如苯 乙烯、 乙烯、甲基丙烯酸甲酯等均 具有如图所示的“ 形转化 具有如图所示的“S”形转化 时间关系曲线。 率——时间关系曲线。整个 时间关系曲线 聚合反应过程可分为四个阶 诱导期、匀速期、 段,即诱导期、匀速期、加 速期和减速期。 速期和减速期。
在一般情况下链引发速率与单体浓度无关。 在一般情况下链引发速率与单体浓度无关。 而且只有一部分初级自由基参与引发单体生成单 体自由基, 体自由基,而另一部分初级自由基却发生了副反 所以应该将引发效率 考虑进去。 引发效率f 应,所以应该将引发效率f考虑进去。 链引发反应动力学方程
R i = 2 fkd [I]
d [M ] R总= − = Ri + RP ≈ RP dt
(二)各基元反应的动力学方程 1 链引发 I → 2R• R • + M → RM • 引发剂的分解速率 初级自由基的生成速率 单体自由基的生成速率 链引发反应包括两个步骤: 链引发反应包括两个步骤:
引发剂分解, 第一步 引发剂分解,产生初级自由基 第二步初级自由基与单体加成, 第二步初级自由基与单体加成, 初级自由基与单体加成 形成单体自由基
(一)、推导微观动力学方程的基本假设 )、推导微观动力学方程的基本假设
▲ 自由基等活性理论
k P1 = k P 2 = k P 3 = ⋯ = k Pn = k P
链自由基活性与链长无关, 链自由基活性与链长无关,即各 步链增长速率常数相等, 用表示; 步链增长速率常数相等,用kp 用表示;
第二章 自由基聚合-2.4 自由基聚合反应动力学

Rd=d[R·]/dt=2kd[I] Ri =-d[M]/dt=ki[R·][M] Rp1=-d[M]/dt =kp1[M][M1·] Rp2=-d[M]/dt =kp2[M][M2·]
••••••
Rpn=-d[M]/dt=kpn[M][Mn·]
Rtc=-d[Mx·]/dt=ktc[Mx·][My ·]
2.4.1聚合反应动力学研究方法 二、聚合速率的测定-间接法
C% V Vo K
K Vm Vp 100% Vm
其中,Vo为起始体积,△V为t时刻的
体积收缩值,由高度变化计算得到
Rp
d[M ] dt
[M ]2 t2
[M ]1 t1
C2[M ]o C1[M ]o t2 t1
••••••
Rpn=-d[M]/dt=kpn[M][Mn·]
2.4.2自由基聚合初期反应速率 一 动力学方程的推导
d[M ] R dt Ri Rp1 Rp2 ... Rpn
ki[R][M ] k p1[M1][M ] k p2[M 2][M ] ...... k pn[M n ][M ]
(7) Mx • M y • ktcMxy
(8) Mx • M y • ktd Mx M y
(9) M x • XH kts M x H X •
(无活性)
(10) M x • M ktr,M Mx M • (11) Mx • S ktr,s Mx S • (12) M x • I ktr,I M x I •
H
2.4.2自由基聚合初期聚合反应速率 一 动力学方程的推导
空间效应
空间效应对不同链长自由基的活性影响相同
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
大分子生成速率
Rp R poly
d [ polymers ] ? dt
R poly
全部偶合终止
~~~Mx·+ ~~~My· ~~~Mx + ~~~My
两个自由基生成一个大分子,大分子生成速率是自由基消失速率 的一半
=Rp1+Rp2+· · · · · · +Rpn
R-(M)n-M·
R pn k pn [M n ][ M ]
k pi [ M i ][ M ]
i 1
n
假设①
链自由基的活性与链长无关 (等活性理论)
n n i 1 i 1
Kp1=Kp2=· · · · · · =Kpn=Kp R p k pi [ M i ][ M ] k p [ M ] [ M i ]
反 应 速 率
100% 80%
40%
20%
t
(1) 凝胶效应
转化率增加,粘度增大,长链自由基扩散受阻,双基终止困难,kt↓,Rt↓, 单体扩散不受阻碍,kp 基本不变
在
fk d K kp k t
1
2
中, kt↓, kp 不变,K↑
R p↑
(2)影响因素 a) 溶剂 溶剂多,浓度低,粘度低 可以不出现自动加速 b) 温度 温度高, 粘度低,也可能不出现自动加速。 但温度高,速度本身就高。
[ M ]0 [ M ] 转化率 100% [ M ]0
[ M ]0 [ M ] d转化率 d[M ] d dt k [M ] dt dt 0
2.聚合速率方程
各基元反应的速率方程 (1) 链引发
d[ R ] 2k d [ I ] RM· Rd R· +M dt 链引发速率 Ri 2 fkd [ I ]
1 2
2k t [ M ] 2 2 fk d [ I ]
[ M n ] [ M n 1 ]
其它引发方式,引发机理不同,Ri不同,但Rp和Rt是一样的 上述Rp适合于描述聚合初期的速率
fkd 1 2 Rp k p [ I ] [M ] kt
2
1
k p [M ][ M ]
(3) 链终止
终止反应速率定义
d[M ] Rt dt
(mol/L.s)
~~~Mx+y~~~
~~~Mx·+ ~~~My· 偶合终止
ktc
k
Rtc 2k tc [ M ]2
~~CH2–CH2 + ~~CH=CH │ │ X X
td ~~CH2–CH· + ~~CH2–CH· │ │ X X
2.非均相体系
M,I,S
溶剂 均 相 相
──→
M,I,S,P
聚合物不溶于单体或
非均
如:丙烯腈在水中的聚合,丙烯腈溶于水,聚丙烯腈不溶于水 长链自由基不溶于溶剂,从溶剂中沉淀出来,呈卷曲状,链端 被包裹,双 基 终 止困难,反应一开始,就可能自动加速
三.平均聚合度
Xn 反应了的单体数 生成的大分子数
kp 的单位(L/mol.s)
聚合反应总速率为
假设③ 大分子链很长
fkd 1 2 Rp k p [ I ] [M ] kt
2 1
d[M ] R R p Ri dt
fk d K kp k t
1
1
2
R=
R p K [ M ][ I ] 2
一.聚合反应速率及方程式 1.聚合全过程
转 化 率
诱 导 期 初 期
中 期
后 期
t
导 期:聚合速率为零(杂质阻聚) 聚合初期:转化率低,聚合速率可用聚合速率 方程描述 聚合中期:聚合速率加快,用曲线描述 聚合后期:单体浓度降低,聚合速率降低。
诱
聚合速率
d[M ] RP dt
ktrs ' ~~M·+ S’
~~M·+ S
ktrs
~~M + S· ~~M + S’· ~~M + P·
Rtrs k trs [ M ][ S ]
~~M·+ P
ktrp
Rtrs' k trs' [ M ][ S ' ]
Rtrp k trp [M ][ P]
ki
d[I ] I 2 R· Rd dt k d [ I ]
kd
(2) 链增长
RM· +M
1
kp
RMM·
2
kp
R-(M)2-M·
······
n
kp
R p1 k p1 [M 1 ][ M ]
R p2 k p2 [M 2 ][ M ]
d[M ] Rp dt
R poly Rt R tri
Xn
Rt Rtri
Rp
有链转移反应, X n
令
ktrm kp
k trI kp
k trs kp
k trs' kp
k trp
Cm
CI
Cs
Cs'
kp
Cp
转移常数
歧化终止
Rtd 2k td [M ]
2
总速率
Rt Rtc Rtd 2k t [ M ]
2
kt 的单位
假设② 经过一定时间以后,体系中自由基的浓度基本不变 (稳态假设)
[M’] 稳态
t
Rt Ri
fk d [M ] k t
1 2
[I ]
全部歧化终止
~~~Mx·+ ~~~My· ~~~Mx+y~~~
一个自由基生成一个大分子,自由基消失速率就是大分子生成速率
一般情况,既有偶和又有歧化
全部歧化终止 全部偶合终止
四.转移反应对聚合度的影响 ktrm ~~M· + M ~M + M· R k [ M ][ M ] trm trm ktrI ~~M·+ I ~MR + R· RtrI k trI [ M ][ I ]
二二、自动加速效应
转化率升高,单体浓度下降, 聚合速率应下降,不下降反而 上升,出现自动加速。 11、均相体系
本体聚合 ──→
转 化 率
加速 稳 态 t
均 相 均 相 单体相当于溶剂 如:苯乙烯是液体,聚苯乙烯溶于苯乙烯
M,I
M,I,P
溶液聚合
M,I,S
──→
M,I,S,P
均 相 均 相 如:丙烯酰胺,聚丙烯酰胺都溶于水
