骨髓增殖性肿瘤(MPN) WHO 分型解析
血液病免疫分型

血液病免疫分型血液病的免疫分型主要根据免疫表型和免疫遗传学特征进行分类。
以下是一些常见的血液病免疫分型:1. 急性淋巴细胞性白血病(Acute Lymphoblastic Leukemia,ALL)的免疫分型:- B-ALL:由B淋巴细胞系发展而来。
- T-ALL:由T淋巴细胞系发展而来。
2. 慢性淋巴细胞性白血病/小淋巴细胞淋巴瘤(Chronic Lymphocytic Leukemia/Small Lymphocytic Lymphoma,CLL/SLL)的免疫分型:- CD5+/CD23+/CD20+:典型的B淋巴细胞来源。
- CD5-/CD23+/CD20+:非典型的B淋巴细胞来源。
- CD5+/CD23-/CD20+:突变的B淋巴细胞来源。
3. 急性髓系白血病(Acute Myeloid Leukemia,AML)的免疫分型:- 标准化治疗亚组(NCCN标准化治疗亚组):包括核准的AML-M0至AML-M7亚型。
- 非标准化治疗亚组:包括AML-M0、AML-M6和AML-M7亚型以外的亚型。
4. 慢性髓性白血病(Chronic Myeloid Leukemia,CML)的免疫分型:- Ph染色体阳性(Ph+):含有Ph染色体(Philadelphia染色体)。
5. 骨髓增殖性肿瘤(Myeloproliferative Neoplasm,MPN)的免疫分型:- 慢性骨髓性白血病(Chronic Myeloid Leukemia,CML):Ph染色体阳性。
- 原发性骨髓纤维化(Primary Myelofibrosis,PMF):包括JAK2V617F突变和CALR基因突变。
- 骨髓增殖性肿瘤不分类型(Myeloproliferative Neoplasm,NOS):不符合上述分类的其他骨髓增殖性肿瘤。
这些免疫分型对于血液病的诊断、预后评估和治疗选择具有重要意义。
注意,具体的免疫分型细节可能因研究、疾病进展和新兴的治疗手段而不断改变。
2016版造血与淋巴组织肿瘤WHO分类

2016版造血与淋巴组织肿瘤WHO分类一览表一. 髓系肿瘤(一)骨髓增殖性肿瘤(MPN)1. 慢性髓性白血病(CML),BCR-ABL+2. 慢性嗜中性粒细胞白血病(CNL)3. 真性红细胞增多症(PV)4. 原发性骨髓纤维化(PMF)PMF,纤维化前期/早期PMF,明显的纤维化期5. 原发性血小板增多症(ET)6. 慢性嗜酸性粒细胞白血病(CEL),非特指型(NOS)7. 骨髓增殖性肿瘤,未分类型(二)肥大细胞增多症(三)伴嗜酸性粒细胞增多及PDGFRA,PDGFRB,或FGFR1,或PCM1-JAK2异常的髓系/淋巴系肿瘤1. 伴PDGFRA重排的髓系/淋巴系肿瘤2. 伴PDGFRB重排的髓系/淋巴系肿瘤3. 伴PGFR1重排的髓系/淋巴系肿瘤4. 暂定分类:伴PCM1-JAK2的髓系/淋巴系肿瘤(四)骨髓增生异常综合征/骨髓增殖性肿瘤(MDS/MPN)1. 慢性粒单细胞白血病(CMML)2. 不典型慢性髓性白血病(aCML), BCR-ABL-3. 青少年粒单细胞白血病(JMML)4. 伴环铁粒幼细胞及血小板增多的MDS/MPN(MDS/MPN-RS-T)5. MDS/MPN, 不可分类(五)骨髓增生异常综合征(MDS)1. 伴单系病态造血的MDS2. 环铁粒细胞增多的MDS环铁粒细胞增多及单系病态造血的MDS环铁粒细胞增多及多系病态造血的MDS3. 伴多系病态造血的MDS4. 原始细胞过多型MDS5. 伴孤立del(5q)的MDS6. MDS,未分类型7. 待定:儿童难治性血液细胞减少(六)伴遗传易感性的髓系肿瘤1. 无既往病史或器官发育异常者AML伴遗传性CEBPA基因突变*髓系肿瘤伴遗传性DDX41 基因突变2. 既往有血小板疾病者*髓系肿瘤伴遗传性RUNX1 基因突变髓系肿瘤伴遗传性ANKRD26基因突变髓系肿瘤伴遗传性ETV6基因突变3. 伴有其它器官功能异常髓系肿瘤伴遗传性GATA2基因突变与遗传性骨髓衰竭综合征相关的髓系肿瘤(范可尼贫血)与端粒酶生物缺陷相关的髓系肿瘤(角化不良症)与神经纤维瘤病、Noonan综合征(目前确定与PTPN11、SOS1、RAF1、BRAF、KRAS、NRAS、SHOC2和CBL突变有关,50%PTPN11突变)或Noonan 综合征样疾病相关的青少年慢性粒单核细胞白血病与唐氏综合征相关的髓系肿瘤(七)急性髓性白血病(AML)及相关恶性肿瘤1. 伴重现性基因异常的AMLAML伴t(8;21)(q22;q22.1);RUNX1-RUNX1T1AML伴inv(16(p13.1q22)或t(16;16)(p13.1;q22);CBFB-MYH11急性早幼粒细胞白血病(APL)伴PML-RARAAML伴t(9;11)(p21.3;q23.3);MLL-KMT2AAML伴t(6;9)(p23;q34.1);DEK-NUP214AML伴inv(3)(q21.3q26.2)或t(3;3)(q21.3;q26.2);GATA,MECOM AML(原始巨核细胞型)伴t(1;22)(p13.3;q13.3);RBM15-MKL暂定型:AML伴BCR-ABL1AML伴NPM1基因突变AML伴双CEBPA基因突变暂定型:AML伴RUNX1基因突变2. 伴MDS相关改变的AML3. 治疗相关性髓系肿瘤4. AML, NOS微分化型AML未成熟型AML成熟型AML急性粒单核细胞白血病急性原始单核细胞/单核细胞白血病纯红血病急性巨核细胞白血病急性嗜碱粒细胞白血病伴骨髓纤维化的全髓性白血病5. 髓系肉瘤6. 唐氏综合征相关的髓系增殖一过性髓系增生异常唐氏综合征相关性髓系白血病二、混合细胞肿瘤(一)急性混合细胞白血病(MPAL)1. 急性未分化型白血病2. MPAL伴t(9;22)(q34.1;q11.2); BCR-ABL13. MPAL伴t(v;11q23.3);MLL重排4. MPAL, B/髓系,NOS5. MPAL, T/髓系,NOS三、淋巴细胞系肿瘤(一) B淋巴母细胞白血病/淋巴瘤1. B淋巴母细胞白血病/淋巴瘤,NOS2. 伴重现性基因异常的B淋巴母细胞白血病/淋巴瘤B淋巴母细胞白血病/淋巴瘤伴t(9;22)(q34.1;q11.2);BCR-ABL1 B淋巴母细胞白血病/淋巴瘤伴t(v;11q23.3); KMT2A重排B淋巴母细胞白血病/淋巴瘤伴t(12;21)(p13.2;q22.1);ETV6-RUNX1 B淋巴母细胞白血病/淋巴瘤伴超二倍体染色体B淋巴母细胞白血病/淋巴瘤亚二倍体染色体伴B淋巴母细胞白血病/淋巴瘤伴t(5;14)(q31.1;q32.3)IL3-IGHB淋巴母细胞白血病/淋巴瘤伴t(1;19)(q23;p13.3);TCF3-PBX1暂定类: B淋巴母细胞白血病/淋巴瘤,BCR-ABL1样B淋巴母细胞白血病/淋巴瘤伴iAMP213. T淋巴母细胞白血病/淋巴瘤暂定类:早期T前体细胞淋巴母细胞白血病NK细胞淋巴母细胞白血病/淋巴瘤(二)成熟B细胞肿瘤1. 慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)2. 单克隆B细胞增多症(MBL)3. B幼淋细胞白血病(B-PLL)4. 脾脏边缘带淋巴瘤(SMZL)5. 毛细胞白血病6. 脾脏B细胞淋巴瘤/白血病,未分类脾脏弥漫红髓小B细胞淋巴瘤变异型毛细胞白血病(HCLv)7. 淋巴浆细胞淋巴瘤Waldenstrm 巨球蛋白血症8. 未明意义的单克隆球蛋白病,IgM型9. μ重链病10. γ重链病11. α重链病12. 未明意义的单克隆球蛋白病,IgG/A型13. 浆细胞骨髓瘤(PCM)14. 骨孤立性浆细胞瘤15. 单克隆免疫球蛋白沉积病粘膜相关组织结外边缘带淋巴瘤(MALT 淋巴瘤)16. 结内边缘带淋巴瘤儿童结内边缘带淋巴瘤17. 滤泡淋巴瘤(FL)原位滤泡恶性肿瘤十二指肠型滤泡淋巴瘤18. 儿童滤泡淋巴瘤19. 伴IRF4重排的大B细胞淋巴瘤20. 原发皮肤滤泡中心淋巴瘤21. 套细胞淋巴瘤(MCL)原位套细胞恶性肿瘤22. 弥漫大B细胞淋巴瘤,非特指型(DLBCL, NOS)生发中心型(GCB型)激活B细胞型(ABC型)23. 原发中枢DLBCL24. 原发皮肤DLBCL,腿型25. EBV+ DLBCL26. EBV+皮肤粘膜溃疡27. 与慢性炎症相关的DLBCL28. 淋巴瘤样肉芽肿病29. 原发纵膈(胸腺)大B细胞淋巴瘤30. 血管内大B细胞淋巴瘤31. ALK+大B细胞淋巴瘤32. 浆母细胞淋巴瘤33. 原发渗出性淋巴瘤34. HHV8+DLBCL,NOS35. 伯基特淋巴瘤36. 伴11q异常的伯基特样淋巴瘤37. 伴MYC及BCL2和/或BCL6重排的高度恶性B细胞淋巴瘤(HGBCL)38. HGBCL, NOS39. B细胞淋巴瘤,未分类型,有DLBCL与经典型何奇金氏淋巴瘤之间的特征(三)成熟T及NK细胞恶性肿瘤1. T幼淋细胞白血病(T-PLL)2. T大颗粒淋巴细胞白血病(T-LGL)3. 慢性NK细胞淋巴增殖性疾病4. 侵袭性NK细胞白血病5. 儿童系统性EBV+T细胞淋巴瘤6. 水疱种豆样淋巴增殖性疾病7. 成人T细胞白血病、淋巴瘤8. 结外NK/T淋巴瘤,鼻型9. 肠道病相关T细胞淋巴瘤10. 单形性嗜上皮细胞小肠T细胞淋巴瘤胃肠道惰性T淋巴细胞增殖性疾病11. 肝脾T细胞淋巴瘤12. 皮下脂膜炎样T细胞淋巴瘤13. 菌样肉芽肿14. Sèzary 综合征15. 原发皮肤CD30+T淋巴细胞增殖性疾病淋巴瘤样丘疹原发皮肤间变大细胞淋巴瘤16. 原发皮肤 T细胞淋巴瘤17. 原发皮肤CD+8+侵袭性嗜表皮细胞毒性T细胞淋巴瘤18. 原发皮肤肢端CD8+ T细胞淋巴瘤19. 原发皮肤CD4+小/中T细胞淋巴增殖性疾病20. 外周T细胞淋巴瘤,NOS (PTCL, NOS)21. 血管免疫母细胞T细胞淋巴瘤(AITL)22. 滤泡T细胞淋巴瘤23. 伴TFH表型的结内外周T细胞淋巴瘤24. 间变大细胞淋巴瘤(ALCL),ALK+25. ALCL, ALK-26. 乳腺植入相关ALCL四、何奇金氏淋巴瘤(HL)1. 结节淋巴细胞为主的HL2. 经典型HL(cHL)结节硬化型cHL富淋巴细胞cHL混合细胞型cHL淋巴细胞耗竭性cHL五.移植后淋巴细胞增殖性疾病(PTLD)(一)浆细胞高增殖性PTLD(二)传染性单核细胞增多性PTLD (三)明显滤泡增殖性PTLD(四)多形性PTLD(五)单形性PTLD(B-及T/NK细胞型) (六) cHL 型PTLD六、组织细胞及树突细胞恶性肿瘤(一)组织细胞肉瘤(二)朗格罕细胞组织细胞增多症(三)朗格罕细胞组织细胞肉瘤(四)中度树突细胞肿瘤(五)指突状树突细胞肉瘤(六)滤泡树突细胞肉瘤(七)成纤维母细胞网状细胞肿瘤(八)弥漫性青少年黄色肉芽肿(九) Erdheim-Cheter 病。
2016年世界卫生组织(WHO)髓系肿瘤新分类
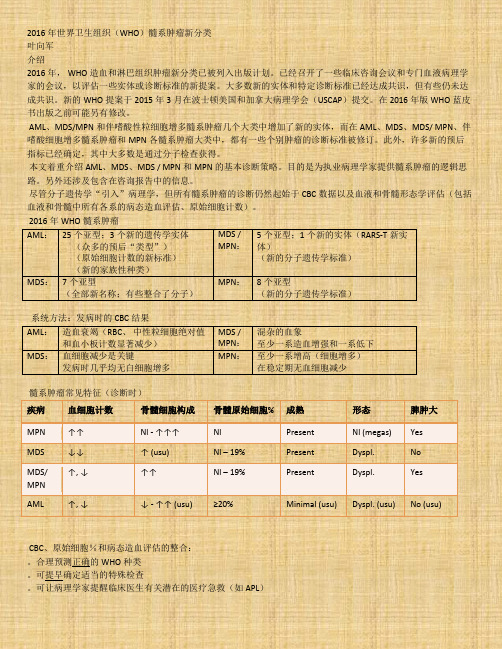
2016年世界卫生组织(WHO)髓系肿瘤新分类叶向军介绍2016年, WHO造血和淋巴组织肿瘤新分类已被列入出版计划。
已经召开了一些临床咨询会议和专门血液病理学家的会议,以评估一些实体或诊断标准的新提案。
大多数新的实体和特定诊断标准已经达成共识,但有些仍未达成共识。
新的WHO提案于2015年3月在波士顿美国和加拿大病理学会(USCAP)提交。
在2016年版WHO蓝皮书出版之前可能另有修改。
AML、MDS/MPN和伴嗜酸性粒细胞增多髓系肿瘤几个大类中增加了新的实体,而在AML、MDS、MDS/ MPN、伴嗜酸细胞增多髓系肿瘤和MPN各髓系肿瘤大类中,都有一些个别肿瘤的诊断标准被修订。
此外,许多新的预后指标已经确定,其中大多数是通过分子检查获得。
本文着重介绍AML、MDS、MDS / MPN和MPN的基本诊断策略。
目的是为执业病理学家提供髓系肿瘤的逻辑思路。
另外还涉及包含在咨询报告中的信息。
尽管分子遗传学“引入”病理学,但所有髓系肿瘤的诊断仍然起始于CBC数据以及血液和骨髓形态学评估(包括血液和骨髓中所有各系的病态造血评估、原始细胞计数)。
2016年WHO髓系肿瘤AML:25个亚型;3个新的遗传学实体(众多的预后“类型”)(原始细胞计数的新标准)(新的家族性种类)MDS /MPN:5个亚型;1个新的实体(RARS-T新实体)(新的分子遗传学标准)MDS:7个亚型(全部新名称;有些整合了分子)MPN:8个亚型(新的分子遗传学标准)系统方法:发病时的CBC结果AML:造血衰竭(RBC、中性粒细胞绝对值和血小板计数显著减少)MDS /MPN:混杂的血象至少一系造血增强和一系低下MDS:血细胞减少是关键发病时几乎均无白细胞增多MPN:至少一系增高(细胞增多)在稳定期无血细胞减少髓系肿瘤常见特征(诊断时)疾病血细胞计数骨髓细胞构成骨髓原始细胞% 成熟形态脾肿大MPN ↑↑ Nl - ↑↑↑ Nl Present Nl (megas) Yes MDS ↓↓ ↑ (usu) Nl – 19% Present Dyspl. NoMDS/MPN↑, ↓ ↑↑ Nl – 19% Present Dyspl. Yes AML ↑, ↓ ↓ - ↑↑ (usu) ≥20% Minimal (usu) Dyspl. (usu) No (usu)CBC、原始细胞%和病态造血评估的整合:。
临床血液学检验 白细胞检验 MPN、MDS、MM等

骨髓增殖性肿瘤(MPN):是以骨髓中分化成熟相对正常的一系或多系髓系(粒系、红系、巨核系)细胞持续异常增殖为特征的一组克隆性造血干细胞疾病。
与MDS所见无效造血相反,增殖的细胞分化成熟相对正常。
临床一般起病缓慢,有血细胞质和量的改变,肝、脾肿大,常并发出血、血栓及髓外造血。
疾病进展到终末期,可出现骨髓纤维化、无效造血,或转化为急性白血病。
本组疾病中典型的4种,除了慢粒还包括真性红细胞增多症、原发性血小板增多症及原发性骨髓纤维化等。
一、原发性血小板增多症(ET)是一种主要累及巨核细胞系的克隆性骨髓增殖性疾病,以血小板数持续增多、血栓形成和(或)出血和骨髓巨核细胞异常增生为特征。
【临床表现】本病好发于50~70岁,男女发病率无明显差异,多缓慢起病,50%的病人发病时无症状,在血常规检查时才偶然发现PLT显著增高,偶尔因发现血小板增多或脾大或手术后出血不止而确诊。
但约20~30 %的患者初诊时已表现为血管梗死或出血,多数病人有出血或血栓形成。
出血症状以胃肠道、上呼吸道黏膜出血较常见(皮肤、粘膜出血少见)。
血栓栓塞以指(趾)小血管、中枢神经血管和肢体血管栓塞为主,患者可有血管性头痛、头昏、意识模糊、手掌及足底灼痛感或手指痉挛及坏死。
初诊时,脾大见于多数病例(>50%),一般为轻到中度肿大,少数病人(约20%)有肝肿大。
【检验】1、血象:血小板计数多在(1000~3000)×10^9/L。
MPV增大,血小板比积明显增加。
可见巨大型、小型及不规则血小板,常自发聚集成堆。
可见巨核细胞碎片。
白细胞计数多在(10~30)×10^9/L,偶可达(40~50)×10^9/L。
分类以中性分叶核粒细胞为主,偶见幼粒细胞。
嗜碱性粒细胞不多或轻度增多。
Hb一般正常或轻度增多,但可因出血导致小细胞低色素性贫血。
2、骨髓象:有核细胞多为增生活跃或明显活跃,偶见增生减低。
最显著的特点是巨核细胞系统增生突出,原始及幼稚巨核细胞的比例增高,常有巨大的巨核细胞,部分病例可见到小巨核细胞。
骨髓增殖性疾病的诊断和分型

PMF
prePMF
overtPMF
CML加速期诊断标准
ELN、WHO加速期诊断标准中 均强调Ph+中期分裂相中出现
克隆性染色体异常提示AP
在2016修订的WHO指南中, 保留了上述Ph+中期分裂相中
核型演变的概念
提出初诊时Ph+中期分裂相中 出现主要类型附加染色体异常 、复杂核型、3q26重排,提示 加速期诊断
William Dameshek发现很多PV患者伴 有全血细胞增殖,并最终进展为骨 髓纤维化。
4
. Dameshek W. Some speculations on the myeloproliferative syndromes. Blood. 1951;6:372-375
MPN的演化
Ann Rev Pathol Mech Dis. 2016. 11:101–26.
MPN
SM
CMML JMML aCML
PCM1-JAK2
MDS/MPN-RS-T MDS/MPN-u
classic
CML
ET PV
non-classic
CNL
CEL-NOS MPN-u
PMF
prePMF
overtPMF
骨髓增殖性肿瘤的分类 (WHO-2016)
MPN-Eo
• MPN的分类更新概述(WHO-2016)
• MPN的更新
• MPN-Eo的更新 • MDS/MPN的更新
骨髓增殖性肿瘤的分类 (WHO-2016)
MPN-Eo
MDS/MPN
PDGFRA重排
PDGFRB重排
FGFR1重排
MPN
SM
MDS骨髓增生异常综合征2022年第5版《WHO造血与淋巴组织肿瘤分类》更新解读

三、由形态学定义的MDS
低增生MDS (MDS-h) 在本版中被列为一个单独的 MDS 类型: MDS-h、阵发性睡眠性血红蛋白尿 (PNH) 和再生障碍性贫血 (AA) 三者之间具有一些重叠特征。
许多MDS-h 患者对AA患者使用的药物(即抗胸腺细胞球蛋白,ATG)具有持续反应。 因此,重点应放在缜密的形态学评估上,除了评估骨髓涂片和印片以及检测突变和/或克隆性细胞遗传 学异常外,通常还需要活检评估。
• MDS更新要点:
• ✓“骨髓增生异常综合征”更名为“骨髓增生异常肿瘤”,仍然简称MDS; • ✓ MDS遗传学类型更新包括:MDS-5q、MDS-SF3B1、MDS-biTP53; • ✓ 低增生MDS(MDS-h)被认为是一种独特的疾病类型;
• ✓ MDS伴低原始细胞(MDS-LB)和MDS伴原始细胞增多(MDS-IB)均为一个新的类型,以提高 逻辑清晰性;
谢谢
慢性粒单核细胞白血病诊断标准
基于原始细胞的 CMML-0 亚组(外周血中原始细胞<2%,骨髓中原始细胞<5%)已被删除
其他术语更新: 不典型慢性髓系白血病更名为 MDS/MPN 伴中性粒细胞增多
“MDS/MPN伴环形铁粒幼红细胞和血小板增多”在SF3B1突变的基础 上重新定义,并重新命名为“MDS/MPN伴SF3B1突变和血小板增多”
二、具有明确遗传学异常的 MDS
1、MDS伴低原始细胞和孤立性5q- (MDS-5q): 诊断标准没有改变。 2、MDS伴低原始细胞和SF3B1突变 (MDS-SF3B1):
其中 90% 以上的 MDS 具有≥5% 的环形铁粒幼红细胞。仍保留“MDS伴低原始细胞和环形铁粒幼红细胞”这一 疾病名称,作为可接受的替代术语,用于伴有野生型 SF3B1 和 ≥15% 环形铁粒幼细胞的病例。
bcr-abl阴性MPN诊断和治疗

BCR/ABL阴性骨髓增殖性肿瘤的诊断和治疗1.概念根据2008年WHO造血与淋巴组织肿瘤分类1所提出的概念,骨髓增殖性肿瘤(MPN)包括以下8种类型:慢性髓性白血病BCR/ABL1阳性(CML),真性红细胞增多症(PV),原发性血小板增多症(ET),原发性骨髓纤维化(PMF),慢性中性粒细胞白血病(CNL),慢性嗜酸性粒细胞白血病非特质型(CEL,not otherwise specified),肥大细胞增多症(Mastocytosis),以及骨髓增殖性肿瘤未分类型(MPN-U)。
基于Dameshek2最初对于骨髓增殖性疾病的归纳,PMF、PV、ET与CML合称为经典MPN,流行病学特点、临床表现及实验室特征均有别于其他四种“非经典MPN”。
而其中CML存在特异性分子学异常BCR/ABL基因的重排,具有诊断意义。
而相应的靶向药物受体酪氨酸激酶抑制剂(TKI)伊马替尼一线应用所累积的大量临床资料和目前二代TKI的临床试验结果均证明,对大部分CML患者的治疗现在已能够达到细胞遗传学甚至分子学起效,并且能够实现预防疾病进展,延长生存期,改善生活质量,甚至治愈疾病的目标。
因此除CML之外其余各类型MPN可统称为BCR/ABL阴性MPN3。
随着对JAK2等分子标志的研究不断深入,有学者认为ET、PV、PMF可能是同一种疾病在不同时期的表现,类似于CML分三期但本质是一个连续的整体,进而提出了“连续统一体模型(continuum model)”的假设4:高危PMF和AML可能代表了疾病进展状态,而ET和PV则体现了疾病慢性期的特点;在这种由ET、PV“进展”至PMF、ET/PV后骨纤,再“进展”至AML的过程中,JAK2等位负荷、遗传不稳定性、有丝分裂重组、基因组环境、获得其他突变以及临床治疗等因素都可能起到了调控作用;与CML不同,这种“进展”速度很慢而且并非必然,且患者可能在整个病程中的任何时点“发病”。
世卫组织(WHO)骨髓瘤和急性白血病临床分型(2016版)

世卫组织(WHO)骨髓瘤和急性白血病临床分型(2016版)整理:血液科那条鱼来源:肿瘤资讯自2008年世卫组织(WHO)血液肿瘤和淋巴瘤临床分型公布之后,骨髓瘤和急性白血病的某些特异性生物学标志物有了长足研究发展,包括基因表达分析和下一代基因测序,对完善疾病的诊断标准以及治疗策略帮助巨大。
因此,WHO纳入最新的临床研究、预后研究、形态学研究、免疫学研究和基因研究等数据,对2008版骨髓瘤和急性白血病临床分型进行修正和更新。
骨髓肿瘤和急性白血病WHO分型骨髓增生性肿瘤(MPN)慢性髓系白血病,BCR-ABL1阳性慢性中性粒细胞白血病真性红细胞增多症原发性骨髓纤维化(PMF)原发性骨髓纤维化,纤维化前期/早期阶段原发性骨髓纤维化,纤维化明显期原发性血小板增多症慢性嗜酸粒细胞白血病,未另作规定(NOS)骨髓增生性肿瘤,未归类肥大细胞增多症髓系/淋系肿瘤伴嗜酸性粒细胞增多和PDGFRA、PDGFRA或FGFR1基因异常,或伴PCM1-JAK2髓系/淋系肿瘤伴PDGFRA基因重组髓系/淋系肿瘤伴PDGFRB基因重组髓系/淋系肿瘤伴FGFR1基因重组暂时分型:髓系/淋系肿瘤伴PCM1-JAK2骨髓增生异常/骨髓增生性肿瘤(MDS/MPN)慢性粒单核细胞白血病(CMML)不典型慢性髓系白血病,BCR-ABL1阴性幼年型粒单核细胞白血病骨髓增生异常综合征/骨髓增生性肿瘤伴环状铁粒幼红细胞和血小板增多(MDS/MPN-RS-T)骨髓增生异常综合征(MDS)MDS伴单系发育异常MDS伴环状铁粒幼红细胞MDS伴单系发育异常和环状铁粒幼红细胞MDS伴多系发育异常MDS伴原始细胞过多MDS伴异常核型del(5q)未分类MDS暂时分型:儿童难治性血细胞减少骨髓肿瘤伴生殖细胞倾向急性髓系白血病(AML)和相关肿瘤AML伴重现型遗传异常AML伴t(8;21)(q22;q22.1);RUNX1-RUNX1T1AML伴inv(16)(p13.1q22) 或t(16;16)(p13.1;q22);CBFB-MYH11AML伴PML-RARAAML伴t(9;11)(p21.3;q23.3); MLLT3-KMT2AAML伴t(6;9)(p23;q34.1); DEK-NUP214AML伴inv(3)(q21.3q26.2) 或t(3;3)(q21.3;q26.2); GATA2,MECOMAML(巨核细胞)伴t(1;22)(p13.3;q13.3); RBM15-MKL1暂时分型:AML伴BCR-ABL1AML伴NPM1突变AML伴CEBPA等位基因突变暂时分型:AML伴RUNX1突变急性髓系白血病伴脊髓发育异常相关改变治疗相关骨髓肿瘤急性髓系白血病,NOSAML伴微分化型AML伴未成熟型急性粒-单核细胞白血病急性单核细胞白血病纯红系白血病急性巨核细胞白血病急性嗜碱性粒细胞性白血病急性全髓白血病伴骨髓纤维化骨髓肉瘤唐氏综合征相关性骨髓增生一过性骨髓细胞生成异常唐氏综合征相关性髓系白血病系列不明性急性白血病急性未分化性白血病混合表型急性白血病伴t(9;22)(q34.1;q11.2); BCR-ABL1 混合表型急性白血病伴t(v;11q23.3); MLL重组混合表型急性白血病,B/髓系,NOS混合表型急性白血病,T/髓系,NOSB淋巴细胞白血病/淋巴瘤B淋巴细胞白血病/淋巴瘤,NOSB淋巴细胞白血病/淋巴瘤伴重现性细胞遗传学异常B淋巴细胞白血病/淋巴瘤伴t(9;22)(q34.1;q11.2);BCR-ABL1B淋巴细胞白血病/淋巴瘤伴t(v;11q23.3);KMT2A重组B淋巴细胞白血病/淋巴瘤伴t(12;21)(p13.2;q22.1); ETV6-RUNX1B淋巴细胞白血病/淋巴瘤伴超二倍体核型B淋巴细胞白血病/淋巴瘤伴亚二倍体核型B淋巴细胞白血病/淋巴瘤伴t(5;14)(q31.1;q32.3) IL3-IGHB淋巴细胞白血病/淋巴瘤伴t(1;19)(q23;p13.3);TCF3-PBX1暂时分型:BCR-ABL1样B淋巴细胞白血病/淋巴瘤暂时分型:B淋巴细胞白血病/淋巴瘤伴iAMP21T淋巴细胞白血病/淋巴瘤暂时分型:早期前T细胞淋巴细胞白血病暂时分型:自然杀伤(NK)细胞淋巴细胞白血病/淋巴瘤慢性髓系白血病加速期的诊断标准符合下列至少1项血液学/细胞学指标或TKI治疗响应条件·白细胞计数持续性增加(>10 x 10^9/L),且治疗无效。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
WHO (2008)MPN分型
• 慢性粒细胞白血病,BCR-ABLI阳性 • 慢性中性粒细胞白血病 • 真性红细胞增多症 • 原发性骨髓纤维化 • 原发性血小板增多症 • 慢性嗜酸性粒细胞白血病,非特殊类型 • 肥大细胞增生症
皮肤肥大细胞增生症 系统性肥大细胞增生症 肥大细胞白血病 肥大细胞肉瘤 皮肤外肥大细胞肿瘤 • 骨髓增殖性肿瘤,无法分类
的恶性疾病。 • 第一个发现染色体异常导致遗传物质从一条染色体向另外
一条染色体易位形成的融合基因(BCR/ABL)。 • 也是第一个采用针对特异性分子缺陷靶点治疗的疾病
(格列卫)。
CML临床分期及诊断标准(WHO)
• 1.慢性期(Chronic phase,CP)
(1)临床: 无症状或有低热、乏力、体重减轻,贫血 或脾脏肿大等。 (2)血象:WBC增高,常> 30×109/L,主要为中晚 幼粒细胞及杆状核粒细胞,原始细胞<10%。嗜酸性 和嗜碱性粒细胞增多。NAP积分减低或消失。 (3)骨髓象:增生明显至极度活跃,以粒系增生为主, 中晚幼粒和杆状核细胞增多,原始细胞≤10%。 (4)染色体:有Ph´染色体。BCR-ABL融合基因阳性。 (5)骨髓培养:集落明显增加。
一、慢性粒细胞白血病(CML)
Chronic Myelogenous Leukemia , BCR-ABL1–positive
• 在WHO分类中,CML被明确的定义为一种以Ph染色体阳 性,即t(9;22)(q34;q11)和 BCR/ABL融合基因的恒定存 在为特征的骨髓增殖性肿瘤。
• CML100%有BCR/ABL融合基因。 • 也是世界上第一个被发现染色体异常(Ph染色体)相关
• 2.加速期(Accelerated phase,AP)
• 具有下列之一或以上者。
(1)治疗无效的进行性白细胞增多和/或脾肿大。 (2)治疗无效的持续性血小板增高( > 1000×109/L ) (3)与治疗无关的持续性血小板减少( <100×109/L ) (4)细胞遗传学示有克隆演变。 (5)外周血嗜碱粒细胞≥20%。 (6)外周血白细胞和(或)骨髓有核细胞中原始细胞占 10%~ 19%
WHO (2001)MPD分型
• ①慢性粒细胞白血病(CML) • ②慢性中性粒细胞白血病(CNL) • ③慢性嗜酸性粒细胞白血病 / 高嗜酸性粒细胞综
合症(CEL / HES) • ④真性红细胞增多症(PV) • ⑤慢性特发性骨髓纤维化(CIMF) • ⑥原发性血小板增多症(ET) • ⑦慢性骨髓增殖性疾病,不能分类(CMPD-U)。
WHO (2008)MPN分型
WHO (2001)MPD分型
慢性粒细胞白血病,BCR-ABLI阳性 慢性粒细胞白血病(CML)
慢性中性粒细胞白血病(CNL)
慢性中性粒细胞白血病(CNL)
真性红细胞增多症(PV)
真性红细胞增多症(PV)
原发性骨髓纤维化(PMF)
慢性特发性骨髓纤维化(CIMF)
原发性血小板增多症(ET)
临床表现
• 起病缓慢,血细胞有质和量的改变,肝、脾肿 大,常并发出血、血栓及髓外造血。
• 与骨髓增生异常综合征(MDS)所见无效造血 相反,增殖的细胞分化相对成熟,外周血粒细 胞、红细胞和/或血小板增多。
• 常见肝、脾肿大,是由于脾或肝扣留了过多的 血细胞、髓外造血、白血病细胞浸润或以上多 因素所致。
原发性血小板增多症(ET)
慢性嗜酸性粒细胞白血病(CEL), 慢性嗜酸性粒细胞白血病 / 高嗜酸性
非特殊类型
粒细胞综合症(CEL / HES)
肥大细胞增生症
皮肤肥大细胞增生症
系统性肥大细胞增生症
肥大细胞白血病
肥大细胞肉瘤
皮肤外肥大细胞肿瘤
骨髓增殖性肿瘤,不能分类(MPN-U) 慢性骨髓增殖性疾病,不能分类 (CMPD-U)
CML-慢性期 Chronic phase (CP)
一、血象
• ①白细胞总数显著增高 (12-1000 ) × 109 /L, 中位数 100 × 109 /L;少数可达1000×109/L以上。
• 血片
• 原始粒细胞通常<2%。嗜中性中幼粒、晚幼粒及杆状核 粒细胞占大多数。NAP染色 通常减低或阴性。
骨髓增殖性肿瘤(MPN) WHO 分型解析
骨髓增性肿瘤
(myeloproliferative neoplasms,MPN)
• 2008年之前称为骨髓增殖性疾病 (myeloproliferative diseases,MPD)
• MPN 是以骨髓一系或多系髓系细胞(粒、红、巨 核系)持续增殖为特征的一组克隆性造血干细胞 疾病。
WHO(2008)MPN修订
• (1)慢性骨髓增殖性疾病改为骨髓增殖性肿瘤 • (myeloproliferative neoplasms,MPN)。 • (2)由于JAK2V61 7F基因的突变在大部分真性
红细胞增多症(PV)及约一半的原发性骨髓纤维化 (PMF)及特发性血小板增多症(ET)中存在。为此 PV、PMF、ET的诊断标准都有所改变。 • (3)把肥大细胞增多症(mastocytosis)归于此 栏中,且分为5类肥大细胞肿瘤。
• 嗜碱性粒细胞绝对值增高,比例常>2% ,是CML的特征 之一。
• 很多患者嗜酸性粒细胞增多; • 部分患者单核细胞绝对值也可增高,但比例常< 3%
• 一、血象
• ②红细胞及血红蛋白 早期正常或稍增高,也可轻 度减低。随着病情发展,逐渐呈轻度至中度减低。 网织红细胞多有增高。
• 血片 成熟红细胞呈正细胞正色素或大小不均,可 见有核红细胞、异形红细胞,嗜多色及点彩红细 胞。
• 3.急变期(Blast phase,BP) :
• 具有下列之一或以上者。
(1)外周血白细胞和(或)骨髓有核细胞中原始细胞≥20% 。 约70%为急性髓系变,原始细胞可以为嗜中性粒细胞、嗜 酸性粒细胞、嗜碱性粒细胞、单核细胞、红细胞、巨核细 胞的或混合的。约20% ~ 30%为急淋变。 (2)髓外浸润:常见部位为皮肤、淋巴结、脾脏、骨骼或中 枢神经系统。 骨髓活检 示原始细胞大量聚集或成簇。如果原始细胞明显 地呈局灶性聚集于骨髓,即使其余部位的骨髓活检示为慢 性期,仍可诊断为BP。
