结肠癌辅助治疗突破进展,轰动全球!
结直肠癌辅助化疗的研究进展

1 C C术后 复发转 移风 险的判 断 R
C C术后出现复发转移将影响患者生存 , R 因此预后评估
在 临 床 上 非 常 重 要 。 为 降 低 术 后 复 发 转 移 , 高 5年 存 活 提 率 , 复发 风 险 的患 者 需 要 进 行 术 后 辅 助 化 疗 。 目前 采 用 的 高
位 … 。 我 国 近 年 C C发 病 明显 上 升 , 海 市 20 R 上 0 5年 肿 瘤 报 告 C C 位 居 肿 瘤 发 病 和 死 亡 的 第 4位 。C C 根 治 手 术 后 R R 4 % ~ 0 患 者 最 终 会 出 现 复 发 或 死 于 转 移 性 疾 病 。 随 着 0 5% C C基 础 与 临 床 研 究 的 深 入 , 别 是 新 化 疗 药 物 的 应 用 , R 特 辅
结直肠癌( o rc l acr C C 是消化道最常 见恶性 cl et ne, R ) o ac 肿瘤 , 全球 每年 新发病 例8000 , 5 0 例 死亡 病例500 0 , 0 0 例 美 国 C C占恶 性 肿 瘤 发 病 的 第 3位 和 因肿 瘤 死 亡 的 第 2 R
维普0 0 8年 9月第 1 3卷第 9期
C ieeCi cl no g ,e.20 , o 1 ,o9 h s l ia O cl ySp 0 8 V 1 3 N . n n o .
结 直 肠 癌 辅 助 化 疗 的 研 究 进 展
的关 联 , 年 患 者 接 受 5F 为 基 础 的辅 助 化 疗 一 样 能 够 取 老 一u 得 在 其 他 年 龄组 中取 得 的疗 效 , 治 疗 相 关 的毒 性 反 应 也 没 与 有 因 年 龄 而 明显 增 加 。 Z cem n等 ” 在 A C 0 8年会 ukr a S O 20
NCCN指南变更:结肠癌辅助化疗可缩短至3个月!

NCCN指南变更:结肠癌辅助化疗可缩短至3个月!结直肠癌是全球第三大常见恶性肿瘤,根据世界卫生组织国际癌症研究所发布的数据,全球每年新诊断为结直肠癌的病例超过136万。
其中,结肠癌好发于直肠与乙状结肠交界处,以40-50岁年龄组发病率最高,男女比为2-3:1,发病率占胃肠道肿瘤的第3位。
结肠癌治疗方案的选择主要取决于肿瘤在结肠的位置,以及癌症的分期。
结直肠癌的治疗方法包括手术、化疗、生物疗法和放疗。
一些患者需要联合治疗。
手术和放疗属于局部治疗,切除或破坏结肠附近的癌症。
而化疗和生物疗法属于全身治疗,通过将药物注入血流,破坏或控制全身的癌症。
今年3月,在第23届NCCN年会上,美国国家综合癌症网络(NCCN)对结肠癌临床实践指南做出了一个重要调整,明确低危Ⅲ期结肠癌患者术后辅助化疗时间可以缩短。
这一改变是基于一项大型3期临床试验IDEA的研究结果。
在IDEA研究中,研究者根据临床医生及患者选择,随机分配12 834例患者接受3个月或6个月奥沙利铂为主辅助化疗方案(FOLFOX或CAPEOX方案),分析3个月化疗疗效是否不劣于6个月化疗。
研究结果显示,在接受FOLFOX(氟尿嘧啶,亚叶酸和奥沙利铂)或CAPOX方案(卡培他滨和奥沙利铂)辅助治疗的Ⅲ期结肠癌患者中,3个月治疗与6个月相比,在总体人群中没有证实其非劣效性。
然而,在接受CAPOX方案治疗的患者中,3个月的治疗效果与6个月的疗效相似,特别是在低风险亚组中。
更重要的是,缩短化疗时间可显著降低神经毒性。
3个月治疗组相比于6个月组,其神经毒性发生率显著降低(FOLFOX:17% vs. 48%;CAPEOX:15% vs. 45%;P<0.0001)。
NCCN指南根据风险分型对Ⅲ期结肠癌辅助治疗给出了不同的治疗策略:(1)病理分期为T1-3N1的Ⅲ期低危人群,优选CAPEOX 3个月或FOLFOX 3-6个月辅助治疗。
(2)病理分期为T4N1-2和T任何N2的Ⅲ期高危人群,优选CAPEOX 3-6个月或FOLFOX 方案6个月治疗。
结直肠癌的新辅助化疗概述

结直肠癌的新辅助化疗概述结直肠癌是常见的消化道恶性肿瘤之一,近年来其发病率逐年上升,手术治疗是其首选治疗方案,但多数病例就诊时已为进展期肿瘤。
因此20世纪80年代以来,术前新辅助化疗逐渐应用于临床,并表现出较好的疗效,加之新的化疗药物及分子靶向药物的应用,大大改善了结直肠癌患者的预后,为结直肠癌的治疗做出了重要贡献。
本文就结直肠癌新辅助化疗的研究进展做以综述。
标签:结直肠癌;新辅助化疗结直肠癌是常见的恶性肿瘤之一,其发病率已跃居常见肿瘤第3位,全球每年新发病例近1 20万,死亡人数达60万[1,2]。
据报道,有25%的结直肠癌患者就诊时已为中晚期,超过25%的患者第一次根治术后将复发或转移。
尽管近年来结直肠癌的治疗得到长足发展,但是IIIC期及Ⅳ期结直肠癌患者的5年生存率仍不超过50%,Ⅳ期更是低于10%[3]。
新辅助化疗(Neoadjuvant chemotherapy)是指对结直肠癌患者在手术之前给予全身化疗,已作为结直肠癌的主要治疗手段之一。
1989年,Wilke[4]等报道了新辅助化疗在进展期胃癌患者中的应用。
随着大规模的研究和临床应用,目前新辅助化疗已应用于多种肿瘤,并取得肯定疗效,成为综合治疗重要的组成部分。
1新辅助化疗的概念新辅助治疗(neoadjuvant therapy)是指针对局部晚期的结直肠癌患者或伴同时性肝转移的患者术前采用的治疗方法,包括新辅助化疗(neoadjuvant chemotherapy,NC)、新辅助放疗(neoadjuvant radiotherapy)和新辅助放化疗(neoadjuvant chemoradiotherapy)。
NC是其中最常用的一种,可以不同程度地减轻肿瘤负荷,降低肿瘤临床分期。
因此,近年来NC在结直肠癌中的应用已受到越来越多的重视。
2新辅助化疗的可行性新辅助化疗的作用原理:①减低肿瘤负荷,降低肿瘤分期,使不能切除的肿瘤变为可以切除,提高治愈性、手术切除率[5];②控制微小及潜在的转移灶,减少术中播散及术后转移复发,清除肝内的微小转移灶[6];③防止术后肿瘤血供改变以致影响化疗效果,效果优于术后;④可使手术时肿瘤细胞增殖能力处于最低状态,减少术中癌细胞医源性播散;⑤在化疗敏感性试验中,有助于了解肿瘤对化疗药物的敏感性,有利于术后化疗药物的选择,以指导制定术后治疗计划,并可协助判断预后[7];⑥对于伴有肝转移的患者,使不可切除的患者变为可切除,并且减少肝脏的切除范围,最大限度的保留肝体积[8]。
结肠癌最新化疗方案

结肠癌最新化疗方案结肠癌是一种常见的消化系统恶性肿瘤,其发病率和死亡率在全球范围内均呈上升趋势。
针对结肠癌的治疗手段不断演进,化疗作为结肠癌综合治疗的重要组成部分,也在不断创新和改进。
本文将介绍结肠癌最新的化疗方案,以期提供参考和指导。
一、术前化疗术前化疗是指在结肠癌手术前进行的化疗治疗。
这种治疗方案的目的是通过减小肿瘤体积,缩小肿瘤边缘,达到手术切除的目的。
目前,广泛采用的术前化疗方案是FOLFOX方案,即同时使用氟尿嘧啶、奥沙利铂和亚叶酸钙。
该方案在多项临床试验中表现出较好的疗效和耐受性。
二、术后化疗术后化疗是指在结肠癌手术后进行的辅助化疗治疗。
其主要目的是杀灭和抑制术后微小残留癌细胞,预防癌细胞复发和转移。
常用的术后化疗方案包括CAPOX方案和FOLFOX方案。
前者是指使用氟尿嘧啶、奥沙利铂和卡培他滨进行化疗,后者与术前化疗方案相同。
三、个体化化疗个体化化疗是指根据患者结肠癌的分子特征和药物敏感性,进行个体化针对性的化疗方案。
目前,个体化化疗在结肠癌治疗中越来越受关注。
例如,一些针对KRAS突变阳性患者的药物已得到临床应用,如带铂类药物和EGFR抑制剂的联合应用。
此外,DNA修复缺陷患者也可选用PD-1/PD-L1免疫疗法。
四、靶向治疗靶向治疗是指通过作用于癌细胞特定的分子靶点,抑制肿瘤生长和扩散的治疗手段。
在结肠癌最新的化疗方案中,靶向治疗起到了重要作用。
EGFR抑制剂和血管生成抑制剂是常用的靶向治疗药物。
使用单抗结合化疗药物,可提高化疗的疗效。
五、免疫治疗免疫治疗是近年来结肠癌治疗领域的新进展。
通过激活患者自身免疫系统,增强抗肿瘤免疫应答,进而达到治疗结肠癌的效果。
PD-1/PD-L1免疫检查点抑制剂是目前最常用的免疫治疗药物。
临床试验表明,与传统化疗方案相比,免疫治疗在一些结肠癌患者中表现出更好的疗效和耐受性。
综上所述,结肠癌最新的化疗方案包括术前化疗、术后化疗、个体化化疗、靶向治疗和免疫治疗等多种手段。
结肠癌肿瘤分期与术后辅助治疗

结肠癌肿瘤分期与术后辅助治疗结肠癌是一种常见的恶性肿瘤,临床上常采用肿瘤分期来确定患者的病情和预后,并选择合适的治疗方案。
目前,最常用的肿瘤分期系统是美国癌症学会(AJCC)和国际癌症联盟(UICC)联合发布的TNM分期系统。
该系统基于肿瘤的深度侵犯、淋巴结转移和远处转移三个方面来评估患者的肿瘤分期。
结肠癌的分期一般分为0期到Ⅳ期,其中0期是指癌前病变,一般不需要进行手术治疗,而Ⅰ~Ⅳ期则是需要进行手术治疗的阶段。
Ⅰ~Ⅱ期是结肠癌的早期,一般通过手术切除肿瘤,达到根治目的。
此外,对于Ⅱ~Ⅲ期的患者,术后辅助治疗也是必不可少的。
术后辅助治疗是指手术切除肿瘤后,在恢复期结束后给予的一种治疗方法。
术后辅助治疗的主要目的是降低复发率和提高患者的生存率。
根据患者的具体情况,术后辅助治疗可以包括化学治疗、放射治疗和靶向治疗等。
化学治疗是目前最常用的术后辅助治疗方法之一。
通过给予化疗药物,可以清除残留的癌细胞,减少复发的风险。
化疗药物可以根据患者的分期和个体化情况进行选择,一般常用的有5-氟尿嘧啶、奥沙利铂等。
化学治疗的疗程一般为6个月,通过连续多个周期的治疗,可以有效地降低癌细胞的存活率,并达到控制肿瘤复发的目的。
放射治疗是通过应用高能射线照射肿瘤部位,杀死癌细胞或阻止其生长和扩散。
对于结肠癌来说,放射治疗主要用于Ⅲ~Ⅳ期患者术前辅助治疗,目的是缩小肿瘤的体积,提高手术切除的可行性。
术后,放射治疗一般不是主要的辅助治疗方式,但在某些特殊情况下仍然可以考虑应用。
靶向治疗是近年来快速发展的一种治疗方法,通过干扰肿瘤的生长信号通路,抑制癌细胞的生长和扩散。
对于结肠癌来说,最常用的靶向治疗药物是靶向表皮生长因子受体(EGFR)抑制剂和血管内皮生长因子(VEGF)抑制剂。
靶向治疗的优势在于可以减少化疗的毒副作用,提高患者的生存率。
但靶向治疗并不适用于所有患者,需要根据具体情况进行选择。
总的来说,结肠癌的肿瘤分期和术后辅助治疗是密切相关的。
肠癌(新)辅助化疗进展

60 T2-T3 Capecitabine
pCR% 19 34 29 25 37 28.3
1 Rodel C, et al. Journal of Clinical Oncology. 2003; 21: 3098-3104. 2 Valentini V, et al. Proc Am Soc Clin Oncol. 2002;21: 151A. 3 Aschele C, et al. Proc Am Soc Clin Oncol. 2002; 21: 132A. 4 Mitchel EP, et al. Proc Am Soc Clin Oncol. 2003; 22: 262A,.
Yu BM, et al. Chinese Journal of Practical Surgery. 2005;25(5):270-2
结肠癌的辅助治疗
静脉推注5-FU/LV曾经是III期 结肠癌的标准辅助治疗
DFS (%)
OS (%)
Study
Regimens
Patients 5-FU/LV Control 5-FU/LV Control
5'-DFCR CyD
5'-DFUR
5'-DFUR 胸苷磷酸化酶 (TP)
5-FU
5'-DFCR = 5’-脱氧-5-氟胞嘧啶核苷; 5'-DFUR = 5-脱氧-5氟嘧啶; CyD =胞嘧啶脱氨酶; CE =羧酸脂酶
卡培他滨治疗结直肠癌理论基础
卡培他滨是口服, 肿瘤内激活的氟尿嘧啶氨基甲酸酯 1 卡培他滨已经成为晚期结直肠癌的一线治疗药物 NCCN指南推荐卡培他滨为结直肠癌单药一线治疗药物 10例患者中有9例更愿意口服治疗2 门诊患者口服化疗,方便患者过正常的生活 卡培他滨一线治疗较5-FU/LV静脉给药治疗反应更好,安
Nature Cancer:突破!新方法将结肠癌细胞转变为正常细胞
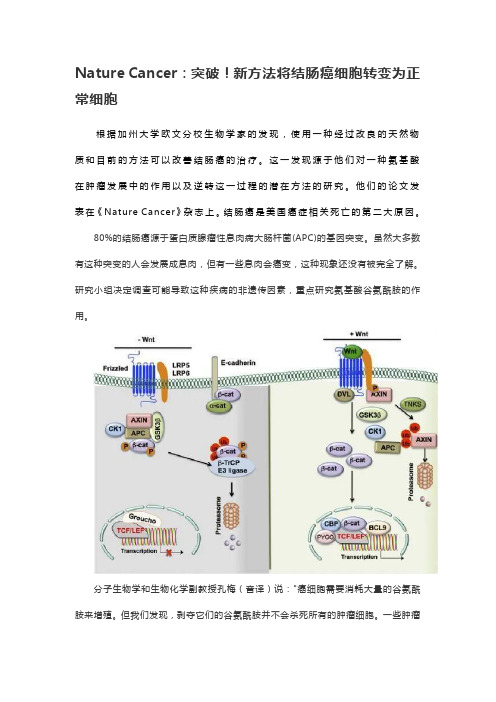
Nature Cancer:突破!新方法将结肠癌细胞转变为正常细胞根据加州大学欧文分校生物学家的发现,使用一种经过改良的天然物质和目前的方法可以改善结肠癌的治疗。
这一发现源于他们对一种氨基酸在肿瘤发展中的作用以及逆转这一过程的潜在方法的研究。
他们的论文发表在《Nature Cancer》杂志上。
结肠癌是美国癌症相关死亡的第二大原因。
80%的结肠癌源于蛋白质腺瘤性息肉病大肠杆菌(APC)的基因突变。
虽然大多数有这种突变的人会发展成息肉,但有一些息肉会癌变,这种现象还没有被完全了解。
研究小组决定调查可能导致这种疾病的非遗传因素,重点研究氨基酸谷氨酰胺的作用。
分子生物学和生物化学副教授孔梅(音译)说:"癌细胞需要消耗大量的谷氨酰胺来增殖。
但我们发现,剥夺它们的谷氨酰胺并不会杀死所有的肿瘤细胞。
一些肿瘤细胞能够适应,事实上,当它们的谷氨酰胺供应不足时,它们就会变成一种更具侵袭性的癌症。
"研究人员发现,在谷氨酰胺饥饿后,细胞代谢物-酮戊二酸水平的下降伴随着良性细胞向癌细胞的转变。
这一发现促使他们进一步研究代谢物的作用。
当他们为APC 突变的动物模型提供修改版的酮戊二酸时,结果是显着的。
只有23%的接受了这种改良代谢物的小鼠出现了直肠出血,这是肠道肿瘤的一种迹象,而没有接受这种代谢物的小鼠有90%出现了直肠出血。
它还能抑制肿瘤生长,防止体重减轻等疾病相关症状。
该论文的第一作者Thai Q. Tran说:"补充经过修饰的酮戊二酸盐可抑制结肠癌细胞中一个关键的癌症发展信号通路,使它们变成更正常的细胞。
同样值得注意的是,我们将它与饮用水混合使用,所以服用起来很容易,也不会影响整体健康。
"研究小组希望进一步研究代谢产物的修饰,以明确针对结肠癌细胞。
孔教授说:"我们相信,这项新发现显示出,使用毒性更小、更天然的方法,结合目前的治疗方法,可以更成功地治疗结肠癌,同时更好地保护患者的整体健康,具有巨大的潜力。
结直肠癌黏液腺癌临床病理及治疗进展2024(全文)

结直肠癌黏液腺癌临床病理及治疗进展2024(全文)结直肠癌(colorectal cancer,CRC)是全球范围内的一种常见恶性肿瘤,流行病学数据表明全球CRC总体发病率已经升至第三位,也是癌症相关死亡的第二大原因[1]。
在CRC中,黏液腺癌(mucinous carcinoma,MC)是非特异性腺癌(adenocarcinoma not otherwise specified,AC)中一个独特的组织亚型,其特点是细胞外黏液占肿瘤体积50%以上。
一、黏液腺癌临床病理特征统计数据表明,MC发病率具备一定地域差异,MC的发病率从亚洲国家的3.9%到欧美国家的10%~13.6%不等[2]。
通过对发病部位的研究发现,MC在近端结肠的发病率显著高于直肠或远端结肠。
针对相同部位肿瘤进行分层分析后发现,MC常发现于疾病进展期[3]。
对这一现象有两种假说。
其一可能与MC中黏液蛋白物理特性相关,MC中黏液蛋白基因MUC2的过度表达和抑癌基因转录因子HATH1沉默密切相关,与AC中的表达趋势相反[4]。
染色体不稳定可能是MC疾病快速进展的另一种机制,相对于AC,MC出现微卫星不稳定性(microsatellite instability,MSI)频率更高。
高MSI发生率在Lynch综合征患者中也可以观察到,这表明MC与AC可能具备不同的致癌途径[5]。
MC与AC的转移模式存在明显差异,AC常见远处转移器官为肝脏,而MC更容易出现腹膜转移,且MC术后淋巴结阳性率高于AC。
转移模式差异的原因目前认为与黏液组分密切相关[6]。
正常黏液与肠道微生物构成了菌群生物膜。
MC中菌群生物膜的失调导致肠道上皮通透性增强,黏液组分会由肠道向腹腔内移动,导致肿瘤的腹膜转移及对邻近脏器侵犯[7]。
另外,菌群生物膜将诱导肠道炎症反应。
炎症反应导致大量细胞因子的产生,如TNF-α、IL-22,研究表明此类细胞因子促进肿瘤细胞的黏液分泌。
例如,TNF-α处理的结肠癌细胞ATOH1蛋白的稳定性增强,进而促进黏液分泌。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
结肠癌辅助治疗突破进展,轰动全球!
这研究结果,还真是结肠癌辅助治疗的重磅炸弹啊……记者丨Joy来源丨医学界肿瘤频道
如果说美国临床肿瘤学会(ASCO)和欧洲肿瘤内科学会(ESMO)一年一度的学术大会是全球肿瘤学界的“两会”,那么由中国临床肿瘤学会(CSCO)联合ASCO共同举办的Best of ASCO(BOA)event in China绝对是我国临床肿瘤学者自己的饕餮盛会,也是每年盛夏里的一块学术绿荫。
今儿会议第一天,《医学界》记者就在现场感受到了极其热烈的学术讨论氛围。
在胃肠肿瘤专场的报告中,中山大学附属肿瘤医院陈功教授和浙江大学附属邵逸夫医院潘宏铭教授主要围绕今年ASCO上万众瞩目的焦点——IDEA研究进行了详细的分析评述。
随后的讨论环节,更有解放军八一医院全军肿瘤中心秦叔逵教授、中山大学肿瘤防治中心院长徐瑞华教授发表精彩观点,内容绝对有料!
IDEA研究为啥这么火?
首先,IDEA研究坐拥全球12个国家1w+例超大样本量,成为迄今为止肿瘤学领域最大样本数的前瞻性荟萃分析,在胃肠肿瘤领域几乎是空前绝后。
其次,IDEA研究对结肠癌现行标准辅助治疗发起了挑战,
旨在评估III期结直肠癌FOLFOX(氟尿嘧啶,亚叶酸钙,奥沙利铂)/CAPOX(卡培他滨,奥沙利铂)方案辅助化疗3个月的疗效是否非劣效于6个月术后标准辅助治疗。
虽然从统计学角度分析其主要研究终点(DFS)3个月非劣效于6个月为阴性结果,但3个月组患者与6个月组患者的3年生存率仅相差0.9%。
所以,IDEA研究结果一发布就引起全场轰动,成为大家关注的焦点。
而且近10年来,结直肠癌辅助化疗领域一直没有突破性的进展,再基于当前方案神经毒性较明显、患者依从性较差的情况,IDEA研究必将对今后的临床实践产生重大影响。
IDEA研究基本情况
研究背景:对于III期或高危II期的结肠癌患者,6个月的含奥沙利铂方案是当前的标准辅助化疗方案。
但由于奥沙利铂累积性的外周神经毒性,临床实践中的完成度不佳,所以疗效差别不大的情况下缩短疗程可减轻毒性,降低治疗费用,更好的节约资源。
研究方法:该研究为开放的多中心III期研究。
自2007年6月~2015年12月共纳入12834例III期结肠癌患者,1:1随机分配至3个月或6个月组,研究者自行选择FOLFOX或CAPOX方案,研究的主要终点为3年无病生存时间(DFS),预设的分层因素包括治疗方案和T/N分期,非劣效设计边界
为3个月DFS HR<1.12。
主要研究结果:
·3个月治疗组的DFS为74.6%,6个月治疗组为75.5%,绝对差值仅为0.9%。
预计DFS HR=1.07(95%CI 1.00-1.15),超过预设边界值1.12,非劣效不成立。
·3个月治疗组比6个月治疗组的依从性更高:FOLFOX DFS HR=1.16 (95%CI 1.06-1.26) ;CAPOX DFS HR=0.95 (95% CI 0.85-1.06) 。
·3个月治疗组相关神经毒性较6个月治疗组低2倍以上:FOLFOX(17% vs 48%);CAPOX(15% vs 45%)。
IDEA临床专家共识:低危人群推荐3个月辅助化疗,高危人群推荐6个月辅助化疗,同时考虑患者耐受性、个人意愿、复发风险以及药物方案(CAPEOX 或FOLFOX)。
对此,IDEA临床专家主要考量了以下因素:
①临床治疗决策中应考虑不同疗程DFS潜在损失和减少(神经)毒性之前的权衡;
②虽然3年DFS是总生存的有效替代终点,仍需要长期总生存数据来充分证明这一结果;
③由于每个IDEA试验组中使用CAPOX方案的患者比例不同(0-75%),方案疗程的交互作用可能导致在各个研究组观察到不同的结果;
④由于IDEA研究设计时不是为了比较不同方案间的DFS,
患者选择何种方案也不是随机化的,因此在比较FOLFOX和CAPOX方案的DFS时有潜在的选择偏倚影响;
⑤两种方案的不同表现可能源于化疗方案的给药方式和间隔的不同,这需要进一步的研究。
陈功教授:IDEA研究开创III期结肠癌辅助化疗新纪元IDEA 给我们带来的临床启示是——III期结肠癌奥沙利铂辅助化
疗的最佳疗程值得关注,该研究中3个月与6个月的非劣效终点未达到,但两组间的实际差值非常小,短疗程带来的安全性即毒副反应的改善是明显的,所以我们要认真平衡缩短疗程后潜在的DFS受损与显著的患者安全性改善。
陈功教授表示,IDEA研究开创了III期结肠癌辅助化疗新纪元,将会改变他的临床实践。
不仅要将国际上的这些信息与患者进行沟通,充分了解其治疗意愿,还要将III期结肠癌患者进一步危险度分层:
低危:T1-3N1,T1-2N2(Ⅲa,部分Ⅲb);高危:T4(尤其T4b),T3以上且N2(部分Ⅲb,Ⅲc)。
再基于“危险度+耐受性+治疗意愿”的个体化辅助化疗模式,推荐:
·低危患者3个月疗程治疗(如果治疗意愿强烈、耐受性好,可以延长到6个月);
·高危患者6个月疗程治疗(如果耐受性差或毒性大,充分知情后选择短疗程);
·对于具体方案的选择(CAPOX vs FOLFOX),暂不改变既往的选择标准。
秦叔逵教授:IDEA研究对我来说更多的是教训
在会议的讨论环节,秦叔逵教授从研究本身出发,和大家分享了他的一些思考和看法:“我认为IDEA研究是个‘三差’研究,哪三差呢?首先是研究设计差,它开始于10年前,设计非常粗糙,与今日的研究水平不可同日而语;再就是样本质控差,IDEA研究包含了6个相关研究,跨国家跨种族,均衡性较差;最后是研究结果差,没有达到预设的研究结果,从统计学角度看是阴性结果。
”
秦教授认为,IDEA研究不能改变我们的临床实践,虽然引发了我们对标准化疗方案的思考,并提出根据不同危险分层选择治疗方案,但是在精准医学时代,我们不仅要考虑肿瘤分期,还要评估其分子分型以及基因组学等因素。
而且该研究耗时耗资巨大,但从设计到结果的分析都出现了很多问题,也是一种资源的浪费,需要以为戒,并作更多思考。
徐瑞华教授:仁者见仁,智者见智徐教授最后总结道:“IDEA 研究确实引起了我们很多的关注和争议,但就目前的政策的限制以及各国治疗情况来看,我们很难再组织一个这么大的研究,可是只有这样的研究才有可能回答我们临床上遇到的问题,所以它值得我们尊敬。
”
“而且,IDEA研究确实带来了不错的数据,低危患者3个
月治疗组和6个月治疗组的3年DFS分别为83.1%、83.3%,仅提高0.2%;高危患者分别为62.7%、64.4%,差距也不是很明显。
”所以徐瑞华教授强烈推荐,低危患者接受3个月疗程的治疗,高危患者经过具体分析后再做决定。
(本文为医学界肿瘤频道原创文章,转载需经授权并标明作者和来源。
)。
