[医学]第八章 B核磁共振谱
第八章 B核磁共振谱ppt课件

⑤采用噪声去偶可去掉所有1H对13C的偶合,每个碳出一 个峰。 ⑥DEPT技术使连有奇数质子与连有偶数质子13C峰 分开。
1-庚炔
2-己炔
1,7-辛二炔
1-氟代戊烷 异戊醛
1-氯代戊烷
乙基乙烯基酮 乙酸丁酯 乙酸酐 2-氯代丙酰氯
α-甲基丙烯酸乙酯 丁酰胺 正丁苯
丙胺 3-甲基-1-乙基苯
1,3-二乙基苯
4-甲基苯乙酮
4-甲氧基苯乙烯
4-乙基苯乙酮
4-硝基苯酚
3-乙氧基苯甲醛
正庚烷
顺-2-庚烯
反-2-庚烯
2-甲基-1-庚烯
4.谱图解析
(1).先看有几组峰,确定化合物有几种氢核。
(2).从积分线确定各组质子个数比。 (3).从偶合裂分情况判断各组质子间的相互作用。
例1:CH3CH2CH2NO2的NMR谱。
例2:CH3CH2OH的NMR谱。
通常,只有相邻碳上1H才相互偶合。
1,1,2-三溴乙烷
(乙) 解析实例 例1:C3H7Cl的NMR。
h E H 0 2
当用频率为ν 的电磁波照射处于磁场的样品时,如果 hν =Δ E, 电磁波被吸收,核从 α 态跃迁到 β 态,这样就 产生了核磁共振吸收,用仪器记录下来就是核磁共振 谱(NMR)。
注:
1.对1H、13C来讲,没有外磁场时,两种自旋 方向不同核能级相同。
rh H E 2.产生核磁共振的条件是:h 0 2 即 H0 2
CHBr2 a
ý Ö È Ø å · ¨1H£ £ ©
CH2Br b
« å Ë · ¨2H£ £ ©
å µ · Ä Á Ñ · Ö
CHBr2-CH2Br中质子的偶合及峰的裂分: a b
核磁共振谱学

1991年,Wü thrich开创了生物大分子NMR领域,维特里希因“发明了 利用核磁共振技术测定溶液中生物大分子三维结构的方法”并获得 2002年的诺贝尔化学奖。
一. 核磁共振基本原理
1.1 核磁共振三要素
1. 磁性核
核磁共振的研究对象:磁性核。
磁性核:具有磁矩的原子核。
磁矩是由于核的自旋运动产生的。
在一定温度下,原子核处在高、低能级的数目达到热力学 平衡,原子核在两种能级上的分布应满足Boltzmann分布:
n 1
2 2
n 1
n
1 +2
e
E
kT
:低能态的核数
n
1 -2
:高能态的核数
k : Boltzmann 常数
T : 热力学温度
当H0 = 1.409 T(相当于60MHz的射频) 温
γhB0/2π。用一个频率为ν的射频 场(电磁波)照射磁场中的
自旋核时,如果电磁波的能量hν与该能级差相等,即 E=hν=ΔE=γ hB0/2π ν= γ · B0/2π
低自旋能态的核即可吸收电磁波的能量而跃迁到高自旋能态,
同时自旋取向发生改变,即发生核磁共振。
共振条件: = B0 / 2
1.2 屏蔽原理和化学位移
1.2.1 屏蔽原理
在外磁场B0作用下,核外电子云产生一个感生磁场,方向与
Bo相反,强度与 Bo成正比。它使原子核实际感受到的外磁场 强度减小,称为电子屏蔽效应。感生磁场的大小用s .B0表示, s称为屏蔽常数。
s的大小与核外电子云的密度有关。核外电子云密度越大, s就越大,s .B0也就越大。在B0中产生的与B0相对抗的感生磁场
• 去屏蔽作用使得质子共振需要的磁场强度变小,吸收峰移 向左侧(低场)。
核磁共振谱

例:无色,只含碳和氢的化合物
谱上的共振信号位置反映样品分子的局部结构(例如官能 团,分子构象等); 信号强度则往往与有关原子核在样品中存在的量有关; 目前常用的磁场强度下测量NMR所需照射电磁波落在射 频区(60-600MHz)。 NMR谱是由具有磁矩的原子核,受电磁波辐射而发生跃 迁所形成的吸收光谱。 电子能自旋,质子也能自旋,原子的质量数为奇数的原子 核,如1H、13C、19F、31P等,由于核中质子的自旋而在沿 着核轴方向产生磁矩,因此可以发生核磁共振。
图6 甲醇(CH3OH)的核磁共振谱
2. 化学位移
由于化合物分子中各种质子受到不同程度的屏蔽效应, 因而在NMR谱的不同位置上出现吸收峰,但这种屏蔽效应所 造成的位置上的差异是很小的,难以精确地测出其绝对值, 因而需要用一个标准来作对比,常用四甲基硅烷((CH3)4Si) 作为标准物质,人为将其吸收峰出现的位置定为零。某一质 子吸收峰出现的位置与标准物质质子吸收峰出现的位置之间 的差异作为该质子的化学位移,常以“δ”表示。
例如:用核磁共振方法测定重水中的H2O的含量,
D2O和H2O的化学性质十分相似,但两者的核磁共
振频率却相差极大。因此核磁共振法是一种十分敏
感而准确的方法。 (2)对于同一种核,γ值一定。 因此当外加磁场一定时,共振频率也一定;当 磁场强度改变时,共振频率也随之改变。
例如:氢核在1.409T的磁场中,共振频率为60MHz, 而在2.350T时,共振频率为100MHz。
E
H 0
I
由于I=1/2,则
E 2H 0
式中μ 为自旋核产生的磁矩
图3 在外磁场作用下,核自旋能级的裂分示意图
核磁共振谱光谱解读

第八章核磁共振谱光谱学习要求:1、学会如何借助光学技术来分析化合物的结构。
2、掌握谱图分析,了解各种质子化学位移的位置。
3、知道影响化学位移的因素。
由上面的讨论可知,对于一个未知物,红外光谱可以迅速地鉴定出未知物分子中具有的哪些官能团,能指出是什么类型的化合物,但它难以确定未知物的精细结构。
自20世纪50年代中期,核磁共振技术开始应用于有机化学,对有机化学产生了巨大的影响,已发展成为研究有机化学最重要的工具之一,成为有机化合物结构测定不可缺少的手段。
8.1基本原理(1)核磁共振现象核磁共振是由原子核的自旋运动引起的。
不同的原子核,自旋运动的情况不同,它们可以用核的自旋量子数I来表示。
核的自旋量子数与原子的质量数和原子序数之间存在着一定的关系:当原子的质量数和原子序数两者之间是奇数或两者均为奇数时,I≠0,该原子核就有自旋现象,产生自旋磁矩。
如等。
当原子的质量数和原子序数均为偶数时,I=0,原子核不能产生自旋运动,也没有磁矩,如等。
当I≠0的原子核置于一均匀的外磁场(H O)中时,核的自旋具有(2I+1)个不同的取向。
对于氢原子核(I=1/2),其自旋产生的磁矩在外磁场中可有两种取向:一种是与外磁场方向相同,称为顺磁取向。
该取向的磁量子数m=+1/2,或用α表示。
另一种是与外磁场方向相反,称为反磁取向。
该取向的磁量子数m=-1/2,或用β表示。
反磁取向的能量较顺磁取向的能量高,这两种取向的能量差⊿E与外加磁场的强度成正比。
⊿E=式中h为普朗克常量,γ为核常数,称为核磁比。
对于氢原子,γ=26750。
以上关系如图9-28所示。
不过即使在很强的外加磁场中,⊿E数值也很小。
对于氢原子核,当H0=14092G(高斯,1G=10-4T)时,⊿E仅为2.5×10-5kJ/mol,当H0=23468G时,⊿E约为4×10-5kJ/mol,相当于电磁波谱中射频区的能量。
若外界提供电磁波,其频率适当,能量恰好等于核的两个自旋能级之差,hγ=⊿E则此原子核就可以从低能级跃迁到高能级,发生核磁共振吸收。
核磁共振谱

常见:氢谱(1H NMR)、碳谱(13C NMR)
8.1.2 化学位移
根据核磁共振基本原理,核磁共振只能区分不同元素 的核。
如,H0=1.4092T时,
1H
的共振频率为60 MHz
13C
的共振频率为15.1 MHz
实际情况并非如此!!! 例如:乙醇的氢谱中有三个共振吸收峰。
乙醇的核磁共振氢谱
化学位移:由于化学环境的差异而引起的同类磁核在核磁 共振中出现不同共振信号的现象。
2. 磁性核在外磁场(B0)中的行为
原子核在外磁场中的自旋取向和能级裂分 核在外磁场中的取向是空间方向量子化的。相对于外磁场 方向,可以有(2I + 1 )种取向。
磁量子数m=I,I-1,…,-I,可取2I+1个不同数值。
磁矩μ与H0之间的相互作用能为:
E = -μH0cosθ θ为磁矩μ与外磁场H0之间的夹角 原子核的不同取向就代表了不同的能级 I = 1/2的核,
H C O C Hb CH3 CH3 a
a
> b
a < b
a < b < c
•
下面化合物中所标出的质子其1H NMR化学位移从低场
到高场的顺序为(
O
)
CH3CH2C O CH2CH3 a b c d
c 、 b 、d 、a
(2) 磁的各向异性效应
化合物中非球形对称的电子云,如:π电子系统,因
电子的流动将产生一个小的诱导磁场,这个磁场是一个 各向异性的磁场。也就是说,在不同的区域,磁场方向 不一致,对处于其中的氢核产生的影响是不同的。
低场
高场
• 横坐标为化学位移值,代表谱峰位臵—化学环境 • 台阶状的积分曲线高度表示对应峰的面积。在1H谱中与 相应的质子数目成正比—氢的数目 • 谱峰呈现出的多重峰形是自旋-自旋耦合引起的谱峰裂 分—耦合作用
核磁共振谱学8 PPT课件
y
tD
x
y
y
x
(b)
去偶
(a)
tD
x
y
x
y x
现在我们取不同tD值,可以得到不同的信号强度。对CH2和CH3,分析是相 似的。
CH
CH2
tD= 1 / 2J
tD= 1 / J
tD= 1 / 2J
tD
tD
tD= 1 / J
CH3
tD= 1 / 2J
tD= 1 / J
最基本也是最简单的脉冲序列是通常的1D-1H谱所采用的单脉冲序列:
矢量形式:
z
Mo
y
x 90y pulse
y
z
x
Mxy
acquisition
简化形式:
90y
90y
n
1D-13C谱中的质子宽带去偶谱和门控去偶谱也属单脉冲序列实验。
质子宽带去偶谱 f
tD 13C:
{1H} 1H:
反门控去偶谱
tD
tD
{1H} 1H:
APT实验,是早期的多脉冲序列之一,f(<90)脉冲使部分磁化矢量留在+z 方向,下一个180脉冲使其翻转到-z方向,-180-脉冲单元是为了把-z方 向的磁化矢量翻转到+z方向。为接收机恢复所设置。
实验时,tD设为1/J。该实验的成功之处在于其结果对tD=1/J的条件不敏感, 即允许JCH有一定的取值范围。至于如何区分季碳和CH2,CH和CH3,则比较 麻烦。现在APT已由DEPT序列所取代。
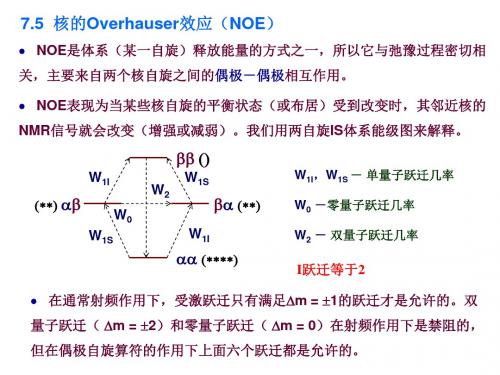
W1I
(**) ab
W0 W1S
bb ()
W2 W1S
ba (**)
第八章红外光谱和核磁共振氢谱IRandHNMR

4 、红外光谱仪和红外光谱图
红外光谱仪组成:光源、单色器、检测器、放大器和记录器 横坐标: 数() 纵坐标: 度( A ) 吸收图谱: cm-1 ) 透
过 率 %
上线:波长() 右側:透过率( T% )
波长 λ/μm -1 指纹区( 1400-400cm )
下线:波 左侧:吸光 官能团区( 4000-1400
- 1
, RCOCl/~1800 cm - 1 ,因氯有强的吸电子诱导效应。
③ 减弱键强度的共轭效应能使吸收向低频移动。如: CH3COCH =CH2 中 C=O 的吸收峰 1720 cm - 1 移至 ~1685 cm - 1 , C=C 的吸 收峰由 1647 cm - 1 移至 1623 cm - 1 。
波数 /cm-1
二、有机基团的特3000c m-1 O-H 3600~3200 N-H 3500~3100 C-H 3300~2700 三键或累积 双键吸收区 2400 ~ 1950 cm - 1 C=C 2260~2100 C=N 2400~2100 C=Y=Z ~1950 C=X 双键振动 区 1800 ~ 1300 cm - 1 C=O 1800~1650 C=C 1690~1600 芳环 1600 ~ 1 450 C=N 1960~1460 δN-H 1650~150 0 δC-H 1475~130 0 指纹区 C - X 伸缩或弯曲振动 区 1300 ~ 600 c m-1 C-O 1300~1000 C-N 1360~1030 C-C 1200~600 δ=C-H 1000~650
影响化学键和基团特征吸收频率的因素 ① 键的力常数 k 越大,红外吸收频率越大。如:炔键 /2150 cm -
1
, C=C /1650 cm - 1 , C - C /1200cm - 1 。
有机化合物波谱解析智慧树知到答案章节测试2023年重庆医科大学

绪论单元测试1.本课程学习的四大谱主要是哪四类?A:质谱 (Mass Spectra, 简称MS)B:核磁共振谱 (Nuclear Magnetic Resonance Spectra,简称NMR)C:紫外-可见光谱(Ultraviolet-visible Absorption Spectra,简称UV)D:红外光谱(Infrared Spectra, 简称IR )答案:ABCD2.凡是合成、半合成药物或者是由天然产物中提取的单体或组分中的主要组分,都必须确证其化学结构。
A:错B:对答案:B3.确证结构的方法主要有两种:第一,可以采用经典的理化分析和元素分析方法;第二,目前国内外普遍使用的红外、紫外、核磁和质谱四大谱解析,必要时还应增加其他方法,如圆二色散、X光衍射、热分析等。
A:错B:对答案:B4.红外光谱特别适用于分子中功能基的鉴定。
A:错B:对答案:B5.核磁共振谱对有机化合物结构的解析非常有用,应用在四大谱中最为广泛。
A:对B:错答案:A第一章测试1.在关于紫外光谱正确的是()。
A:紫外光谱也叫振-转光谱B:紫外光谱是电子能级跃迁,不涉及振动能级和转动能级的跃迁C:紫外光谱能级跃迁需要吸收0.5―1eV能量D:紫外光谱属于电子光谱答案:D2.丙酮的紫外-可见光区中,对于吸收波长最大的那个吸收峰,在下列四种溶剂中吸收波长最短的是哪一个()。
A:水B:甲醇C:乙醚D:环己烷答案:A3.分子的紫外-可见吸收光谱呈带状光谱,其原因是什么()。
A:分子电子能级的跃迁伴随着振动、转动能级的跃迁B:分子中价电子运动的离域性质C:分子中价电子能级的相互作用D:分子振动能级的跃迁伴随着转动能级的跃迁答案:A4.在下列化合物中,哪一个在近紫外光区产生两个吸收带()。
A:丁二烯B:环己烷C:丙烯醛D:丙烯答案:C5.在化合物的紫外吸收光谱中K带是指()。
A:共轭非封闭体系π→π的跃迁B:σ→σ跃迁C:n→σ跃迁D:共轭非封闭体系n→π的跃迁答案:A6.紫外光谱一般都用样品的溶液测定,溶剂在所测定的紫外光谱区必须透明,以下溶剂可适用于210 nm的是()A:乙醇B:环己烷C:丙酮D:正己烷答案:B7.某化合物在正己烷中测得λmax = 305 nm,在乙醇中测得λmax = 307 nm,请指出该吸收是由下述哪一类跃迁类型所引起的?()A:n→π*B:n→σ*C:σ→σ*D:π→π*答案:D8.在环状体系中,分子中非共轭的两个发色团因为空间位置上的接近, 发生轨道间的交盖作用, 使得吸收带长移, 同时吸光强度增强。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2.化学位移
化学位移是由核外电子的屏蔽而引起的。
有机分子的氢核被电子云包围着。电子云在外加磁场H0 的作用下,产生一个外加感应磁场ΔH0,多数情况下,感应 磁场的方向与外磁场相反,氢核实际感应的磁场为:(H0ΔH0)。由于不同质子所处周围的电子的密度不同,它们实 际感受到的磁场也不相同,发生的共振频率也不相同。
通常用化学位移来表示质子共振吸收相对位置。
试样TMS106 0
ν试样 试样共振频率频率 νTMS 四甲基硅烷的共振频率 ν0 操作仪器选用频率
影响化学位移的因素:
A.电负性影响:取代基的电负性越大,相应碳上 质子的化学位移越大。 B.磁各向异性效应:
自旋偶合和自旋裂分
1.定义:
自旋偶合:指自旋核受邻近自旋核所产生的感应磁场影响 的现象。
1,3-二乙基苯
4-甲氧基苯乙烯
4-硝基苯乙醚
4-硝基苯酚
4-甲基苯乙酮
4-乙基苯乙酮
4-乙氧基苯甲醛
13C 谱简介
①13C 丰度低(1.1%),磁距小,灵敏度仅为1H的 1/5700。 ②13C对1H的偶合可忽略,但1H对13C的偶合较复杂。 ③化学位移在0~240ppm之间变化,很少有谱线重叠 现象。 ④摄谱时间长,几分钟到几天。 ⑤采用噪声去偶可去掉所有1H对13C的偶合,每个碳出一 个峰。 ⑥DEPT技术使连有奇数质子与连有偶数质子13C峰 分开。
(苯氢)
O
CH2CH2O C CH3
bc
d
a
(与氧原子相连 的亚甲基氢)
(与羰基相连 的甲基氢)
(4).谱图分析举例
正庚烷
顺-2-庚烯 反-2-庚烯 2-甲基-1-庚烯 顺,反-2,4-己二烯
2-甲基-1-丁烯-3-炔 1-庚炔 2-己炔 1,7-辛二炔 2-氯丁烷 1-碘丁烷 1-氟代戊烷 1-氯代戊烷
Cl2C C( H2 O C3 C H )2H C2l CHC2 H C3 ( H )2OCH C3H C2H OCH-2CC3HH
Cl
Cl Cl
A
B
C
ab c d Cl2CHCH(OCH2CH3)2
(B)
例4:芳香酮C8H7ClO的NMR谱。
O C CH3 Cl
(连在羰基上)
例5:指出C6H5CH2CH2OCOCH3的NMR谱图中各峰的归 属。
场强度H0成正比。
E
h
2
H0
当用频率为ν的电磁波照射处于磁场的样品时,如果 hν=ΔE,电磁波被吸收,核从α 态跃迁到β 态,这样就 产生了核磁共振吸收,用仪器记录下来就是核磁共振 谱(NMR)。
注:
1.对1H、13C来讲,没有外磁场时,两种自旋 方向不同核能级相同。
2即.产生核2磁H共0振的条件是:h2rhH0 E
顺,反-2,4-己二烯
2-甲基-1-丁烯-3-炔
1-庚炔
2-己炔
1,7-辛二炔
2-氯丁烷
1-碘丁烷
1-氟代戊烷
1-氯代戊烷
1-己醇
甲丁醚
异戊醛
乙基乙烯基酮
丁酸
α-甲基丙烯酸乙酯
乙酸丁酯
乙酸酐
2-氯代丙酰氯
丙酰胺
丁酰胺
丙胺
异丙苯
正丁苯
3-甲基-1-乙基苯
两个自旋核相距越远,偶合常数越小,超过三个 碳就可忽略不计。
3.一级谱的特点
一级谱是指Δν>6J时,是简单的一级谱。
特点:
(n+1)规律——一个信号被裂分的数目取决于相邻碳上1H 的数目,如果相邻碳上有n个氢,则该信号被裂分为(n+1) 重峰。裂分峰强度比符合二项式展开系数比,可由巴斯卡 三角形求得。
1-己醇 甲丁醚 异戊醛 乙基乙烯基酮
丁酸 α-甲基丙烯酸乙酯 乙酸丁酯 乙酸酐 2-氯代丙酰氯
丙酰胺 丁酰胺 丙胺
异丙苯 正丁苯
3-甲基-1-乙基苯
1,3-二乙基苯 4-甲氧基苯乙烯 4-硝基苯酚
4-甲基苯乙酮 4-乙基苯乙酮
3-乙氧基苯甲醛
正庚烷
顺-2-庚烯
反-2-庚烯
2-甲基-1-庚烯
第八章 B核磁共振 谱
某些质量数或原子序数为奇数的原子核,其自旋量子 数 不 为 零 。 其 中 1H 、 13C 、 19F 、 31P 核 的 自 旋 量 子 数 I=1/2,它们在磁场中有两种自旋方向。
与外磁场方向相同的自旋能级较低(α ) 与外磁场方向相反的自旋能级较高(β)
分子的二能级差用ΔE表示,ΔE与外磁
自旋裂分:指自旋偶合引起的谱线增多的现象。
CaHBr2 CHb2Br
Èý ÖØ · 壨1H£© Ë« · 壨2H£©
· å µÄ ÁÑ · Ö
CHBr2-CH2Br中质子的偶合及峰的裂分:
a
b
Ha
Hb
H0
Jab Jab
Jab
峰强度 1 : 2 :1
1 :1
2.偶合常数
自旋裂分谱线之间的距离称为偶合常数。一般用J 表示,单位Hz。J=ΔS×ν0(ν0为仪器固有频率, ΔS 为两条谱线化学位移差值)。 常见有邻碳偶合、同碳偶合和远程偶合。
µ¥ · å
1
¶þ ÖØ · å
11
Èý ÖØ · å 1 2 1
ËÄ ÖØ · å 1 3 3 1
Îå ÖØ · å 1 4 6 4 1
注 意:
① 相互偶合的两组峰的外形特点是“中间高,两边低”; ② 等价质子间不发生峰的裂分。
例如:CH3CH3的NMR只有一个单峰。 ClCH2CH2Cl的NMR只有一个单峰。
1,1,2-三溴乙烷
(乙) 解析实例 例1:C3H7Cl的NMR。
a bc CH3CH2CH2Cl
例2:下列谱图是否 Cl
Cl
OCH3 的NMR?
Cl
与氧原子相 连的甲基氢
δ3.9(单峰) -OCH3
苯氢
δ6.7~7.3 苯环氢
所以,该图是2,3,4-三氯苯甲醚的NMR。
例3:下图与A、B、C哪个化合物的结构符合?
③ (n+1)规律只适用于一级谱((△ν/J)>6)。
4.谱图解析
(1).先看有几组峰,确定化合物有几种氢核。 (2).从积分线确定各组质子个数比。 (3).从偶合裂分情况判断各组质子间的相互作用。
例1:CH3CH2CH2NO2的NMR谱。
例2:CH3CH2OH的NMR谱。 通常,只有相邻碳上1H才相互偶合。
