铝及其重要化合物
铝的化合物

镁及其重要化合物之间的转化
MgCl2
③ ② ① ④ ⑥ ⑤
Mg →
MgO → Mg(OH)2
⑦
① 2Mg + O2 == 2MgO
② Mg + 2HCl==MgCl2+ H2↑ 电解 ③ MgCl2 ==== Mg+ Cl2↑
思考: 不加其它试剂,仅用试管和胶头滴管能否 鉴别下列两种溶液:
NaOH和AlCl3 滴加顺序不同,产生现象不同。 Al3++4 OH-= AlO2-+2H2O Al3+ + 3 AlO2-+6H2O = 4Al(OH)3↓
3、硫酸铝钾 KAl(SO4)2
复盐: 由两种不同的金属离子和一种酸根离子组 成的盐。 KAl(SO4)2· 12H2O 俗名明矾 或K2SO4•Al2(SO4)3•24H2O
⑶化学性质 a、两性
Al(OH)3+3HCl= AlCl3+3H2O
Al(OH)3+3H+= Al3+ +3H2O Al(OH)3 +NaOH=NaAlO2+2H2O
Al(OH)3 + OH-=AlO2-+2H2O
像Al(OH)3这样既能与酸反应生成盐和水, 又能与碱反应生成盐和水的氢氧化物,称为两 性氢氧化物。 注意:Al(OH)3不能溶于较弱的酸和弱碱
0 2 5 8 9 10 NaOH的物质的量
由此可知,该溶液中肯定含有 的阳离子是 H+ 、Al3+、NH4+ 各离子物质的量之比是 2:1:3 2+、Fe3+ Mg 肯定不含的阳离子是 。
沉 淀 物 质 的 量
0 2
5 8 9 10 NaOH的物质的量
O→A: 沉 A→B: 淀 物 B→C:
质 的 量
高考化学总复习 第二节 铝及其重要化合物课件 新人教
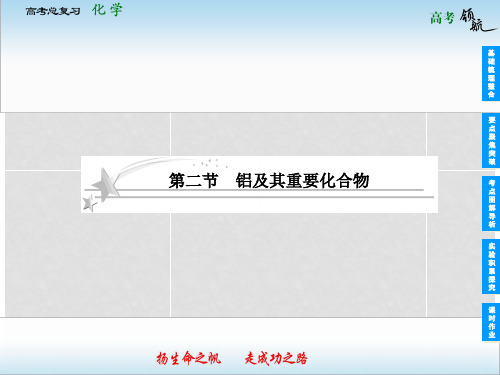
生成H2的关系
导 析
实
验
积
累
探
究
课 时 作 业
基 础 梳 理 整 合
等量
足量
n(HCl)(H2)=32n(Al),n(NaOH)(H2)=32n(Al)
要 点 聚 焦 突
破
n(HCl)(H2)∶n(NaOH)(H2)=1∶1
考
点
二者等物 足量
n(HCl)(H2)=12n(HCl) n(NaOH)(H2)=32
图 解 导 析
质的量 n(NaOH) n(HCl)(H2)∶n(NaOH)(H2)=1∶3
实 验
积
累
探
究
课 时 作 业
基
1.(2012 年临沂模拟)将 5.4 g 金属 Al 投入 200.0 mL 2.0 mol·L-1
础 梳 理
整
的某溶液中有氢气产生,充分反应后有金属剩余。该溶液可能为 合
焦 突
破
明矾的化学式为 KAl(SO4)2·12H2O,可溶于水,电离方程式为 考
点
KAl(SO4)2===K++Al3++2SO42- ,明矾可用于净水,其净水的原理
图 解
导
用离子方程式表示为 Al3++3H2
3(胶体)+3H+,产生的 析
实
Al(OH)3 胶体可以和悬浮于水中的泥沙形成絮状不溶物而沉降下来,
突
ห้องสมุดไป่ตู้
破
2.化学性质
考
点
图
解
导
析
实
验
积
3.用途
累 探
究
熔点 高 ,是一种较好的 耐火 材料,天然产刚玉的成分是
课
Al2O3,还可制作各种宝石。
铝及其重要化合物-必刷题(新教材新高考)(解析版)

专题10铝及其重要化合物(建议完成时间:45分钟实际完成时间:_______分钟)目录考点一铝及其化合物的结构、性质及其应用考点二铝及其化合物制备的工艺流程考点三铝及其化合物与强酸、强碱反应有关计算考点一铝及其化合物的结构、性质及其应用1(2023·江苏·统考二模)下列物质的性质和用途具有对应关系的是A.Al2O3熔点高,可用作电解制铝B.Al OH3不稳定,可用于治疗胃酸过多C.明矾水解生成胶体,可用做絮凝剂D.铝具有导热性,可用于制备铝热剂【答案】C【解析】A.Al2O3熔融可以电解生成铝单质,可用作电解制铝,而不是因为其熔点高,物质的性质和用途不具有对应关系,A不符合题意;B.Al OH3能和胃酸盐酸反应,可用于治疗胃酸过多,物质的性质和用途不具有对应关系,B不符合题意;C.明矾水解生成胶体从而吸附水中悬浮物加速沉降用于净水,可用做混凝剂,物质的性质和用途具有对应关系,C符合题意;D.铝具有还原性能还原一些金属氧化物,可用于制备铝热剂,物质的性质和用途不具有对应关系,D不符合题意;故选C。
2(2023·广东·广州市第二中学校联考三模)下图为铝的生产原理示意图,下列相关说法不正确的是A.冰晶石做助熔剂B.氧化铝属于过渡晶体C.金属铁、铜的冶炼方法与铝类似D.铝在工业上是一种很好的还原剂【答案】C【解析】A.冰晶石在电解铝工业中常用作助熔剂,正确;B.氧化铝的晶体结构具有某些过渡金属的特征,因此被称为过渡晶体,正确;C.工业上用电解熔融的氧化铝,得到金属铝和氧气,而工业上用热还原法来冶炼金属铁、铜,错误;D.Al为活泼金属,冶金工业中常作还原剂,正确;故选C。
3(2023·上海黄浦·一模)去了膜的铝条放入硫酸铜溶液中,不可能观察到的现象A.金属表面有气泡B.银白色金属转变为紫红色C.出现蓝色沉淀D.溶液蓝色变浅【答案】C【解析】A.硫酸铜溶液由于是强酸弱碱盐溶液,故Cu2+水解使溶液显酸性,把去了膜的铝条放入硫酸铜溶液中,会生成氢气,金属表面产生气泡,A不合题意;B.由2Al+3CuSO4=Al2(SO4)3+3Cu可知,银白色金属转变为紫红色,B不合题意;C.由2Al+3CuSO4=Al2(SO4)3+3Cu可知,不会出现蓝色沉淀,C符合题意;D.由2Al+3CuSO4=Al2(SO4)3+3Cu可知,溶液蓝色变浅,D不合题意;故答案为:C。
高考化学一轮复习 铝及其重要化合物第二课时 ppt
【例2】将100 mL amol/L的NaOH溶液滴加到100mL bmol/L的
AlCl3溶液中,试推导a与b的关系,并计算能得到Al(OH)3的物质 的量。 [解析]1. 此时必须注意整个反应过程中的现象: 将NaOH溶液滴入AlCl3 溶液中,开始时有沉淀生成,反应为 Al3++3OHˉ= Al(OH)3↓; 当溶液中Al3+全部转变为Al(OH)3沉淀后,继续加入NaOH,沉 淀将溶解,其反应为Al(OH)3+OHˉ=AlO2ˉ+2H2O。 2.当n(OHˉ) = 3n(Al3+)时,Al3+恰好完全转变为Al(OH)3沉淀,沉 淀达到最大值。
(2)化学性质:
a)两性氢氧化物
b)不稳定,受热易分解:2Al(OH)3→Al2O3+3H2O 讨论:氢氧化铝能否溶于氨水?为什么?实验室如 何制备氢氧化铝? (3)制备:
当加入弱酸或弱碱时,因H+或OH—浓度 太小,不足以使上述平衡移动,因此Al(OH)3 只溶于强酸或强碱,而不溶于弱酸或弱碱。 应用:实验室用可溶性的铝盐和氨水反 应制取氢氧化铝。
本课小结
1、氧化铝
2、氢氧化铝
3、Al3+ 和AlO2-
4、方法“铝三角”、“线型学铝”
(酸式电离)
Al(OH)3
Al3++3OH—
(碱式电离)
其电离程度相当微弱,加入强碱(或强 酸)时,大量的H+ (或OH—)才能破坏氢氧化 铝的电离平衡,使平衡向右(或向左)移动, 生成铝盐(或偏铝酸盐),所以氢氧化铝既具 有碱性,又具有酸性。
归纳:氢氧化铝Al(OH)3
(1)物理性质:不溶于水的白色胶状固体 。
高中化学铝及其重要化合物

非氧化性酸 2Al+6H+==2Al3++3H2
3.用途 纯铝用作导线,铝合金用于制造汽车、飞机、生活用品等。
返回导航页
结束放映
【思考与探究】
1.金属铝是活泼的金属,能与酸反应,为什么能用铝槽储 运浓H2SO4或浓HNO3? 常温下浓H2SO4、浓HNO3能使铝钝化(在表面形成一层致密 的氧化膜),阻止反应的继续进行。
(3)制得Al(OH)3的最大质量是________。
返回导航页
结束放映
考点三 用数形结合思想理解Al3+、Al(OH)3、AlO2-之间转化 量的关系
【知识梳理】 1.用转化图探究Al3+、AlO、Al(OH)3的转化关系
写出转化(2)、(5)、(6)离子方程式:
返回导航页
结束放映
2.用数轴探究可溶性铝盐与强碱(如NaOH溶液)反应,铝元 素的存在形式
(1)Al3++4OH-===AlO+2H2O 3AlO+Al3++6H2O===4Al(OH)3↓
(2)
返回导航页
结束放映
题型一
【题型建模】
1.下列各组物质,前者逐滴滴加到后者中直至过量,先出
现白色沉淀,后来沉淀又消失的是( A )
A.H2SO4滴入NaAlO2溶液中 B.Ba(OH)2溶液滴入Al2(SO4)3溶液中 C.Al2(SO4)3溶液滴入NaOH溶液中 D.氨水滴入Al2(SO4)3溶液中
【思考与探究】 1.下列变化可通过一步化学反应直接完成的是___①_____。 (1)Al(OH)3→Al2O3 (2)Al2O3→Al(OH)3 (3)Al→Al(OH)3 2.既能与盐酸反应,又能与NaOH溶液反应的物质有哪些?
3_2《铝及其重要化合物》(新人教版必修1)

第2讲 铝及其重要化合物[考纲要求] 理解铝及其重要化合物的主要性质和应用。
1.铝的结构和存有铝位于元素周期表第三周期ⅢA 族,原子结构示意图为。
铝元素在地壳中含量丰富,仅次于硅。
自然界中的铝全部以化合态存有。
2.金属铝的物理性质银白色有金属光泽的固体,有良好的延展性、导电性和传热性等,密度较小,质地柔软。
3.金属铝的化学性质写出图中相关反应的化学方程式或离子方程式:①Al O2⎪⎪⎪⎪――→ 常温 形成致密的氧化膜――→ 点燃 4Al +3O2=====点燃2Al2O3②2Al +3Cl2=====点燃2AlCl3 ③Al 酸⎪⎪⎪⎪――→氧化性酸遇冷的浓硫酸或浓硝酸钝化――→非氧化性酸2Al +6HCl===2AlCl3+3H2↑④2Al +2NaOH +2H2O===2NaAlO2+3H2↑⑤2Al +Fe2O3=====高温Al2O3+2Fe(铝热反应)4铝 镁 与非金属反应能被Cl2、O2氧化 2Mg +O2=====点燃2MgO 3Mg +N2=====点燃Mg3N2 与水反应 反应很困难 能与沸水反应Mg +2H2O=====△Mg(OH)2+H2↑与碱反应能溶于强碱溶液 不反应 与某些氧化物反应 能与Fe2O3、MnO2、Cr2O3等金属氧化物发生铝热反应 能在CO2中燃烧:2Mg +CO2=====点燃2MgO +C5.铝的用途纯铝用作导线,铝合金用于制造汽车、飞机、生活用品等。
深度思考1.铝的化学性质活泼,为什么日常生活中广泛使用的铝制品通常具有较好的抗腐蚀性能? 答案 铝在常温下迅速被氧气氧化,形成一层致密的氧化膜,保护铝不再被氧化,因而铝制品通常具有较强的抗腐蚀性能。
2.金属铝是活泼的金属,能与酸反应,为什么能用铝槽储运浓H2SO4或浓HNO3?答案 常温下浓H2SO4、浓HNO3能使铝钝化(在表面形成一层致密的氧化膜),阻止反应继续实行。
3.实验室能否用硫化物与铝盐溶液混合制取Al2S3?用离子方程式说明原因。
第三章第2节 铝及其重要化合物 (共73张PPT)

解析:Al(Mg) 淀。
NaOH 过量CO ――→ NaAlO2溶液 ――→ 2 Al(OH)3沉 溶液过滤 过滤
牢记1种地壳中含量最多的金属元素 Al。 熟记2种两性化合物 Al2O3、Al(OH)3。 掌握3种制备Al(OH)3的方法 Al3++3NH3· H2O===Al(OH)3↓+3NH4+, AlO2-+CO2(足量)+2H2O===Al(OH)3↓+HCO3-, Al3 +3AlO2 +6H2O===4Al(OH)3↓。
12H2O 明矾的化学式为 KAl(SO4)2·
,可溶于水,电离方
程式为 KAl(SO4)2===K++Al3++2SO42-。 明矾可用于净水,其原因是 Al 水解产生Al(OH)3胶体, Al(OH)3胶体可以和悬浮于水中的泥沙形成絮状不溶物而
沉降下来,使水澄清
3+
。
[特别提醒]
(1)Al(OH)3是不溶于水的白色胶状物质,能
知识点二
铝的重要化合物
1.氧化铝 (1)物理性质 大 高 色态: 白色固体 ;硬度: ;熔点: (2)化学性质 ①两性 +===2Al3++3H O Al O + 6H 2 与强酸反应: 2 3 与强碱溶液反应: Al2O3+2OH-===2AlO2-+H2O 。
。
,
+ -
掌握8个化学方程式 ①2Al+6H ===2Al3 +3H2↑,
+ +
②2Al+2OH +2H2O===2AlO2 +3H2↑, 高温 ③2Al+Fe2O3=====2Fe+Al2O3, ④Al2O3+6H ===2Al3 +3H2O,
[特别提醒] (1)铝制品表面的氧化膜起着保护内 部金属的作用,所以铝制品在空气中能稳定存 在,具有很强的抗腐蚀性。 (2)常温下,铝遇浓硝酸、浓硫酸会在表面生成 致密的氧化膜而发生钝化,从而阻止内部金属 进一步发生反应。因此可用铝制容器盛放和运 输浓H2SO4、浓HNO3。 (3)铝和氢氧化钠溶液的反应,还原剂是铝,氧 化剂是水而不是NaOH。
(完整版)铝及其重要化合物

铝及其重要化合物一、铝1.物理性质:银白色有金属光泽的固体,有良好的延展性、导电性和传热性等,密度较小,质地柔软。
2.化学性质:(1)与非金属单质的反应:①铝与O 2反应:Al+3O 22Al 2O 3(在纯氧中,剧烈燃烧,发出耀眼的白光)②铝与S 反应:2Al+3SAl 2S3③铝与Cl 2反应:2Al +3Cl 2=====点燃2AlCl 3(2)与金属氧化物的反应(铝热反应):2Al+Fe 2O 32Fe+Al 2O 3 ;4Al+3MnO 23Mn+2Al 2O 3(3)铝与非氧化性酸反应:2Al + 6HCl =2Al Cl 3 + 3H 2↑ 2Al + 3H 2SO 4 =Al 2(SO 4)3 + 3H 2↑(4)铝与氧化性酸反应:遇冷的浓硫酸或浓硝酸钝化。
在加热条件下可与浓硫酸、浓硝酸反应但无H 2产生。
(5)铝与氢氧化钠溶液的反应:铝和碱溶液反应,不是直接和碱反应,而是铝先和强碱溶液中的水反应生成Al(OH)3,然后Al(OH)3再和强碱反应生成偏铝酸盐。
2Al +6H 2O=2Al(OH)3+3H 2↑, Al(OH)3+NaOH=2NaAlO 2+2H 2O总反应化学方程式为:2Al +2H 2O +2NaOH=2NaAlO 2+3H 2↑,其中氧化剂只是H 2O ,而不是NaOH 。
3.制备:工业上采用电解法:2Al 2O 3=====电解4Al +3O 2↑4.用途:纯铝用作导线(不能用作电缆线),铝合金用于制造汽车、飞机、生活用品等。
二、氧化铝(1)物理性质:高熔点,高沸点,高硬度,难溶于水的白色固体。
(2)化学性质:氧化铝难溶于水,却能溶于酸或强碱溶液中。
Al 2O 3 + 6HCl =2AlCl 3 + 3H 2O Al 2O 3 + 2NaOH = 2NaAlO 2 + H 2O因此说Al 2O 3是两性氧化物(既能与酸反应生成盐和水,又能与碱反应生成盐和水的金属氧化物。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
铝及其重要化合物1.下列叙述不正确的是()A.铝制容器可盛装冷的浓硫酸B.用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-===2AlO-2+H2OC.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化D.日用铝制品表面覆盖着氧化膜,对内部金属起保护作用,所以能用铝制容器存放盐酸解析:选D。
铝在冷浓硫酸中发生钝化。
Al2O3能溶于NaOH溶液,生成偏铝酸盐;明矾净水的原理是Al3+水解生成Al(OH)3胶体,利用Al(OH)3胶体的吸附性进行净水;铝表面生成致密的氧化膜Al2O3,其熔点高,难熔化,起保护作用,但存放盐酸时,会与酸反应,即D项不正确。
2.铝是一种低毒金属元素,它并非人体需要的微量元素,不会导致急性中毒,但食品中铝的含量超过国家标准就会对人体造成危害。
下列关于铝元素的说法正确的是() A.铝在空气中不易氧化是因为其性质不活泼B.氢氧化铝可与胃酸反应,常用作中和胃酸的药物C.明矾可用于饮用水的杀菌消毒D.硫酸铝铵常用作面粉膨化剂,该物质不溶于水解析:选B。
铝在空气中会与O2反应生成致密的氧化物薄膜,A项错误;C项中明矾溶于水生成Al(OH)3胶体,具有吸附杂质的性能,通常用作净水剂,但不能用于杀菌消毒;铵盐都溶于水,D项错误。
3.(2013·哈尔滨高三模拟)下列有关铝及其化合物的叙述正确的是()A.铝粉与氧化镁共热可制取金属镁B.足量铝分别与含1 mol HCl、1 mol NaOH的溶液反应,产生相同量的氢气C.工业上用电解熔融Al2O3的方法冶炼铝D.在浓硝酸中加入等体积的浓硫酸后,立即加入铝片,铝片表面发生钝化解析:选C。
Mg的活泼性强于铝,因而A项不能发生反应;B项后者产生的H2多;D 项不再发生钝化,因为浓H2SO4稀释后会释放出大量的热,而热的浓HNO3与铝会发生反应。
4.(2013·黄冈高三模拟)等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出氢气最多的是()A.2 mol·L-1H2SO4溶液B.18 mol·L-1H2SO4溶液C.6 mol·L-1KOH溶液D.3 mol·L-1HNO3溶液解析:选A。
Mg、Al都可与稀H2SO4反应放出H2,但遇浓H2SO4时Al在常温下发生钝化,Mg虽反应但不产生H2。
与KOH只有Al反应。
Mg、Al都与HNO3反应,但HNO3为强氧化性酸,都不会产生H2。
5.下列各组物质,前者逐滴滴加到后者中直至过量,先出现白色沉淀,后来沉淀又消失的是()A.H2SO4滴入NaAlO2溶液中B.Ba(OH)2溶液滴入Al2(SO4)3溶液中C.Al2(SO4)3溶液滴入NaOH溶液中D.氨水滴入Al2(SO4)3溶液中解析:选A。
将H2SO4滴入NaAlO2溶液中,先生成Al(OH)3沉淀,Al(OH)3又溶于过量的H2SO4中,A正确;Ba(OH)2滴入Al2(SO4)3溶液中,先生成BaSO4、Al(OH)3沉淀,而Al(OH)3又溶于Ba(OH)2,但BaSO4不溶解,B错误;Al2(SO4)3滴入NaOH溶液中,开始由于OH-过量发生Al3++4OH-===AlO-2+2H2O,故开始无沉淀生成,C错误;氨水滴入Al2(SO4)3溶液中,立即产生Al(OH)3沉淀,但沉淀不溶于过量氨水,D错误。
6.(2013·南京高三模拟)在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液,直至过量。
下列表示氢氧化钠加入量(x)与溶液中沉淀的量(y)的关系示意图中正确的是()解析:选C。
向混合溶液中加入NaOH溶液的过程中,Mg(NO3)2会生成难溶物Mg(OH)2,Al(NO3)3会生成难溶物Al(OH)3,随着NaOH溶液的加入,Al(OH)3逐渐溶解,而Mg(OH)2不能溶解。
7.将2.7 g Al与100 mL 2 mol/L H2SO4溶液充分反应后,再慢慢滴入25 mL 4 mol/L NaOH溶液,其结果是()A.所得溶液的pH<7B.溶液中有较多Al(OH)3沉淀C.取少量所得溶液,加NaHCO3,无明显现象发生D.另取少量所得溶液,加入几滴浓NaOH溶液,无明显变化解析:选A。
先求出各物质的物质的量,然后按照反应先后写出反应式,根据反应式求解。
特别注意反应的先后,NaOH遇到H2SO4和Al2(SO4)3,先发生酸碱中和反应,然后才有沉淀反应。
8.(2013·辽宁五校高三教学质量检测)将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1 mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是()A.原合金质量为0.92 gB.标准状况下产生氢气896 mLC.图中m值为1.56 gD.图中V2为60 mL解析:选C。
由已知可得反应过程为钠与水反应生成氢氧化钠,铝与氢氧化钠溶液反应生成偏铝酸钠,因溶液pH为14,则说明氢氧化钠过量,滴加盐酸后先与氢氧化钠反应,再与偏铝酸钠反应生成氢氧化铝沉淀,继续滴加盐酸,则氢氧化铝沉淀溶解。
当沉淀量最大时溶液中只有氯化钠,n(Na+)=n(Cl-)=1 mol·L-1×0.04 L=0.04 mol,即合金中钠的物质的量为0.04 mol,与水反应生成0.04 mol NaOH,由合金全部溶解后的溶液为20 mL,pH=14,可知铝与氢氧化钠反应后过量的氢氧化钠为0.02 mol,则反应的氢氧化钠为0.02 mol,铝的物质的量也是0.02 mol,所以原合金的质量为0.92 g+0.54 g=1.46 g。
0.04 mol钠与水反应生成0.02 mol氢气,0.02 mol 铝与氢氧化钠溶液反应生成0.03 mol 氢气,故标况下体积为1 120 mL,B错误。
沉淀量最大时生成氢氧化铝的质量为0.02 mol×78 g·mol-1=1.56 g,C 正确。
0.02 mol氢氧化铝完全溶解需1 mol·L-1的HCl 60 mL,则V2=100 mL,D错误。
9.某校化学兴趣小组用如图所示过程除去AlCl3中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失。
请回答下列问题:(1)写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:_____________________________________________________________________、________________________________________________________________________、________________________________________________________________________。
氢氧化钠溶液________(填“能”或“不能”)用氨水代替,为什么?________________________________________________________________________ ________________________________________________________________________。
(2)溶液a中存在的离子有________________________________________________________________________;在溶液a中加入盐酸时需控制溶液的pH,为什么?_________________________________________________________________________;为此,改进方法是________________________________________________________________________ ________________________________________________________________________。
(3)为了研究AlCl3晶体的性质,在得到AlCl3溶液后,如何得到AlCl3晶体?________________________________________________________________________ ________________________________________________________________________。
解析:(1)加入足量氢氧化钠溶液,Mg2+可与OH-反应生成Mg(OH)2沉淀,Al3+与OH -反应生成AlO-2;氢氧化钠溶液不能用氨水代替,因为在Al3+与氨水反应生成Al(OH)3后,Al(OH)3不能与氨水继续反应,从而不能将Al(OH)3与Mg(OH)2分开;(2)加入氢氧化钠溶液后除去了Mg2+,但又引入了Na+,同时Al3+转化成了AlO-2;因为氢氧化铝能与强酸反应,所以在加入盐酸时,需要控制溶液的pH,以防止部分铝转化成Al3+;氢氧化铝只能与强碱或强酸反应,因此,可在溶液a中通入过量二氧化碳气体;(3)直接加热蒸发AlCl3溶液会因为AlCl3的水解而得不到AlCl3晶体,为此可在酸性气氛下进行蒸发结晶。
答案:(1)Mg2++2OH-===Mg(OH)2↓Al3++3OH-===Al(OH)3↓Al(OH)3+OH-===AlO-2+2H2O不能因为在Al3+与氨水反应生成Al(OH)3后,不能继续与氨水反应,不能将Al(OH)3与Mg(OH)2分开(2)K+、Cl-、Na+、AlO-2因为Al(OH)3能溶于强酸,所以需控制pH,防止部分Al(OH)3转化成Al3+在a溶液中通入过量CO2气体(3)在HCl气氛中对AlCl3溶液进行蒸发结晶10.对金属制品进行抗腐蚀处理,可延长其使用寿命。
以下为铝材表面处理的一种方法:(1)碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是________________________________________________________________________(用离子方程式表示)。
(2)为将碱洗槽液中铝以沉淀形式回收,最好向槽液中加入下列试剂中的________。
a.NH3b.CO2c.NaOH d.HNO3(3)若向碱洗槽液中加入过量的(2)中选择的试剂,试写出反应的离子方程式:________________________________________________________________________。
