燃料及燃烧基本理论解析
《燃料的燃烧》 讲义

《燃料的燃烧》讲义一、引言燃料的燃烧是我们日常生活和工业生产中不可或缺的一部分。
从家庭取暖、烹饪到汽车驱动、发电,燃料的燃烧为我们提供了能源和动力。
然而,燃烧过程并非简单的化学反应,它涉及到众多的物理和化学原理,以及对环境和能源利用的重要影响。
二、燃料的种类1、固体燃料常见的固体燃料包括煤炭、木材和生物质等。
煤炭是一种重要的化石燃料,其种类繁多,如无烟煤、烟煤和褐煤等。
不同种类的煤炭在热值、含碳量和杂质含量等方面存在差异。
木材作为一种传统的燃料,在一些地区仍然被广泛使用,但燃烧效率相对较低,且会产生较多的烟尘。
生物质燃料如秸秆、木屑等,具有可再生的特点,但也需要合适的燃烧技术来提高效率和减少污染。
2、液体燃料液体燃料主要有石油及其衍生品,如汽油、柴油和煤油等。
石油是一种复杂的混合物,通过精炼可以得到不同用途的液体燃料。
汽油通常用于轻型车辆,柴油则适用于重型车辆和工业设备。
此外,还有一些生物液体燃料,如生物柴油和乙醇,它们来自可再生资源,对环境相对友好。
3、气体燃料气体燃料包括天然气、液化石油气(LPG)和煤气等。
天然气是一种清洁高效的燃料,主要成分是甲烷。
LPG 通常由丙烷和丁烷组成,易于储存和运输。
煤气则是通过煤炭的气化过程产生的,但其使用范围相对较窄。
三、燃烧的基本原理1、燃烧的化学方程式燃烧是燃料与氧气发生的剧烈氧化反应。
以甲烷(CH₄)的燃烧为例,其化学方程式为:CH₄+ 2O₂ → CO₂+ 2H₂O +热量。
在这个过程中,燃料中的碳和氢与氧气结合,生成二氧化碳和水,并释放出大量的热能。
2、燃烧的条件燃烧需要同时满足三个条件:可燃物、助燃物(通常是氧气)和达到着火点的温度。
只有当这三个条件都具备时,燃烧才能发生。
例如,纸张是可燃物,在空气中(含有氧气),当受到足够高的温度(着火点)时,就会燃烧起来。
3、完全燃烧与不完全燃烧完全燃烧是指燃料中的碳和氢完全与氧气反应,生成二氧化碳和水,此时释放的热量最多,对环境的污染也相对较小。
燃料及燃烧2 燃烧计算及燃烧理论
Va0 VO0 2
100 8.9Car 26.7 H ar 3.3( Sar Oar )(Nm3 / kg) 21
洛阳理工学院
材料工程基础
②气体燃料
院系:材料科学与工程系
教师:罗伟
可燃组成有CO2、 CO、H2、CH4、CmHn、H2S、H2O、N2、O2(体积百 分含量)
0 百分含量,VO 和 VO0分别为生成RO2和H2O的需氧量( /m3) 2 2
0 0 (VO2 RO2 VO2 H 2 O ) O2
V
0 O2
RO2 V H 2 O
0 O2
令k
0 0 VO2 RO2 VO2 H 2O
RO2
K:单位燃料燃烧时的理论需氧量 与该烟气中RO2百分含量的比值。 组成变动不大的同种燃料的k值近 似为常数。列于表。
洛阳理工学院
材料工程基础
院系:材料科学与工程系
教师:罗伟
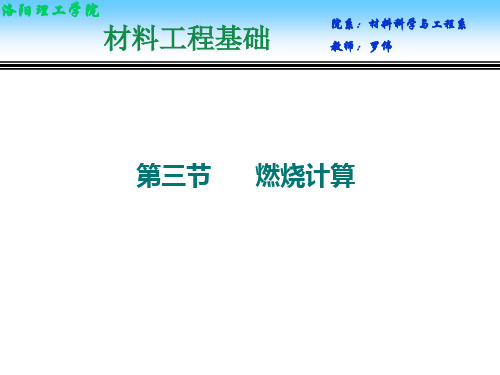
第三节
燃烧计算
洛阳理工学院
材料工程基础
院系:材料科学与工程系
教师:罗伟
在设计窑炉时(设计计算) 1、已知燃料的组成及燃烧条件, 2、需计算单位质量(或体积)燃料燃烧所需的空气量、烟气 生成量、烟气组成及燃烧温度 3、以确定空气管道、烟道、烟囱及燃烧室的尺寸,选择风机 型号。
CO2=
VCO2 0 V
0
×100(%)
洛阳理工学院
材料工程基础
② 气体燃料
院系:材料科学与工程系
教师:罗伟
可燃组成有CO2、CO、H2、CH4、CmHn、H2S、H2O、N2、O2(体积百 分含量)
CO + 1/2O2 → CO2 CO2 H2 + 1/2O2 → H2O CH4 + 2O2 → CO2 + 2H2O CmHn +(m+n/4)O2→ m CO2 + n/2 H2O 1Nm3 H2生成 1 Nm3 HO2 …… ...... 1Nm3 CO 生成 1 Nm3
燃料与燃烧知识点归纳.docx

第六章燃烧与燃料第一节燃烧与灭火一•燃烧的条件(重点)1 •燃烧:是可燃物跟氧气发生的剧烈的发光、发热的氧化反应。
(1)燃烧的现象:发光、发热,反应剧烈。
(2)燃烧的反应类型:氧化反应,不一定是化合反应。
(3)燃烧的反应物:常见的燃烧都是可燃物跟氧气发生反应,但是,不是所有的燃烧都一定有氧气参加。
例如,镁就能在二氧化碳中燃烧:2Mg+CO点燃C+2MgO钠能在氯气中燃烧:2Na+ Cl 2 点燃2 NaCl(4)燃烧的反应条件:点燃(5)燃烧的分类及燃烧的产物注意:①“完全燃烧”和“不完全燃烧”又叫“充分燃烧”和“不充分燃烧”②要掌握含C H 0等元素的燃料完全燃烧的化学方程式:2.燃烧的条件:①物质具有可燃性②可燃物要与氧气接触;③可燃物的温度达到其自身的着火点(即可燃物燃烧所需要的最低温度)燃烧必须要同时满足三个条件,才能发生燃烧的现象。
二.灭火的原理:①•移走可燃物可燃物②.隔绝氧气③•使温度降到着火点以下1 •灭火原理实质就是破坏物质燃烧的条件,三者破坏其一即可灭火。
2.几种常见的灭火方法:(1)移走可燃物可燃物:森林火灾开辟隔离带,管道煤气着火先关掉阀门,釜底抽薪等;(2)隔绝氧气:酒精灯用等冒盖灭,油锅着火用用锅盖盖灭,向着火的木柴上覆盖沙子,少量酒精燃烧用湿抹布盖灭等;(3)使温度降到着火点以下:用水等大量的冷却剂灭火,用嘴将灯吹熄,(4)用灭火器灭火:①泡沫灭火器:可用于扑灭木材、棉布等燃烧而引起的一般火灾,不能用于扑灭电器火灾;②干粉灭火器:除了用来扑灭一般火灾外,还用于扑灭电器、油、气等燃烧引起的火灾;③液态二氧化碳灭火器:用于扑灭图书档案、贵重设备、精密仪器的火灾。
3•二氧化碳与灭火(1)原理:二氧化碳不能燃烧也不能支持燃烧,且密度比空气大。
(2)灭火器主要是用二氧化碳灭火,二氧化碳不能扑灭所有的火灾:如镁带燃烧就不能用二氧化碳扑灭。
4火灾处置、自救(1)火警电话:119(2)电器、管道煤气、天然气着火,首先要关闭电源或气阀。
3 燃料与燃烧

87.91 5.49 5.49 0.55 0.55 100Car=Cad(100-Mar,f) 100Car=Cdaf(100-Mar-Aar) 其转化关系见表5-2(改错)
总量
100% 100% 100% 100%
材料工程基础-lvshuzhen
3.1.4 燃料有哪些热工性质?(掌握)
1、基本热工性质——发热量(简称:热值) 2、其它热工性质
3.1.1 燃料是如何分类的?(掌握) 3.1.2 燃料的组成有哪两种表示方法?其基准 内容 有哪些?各种基准之间如何换算?(掌握) 3.1.3 燃料有哪些热工性质?(掌握) 3.1.4 如何选择燃料?(了解)
材料工程基础-lvshuzhen
3.1.燃料的种类和组成
3.1.1 燃料是如何分类的?(掌握) 气体燃料:天然气、煤气、液化气等 液体燃料:汽油、煤油、柴油、重油 固体燃料:煤、柴禾等
根据化学反应计算空气量、烟气量、烟气组成 根据热平衡原理计算火焰温度 计算方法:分析计算法、近似计算法、操作计算法
材料工程基础-lvshuzhen
3.2.2.1 设计计算
分析计算法:已知燃料的种类和元素分析成分,通过化学 反应,根据质量守衡进行定量计算。 假定:
–气体的体积均以标准状态计算; –气体均为理想气体; –计算的基准温度为0℃; –计算时固体、液体燃料用收到基(ar),气体燃料用湿基 – 均在完全燃烧条件下计算空气量 ; – 空气由氧气和氮气组成,其体积百分比为21:79。
(2)实际空气量的计算(掌握)
Va Va0 1.2 5.08 6.09(Nm3 Kg)
例题
材料工程基础-lvshuzhen
(3)理论烟气量V0的计算(掌握)
理论烟气由以下两部分组成:
燃料及燃烧

理论燃烧产物量
(二)实际空气需求量和实际燃烧产物量的计算 实际空气需要量 实际燃烧产物量 (三)燃烧产物成分和密度的计算 1.燃烧产物成分 用
烟煤 :烟煤比褐煤炭化更完全,水分和挥发分进一步减少,固体碳 增加。低发热量较高;一般都在23000~29300千焦/千克。 作冶金炉燃料时,主要考虑的指标是:挥发分和发热量;灰分 含量及其熔点;含硫量;煤的粒度大小。 分类:长焰煤、气煤、肥煤、结焦煤、瘦煤。 无烟煤 :无烟煤是炭化程度最完全的煤,其中挥发分很少。无烟煤 挥发分少,燃烧时火焰很短,故在冶金生产中很少使用。焦炭缺乏 时,可用无烟煤暂代。
②氢(H): H 2 1 O2 H 2O(汽) 119915( KJ / Kg )
③氧(O):有害元素 ④氮(N):惰性物质
1 C O2 CO 10258( KJ / Kg ) 2
2
⑤硫(S):有害杂质。S
O2 SO2 409930 KJ
存在形式:有机硫,黄铁矿硫硫酸盐 ⑥水分(W):有害成分。水分来源:外部水、吸附水、结晶水。 ⑦灰分(A):
2.焦炭 要求:①化学成分 ②机械强度
③块度
④灰分 ⑤反应能力 3.粉煤 将块煤或碎煤磨至0.05~0.07毫米的粒度称为粉煤。
任务2 燃烧计算
一 概述 1.完全燃烧与不完全燃烧 燃料中的可燃物全部与氧发生充分的化学反应,生成不能 燃烧的产物,叫完全燃烧。 燃料的不完全燃烧存在两种情况: ①化学性不完全燃烧:燃烧时燃料中的可燃物质没有得到足 够的氧,或者与氧接触不良,因而燃烧产物中还含有一部分 能燃烧的可燃物被排走,这种现象叫化学不完全燃烧。 ②机械不完全燃烧:燃料中的部分可燃成分未参加燃烧反应 就损失掉的那部分。如灰渣裹走的煤,炉栅漏下的煤,管道 漏掉的重油或煤气。
燃料的燃烧

燃料的燃烧燃料的燃烧是可燃成分与氧气{主要是助燃空气中的氧气}所进行的一种激烈的氧化反应。
燃烧三要素:可燃物、着火温度。
氧气。
燃料的燃烧可分为完全燃烧与不完全燃烧。
完全燃烧:燃烧中的可燃物和氧化进行了充分的燃烧反应,燃烧产物中已不存在可燃成分,成为完全燃烧。
不全然冷却:燃料经过冷却后在冷却产物中存有着易燃成分,称作不全然冷却,他又分成化学不全然冷却和机械不全然冷却两种情况。
化学不全然冷却:冷却中的易燃成分由于空气中严重不足或燃料与空气混合不好,而没获得充份反应的冷却,称作化学不全然冷却。
机械不全然冷却:燃料中部分易燃成分没出席冷却反应就损失的冷却过程,称作机械不全然冷却。
可燃成分发生不完全燃烧的发热量远低于完全燃烧的发热量,因此在加热操作中应尽量避免不完全燃烧。
理论空气需要量:冷却中的易燃成分全然冷却须要存有一定量的空气,这种空气量叫作理论空气需要量。
空气消耗系数:燃烧在实际燃烧过程中,为了实现燃料的完全燃烧,实际空气需要量必须大于理论空气需要量,该实际空气需要量与理论空气需要量的比值就叫做空气消耗系数,一般用n表示。
空气消耗系数的大小与燃料的种类、燃烧方式、燃烧装置结构及工况好坏等有直接关系。
在实际加热操作中,应在保证完全燃烧的基础上使n越接近1越好。
各种燃料的空气消耗系数经验数据如下:固体燃料:n=1.20~1.50液体燃料:n=1.15~1.25气体燃料:n=1.05~1.15蓄热式加热炉由于可以实现贫氧燃烧(氮的氧化少,需要空气少),理论空气需要量可以笑与常规燃烧的理论空气需要量,具体数值依不同燃烧和不同燃烧方式而有所不同。
蓄热式加热炉空气消耗系数和常规燃烧的基本相同,及实际空气空气量与理论空气需要量的比值,前者大于后者主要保证完全燃烧。
冷却温度:冷却产物所能够达至的温度叫做燃料的冷却温度,又叫作火焰温度。
在全然冷却状态下午热损失的冷却温度及理论冷却温度。
提升加热炉冷却温度的途径存有:(1)提高燃烧的发热量(2)实现燃烧的完全燃烧(3)降低炉体热损失(4)预热空气和燃料(5)尽量减少烟气量。
燃烧的原理是什么
燃烧的原理是什么
燃烧的原理是指物质在氧气存在下,释放化学能量的过程。
燃烧通常涉及三个基本要素:燃料、氧气和燃烧温度。
燃料可以是固体、液体或气体,它与氧气发生反应,产生二氧化碳、水和能量。
燃烧的反应可以用简化的化学方程式表示:
燃料 + 氧气→ 二氧化碳 + 水 + 能量
在燃烧过程中,热能和光能被释放出来。
其中,热能是由于化学反应释放出的能量,导致气体和周围物质的温度升高。
光能则表现为火焰的亮度和颜色。
燃烧是一种氧化反应,也称为氧化燃烧。
燃料内部的化学键被氧气断裂,然后形成新的键以产生二氧化碳和水。
化学反应中,能量被吸收和释放。
在燃烧过程中,燃料的化学能转化为热能和光能。
燃料的燃烧需要满足三个条件:燃料、氧气和燃烧温度必须同时存在。
缺一不可。
燃烧过程可以是自然的,也可以通过外部提供燃烧物质和氧气来创造、控制。
燃烧在日常生活中具有广泛的应用,如烹饪、取暖、交通工具驱动等。
然而,燃烧也会产生烟雾、废气和温室气体等污染物。
因此,在燃烧过程中要采取控制措施,以减少对环境和健康的影响。
《燃料的燃烧》 讲义
《燃料的燃烧》讲义一、燃料的定义与分类在我们的日常生活和工业生产中,燃料扮演着至关重要的角色。
燃料,简单来说,就是能够通过燃烧过程释放出能量的物质。
根据其状态和来源的不同,燃料可以分为多种类型。
固体燃料是我们较为常见的一类,比如煤炭、木材等。
煤炭在过去的工业革命中发挥了巨大作用,至今仍是许多国家的重要能源之一。
木材则在一些农村地区或者特定的工业用途中被使用。
液体燃料包括石油及其衍生产品,如汽油、柴油、煤油等。
石油是现代交通和工业的血液,驱动着汽车、飞机、轮船等交通工具,也为许多工业生产提供了动力。
气体燃料主要有天然气、煤气等。
天然气是一种相对清洁的能源,在城市燃气供应和工业领域的应用越来越广泛。
二、燃料燃烧的条件要使燃料发生燃烧,必须同时满足三个条件:可燃物、助燃物(通常是氧气)以及达到可燃物的着火点。
可燃物就是能够燃烧的物质,不同的燃料其可燃性和燃烧特性各不相同。
助燃物一般是空气中的氧气,但在一些特殊情况下,其他气体也可以作为助燃物。
着火点则是燃料能够开始燃烧的最低温度,每种燃料都有其特定的着火点。
例如,纸张的着火点相对较低,而煤炭的着火点则较高。
只有当燃料达到了着火点,并且有充足的氧气供应,燃烧才能持续进行。
三、燃料燃烧的化学过程燃料的燃烧本质上是一种化学反应。
以碳的燃烧为例,当碳与氧气充分反应时,会生成二氧化碳:C + O₂= CO₂。
如果氧气不充足,则会生成一氧化碳:2C + O₂= 2CO 。
对于烃类燃料,如甲烷(CH₄),燃烧的化学方程式为:CH₄+2O₂= CO₂+ 2H₂O 。
在燃烧过程中,燃料中的化学键被打破,新的化学键形成,从而释放出能量。
这个化学过程中,燃料分子与氧气分子发生碰撞和相互作用,导致化学键的断裂和重组。
释放出的能量以热能和光能的形式表现出来。
四、燃料燃烧的效率燃料燃烧的效率是衡量燃料利用程度的重要指标。
影响燃料燃烧效率的因素有很多。
首先是燃料与氧气的接触面积。
燃料颗粒越小、表面积越大,与氧气的接触就越充分,燃烧效率也就越高。
燃料和燃烧原理共54页文档
E—反应活化能;
R—通用气体常数;
T—反应温度:
k—反应速度常数(浓度不变)。
阿累尼乌斯定律说明了燃料本身的“活性”与反应温度对化学反应速度的 影响的关系。
什么是燃料的“活性”呢?可以简单地理解为燃料着火与燃尽的难易程度。 例如,气体燃料比固体燃料容易着火,也容易燃尽。而不同的固体燃料, “活性”也不同,烟煤比无烟煤容易着火,也容易燃尽。因此,燃料的 “活性”也表现为燃料燃烧时的反应能力。燃料的“活性”程度可用“活 化能”来表示。
第一章 燃烧理论基础
二. 阿累尼乌斯定律
在实际燃烧过程中,由于燃料与氧化物 (空气)是按一定比例连续供给的,当混 合十分均匀时,可以认为燃烧反应是在反应物质浓度不变的条件下进行的.这 时,化学反应速度与燃料性质及温度的关系为:
式中,
k=k0e(-E/RT)
k数0 --相当于单位浓度中,反应物质分子间的碰撞频率及有效碰撞次数的 系
在燃料着火区,可燃物浓度比较高,而氧浓度比较低。 这主要是为了维持着火区的高温状态,使燃料进入炉内 后尽快着火。但着火区如果过分缺氧则着火就会终止, 甚至引起爆炸。因此在着火区控制燃料与空气的比例达 到一个恰到好处的状态,是实现燃料尽快着火和连续着 火的重要条件。反应物浓度对燃烧速度的影响关系比较 复杂,将在后面的内容中加以分析。
燃烧是一种发光发热的化学反应。燃烧速度可以用化学反应速度 来表示。
在等温条件下,化学反应速度可用质量作用定律表示,即反应速 度一般可用单位时间,单位体积内烧掉燃料量或消耗掉的氧量来表 示。 可用下面的式子表示炉内的燃烧反应:
aA+bB= gG+hH (燃料) (氧化剂) (燃烧产物) 化学反应速度可用正向反应速度表示,也可用逆向反应速度来表示。 即:
《燃料与燃烧》课件
如燃料的颗粒大小、密度、热导 率等,都会影响燃料的燃烧性能 。颗粒越小,比表面积越大,燃 烧越充分。
燃烧环境
氧气浓度
氧气是燃烧反应的必要条件,氧气浓 度越高,燃烧反应越剧烈。
环境温度
环境温度影响燃料的蒸发和热解,进 而影响燃烧反应。温度越高,燃烧反 应越快。
燃烧设备
燃烧器的Байду номын сангаас计
燃烧器的设计,如喷嘴、空气混合装置等,都会影响燃料与空气的混合程度, 从而影响燃烧效果。
废气处理
对燃烧产生的废气进行净化处理,减少对环 境的污染。
废热回收
利用燃烧产生的余热进行发电或供热,提高 能源利用效率。
燃料选择
优先选择清洁能源,减少化石燃料的消耗。
05
燃料燃烧的未来发展
清洁能源的发展
太阳能
利用太阳能进行发电和供热,减少对化石燃料的依赖。
风能
通过风力发电,实现可再生能源的利用。
燃烧室的结构
燃烧室的结构,如容积、形状、出口设计等,都会影响火焰的稳定性、燃烧速 度和燃烧效率。
04
燃料燃烧的产物与污染
燃烧产物的种类
01
02
03
04
燃烧产物
燃烧过程中产生的气体、液体 和固体物质。
燃烧气体
包括二氧化碳、一氧化碳、氮 氧化物、硫氧化物等。
燃烧液体
燃烧过程中产生的油滴、水蒸 气等。
燃烧固体
燃烧过程中产生的灰烬、烟尘 等。
燃烧产物的危害
01
二氧化碳
导致温室效应,引起全球气候变暖 。
氮氧化物
形成酸雨和光化学烟雾,对环境和 人体健康造成危害。
03
02
一氧化碳
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
京能集团运行人员培训教程BEIH Plant Course燃料及燃烧基本理论The Basic Theory of Fuel And CombustionMAJTD NO.100.2目录1燃煤的形成与分类 (1)1.1燃料 (1)1.2煤的生成 (1)1.3煤炭的分类 (1)2燃煤的成分与分析 (3)2.1煤的元素分析 (3)2.2煤的工业分析 (3)2.3煤的成分基准及其换算 (4)3燃煤的性质 (6)3.1燃烧特性 (6)3.2常规性指标 (6)3.3实验室指标 (9)3.4煤粉的颗粒特性 (10)3.5自燃特性 (12)3.6爆炸特性 (13)3.7可磨特性 (15)3.8磨损特性 (17)3.9黏结特性 (19)3.10燃烧产物的腐蚀特性 (19)3.11飞灰磨损性 (20)3.12灰的熔融性 (20)3.13堆积特性 (20)3.14流动特性 (21)4电煤技术条件、要求与标准 (22)5煤粉(粒)燃烧技术 (24)5.1燃烧的基础知识 (24)5.2煤粉的燃烧 (26)5.3独立有限空间冷态(单体燃烧器)燃烧运行技术 (32)5.4自由空间热态(整体成组)燃烧运行技术 (33)6燃油的燃烧研究 (35)6.1燃油及其化学成分 (35)6.2燃油的物理特性 (35)6.3燃油的燃烧 (36)7 延伸阅读 (39)7.1质量作用定律 (39)7.2阿累尼乌斯定律 (40)7.3影响化学反应速度的因素 (40)7.4热力着火理论 (42)7.5火焰的传播 (46)7.6链锁反应 (47)7.7煤粉的着火燃烧 (48)7.8碳粒的燃烧 (49)8 题库 (52)8.1填空题 (52)8.2问答题 (53)1燃煤的形成与分类1.1燃料燃料是指能广泛用于工农业生产和人民生活以提供热能或动力的原料。
世界上所用的燃料可分为两大类,一类是核燃料,另一类是有机燃料,也称为矿物燃料。
火力发电厂锅炉燃用的是有机燃料。
有机燃料就是含有元素碳、氢等有机物质的天然燃料及其加工后的人工燃料。
有机燃料按其物态可以分为固体燃料、液体燃料和气体燃料三种。
燃料特性是锅炉设计、运行的基础。
所用燃料的种类不同,锅炉的炉膛尺寸、燃烧器种类、制粉系统类型、受热面布置、锅炉的型式等各不相同,对锅炉运行出现的结渣、积灰、磨损、腐蚀、大气污染物排放和飞灰含碳量等情况的影响亦有差别。
因此,对于锅炉的设计和运行工作者来说,掌握好燃料的成分、特性及其对锅炉生产的影响是非常必要的。
1.2煤的生成煤是古代植物在数百万年以前以致更远的年代,由于地壳运动被覆埋在地下,长期受到地层压力和地热的作用,发生了复杂的生物化学和物理化学反应后演变而成的,通常要经历泥炭化作用和煤化作用两个阶段。
泥炭化作用:古代植物由于细菌的作用而发生腐烂和分解,使其内部组织破坏,一部分物质转为气体逸出,残余的物质开始转变为泥炭,称为泥炭化作用,这是成煤的第一阶段。
煤化作用:泥炭在地下受到不断增高的地层压力和温度影响,逐渐被压紧和硬化,继续排出气体和水分,从而使综合碳比例日趋增大形成了固体有机可燃沉积岩,称为煤化作用,这是成煤的第二阶段。
煤炭:主要是由植物遗体经煤化作用转化而成的富含碳的固体可燃有机沉积岩,含有一定量的矿物质,相应的灰分产率小于或等于50%(干基质量分数)。
1.3煤炭的分类由于成煤植物、成煤年代及成煤条件的不同,特别是在变质程度上的区别,导致各种煤具有不同的化学组成及其特性。
根据煤的煤化程度(干燥无灰基挥发分Vdaf等指标),将煤分为无烟煤、烟煤及褐煤,无烟煤是煤化程度最高的煤,挥发分含量最低,发热量高,密度最大,着火点高,燃烧稳定性差,无粘结性,燃烧时多不冒烟;褐煤是最浅的煤,光泽暗淡,质地较软,内在水分较高,具有不同程度的腐殖酸,挥发分含量高,发热量低;烟煤介于两者之间。
干燥无灰基挥发分的大小,作为煤炭分类的主要指标,无烟煤的V daf≤10%,褐煤的V daf≥37%,烟煤的V daf大致可分为四个区段,即10%~20%、20%~28%、28%~37%、37%以上,烟煤可分为12个类别。
中国煤炭分类简表如表格1-1:当G>85的情况下,用Y值或b值来区分肥煤、气肥煤和其他煤类。
当Y>25.00mm时,根据V daf的大小可划分为肥煤或气肥煤;当Y≤25.00mm时,则根据V daf的大小可划分为焦煤、1/3焦煤或气煤。
按b值来划分类别时,当V daf≤28%时,b>150%的为肥煤;当V daf>28%时,b>220%的为肥煤或气肥煤;如按b值和Y值划分的类别有矛盾时,以Y值划分的类别为准。
表格1-12燃煤的成分与分析燃煤的成分通过元素分析和工业分析来确定,用质量百分数来表示。
2.1煤的元素分析煤是复杂的高分子碳氢化合物,其主要成分是碳(C)、氢(H)、氧(O)、氮(N)、硫(S)、灰分(A)及水分(M),见表格2-1。
表格2-12.2煤的工业分析在煤的着火、燃烧过程中,煤中各种成分的变化情况是:将煤加热到一定温度时,首先水分被蒸发出来;接着再加热,煤中的氢、氧、氮、硫及部分碳所组成的有机化合物便分解,变成气体挥发出来,这些气体称为挥发分;挥发分析出后,剩下的是焦炭,焦炭就是固定碳和灰分。
水分和灰分是煤中的不可燃组分,挥发分和固定碳则是煤中的可燃组分。
水分包括外在水分与内在水分,无烟煤、烟煤的全水分一般在5%-15%之间,褐煤的全水分往往高达25%以上。
挥发分是煤中最易燃烧的成分,随着煤的变质程度加深,挥发分含量逐渐减少,而挥发分开始逸出的温度及挥发分的发热量则逐渐升高,见表格2-2。
表格2-2计算煤中水分(M)、挥发分(V)、固定碳(FC)和灰分(A)四种成分的质量百分数,称为煤的工业分析。
2.3煤的成分基准及其换算2.3.1成分基准常用的成分基准有收到基、空气干燥基、干燥基和干燥无灰基四种,它们的工业和元素分析如图2-1,结果表达如下:(1)收到基:以收到状态的煤为基准来表示煤中各组成成分的百分比。
用下标“ar”表示,它计入了煤的灰分和全水分。
其成分可用下列平衡式表示:工业分析:M ar + A ar + V ar + FC ar =100%(2-1)元素分析:C ar + H ar + N ar + S ar + O ar+ A ar + M ar = 100%(2-2)式中:M ar,A ar,V ar,FC ar,C ar,H ar,N ar,S ar,O ar分别为煤中的水分、灰分、挥发分、固定碳、碳、氢、氮、硫、氧成分的收到基含量的百分数。
(2)空气干燥基:由于煤的外部水分变动很大,在分析时常把煤进行自然风干,使它失去外部水分,以这种状态为基准进行分析得出的成分称为空气干燥基,以下标“ad”表示。
其成分可用下列平衡式表示:工业分析:M ad + A ad + V ad + FC ad=100%(2-3)元素分析:C ad + H ad + N ad + S ad + O ad+ A ad + M ad=100%(2-4)(3)干燥基:以无水状态的煤为基准来表达煤中各组成成分,以下标“d”表示。
其成分可用下列平衡式表示:工业分析:A d + V d + FC d=100%(2-5)元素分析:C d + H d + N d + S d + O d + A d =100%(2-6)(4)干燥无灰基:除灰分和水分后煤的成分,这是一种假想的无水无灰状态,以此为基准的成分组成,以下标“daf”表示。
其成分可用下列平衡式表示:工业分析:V daf + FC daf =100%(2-7)元素分析:C daf + H daf + N daf + S daf + O daf =100%(2-8)图2-1 燃料成分与各种“基”的关系图2.3.2各种基准成分的换算煤的各种基准成分之间可以互相换算。
换算公式如下:Y=K×X O(2-9)式中:X O—按原基准计算的某一组成含量百分比;Y —按新基准计算的同一组成含量百分比;K —基准换算的比例系数,见表格2-3。
不同基准成分的换算系数表欲求基准已知基准收到基空气干燥基干燥基干燥无灰基收到基 1空气干燥基 1干燥基 1干燥无灰基l表格2-3注:挥发分和高位发热量可按此表计算,此表不能用于煤的水分之间的换算。
3燃煤的性质3.1燃烧特性燃煤成分中的可燃性元素具有与氧进行完全剧烈反应而达到着火温度后发热、放光的性质,称为燃烧特性。
3.2常规性指标3.2.1发热量(1)定义单位质量燃煤(1kg)完全燃烧时放出的热量称为煤的发热量。
煤的发热量分为高位发热量和低位发热量。
燃煤在空气中大气压条件下完全燃烧后所放出的全部热量称为高位发热量,用“Qgr”表示。
从高位发热量中扣除煤中水分(煤中有机质中的氢燃烧后生成的氧化水,以及煤中的游离水和化合水)的汽化潜热后,剩余的可以实际使用的热量,称为低位发热量,用“Qnet”表示。
实际工程中常应用的是燃煤的收到基低位发热量。
发热量作为燃烧特性指标,反映炉内温度水平,综合了煤质灰分、水分对着火的影响。
根据国内燃煤锅炉的运行经验,煤粉锅炉不投油助燃而稳定燃烧可适应的发热量见表格3-1。
表格3-1注:褐煤的发热量最低限很低的原因在于,经制粉系统干燥后,水分很高的褐煤的发热量几乎成倍增长,而水分较低的烟煤、贫煤和无烟煤干燥后,煤粉和收到基煤的发热量变化不大。
(2)发热量的换算各种基准的高位发热量之间的换算可按成分换算系数进行。
低位发热量之间的换算还必须考虑汽化潜热的影响,由于1吨氢燃烧后生成9吨水蒸汽,所以每千克燃煤燃烧时将形成(9Har+Mar)/100千克水蒸汽。
如果取水的汽化潜热r=2508kJ/kg,则燃煤收到基的高、低位发热量之间的换算关系如下表格,3-2。
各基准下高位发热量与低位发热量的换算公式(单位:kj/kg)表格 3-2(3) 标准煤以收到基低位发热量为29308kj/kg (7000kcal/kg )的燃煤,称为标准煤。
由于各种煤的发热量不同,有时差别很大,在工业上为了核算企业的能耗量,统一计算标准,便于比较与管理,采用标准煤及其折算的概念。
实际燃煤量B 折合成标准煤重量B bz 的公式为:B bz =B×Q net,ar ÷29308 (kJ/kg ) (3-1)(4) 折算成分燃料的成分是以质量百分数来表示的,但对于某些成分,例如水分,灰分和硫分,由于它们对锅炉机组的工作(例如着火、磨损、积灰、腐蚀等)的影响较大,只通过元素分析和工业分析所得到的应用基成分百分数不能完全说明问题。
这是因为燃料的发热量有高有低,在一定的锅炉负荷所带进炉内的水分,灰分和硫分,就不但与它们的应用基成分百分数有关,而且与燃料的发热量有关。
