腺苷脱氨酶测定试剂盒(过氧化物酶法)产品技术要求北京科美生物
人腺苷脱氨酶ADAelisa试剂盒使用说明书

人腺苷脱氨酶(ADA)elisa试剂盒使用说明书Elisa kit规格:48孔配置/96孔配置标准品稀释液:1.5ml×1瓶酶标试剂:3 ml×1瓶(48)/6 ml×1瓶(96)【人腺苷脱氨酶(ADA)elisa试剂盒】本试剂仅供研究使用计算:以标准物的浓度为横坐标,OD值为纵坐标,在坐标纸上绘出标准曲线,根据样品的OD值由标准曲线查出相应的浓度;再乘以稀释倍数;或用标准物的浓度与OD值计算出标准曲线的直线回归方程式,将样品的OD值代入方程式,计算出样品浓度,再乘以稀释倍数,即为样品的实际浓度。
试剂盒组成:封板膜:2片(48)/2片(96)说明书:1份密封袋:1个标准品:2700ng/L 0.5ml×1瓶0.5ml×1瓶2-8℃保存酶标包被板: 1×48 1×96 2-8℃保存样品稀释液: 3ml×1瓶 6 ml×1瓶2-8℃保存显色剂A液: 3ml×1瓶 6 ml×1瓶2-8℃保存显色剂B液: 3ml×1瓶 6 ml×1瓶2-8℃保存终止液: 3ml×1瓶6ml×1瓶2-8℃保存浓缩洗涤液:(20ml×20倍)×1瓶(20ml×30倍)×1瓶2-8℃保存实验原理:本试剂盒应用双抗体夹心法测定标本中人腺苷脱氨酶(ADA)水平。
用纯化的人腺苷脱氨酶(ADA)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入腺苷脱氨酶(ADA),再与HRP标记的腺苷脱氨酶(ADA)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物TMB显色。
TMB在HRP酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的腺苷脱氨酶(ADA)呈正相关。
用酶标仪在450nm波长下测定吸光度(OD值),通过标准曲线计算样品中人腺苷脱氨酶(ADA)浓度。
腺苷脱氨酶(ADA)测定试剂盒(过氧化物酶法)产品技术要求sainuopu
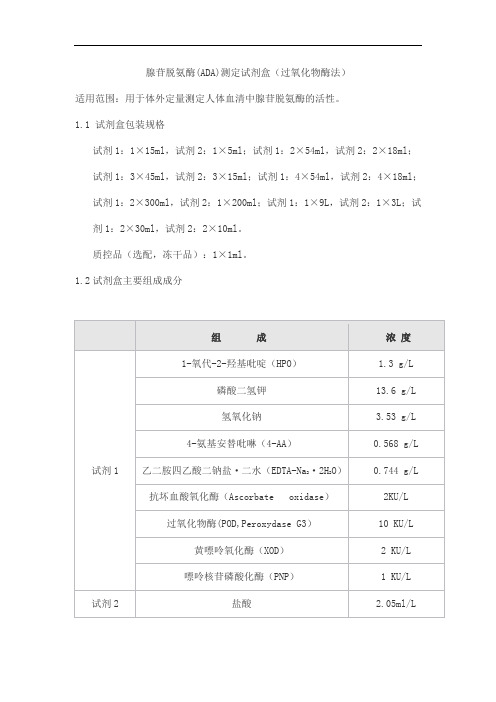
腺苷脱氨酶(ADA)测定试剂盒(过氧化物酶法)适用范围:用于体外定量测定人体血清中腺苷脱氨酶的活性。
1.1 试剂盒包装规格试剂1:1×15ml,试剂2:1×5ml;试剂1:2×54ml,试剂2:2×18ml;试剂1:3×45ml,试剂2:3×15ml;试剂1:4×54ml,试剂2:4×18ml;试剂1:2×300ml,试剂2:1×200ml;试剂1:1×9L,试剂2:1×3L;试剂1:2×30ml,试剂2:2×10ml。
质控品(选配,冻干品):1×1ml。
1.2试剂盒主要组成成分2.1 外观液体双试剂:试剂1无色至浅黄色澄清液体,试剂2无色至浅黄色澄清液体。
质控品:冻干品,溶解后为无色至淡黄色液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3 试剂空白2.3.1试剂空白吸光度:在37℃、546nm波长、1cm光径条件下,试剂空白吸光度应不大于0.3。
2.3.2试剂空白吸光度变化率:在37℃、546 nm波长、1cm光径条件下,试剂空白吸光度变化率(ΔA/min)应不大于0.005。
2.4 分析灵敏度测定活性为25U/L样本时,吸光度变化率(ΔA/min)应不小于0.009。
2.5 线性范围在(2,180)U/L线性范围内,线性相关系数r不小于0.996。
在(60,180)U/L 区间内线性相对偏差不大于±10%;在(2,60]U/L区间内线性绝对偏差不大于±6U/L。
2.6 重复性重复测试两份高低浓度的样本,所得结果的变异系数(CV%)应不大于5%。
2.7 批间差不同批号试剂测试同一份样本,测定结果的批间相对极差应不大于10%。
2.8 准确度相对偏差:相对偏差应不超过±10%。
2.9 质控品赋值有效性测定结果在靶值范围内。
腺苷脱氨酶检测试剂盒

腺苷脱氨酶检测试剂盒【产品名称】通用名称:腺苷脱氨酶检测试剂盒(酶比色法)英文名称:Adenosine deaminase Test Kit(ColorimetricMethod)【预期用途】用于人血清腺苷脱氨酶的体外定量测定。
腺苷脱氨酶是反映肝损伤的敏感指标,可作为肝功能常规检查项目之一,用于判断急性肝损伤及残留病变,协助诊断慢性肝病,并有助于肝纤维化的诊断。
【检验原理】腺苷脱氨酶腺嘌呤核苷+ H2O————→次黄嘌呤核苷+磷酸PNP次黄嘌呤核苷+Pi————→次黄嘌呤+磷酸核糖XOD次黄嘌呤+2H2O+2O2 ———→2H2O2+尿酸POD2H2O2+4-AAP+TOOS————→醌化合物在波长546nm处测定醌化合物生成速率,计算出腺苷脱氨酶活力。
【储存条件及有效期】试剂密闭贮存于2~8℃,可稳定一年。
【样本要求】血浆、脑脊液、胸腹水、血清,采血后应及时分离,避免溶血。
血清、血浆、脑脊液、胸腹水贮2~8℃三天内结果不会改变。
【检验方法】试剂配制:适合加双试剂的仪器直接使用,试剂更稳定;(仪器读取的吸光度A为A主波长-A副波长)试验结果的计算:腺苷脱氨酶(U/L)= (A△测定/min-A△空白/min)×F理论F=1763(1cm光径,546nm)质量控制程序:采用DIZAZYME公司的质控品,控制相对误差在性能指标范围内。
【参考范围】血清:0~15U/L根据正常人95%的分布区间确定【检验结果的解释】溶血对测定有干扰,操作过程中要尽量避免溶血。
【产品性能指标】线性范围:0—150U/L(判定依据:r2≥0.995);准确度:测得值在质控品规定的偏差范围内;精密度:批内CV≤6.0%;批间相对极差≤10.0%;试剂空白吸光度:波长546nm,光径10mm,测得试剂吸光度值A≤0.2;试剂空白吸光度变化率:波长546nm,光径10mm,测得试剂吸光度变化值△A/min≤0.01。
灵敏度:试剂检测下限≤ 2.0 U/L。
腺苷脱氨酶双试剂测定的全自动分析方法

试 剂 为 北 京 科 美 公 司 AD 的 商 品 试剂 , 号 2 0 0 0 。 A 批 0 93 4
1 3 实 验 方 法 . 1 3 1 测 定 原 理 腺 苷 + H . . 0 +NAD H+a 一酮戊 二 酸 次 黄 苷 + NH NH ,
氏) 色 方 法 口 j 酶 偶 联 法 ( DH, 称 偶 联 ) 续 监 测 显 、 GL 简 连 法 ] 利 用 T id r 应 的 酶 联 比色 法 ] 3、 r e反 n 。 。前 者 只 能 手 工 操 作 , 二 者 能 够 实 现 自动 分 析 。虽 然从 原理 上说 已经 相 当成 熟 后
I S主要 用 于 急 性 胰 腺 炎 的诊 断 , 肾脏 疾 病 的诊 治 中应 用 较 P 在
E ] 刘 军 , 好 治 . 抑 素 c 的临 床 意 义 与 测 定 应 用 i] 医学 a 杨 胱 - . J
检 验 与 临床 , 0 8 1 ( ) 7 — 9 2 0 ,9 2 : 87 .
1 材 料 与 方 法
1 3 2 实 验 参 数 ( ) 法 : 率 法 ; 2 波 长 : 波 长 3 0 .. 1方 速 () 主 4
n 副 波 长 40n () 应 方 向 : ;4 样 本 2 L, 12 0 m, 1 m;3 反 负 () R 0 L R24 L;5检 测 时 间参 数 : 1和样 品 加 入 后 2 0S 始 , O () R 4 开 读 取 空 白 ,0 结 束 , 入 R 30S 加 2延 时 3 后 检 测 10S ( ) oS 2 ;6 单 位 计 算 : i一 △ A/ i 1。 2 0 6 2 ×2 X0 5 理 论 K u/ a r n× 0 × 6/ . 2 0 . ,
腺苷脱氨酶(ADA)测定试剂盒(过氧化物酶法)产品技术要求lideman

腺苷脱氨酶(ADA)测定试剂盒(过氧化物酶法)产品技术要求lideman腺苷脱氨酶(ADA)测定试剂盒(过氧化物酶法)适用范围:本产品用于体外定量测定人血清或血浆中腺苷脱氨酶的含量。
1.1规格试剂1(R1):3×60mL、试剂2(R2):1×60mL;校准品(选配):1×1mL。
低值质控品(选配):1×1mL;高值质控品(选配):1×1mL。
1.2组成试剂盒由试剂、校准品(选配)和质控品(选配)组成。
试剂1(R1): Tris缓冲液:50mmol/L pH 8.0;4-氨基安替比林:4mmol/L;4-AA :2mM ;PNP :0.1U/mL;XOD:700U/L;过氧化物酶:2KU/L;试剂2(R2):mops缓冲液:50mmol/L pH 7.0;腺苷:10mM;EHSPT:2mM。
校准品组成:单个水平的冻干校准品,在水基质中添加腺苷脱氨酶,稳定剂0.1%。
定值范围:(80~180)U/L。
质控品组成:两个水平的冻干质控品,在水基质中添加腺苷脱氨酶,稳定剂0.1%。
定值范围:(20~50)U/L和(80~180)U/L。
2.1 外观液体双试剂:试剂1(R1):无色澄清液体,试剂2(R2):无色澄清液体。
校准品:冻干品,溶解后为无色至淡黄色液体。
质控品:冻干品,溶解后为无色至淡黄色液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3 溯源性:根据GB/T 21415及有关规定提供校准品的来源、赋值过程及测量不确定度等内容,该校准品溯源至参考物质(BCR-647,IRMM)。
2.4 试剂空白2.4.1 空白吸光度在37℃、(546nm±10%范围内的)波长、1cm光径条件下,用去离子(或生理盐水)水作为样品加入试剂测试时,试剂空白吸光度应<0.3 ABS。
2.4.2 空白吸光度变化率在37℃、(546nm±10%范围内的)波长、1cm光径条件下,用去离子(或生理盐水)水作为样品加入试剂测试时,试剂空白吸光度变化率(ΔA/min)应≤ 0.003 ABS/min。
过氧化物酶(Peroxidase,POD)试剂盒使用说明

3、细菌或细胞 POD 活性
(1)按样本蛋 反应体系中每分钟 A470 变化 0.01 定义为一个酶活 力单位。
POD(U/mg prot)=245μL(反应体系)÷1000μL×提取酶液总体积(1000μL)÷样 本体积(5μL)÷0.01×ΔA÷蛋白质浓度(mg/mL)=4900×ΔA÷蛋白质浓度(mg/mL)
2、组织 POD 活性
(1) 按样本蛋白浓度计算
单位的定义:每 mg 组织蛋白在每 ml 反应体系中每分钟 A470 变化 0.005 定义为一个酶 活力单位。
POD(U/mg prot)=245μL(反应体系)÷1000μL×提取酶液总体积(1000μL)÷样 本体积(5μL)÷0.005×ΔA 测定÷蛋白质浓度(mg/mL)=9800×ΔA÷蛋白质浓度(mg/mL)
用 96 孔板测定的计算公式如下
1、血清(浆)POD 活性
单位的定义:每 mL 血清(浆)在每 ml 反应体系中每分钟 A470 变化 0.005 定义为一个 酶活力单位。
POD(U/mL)=245μL(反应体系)÷1000μL×血清(浆)总体积(1000μL)÷样本 体积(5μL)÷0.005×ΔA =9800×ΔA
(2)按细菌或细胞密度计算
单位的定义:每 1 万个细菌或细胞在每 ml 反应体系中每分钟 A470 变化 0.01 定义为一 个酶活力单位。
POD(U/104 cell)=245μL(反应体系)÷1000μL×提取酶液总体积(1000μL)÷样 本体积(5μL)÷0.01×ΔA÷细菌或细胞密度(104 cell /mL)=4900×ΔA÷细菌或细胞密 度(104 cell /mL)
(2)按样本鲜重计算
单位的定义:每 g 组织在每 ml 反应体系中每分钟 A470 变化 0.01 定义为一个酶活力单 位。
腺苷脱氨酶测定试剂盒(谷氨酸脱氢酶法)产品技术要求丹大

腺苷脱氨酶测定试剂盒(谷氨酸脱氢酶法)组成:适用范围:用于体外定量测定人血清中ADA的含量。
2.1外观试剂盒外观应整洁,液体无渗漏,文字符号标识清晰;试剂1、试剂2为透明液体,不得有沉淀和絮状物。
校准品质控品为冻干品,复溶后为无色至淡黄色透明液体。
2.2 装量每瓶不少于标示值。
2.3试剂空白吸光度用指定的空白样品测试试剂(盒),在光径1cm下,在波长340nm处测定试剂空白吸光度A≥1.0,试剂空白吸光度变化率ΔA/min≤0.03。
2.4分析灵敏度试剂测定30U/L被测物,吸光度变化△A/min≥0.004。
2.5线性范围2.5.1在[2,200] U/L被内,相关系数R≥0.990。
2.5.2在[2,60] U/L内,线性绝对偏差不超过±6U/L;(60,200] U/L内,线性相对偏差不超过±10%。
2.6精密度2.6.1重复性重复测试(30±10)U/L和(80±20)U/L的样本,所得结果的变异系数(CV%)应不大于5%。
2.6.2批间差测定(30±10)U/L和(80±20)U/L 样本,所得结果的批间相对极差(R)应不大于10%。
2.7准确度回收率应在85%-115%范围内。
2.8 质控品赋值有效性试剂盒内的质控品,检测结果均在质控范围内。
2.9 瓶间差瓶间差CV≤10%。
2.10稳定性2.10.1 效期稳定性试剂有效期为12个月,取到效期后一个月内进行检测,测定结果应符合2.3-2.6.1、2.7和2.8项要求。
2.10.2复溶稳定性校准品、质控品复溶后在2-8℃密闭避光保存24h。
检测开瓶后的工作校准品,测试结果与靶值的偏差应不超过±15%,开瓶后的质控品,检测结果均在质控范围内。
2.11溯源性根据GB/T21415-2008的要求,本产品校准品可溯源至企业内部校准品。
腺苷脱氨酶测定试剂盒(过氧化物酶法)产品技术要求赖皮jiuqiang

腺苷脱氨酶测定试剂盒(过氧化物酶法)适用范围:用于体外定量测定人血清或血浆中的腺苷脱氨酶(ADA)含量。
1.1 包装规格试剂1:2×20mL、试剂2:1×20mL;试剂1:3×40mL、试剂2:3×20mL;试剂1:1×40mL、试剂2:1×20mL;试剂1:3×60mL、试剂2:3×20mL;试剂1:3×20mL、试剂2:1×20mL;试剂1:1×60mL、试剂2:1×20mL;试剂1:1×60mL、试剂2:1×30mL;试剂1:3×60mL、试剂2:3×30mL;试剂1:8×3.7mL、试剂2:4×3.7mL;试剂1:8×4.3mL、试剂2:4×4.3mL;340测试/盒(试剂1:2×20mL、试剂2:1×20mL);210测试/盒(试剂1:1×40mL、试剂2:1×21mL);210测试/盒(试剂1:1×40mL、试剂2:1×20mL);试剂1:1×20mL、试剂2:1×10mL;试剂1:1×42mL、试剂2:1×21mL;160测试/盒(试剂1:1×35mL、试剂2:1×16.5mL);180测试/盒(试剂1:1×35mL、试剂2:1×18mL);180测试/盒(试剂1:2×20mL、试剂2:1×20mL);180测试/盒(试剂1:1×40mL、试剂2:1×20mL);200测试/盒(试剂1:1×42mL、试剂2:1×23mL);240测试/盒(试剂1:2×20mL、试剂2:1×20mL);240测试/盒(试剂1:1×40mL、试剂2:1×20mL);250测试/盒(试剂1:1×50mL、试剂2:1×27mL);250测试/盒(试剂1:1×42mL、试剂2:1×21mL);300测试/盒(试剂1:2×20mL、试剂2:1×20mL);300测试/盒(试剂1:1×40mL、试剂2:1×20mL);360测试/盒(试剂1:2×20mL、试剂2:1×20mL);360测试/盒(试剂1:1×40mL、试剂2:1×20mL);210测试/盒(试剂1:1×42mL、试剂2:1×21mL);340测试/盒(试剂1:1×42mL、试剂2:1×21mL);390测试/盒(试剂1:1×42mL、试剂2:1×21mL);200测试/盒(试剂1:1×40mL、试剂2:1×20mL);330测试/盒(试剂1:1×40mL、试剂2:1×20mL);370测试/盒(试剂1:1×40mL、试剂2:1×20mL);校准品(单水平):1×1mL;1×2mL;质控品(水平1):1×1mL;1×2mL;质控品(水平2):1×1mL;1×2mL。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
腺苷脱氨酶测定试剂盒(过氧化物酶法)
适用范围:本试剂盒用于体外定量测定人血清或血浆中腺苷脱氨酶(ADA)的活性。
1.1包装规格
1)试剂1:5×40mL,试剂2:5×20mL;
2)试剂1:4×40mL,试剂2:4×20mL;
3)试剂1:2×40mL,试剂2:2×20mL。
1.2 主要组成成分
试剂1:Good’s缓冲液(50mmol/L),4-氨基安替比林(2mmol/L),PNP(0.1KU/L),XOD(0.2KU/L),POD(0.6KU/L)。
试剂2:Good’s缓冲液(50mmol/L),腺苷(10mmol/L),EHSPT(2mmol/L)。
2.1 外观
2.1.1 试剂1应为无色至淡粉红色溶液,无混浊,无未溶解物;
2.1.2 试剂2应为无色至淡粉红色溶液,无混浊,无未溶解物。
2.2 净含量
液体试剂的净含量应不少于标示值。
2.3 试剂空白
2.3.1试剂空白吸光度
ADA试剂盒在波长546nm处测定试剂的吸光度值,应不大于0.5000。
2.3.2试剂空白吸光度变化率
ADA试剂盒在波长546nm处测定试剂的空白吸光度变化率,每分钟的变化值应小于0.0100。
2.4 分析灵敏度
ADA试剂盒测试70U/L ADA时,吸光度变化率大于0.0100。
2.5 准确度
用本公司ADA试剂盒和已上市ADA试剂盒同时测定40个临床样本,相关系数(r2)应不小于0.95,在[2,20]U/L区间内,绝对偏差应不超过±2U/L;在(20,200]U/L 区间内,相对偏差应不超过±10%。
2.6 精密度
2.6.1 重复性
重复测试(3±1)U/L、(15±5)U/L和(30±5)U/L的样本,所得结果的变异系数CV应不大于5%;
2.6.2 批间差
测试(30±5)U/L的样本,所得结果的批间相对极差应不大于10%。
2.7 线性范围
ADA试剂盒在[2,200]U/L范围内,线性相关系数(r)应不小于0.990;
2.7.1在[2,20]U/L区间内,线性绝对偏差应不超过±2U/L;
2.7.2在(20,200]U/L区间内,线性相对偏差应不超过±10%。
2.8 稳定性
原包装的ADA试剂盒在2℃~8℃避光保存,有效期为12个月。
在ADA试剂盒有效期满后2个月内,试剂性能应符合2.1、2.3、2.4、2.5、2.6.1、2.7的要求。
