血清天门冬氨酸氨基转移酶测定
ISO15189血清天门冬氨酸氨基转移酶IFCC推荐方法测定

ISO15189血清天门冬氨酸氨基转移酶IFCC推荐方法测定AST是一种酶,存在于细胞质和线粒体中,参与氨基酸代谢和乳酸生成。
AST广泛存在于人体各个组织中,尤其是肝脏、心肌、肌肉和肾脏组织。
因此,AST的测定可以用于评估这些组织的功能和损伤情况。
对AST的测定,通常采用血清样本。
在进行测定之前,需要注意以下几点:1.样本采集和储存:血清样本应用离心法从全血中分离得到,然后尽快进行分析。
分离后的血清可以在2-8摄氏度下存放一段时间,但不宜超过4小时,否则可能对AST活性产生影响。
2.试剂的选择和质量控制:选择高质量的试剂,并根据供应商的说明书正确使用。
为了确保测定结果的准确性和可重复性,建议使用IFCC推荐的AST标准品作为内部质量控制材料,定期进行校准和质控。
3.仪器设备的校准和维护:仪器设备必须按照生产商的要求进行校准和维护。
在每次测定前,都要对仪器进行标定,确保其准确性和稳定性。
AST的IFCC推荐方法测定步骤如下:1.准备工作:收集和处理血清样本,标定仪器,准备试剂。
2.反应体系:将待测血清样本与试剂混合,形成反应体系。
反应体系中应包含AST底物、辅酶和混合底物。
3.测定过程:将反应体系置于恒温培养箱中,在适当的温度下进行反应。
反应时间应根据样品和试剂的性质确定,通常为1-2分钟。
4.反应终止:加入终止剂终止反应,防止进一步反应的发生。
5.测定信号:使用合适的测定设备(如分光光度计或自动化化学分析仪)测量所产生的信号,通常为光吸光度或荧光强度。
6.计算和报告结果:根据仪器的标定曲线和样本的吸光度或荧光强度计算AST的活性,并将结果报告出来。
注意,结果的单位应根据AST活性的参考范围和机构的要求确定。
AST的IFCC推荐方法是一种准确、可靠的测定AST活性的方法。
合理的标本采集、准备、试剂选择和仪器校准都可以提高测定的精确性。
此外,仪器设备的维护、环境条件的控制和质量控制的实施也是确保测定结果准确性的重要步骤。
肝脏疾病患者血清中线粒体型天门冬氨酸氨基转移酶检测的临床意义

0 0 1 均显著高于正常对照组( 0 0 ) 治疗后 , .3 , P< .5 ; 急性 肝炎组和 药物性肝 炎组 m S / S A T A T比值 明显 下降, 其他组无
明显变化 。结论 动态监测血清 m S/ S A T A T比值的变化有利于急性肝 炎、 重型肝 炎的预后判 断和急性肝 炎与慢性肝
ta e ot l ru e oo ig re : vr hpti(. 3 0 0 1 ,ct hpti( .7 0 07 ,rghpti hnt nr opi t lwn drs ee ea t 04 54 .6 ) aue ea t 0 354 .5 ) du eais h c og nh fl o e is - is - t (. 2 00 5 , r i hpti( . 1 0 0 1 ,eat i hs ( .7 00 1 . f rh etettem S/ S 0 3 1 .3 ) c o c e at 0 374 .3 ) hpti c roi 0 2 64 .3 )A t et a n, A T A T - 4 h n is - is r s - et r m h
pt iain a h o vae c n e p ro s ia z t nd t e c n l s e c e d .Re uls W h n pain sfrte tr d h s ia ,herm AS l o i s t e te t s n ee o ptl t i i T/AS rto wee hg e T ai r ih r
a l a h i ci ia i nf a c . e h d Th cii e f swel s ter l c l g i c n e M t o s n s i ea t t so vi mAS n T i e u w r a u e yu i gi T a d AS n s r m e eme s rd b sn mmu o n - n ih iio sy . h b t n a a s T e mAS / T rt sc lu ae n e c a g so i s T AS ai wa ac l td a d t h n e fmAS / T r t r b e 'd d r gt e p t n s h s o h T AS i wee o s n e u i h ai t o — ao n e
心脏病患者血清天门冬氨酸氨基转移酶及其同工酶检测的临床意义

心脏病患者血清天门冬氨酸氨基转移酶及其同工酶检测的临床意义王秀丽;董解菊;邵丽丽;吴杰红;赵捷【期刊名称】《重庆医学》【年(卷),期】2006(035)017【摘要】目的探讨心脏病患者血清中天门冬氨酸氨基转移酶(AST)和线粒体同工酶(m-AST)的变化及其临床意义.方法选择住院心脏病患者54例,其中先心病15例,风心病20例,冠心病19例,正常对照组30例.采用速率法测定血清中AST、m-AST含量并计算m-AST/AST比值.结果冠心病组、风心病组、先心病组m-AST 含量均高于对照组(P<0.05,P<0.01).风心病组、先心病组AST含量、m-AST/AST值显著高于对照组(P<0.01).冠心病组m-AST高于对照组(P<0.05),冠心病组与风心病组相比较AST差异有统计学意义(P<0.05).结论 m-AST、m-AST/AST值测定与心肌细胞损伤程度有关,可作为心脏疾病的辅助诊断指标.【总页数】2页(P1562-1563)【作者】王秀丽;董解菊;邵丽丽;吴杰红;赵捷【作者单位】第三军医大学新桥医院检验科,重庆,400037;第三军医大学新桥医院检验科,重庆,400037;第三军医大学新桥医院检验科,重庆,400037;第三军医大学新桥医院检验科,重庆,400037;第三军医大学检验系,重庆,400038【正文语种】中文【中图分类】R541;R446.112【相关文献】1.肝脏疾病患者血清中线粒体型天门冬氨酸氨基转移酶检测的临床意义 [J], 传良敏;王文建;曹万惠;邓君;黄文芳;饶绍琴2.心脏病患者血清天门冬氨酸氨基转移酶及其同工酶检测的临床意义 [J], 许浩生3.冠状动脉粥样硬化性心脏病患者血清同型半胱氨酸脂蛋白(a)和超敏C反应蛋白水平检测及临床意义 [J], 孟丽玲;何国林4.冠状动脉粥样硬化性心脏病患者血清骨形态发生蛋白4,N1-甲基烟酰胺和血管生成素样蛋白8水平检测的临床意义 [J], 关小明;陈锴;王文会5.血清神经元特异性烯醇化酶同型半胱氨酸联合检测对急性脑梗死合并冠状动脉粥样硬化性心脏病患者的诊断及病情严重程度判断的临床意义 [J], 高伟杰;黑耀宗;王飞因版权原因,仅展示原文概要,查看原文内容请购买。
天门冬氨酸氨基转移酶(AST)测定试剂盒(天门冬氨酸底物法)产品技术要求lideman

天门冬氨酸氨基转移酶(AST)测定试剂盒(天门冬氨酸底物法)适用范围:本产品用于体外定量测定人血清中天门冬氨酸氨基转移酶的含量1.1规格试剂1(R1):4×80mL, 试剂2(R2):4×16mL;试剂1(R1):5×60mL, 试剂2(R2):5×12mL;试剂1(R1):3×40mL, 试剂2(R2):3×8mL;试剂1(R1):2×80mL, 试剂2(R2):2×16mL;试剂1(R1):2×400mL, 试剂2(R2):2×80mL;试剂1(R1):5×45mL, 试剂2(R2):5×15mL;试剂1(R1):2×70mL, 试剂2(R2):1×70mL;试剂1(R1):1×20mL, 试剂2(R2):1×6mL。
1.2试剂组成见表1:试剂1(R1)(以下简称R1),试剂2(R2)(以下简称R2)。
表1 试剂组成2.1 外观液体双试剂:R1(缓冲液):无色液体,R2(启动液):无色液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3 试剂空白2.3.1 空白吸光度在37℃、340 nm波长、1cm光径条件下,试剂空白吸光度>1.0 ABS。
2.3.2空白吸光度变化率在37℃、340 nm波长、1cm光径条件下,用去离子水作为样品加入试剂测试时,试剂空白吸光度变化率(ΔA/min)应<0.004 ABS/min。
2.4 分析灵敏度浓度为50U/L时,吸光度变化率绝对值≥0.014。
2.5 线性范围在[1-600]U/L线性范围内,线性相关系数r2≥0.996。
在(100-600]U/L,范围内的相对偏差不超过10%;测定结果为[1-100]U/L时绝对偏差不超过10U/L。
2.6 精密度试剂盒测试项目精密度CV< 5 %。
血清丙氨酸氨基转移酶与天门冬氨酸氨基转移酶实验室测定水平与男

法: 对 l 5例男性乳腺癌患者和 3 4例对照者进行血清丙氨酸氨基转移酶和天门冬 氨酸氨基转移 酶实验室检查 , 将两者进行统计学
比较分析 。结果 : 乳腺癌患者的 A L T和 A S T水平均高 于良性乳腺病患者 , 其 两者 比值( A S T / A L T ) 与 良性患者相 比d 三 偏高。结论 :
结转移及远处转移 , 一旦 出现远 处转移治疗效果不佳 , 笔者提 倡对于确诊的 T L C , 首次扩大切除或二次手术扩大切除。
4 参考文献
患者 , 在不严重影 响眼、 耳、 鼻、 口的外 形和功 能 的情况 下 , 笔
者建 议安全边界为 1 . 5 a m 但是本研究为 回顾性分析且病例 数有限 , 所 以对于 T L G的安全切缘缺乏循证医学的 I 、 Ⅱ类证
水 平 与男 性 乳腺 癌 的关 系
陈朝霞 , 肖 静 [ 摘 ( 湖北省武汉市江汉大学 医学院 , 湖北 武汉 4 3 0 0 5 6 )
要] 目的: 研 究血清丙氨 酸氨基转移酶 ( A L T ) 与 天门冬氨酸 氨基转移酶 ( A S T ) 比值 与男性乳腺癌发病率 的关 系。方
吉林医学 2 o l 4年 4月第 3 5卷第 1 O期
・
2 0 8 1・
麻烦 , 而且安全切缘 1 . 5 e m以下组 5年生存 率为 8 l %较 切缘 1 . 5 c m以上组差 。所 以对 于术前 或术 中冰冻 结果 为 T L C的
年生存率为 8 3 %。但安全边界极为重要 , 偶有局部 复发 、 淋巴 ’
Z h a o— , X I A O. 1 i n g( ] i a n g h a n U n i v e r s S c h o o l 0 厂 Me d i c i n e , Wu h a n 4 3 0 0 5 6 , C h i n a )
天门冬氨酸氨基转移酶(AST)测定试剂盒(天门冬氨酸底物法)产品技术要求sainuopu
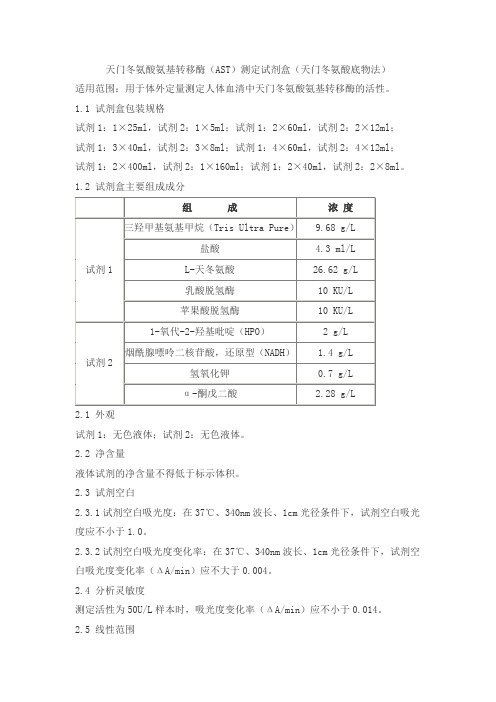
天门冬氨酸氨基转移酶(AST)测定试剂盒(天门冬氨酸底物法)适用范围:用于体外定量测定人体血清中天门冬氨酸氨基转移酶的活性。
1.1 试剂盒包装规格试剂1:1×25ml,试剂2:1×5ml;试剂1:2×60ml,试剂2:2×12ml;试剂1:3×40ml,试剂2:3×8ml;试剂1:4×60ml,试剂2:4×12ml;试剂1:2×400ml,试剂2:1×160ml;试剂1:2×40ml,试剂2:2×8ml。
1.2 试剂盒主要组成成分2.1 外观试剂1:无色液体;试剂2:无色液体。
2.2 净含量液体试剂的净含量不得低于标示体积。
2.3 试剂空白2.3.1试剂空白吸光度:在37℃、340nm波长、1cm光径条件下,试剂空白吸光度应不小于1.0。
2.3.2试剂空白吸光度变化率:在37℃、340nm波长、1cm光径条件下,试剂空白吸光度变化率(ΔA/min)应不大于0.004。
2.4 分析灵敏度测定活性为50U/L样本时,吸光度变化率(ΔA/min)应不小于0.014。
2.5 线性范围在(0,600)U/L线性范围内,线性相关系数r不小于0.996。
在[100,600)U/L 范围内的线性相对偏差不大于±10%;测定结果为(0,100)U/L时线性绝对偏差不大于±10U/L。
2.6 重复性重复测试两份高低浓度的样本,所得结果的变异系数(CV%)应不大于5%。
2.7 批间差不同批号试剂测试同一份样本,测定结果的批间相对极差应不大于6%。
2.8 准确度相对偏差:相对偏差应不超过±15%。
2.9 稳定性效期稳定性:试剂盒在2℃~8℃下有效期为12个月,取失效期的试剂盒进行检测,试验结果应满足2.1、2.3、2.4、2.5、2.6、2.8要求。
天门冬氨酸氨基转移酶 范围

天门冬氨酸氨基转移酶范围《天门冬氨酸氨基转移酶范围:一场关于健康指标的探索之旅》我今天要跟大家聊聊一个特别重要的东西,就是天门冬氨酸氨基转移酶的范围。
这听起来是不是特别复杂?就像一个超级神秘的密码一样。
我先给你们讲讲我是怎么知道这个东西的吧。
我有个邻居叔叔,他最近去医院做体检了。
回来之后呀,就一直愁眉苦脸的。
我就很好奇呀,我问他:“叔叔,你怎么了呀?”叔叔就叹了口气说:“哎呀,小宝贝,叔叔体检报告上有个叫天门冬氨酸氨基转移酶的数值不太对,医生说这个数值不在正常范围呢。
”我当时就特别纳闷,这到底是个啥呀?难道是像我们考试的分数一样,有个固定的对错范围吗?我就跑去问我的爸爸,爸爸可是我们家的“健康小百科”呢。
爸爸就告诉我说:“宝贝呀,这个天门冬氨酸氨基转移酶呀,它在我们的身体里可是有很重要的作用的。
它就像身体里的一个小侦探,在我们的肝脏呀、心脏呀这些重要的器官里到处巡逻。
如果这些器官有什么问题,这个小侦探的数量就可能会发生变化,这个变化就会反映在它的数值上呢。
”我听了之后,眼睛都瞪大了,感觉好神奇呀。
那这个天门冬氨酸氨基转移酶的正常范围是多少呢?爸爸说,在成年人里呀,一般来说它的正常范围是每升血清10 - 40单位。
哇,这个数字就像一个小门槛一样。
我就想啊,如果身体是一个小城堡,这个数值就是城堡大门的守护者。
要是这个数值偏离了正常范围,就像是城堡的大门没守好,那城堡里可能就会出问题啦。
我又问爸爸:“那小朋友的范围是不是也一样呢?”爸爸笑着说:“当然不一样啦,小朋友的身体还在成长发育呢。
对于儿童来说呀,这个数值可能会低一些。
”我当时就想,这就像小朋友和大人穿衣服的尺码不一样,身体里的这些指标也有不同的标准呢。
我把这些告诉了邻居叔叔,叔叔就说:“哎呀,那我得好好去问问医生,我这个数值不在正常范围,是不是我的肝脏或者心脏有问题了呢?”我就对叔叔说:“叔叔,你可一定要好好听医生的话呀。
这个天门冬氨酸氨基转移酶不正常,就像是汽车的仪表盘亮了红灯一样,肯定是哪里需要检查和修理了。
血清天门冬氨酸氨基转移酶测定

血清天门冬氨酸氨基转移酶测定1 检验目的指导本室工作人员规范操作本检测项目,确保检测结果的准确。
2 实验原理本试剂以国际临床化学联合会(IFCC)推荐方法为基础,所采用的反应原理与反应式如下。
⑴样本中的天门冬氨酸氨基转移酶催化L-天冬氨酸和α-氧代戊二酸氨基转移,生成草酰乙酸和L谷氨酸;⑵在还原型辅酶I(NADH+H+)和苹果酸脱氢酶(MDH)的存在下,草酰乙酸被还原为L-苹果酸,还原型辅酶I (NADH+H+)被氧化为辅酶I(NAD),从而使波长340 nm处的吸光度值下降。
通过对波长340 nm处吸光度值的下降速率进行监测,即可测得样本中天门冬氨酸氨基转移酶(AST)的活性L-天门冬氨酸+ -酮戊二酸AST草酰乙酸+L-谷氨酸草酰乙酸+ NADH +H+ MDH苹果酸脱氢酶L-苹果酸+NAD+3 标本3.1 病人准备:12小时禁食。
3.2 类型:血清。
3.3 标本存放:3天内的活性损失:2~8℃保存:<8%;15~25℃保存:<10%;标本稳定性:-20℃保存至少可稳定3个月。
3.4 标本运输:常温条件下保存运输。
3.5 标本拒收标准:标本溶血、细菌污染的标本。
4 实验材料4.1 试剂:上海复星长征医学科学有限公司AST试剂盒(沪食药监械(准)字2014第2400166号 YZB/沪 1546-40-2014)4.1.1 试剂组成试剂1(R1):乳酸脱氢酶>1365 U/L NADH 0.26mmol/ L-天冬氨酸300mmol/L Tris缓冲液 88mmol/L试剂2(R2):苹果酸脱氢酶>1635 U/L α氧代戊二酸36mmol/LTris缓冲液88mmol/L EDTA 5.0mmol/L 4.1.2 试剂准备:试剂为即用式。
4.1.3 试剂稳定性与贮存:在2~8℃避光、密封的储存条件下,试剂盒自生产之日起有效期为12个月。
4.1.4 变质指示:当试剂有看得见的微生物生长,有浊度,或者未开盖的液体有沉淀时,表明试剂已变质,不能继续使用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
血清天门冬氨酸氨基转移酶测定
1. 实验原理:国际临床化学学会(IFCC)推荐的紫外连续监测法,酶偶联反应式为:
L-天门冬氨酸+ -酮戊二酸A S T草酰乙酸
+L-谷氨酸草酰乙酸+ NADH +H+MDH苹果酸脱氢酶L-苹果酸+NAD++H2O
在340nm波长下,监测NADH的氧化速率,即吸光度的下降速率与AST活性呈正比。
2. 标本:
2.1 病人准备:12小时禁食。
2.2 类型:血清,肝素或EDTA血浆。
3. 标本存放:3天内的活性损失:2~8℃保存:<8%;15~25℃保存:<10%;标本稳定性:-20℃保存至少可稳定3个月。
4. 标本运输:常温条件下保存运输。
5. 标本拒收标准:标本溶血、细菌污染的标本。
6. 实验材料
6.1 试剂:欧泰克AST测定试剂盒
6.1.1 试剂组成
Tris缓冲液pH7.8 80mmol/L
L-天门冬氨酸240mmol/L
MDH(苹果酸脱氢酶) ≥600U/L
LDH(乳酸脱氢酶) ≥1200U/L
a-酮戊二酸12mmol/L
NADH 0.18mmol/L
6.1.2 试剂准备:试剂为即用式。
6.1.3 试剂稳定性与贮存
试剂保存于2~8℃,若无污染,可稳定至失效期。
试剂不可冰冻。
6.1.4 变质指示:当试剂有看得见的微生物生长,有浊度,或者未开盖的液体有沉淀时,表明试剂已变质,不能继续使用。
6.1.5 注意事项:试剂中含叠氮钠(0.95g/L)为防腐剂。
不可入口!避免接触皮肤及粘膜。
应采取必要的预防措施使用试剂。
6.2 校准品:使用罗氏公司提供的复合校准品对自动分析仪进行校准,具体参见生化检验校准品和质控品.SOP文件。
6.3 质控品:具体参见生化检验校准品和质控品.SOP 文件。
7. 仪器:日立7060生化分析仪
8. 操作步骤
8.1 项目基本参数:参见生化检验日立7060生化分析仪项目测定参数.SOP文件
8.2 仪器操作步骤:参见生化检验日立7060生化分析仪操作规程.SOP文件
9. 检验结果的判断与分析
10. 质量控制:在每一批标本中都应把非定值血清水平I与II质控做为未知标本进行分析,以2S为质控警告限,3S为失控限,绘制质控图,判断是否在控。
质控规则参见生化室室内质控操作规程.SOP文件。
11. 计算方法:以罗氏复合校准品AST校准值校准仪器后,在病人结果可报告范围内,仪器直接报告可靠的检测结果。
12. 参考值范围[4]
女性<31U/L
男性<37U/L
13. 临床意义
丙氨酸氨基转移酶(ALT)旧称谷丙转氨酶(GPT),天门冬氨酸氨基转移酶(AST)旧称谷草转氨酶(GOT)。
它们是氨基转移酶类的典型代表。
氨基转移酶催化氨基从氨基酸转移给 -酮酸的反应。
ALT是肝脏的特异性酶,仅在肝胆疾病时显著升高。
而AST水平的升高和心肌或骨骼肌损伤,以及肝
组织损害等都有关。
因此同时进行ALT和AST的检测用于鉴别肝损伤和心肌或骨骼肌损伤。
AST/ALT比率可用于肝病的鉴别诊断。
比率<1预示中度的肝损伤;比率>1和严重肝病有关,常见慢性肝病。
14. 线性范围2-800U/L。
15. 超出范围结果处理:本法对AST活力检测的最大ΔA/min在340、334nm为0.16,在365nm为0.08。
当样品测定值超过上限时,应将样品用9g/L氯化钠溶液作1+9稀释,重新测定,结果乘以10。
16. 病危报警值的处理:复查后电话通知临床。
