第一章热力学第一定律及其应用
01章_热力学第一定律及其应用-例题和习题课解析

W V pdV p(V2 V1 ) 330.56 103 (40.00 15.00) 10 3 2864 J
1
V2
上一内容
下一内容
回主目录
返回
2018/12/28
例题
例: 10mol理想气体,压力为1000kPa,温度为300 K , 求下列 各种情况下的W: 1.在空气中( p )体积胀大1dm 3 ; 2.在空气中胀大到气体的压力也为p ; 3.等温可逆膨胀至气体的压力也为p。
3
1000 p1 10 8.314 300 ln 3.W nRT ln 100 p2 57.43kJ
上一内容
下一内容
回主目录
返回
2018/12/28
七、例题
例:气体He从0C, 5 105 Pa, 10dm3,经一绝热可逆 过程膨胀至10 Pa,试计算T2、Q、W、U和H。
物理化学电子教案—第一章
U Q W
上一内容
下一内容
回主目录
返回
2018/12/28
例题
例1:在25C时, 2molH 2的体积为15dm3,此气体 ( 1 )在定温下,反抗外压为105 Pa时,膨胀到体 积为50dm3 ; (2)在定温下可逆膨胀到体积为50dm3 , 试计算两种膨胀过程的功。
3
4865J
上一内容
下一内容
回主目录
返回
2018/12/28
例题
W
(2)
(3)
p(V2 V1 ) 105 (40.00 15.00) 103
2500 J
根据理想气体状态方程
pV nRT nRT 2 8.314 298.2 330.56kPa p 3 V 15.00 10
第一章.热力学第一定律

1.4-2 可逆过程
一次(两次)压缩过程 环境对系统作的功 大于
一次(两次)膨胀过程 系统对环境作的功 原因:多作的功变成热传给了环境 对于准静态膨胀过程的逆过程:压缩可使系统 复原时,环境也同时恢复到原状。这种: 能通过原来过程的反方向而使系统和环境都同 时复原,不留下任何痕迹的过程称为可逆过程
z 可逆过程是一种理想过程,是对真实世 界的科学抽象 一些重要的热力学函数只有通过可逆过 程才能求得
热力学第二定律
开尔文(Lord Kelvin, 1824-1907,英) 1848 克劳修斯(Clausius,1822-1888 ,德)1850
z 构成了热力学的基础
z 人类经验总结,物理化学中最基本定律
z 有着极其牢固的实验基础,其结论具有 高度普遍性和可靠性
z 20世纪初建立了热力学第三定律
一些过程的设计与求算: 1. 理想气体等温过程
∆U =0 ∆H =0 Q=W (可由功求热)
z 等温可逆过程
∫ ∫ W = V2 PdV = V2 nRT dV =nRT ln V2 = Q
V1
V V1
V1
z 对抗恒外压 W= P外 ( V2- V1) = Q
2. 理想气体绝热过程 Q=0 ∆U= nCv.m∆T ∆H = nCp.m∆T W=-∆U(可由内能求功)
浴的温度发生变化即∆T=0, 由此可知
系统 无热传递 环境
Q=0
(2) 气体 向真空膨胀,P外=0, W膨=0
由第一定律则: ∆U=Q-W膨=0 此时:dU=(∂U/∂T)vdT + (∂U/∂V)TdV =0
因dT =0 (∂U/∂v)Tdv=0 但dv≠0 故 (∂U/∂v)T = 0 同理可证 (∂U/∂P)T = 0 即U=f(T)
第一章-物理化学C 作业题 参考答案 5-23

习题 6. 0.500 g 正庚烷放在氧弹量热计中,燃烧后温度升高 3.26℃,燃烧前后的平均温度为
25℃。已知量热计的热容量为 8176 J∙K-1,计算 25℃时正庚烷的等压摩尔燃烧热。
解答:0.500g 正庚烷燃烧后放出的恒容热效应为
QV= {8176×(−3.26)} J= − 26.65 kJ 1 mol 正庚烷燃烧后放出的等容热效应为
解答:∆rCp,m= ∑B νB Cp,m(B)=(31.4+37.7 − 52.3) J∙mol-1∙K-1=16.8 J∙mol-1∙K-1
由基尔霍夫定律:∆rHmy (1000.15K)=∆rHmy (298.15K)+ ∫219080.105.1K5K ∆rCp,mdT ={−36120+16.8×(1000.15-298.15)} J∙mol-1 = − 24.3 kJ∙mol-1
∆cUm=
QV m⁄M
=
(−02.656⁄5130.076)
J∙mol-1= −
5330
kJ∙mol-1
C7H16(l)+11O2(g)=7CO2(g)+8H2O(l)
正庚烷燃烧热为 ∆cHmy (C7H16,298K)=∆cUm+ ∑ νBRT ={−5330+(7 − 11)×8.314×298} J∙mol-1
物理化学 C 作业题 参考答案
第一章 热力学第一定律及其应用(共 4 题)
习题 1. 1 mol 理想气体依次经过下列过程:(1)等容下从 25℃升温至 100℃,(2)绝热自 由膨胀至二倍体积,(3)等压下冷却至 25℃。试计算整个过程的 Q、W、∆U 及∆H。 解答:理想气体的热力学能和焓仅与温度有关,U 和 H 为状态函数,则∆U=0;∆H=0。
热力学第一定律及其应用(D)

dH 2 y C (Y ) Z C (Z ) dT
p,m p,m
d r H m
C
A
p,m
( A) B C ( B) dT
p,m p,m
y C (Y ) z C ( z ) dT
p,m
B C ( B)dT
B
注意:标准摩尔反应焓的数值取决于方程式的写法
0 2H2O(l) 2H2 (g) O2 (g) 0 H2O(l) H2 (g) 1 2 O2 (g)
2) 化合物的标准摩尔燃烧焓 B 1 在标准状态下 完全燃烧产物 指定相态的某化合物 此时的反应热为该化合物的标准摩尔燃烧焓 (standard molar enthalpy of combustion),记 为: C H m ,完全氧化态物质的 C H m 为零。 () () 完全氧化态:
.燃烧和爆炸反应的最高温度
在极限情况下,燃烧爆炸反应几乎瞬间完成, 可以认为系统和环境是绝热的 计算定压燃烧反应的最高火烟温度的依据
Q p H 0
计算定容爆炸反应的最高温度的依据
Q
V
U 0
例 已知在正常沸点时 H2O的摩尔蒸发焓为 40.66kJmol-1,H2O(l)和 H 2 O(g) 的摩尔体积分别 为18.80 cm3mol1和 3.014104 cm3mol1。求 正常沸点 100℃ 下 1molH2O(l)气化为101325Pa的H2O(g)的Q,W,△U,△H. p外=101325Pa; 解:
sol
sol H n2 T , p ,n1
下角标n1表示溶剂量不变,也可理解为是在大量某浓度的 溶液中加入1mol n2溶质所产生的热效应。此时由于是大 量体系中加入1mol溶质,仍可视溶液的浓度不变。 Q-n(溶质)曲线任一点的正切为该浓度时的微分溶解热。
习题课—热力学第一定律及其应用

W = −∆U = 3420.0 J
'
[P26 例1-4]
1-29 求25℃、Pθ下反应 ℃
4 NH 3 ( g ) + 5O2 ( g ) = 4 NO ( g ) + 6 H 2O ( g )
的△rHmθ(298.15k)。已知下列数据 △ 298.15k)。 )。已知下列数据
(1)2 NH 3 ( g ) = N 2 ( g ) + 3H 2 ( g ) (2)2 H 2 ( g ) + O2 ( g ) = 2 H 2O ( l ) (3) H 2O ( l ) = H 2O ( g ) (4) N 2 ( g ) + O2 ( g ) = 2 NO ( g )
∆ H ( 298.15k ) = −5154.19 KJ ⋅ mol c m
θ
−1
, CO ( g ) 、H O ( l ) 的标准摩尔 2 2
分别为-393.51KJ﹒mol-1、 生成焓 ∆ f H m ( 298.15k ) 分别为 试求C (s)的标准摩尔生成焓 -285.84KJ﹒mol-1,试求C10H8(s)的标准摩尔生成焓 θ ∆ H ( 298.15k ) 。 f m
解:原式可由(1)×2+ (2)× 3+ (3)× 6+ (4)× 2所得 原式可由 × × × × 所得
θ θ θ θ θ ∴∆ r H m = 2∆ r H m (1) + 3∆ r H m ( 2 ) + 6∆ r H m ( 3) + 2∆ r H m ( 4 )
= 2 × 92.38 + 3 × ( −571.69 ) + 6 × 44.02 + 2 ×180.72 = −904.69kJ ⋅ mol
热力学第一定律的表述方式及应用

热力学第一定律的表述方式及应用热力学第一定律是热力学中的基本定律之一,也被称为能量守恒定律。
它指出,在任何一个热力学系统中,系统的内能变化等于系统所吸收的热量与对外做的功的代数和。
这一定律为我们理解和描述热力学系统的行为提供了重要的理论依据。
一、热力学第一定律的表述方式热力学第一定律可以用以下三种方式进行表述:1. 微分形式在微分形式下,热力学第一定律可以表示为:[ = Q - W ]其中,( U ) 表示系统的内能,( Q ) 表示系统吸收的热量,( W ) 表示系统对外做的功。
2. 积分形式在积分形式下,热力学第一定律可以表示为:[ U = Q - W ]其中,( U ) 表示系统内能的变化量,( Q ) 表示系统吸收的热量,( W ) 表示系统对外做的功。
3. 宏观形式在宏观形式下,热力学第一定律可以表示为:[ _{i=1}^{n} i = {j=1}^{m} _j ]其中,( _i ) 表示系统从第 ( i ) 个热源吸收的热量,( _j ) 表示系统对外做第 ( j )项功。
二、热力学第一定律的应用热力学第一定律在工程、物理等领域有着广泛的应用,下面列举几个常见的应用实例:1. 热机效率的计算热机效率是指热机所做的功与吸收的热量之比。
根据热力学第一定律,热机所做的功等于吸收的热量减去内能的变化量。
因此,热机效率可以表示为:[ = ]2. 制冷机的性能分析制冷机的工作原理是利用工作物质在循环过程中吸收热量,从而实现低温环境的创造。
根据热力学第一定律,制冷机吸收的热量等于制冷量与制冷机压缩机所做的功之和。
因此,可以通过热力学第一定律来分析制冷机的性能。
3. 太阳能热水器的设计太阳能热水器利用太阳能将光能转化为热能,为用户提供热水。
根据热力学第一定律,太阳能热水器吸收的热量等于水温升高所吸收的热量与热水器损失的热量之和。
因此,在设计太阳能热水器时,需要考虑热量的损失,以提高热水器的效率。
4. 热传导过程的分析热传导是热量在物体内部由高温区向低温区传递的过程。
热力学第一定律应用
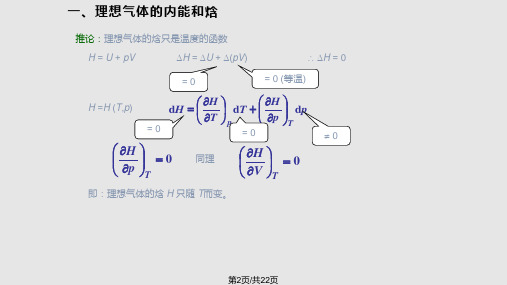
单原子分子
双原子分子 非线性多原子分子 (3) 实际气体 (4) 凝聚系统
CV ,m
3 2
R
5 CV ,m 2 R
CV,m = 3R
Cp, m-CV, m R
Cp, m CV, m
如He
如H2 ,O2 ,N2 如H2O (g)
第4页/共22页
三、理想气体非绝热过程Q,W,U,H计算
1 恒温过程
H = n Cp,m ( T2 -T1 ) = …… = -9005 J
第16页/共22页
五、热力学第一定律对实际气体应用
理想气体U、H只是T的函数,与p、V无关, 因为分子间无作用力,无位能。
实际气体分子间有作用力,p、V的变化影响U、H
1. 焦耳-汤姆逊实验
节流膨胀实验
恒定压力的气体, 经多孔塞膨胀, 使其为压力恒定的低压气体
(1) 恒温可逆
273 K 200 kPa
(2) 向真空 (3) 恒温恒外压
(4) 恒容降温
100 kPa
解 (1) 恒温可逆
U = H = 0
Q = -W (2) 向真空
nRT ln p2 8.314 273 ln 100 = 1573 J
p1
200
U = H = 0
Q =-W=0
第6页/共22页
U = 0 H = 0 Q =-W
按不同过程计算W
2 非恒温过程 先求出终态温度 T2 H = nCp,m (T2-T1 ) U = nCV,m (T2-T1 ) Q = U-W
按不同过程计算W及Q
第5页/共22页
三、理想气体非绝热过程Q,W,U,H计算
例 计算1mol单原子理想气体以下过程的Q、W、U、H
大学化学《物理化学-热力学第一定律及其应用》课件

(1)克服外压为 p ',体积从V1 膨胀到V ' ; (2)克服外压为 p",体积从V ' 膨胀到V " ;
(3)克服外压为 p2,体积从V "膨胀到V2 。
We,3 p '(V 'V1)
p"(V "V ')
p
p1
p1V1
p2 (V2 V ")
p'
所作的功等于3次作功的加和。p "
p 'V ' p"V "
可见,外压差距越小,膨 p2 胀次数越多,做的功也越多。
V1 V ' V "
p2V2
V2 V
上一内容 下一内容 回主目录
返回
2024/9/13
功与过程(多次等外压膨胀)
p"
p' p1
V"
V1
V'
p
p1
p1V1
p2
V2
p'
p 'V '
阴影面积代表We,3
p"
p"V "
p2
p2V2
上一内容
下一内容
V1 V ' V "
第三步:用 p1 的压力将体系从V ' 压缩到 V1 。
p
W' e,1
p"(V "
V2 )
p1
p1V1
p' (V ' V ")
p'
p 'V '
p1(V1 V ' )
回主目录
V2 V
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
能量守恒定律
到1850年,科学界公认能量守恒定律是自 然界的普遍规律之一。能量守恒与转化定律可 表述为:
自然界的一切物质都具有能量,能量有各 种不同形式,能够从一种形式转化为另一种形 式,但在转化过程中,能量的总值不变。
上一内容 下一内容 回主目录
上一内容 下一内容 回主目录
返回
2021/3/2
体系与环境
体系(System)
在科学研究时必须先确定 研究对象,把一部分物质与其 余分开,这种分离可以是实际 的,也可以是想象的。这种被 划定的研究对象称为体系,亦 称为物系或系统。 环境(surroundings)
与体系密切相关、有相互 作用或影响所能及的部分称为 环境。
返回
2021/3/2
பைடு நூலகம்
体系的性质
用宏观可测性质来描述体系的热力学状态, 故这些性质又称为热力学变量。可分为两类:
广度性质(extensive properties) 又称为容量性质,它的数值与体系的物质的
量成正比,如体积、质量、熵等。这种性质有加 和性,在数学上是一次齐函数。
强度性质(intensive properties) 它的数值取决于体系自身的特点,与体系的
数量无关,不具有加和性,如温度、压力等。它 在数学上是零次齐函数。指定了物质的量的容量 性质即成为强度性质,如摩尔热容。
上一内容 下一内容 回主目录
返回
2021/3/2
热力学平衡态
如果处在一定环境条件下的系统,其所有的性质 均不随时间而变化;而且当此系统与环境隔离后 ,也不会引起系统任何性质的变化,则称该系统 处于热力学平衡状态。
上一内容 下一内容 回主目录
返回
2021/3/2
体系分类
(3)孤立体系(isolated system) 体系与环境之间既无物质交换,又无能量交换,
故又称为隔离体系。有时把封闭体系和体系影响所及 的环境一起作为孤立体系来考虑。
上一内容 下一内容 回主目录
返回
2021/3/2
体系分类
上一内容 下一内容 回主目录
上一内容 下一内容 回主目录
返回
2021/3/2
状态方程
体系状态函数之间的定量关系式称为状态方 程(state equation )。
对于一定量的单组分均匀体系,状态函数 T,p,V 之间有一定量的联系。经验证明,只有两个 是独立的,它们的函数关系可表示为:
T=f(p,V) p=f(T,V) V=f(p,T)
例如,理想气体的状态方程可表示为: pV=nRT
上一内容 下一内容 回主目录
返回
2021/3/2
热和功
热(heat)
体系与环境之间因温差而传递的能量称为
热,用符号Q 表示。 Q的取号:
体系吸热,Q>0;
体系放热,Q<0 。
功(work)
体系与环境之间传递的除热以外的其它能量 都称为功,用符号W表示。
功可分为膨胀功和非膨胀功两大类。W的取号:
环境对体系作功,W>0;体系对环境作功,W<0 。
Q和W都不是状态函数,其数值与变化途径有关。
上一内容 下一内容 回主目录
返回
2021/3/2
1.2 热力学第一定律
•热功当量 •能量守恒定律 •热力学能 •第一定律的文字表述 •第一定律的数学表达式
上一内容 下一内容 回主目录
第一章热力学第一定律及其应用
上一内容 下一内容 回主目录
返回
上一内容 下一内容 回主目录
返回
上一内容 下一内容 回主目录
返回
上一内容 下一内容 回主目录
返回
热力学的方法
热力学方法
在经验定律的基础上,通过演绎的方法,得出一般 性的规律。高度的普适性和可靠性) 只考虑过程的初、末态,不考虑过程的细节。(知 其然,不知其所以然)
上一内容 下一内容 回主目录
返回
2021/3/2
体系分类
根据体系与环境之间的关系,把体系分为三类: (1)敞开体系(open system)
体系与环境之间既有物质交换,又有能量交换。
上一内容 下一内容 回主目录
返回
2021/3/2
体系分类
(2)封闭体系(closed system) 体系与环境之间无物质交换,但有能量交换。
改变。
化学平衡(chemical equilibrium ) 反应体系中各物的数量不再随时间而改变。
上一内容 下一内容 回主目录
返回
2021/3/2
热力学平衡态
热平衡 热 力 学 力平衡 平 衡
物质平衡
相平衡 化学平衡
上一内容 下一内容 回主目录
返回
2021/3/2
状态函数
定义:描述(确定)系统状态的系统的各宏观物 理性质(如温度、压力、体积等)称为系统的热 力学性质,又称为状态函数(state function)。 其数值仅取决于体系所处的状态,而与体系的历 史无关;它的变化值仅取决于体系的始态和终态 ,而与变化的途径无关。
热平衡(thermal equilibrium) 体系各部分温度相等。
上一内容 下一内容 回主目录
返回
2021/3/2
热力学平衡态
力学平衡(mechanical equilibrium) 体系各部的压力都相等,边界不再移动。
如有刚壁存在,虽双方压力不等,但也能保持 力学平衡。
相平衡(phase equilibrium) 多相共存时,各相的组成和数量不随时间而
p1,V1 p2 , V2
V总= V1 + V2
P总≠p1+ p2
上一内容 下一内容 回主目录
返回
2021/3/2
状态函数
b. 广度性质是系统所含的物质的量的一次齐函数, 强度性质是零次齐函数。
若 f(x,y, )nf(x,y, )
则称 f(x,y, )是 x,y, 的 n次齐函
c.两个广度性质相除,所得为强度性质
返回
2021/3/2
热功当量
焦耳(Joule)和迈耶(Mayer)自1840年起,历经 20多年,用各种实验求证热和功的转换关系, 得到的结果是一致的。
即: 1 cal = 4.1840 J
这就是著名的热功当量,为能量守恒原理 提供了科学的实验证明。
上一内容 下一内容 回主目录
返回
2021/3/2
状态函数的特性可描述为:异途同归,值变 相等;周而复始,数值还原。
状态函数在数学上具有全微分的性质。
上一内容 下一内容 回主目录
返回
2021/3/2
状态函数
分类:广度性质(extensive property)和强度性质 (intensive property)
a. 广度性质具有部分加和性,强度性质无部分加 和性。
