二氧化碳的制取和收集装置
二氧化碳制备装置图
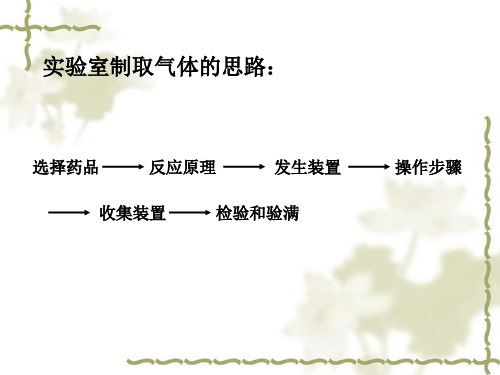
(2) 排空气法 向上排空气法:适用于密度比空气大的气体。 向下排空气法:适用于密度比空气小的气体。
不能与 空气中 的任何 成分发 生反应
制取二氧化碳的装置氧化碳的实验室制取 (1)药品:大理石或石灰石(主要成分是碳酸钙),稀盐酸。 (2)原理:碳酸钙 + 盐酸→ 水 + 二氧化碳 + 氯化钙 CaCO3 HCl H2O CO2 CaCl2
实验室制取气体的思路:
选择药品
反应原理
发生装置
操作步骤
收集装置
检验和验满
1、发生装置 由反应物状态及反应条件决定。
(1) 固固加热制气体,则用高锰酸钾制氧气的装置
(2) 固液不加热制气体,则用过氧化氢制氧气的装置
2、收集装置
收集方法由气体的密度及溶解性决定。
(1) 排水法:适用于难溶或不易溶于水,不与水发生反应的气体。
二氧化碳的制取和收集装置

二氧化碳的制取和收集装置
1:原理利用碳酸钙和盐酸的反应。
2:药品用大理石或者石灰石与稀盐酸反应。
药品选用有几个需要注意的问题
不能用浓盐酸代替稀盐酸,因为浓盐酸也有挥发性,会使制得的二氧化碳不纯,还有氯化氢气体杂质。
不能用稀硫酸代替稀盐酸,因为硫酸与碳酸钙反应生成的硫酸钙微溶于水,会覆盖在大理石表面,阻止反应的进行。
不能用碳酸钠代替大理石或者石灰石,因为反应速率太快,不容易收集。
3:装置的选择,实验室制取的发生装置和收集装置在制取氧气是已详细说明了。
实验室制取二氧化碳的发生装置用固液常温,收集装置用排空气法,不能用排水法。
如果用多功能瓶,应该长进短出。
4:操作步骤:连接仪器—检查装置气密性—加入药品—收集气体
5:验满:用燃着的木条放在集气瓶口,若木条熄灭,则说明已收集满。
6:检验:把生成的气体通入澄清石灰水中,若澄清石灰水变混浊,则说明该气体是二氧化碳。
7:经常会出现说制取一瓶纯净和干燥的二氧化碳,是提示你需要除杂和干燥,先除杂后干燥。
制取二氧化碳中,含有的气体杂质一般是氯化氢,常用饱和的碳酸氢钠溶液除去,然后用浓硫酸干燥。
〖化 学〗二氧化碳的实验室制取课件---2024-2025学年九年级化学人教版上册

方案
现象
1 在试管①中取一定量碳酸钠粉 末,再加入适量稀盐酸
2 在试管②中取一定量CaCO3粉 末,再加入适量稀盐酸
3 在试管③中取一定量块状大理 石,再加入适量稀盐酸
一、制取二氧化碳的药品的选取及原理
一、制取二氧化碳的药品的选取及原理
实验现象:
实验内容 ① Na2CO3粉末、稀盐酸 ② CaCO3粉末、稀盐酸 ③ 块状大理石、稀盐酸
气球变化 迅速胀大 迅速胀大 逐渐胀大
反应速率 快 快 适中
是否易于收集 不易收集 不易收集 容易收集
结论: 实验室常用_石__灰__石__或__大__理__石__和稀__盐__酸__反应制取二氧化碳。
一、制取二氧化碳的药品的选取及原理
资料卡片
研究发现,一般含有碳酸根离子( CO23- )的物质,在常温下能与盐 酸、稀硫酸反应产生二氧化碳。
习题训练
1.厕所用清洁剂中含有盐酸,如果不慎洒到大理石地面上,会发出嘶
嘶声,并有气体产生,这种气体是( A )
A.二氧化碳
B.氧气
C.氢气
D.二氧化硫
2.为鉴别分别盛有空气、氧气、二氧化碳的三瓶气体,应选用的方法
是( D ) A.观察气体颜色
B.倒入澄清石灰水
C.闻气体的气味
D.插入燃着的木条
习题训练
制取 收集
检验 验满
检查气密性: 关闭止水夹,向长颈漏斗注水,若形成一段稳定的水柱, 则装置气密性良好。
注意事项: (1)长颈漏斗下端要_伸__入__液__面__以__下__。(防止气体逸出)
(2)导管要伸近集气瓶_底__部__。(排尽空气 )
(3)导管不能伸入_液__面__以__下__。(利于气体排出 )
《二氧化碳的实验室制取与性质》 讲义

《二氧化碳的实验室制取与性质》讲义一、二氧化碳的性质在了解二氧化碳的制取方法之前,我们先来认识一下二氧化碳的性质。
二氧化碳是一种无色、无味的气体。
在通常状况下,它的密度比空气大,能溶于水,在一定条件下还能与水反应生成碳酸。
二氧化碳不能燃烧,也不支持燃烧。
这一性质使得它在灭火方面有着广泛的应用。
此外,二氧化碳还是一种重要的温室气体,对地球的气候有着重要的影响。
二、实验室制取二氧化碳的原理实验室制取二氧化碳通常使用大理石(或石灰石)与稀盐酸反应。
化学方程式为:CaCO₃+ 2HCl = CaCl₂+ H₂O + CO₂↑选择大理石(或石灰石)与稀盐酸反应制取二氧化碳,主要是因为该反应速率适中,便于控制,且原料易得。
三、实验装置1、发生装置实验室制取二氧化碳的发生装置通常采用“固液不加热型”。
这是因为反应不需要加热,且大理石(或石灰石)是固体,稀盐酸是液体。
常见的发生装置有以下几种:(1)简易装置:由长颈漏斗、锥形瓶和双孔橡皮塞组成。
长颈漏斗的下端要伸入液面以下,以防止生成的气体从长颈漏斗逸出。
(2)启普发生器:这是一种能控制反应随时发生和停止的装置。
当打开导气管上的活塞时,酸液与固体接触,反应发生;当关闭活塞时,产生的气体使容器内压强增大,将酸液压回长颈漏斗,使酸液与固体脱离接触,反应停止。
2、收集装置由于二氧化碳的密度比空气大,且能溶于水,所以通常采用向上排空气法收集二氧化碳。
收集装置一般由集气瓶和玻璃片组成。
收集时,导气管要伸到集气瓶的底部,以保证收集到的二氧化碳较为纯净。
四、实验步骤1、检查装置的气密性在装入药品之前,首先要检查装置的气密性。
方法是:连接好装置,将导管的一端放入水中,然后用手握住锥形瓶,若导管口有气泡冒出,松开手后,导管内形成一段水柱,则说明装置气密性良好。
2、装入药品先在锥形瓶中放入适量的大理石(或石灰石),然后通过长颈漏斗或分液漏斗向锥形瓶中加入稀盐酸。
3、收集气体用向上排空气法收集二氧化碳。
学生实验6 二氧化碳的实验室制取与性质(课件)鲁教版(2024)化学九年级上册

感悟新知
知1-练
(4)若要用F 装置检验CO2,在F 装置中盛放的试剂名称是 ___澄__清__石__灰__水___,CO2 应从____c__(填“b”或“c”)端通入, 实验现象为______澄__清__石__灰__水__变__浑__浊_______。
感悟新知
知1-练
解题秘方:解答本题应采用标准实验对照法,即对照 实验原理和气体的性质来选择装置。
教你一招:
知1-练
1. 应用实验室制取气体的思路和方法解题时,首先要
根据信息抓住关键字眼,如“~~加~~热~~”~~“~~固~~体~~”~~“~~液~~体~~”
“~~易~~(或~~难~~)~溶~~于~~水~~”等,然后根据这些信息来选择发生装 置和收集装置。
2. 选择实验仪器时,先发生装置,后收集装置。发生
操作
向盛有二氧化碳的塑料瓶B 中倒入适量澄清石 灰水,振荡
现象 澄清石灰水变浑浊
二氧化碳可以与澄清石灰水反应。化学方程式:
结论
Ca(OH)2+CO2
CaCO3 ↓ +H2O
感悟新知
知1-讲
(3)实验三:探究二氧化碳能否燃烧及支持燃烧
操作 将准备好的两支蜡烛放入500 mL 的烧杯中,分别 点燃,然后慢慢倒入塑料瓶C 中的二氧化碳气体
(1)仪器a 的名称是__长__颈__漏__斗___。
感悟新知
知1-练
(2)实验室需纯净的氧气用于铁丝燃烧实验,从A~E 中选择合适的制取和收集氧气的装置是_A__、__E__或__B_、__E__ (填字母序号)。
感悟新知
知1-练
(3)为探究二氧化碳的性质,小丽制取并收集了一瓶二氧 化碳气体,小丽应选择的药品是__大__理__石__或__石__灰__石__和__稀__盐__酸____ (填名称),反应的化学方程式是_C__a_C_O__3+__2_H_C__l _____________ __C__a_C_l_2+__H_2_O_+_C__O_2__↑__;从A~E 装置中选择的收集装置应该 是____C____(填字母序号)。
《二氧化碳的实验室制取与性质》 讲义

《二氧化碳的实验室制取与性质》讲义一、二氧化碳的性质在我们深入了解二氧化碳的实验室制取方法之前,先来认识一下二氧化碳的性质。
二氧化碳是一种无色、无味的气体。
它的密度比空气大,所以在实验中,我们常常能看到二氧化碳会像“瀑布”一样向下倾倒。
二氧化碳能溶于水,通常情况下,一体积水大约能溶解一体积的二氧化碳。
溶解在水中的二氧化碳会部分与水发生反应,生成碳酸。
这也是为什么我们将二氧化碳通入紫色石蕊试液中,试液会变红的原因。
二氧化碳不可燃烧,一般也不支持燃烧。
这一性质在灭火中有着重要的应用。
二、二氧化碳的实验室制取(一)实验药品实验室制取二氧化碳通常使用大理石(或石灰石)与稀盐酸反应。
大理石和石灰石的主要成分都是碳酸钙(CaCO₃),稀盐酸的溶质是氯化氢(HCl)。
(二)反应原理碳酸钙与稀盐酸反应的化学方程式为:CaCO₃+ 2HCl = CaCl₂+ H₂O + CO₂↑(三)实验装置制取二氧化碳的实验装置包括发生装置和收集装置两部分。
1、发生装置由于反应物是固体和液体,且反应不需要加热,所以我们选择“固液不加热型”发生装置。
常见的有以下两种:(1)简易装置:用长颈漏斗和锥形瓶组成。
长颈漏斗的下端要伸入液面以下,形成液封,防止气体从长颈漏斗逸出。
(2)启普发生器:它能随时控制反应的发生和停止。
2、收集装置因为二氧化碳的密度比空气大,且能溶于水,所以我们采用向上排空气法收集二氧化碳。
收集装置通常由集气瓶和导管组成。
导管要伸到集气瓶的底部,以便将瓶内的空气排尽,收集到更纯净的二氧化碳。
(四)实验步骤1、检查装置的气密性在装入药品之前,我们要先检查装置的气密性。
方法是:连接好装置,将导管的一端放入水中,然后用手紧握容器外壁,如果导管口有气泡冒出,松开手后导管内形成一段水柱,说明装置的气密性良好。
2、装入药品先向锥形瓶(或反应容器)中加入大理石(或石灰石),然后通过长颈漏斗(或其他添加仪器)慢慢加入稀盐酸。
3、收集气体用向上排空气法收集二氧化碳。
模块复习06 二氧化碳的制取(解析版)
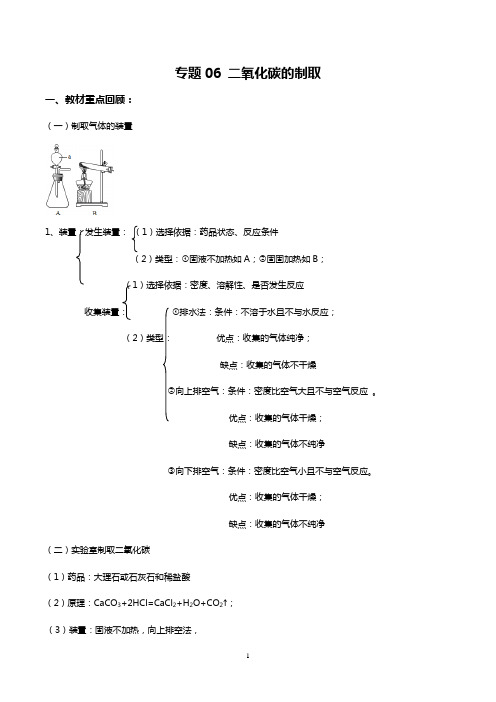
专题06 二氧化碳的制取一、教材重点回顾:(一)制取气体的装置1、装置:发生装置:(1)选择依据:药品状态、反应条件(2)类型:①固液不加热如A;②固固加热如B;(1)选择依据:密度、溶解性、是否发生反应收集装置:①排水法:条件:不溶于水且不与水反应;(2)类型:优点:收集的气体纯净;缺点:收集的气体不干燥②向上排空气:条件:密度比空气大且不与空气反应。
优点:收集的气体干燥;缺点:收集的气体不纯净③向下排空气:条件:密度比空气小且不与空气反应。
优点:收集的气体干燥;缺点:收集的气体不纯净(二)实验室制取二氧化碳(1)药品:大理石或石灰石和稀盐酸(2)原理:CaCO3+2HCl=CaCl2+H2O+CO2↑;(3)装置:固液不加热,向上排空法,(4)步骤:①连接装置;②检查装置的气密性;③向锥形瓶中加入大理石;④从长颈漏斗加入稀盐酸;⑤收集二氧化碳;⑥验满。
(5)收集法:向上排空气法:原因密度比空气大且不与空气反应;能溶于水,不能用排水法。
(6)验满:向上排空气法,用燃着的木条放在,瓶口,木条熄灭则收集满。
(7)检验:将气体通入澄清石灰水,若石灰水浑浊,则是二氧化碳。
原理:Ca(OH)2+CO2 =CaCO3↓+H2O(8)注意事项:①长颈漏斗的下端要伸到液面以下(防止产生的气体从长颈漏斗口逸出);②锥形瓶中的导管只能刚刚露出橡皮塞(有利于产生的气体排出);③集气瓶中的导管口要接近集气瓶底(目的:便于排净空气)。
(9)药品的选择:①实验室制取二氧化碳不能用稀硫酸和大理石反应是因为(稀硫酸和大理石反应生成的硫酸钙微溶于水,会附着在大理石表面,阻碍反应的继续发生)。
②也不用浓盐酸是因为(浓盐酸易挥发,使制得的二氧化碳中混有氯化氢气体而不纯)。
二、中考考点梳理二氧化碳的制取,是每年中考的必考内容之一,考查的知识点包括制取二氧化碳的装置、药品、原理、步骤、收集、验满、检验、注意事项等;以实验探究题为主。
也有少量选择题。
二氧化碳的制取(实验教案)

实验室制取二氧化碳一、实验目的1、使学生初步掌握实验室制取二氧化碳的药品、原理、实验装置、收集方法等。
2、进一步培养学生的观察能力和思维能力。
3、渗透物质的性质决定制法的思想方法。
二、反应原理CaCO3+2HCl=CaCl2+H2O+CO2↑三、仪器装置(如下图所示)四、实验步骤“查”:检查装置的气密性。
“装”:从锥形瓶口装大理石,塞紧塞子。
“加”:从长颈漏斗(或分液漏斗)加入稀盐酸。
“收”:收集气体。
“验满”:用燃着的木条放在集气瓶口,木条熄灭证明已收集满。
五、收集方法用向上排空气法收集二氧化碳(因为二氧化碳密度比空气大)。
不能用排水法收集二氧化碳(因为二氧化碳溶于水)。
六、注意事项装置注意事项:发生装置的导管露出塞子即可,不能伸入过长;长颈漏斗下端要伸入液面以下。
操作注意事项:用向上排空气法收集二氧化碳时导管要伸入集气瓶底部。
七、实验室制取二氧化碳析疑(一)为什么选用大理石或石灰石制取二氧化碳?答:大理石或石灰石的主要成分是碳酸钙。
碳酸盐跟酸起反应,一般都有二氧化碳生成。
若选用可溶性的碳酸盐(如碳酸钠等),与酸反应速度过快,难以控制;若选用不溶性碳酸盐(如碳酸镁等),则其来源一般较少。
大理石或石灰石与酸反应适中,其在自然界中含量也极其丰富,价格低廉。
所以,选用大理石或石灰石制二氧化碳。
(二)实验室制取二氧化碳时,为什么最好选用稀盐酸?答:如果用稀硫酸和大理石或石灰石反应,有关化学方程式为:CaCO3+H2SO4=CaSO4+H2O+CO2↑,结果生成微溶性固体硫酸钙,它覆盖在大理石或石灰石表面,使酸与大理石或石灰石脱离接触,导致反应太缓慢。
如果用硝酸与大理石或石灰石反应,由于硝酸是一种不稳定性的酸,在见光或受热时易分解:4HNO3光照4NO2↑+O2↑+2H2O,从而使制得的CO2中混有NO2和O2等杂质。
如果用浓盐酸和大理石或石灰石反应,由于浓盐酸具有挥发性,使制得的CO2中混有较多的氯化氢气体。
