西洛他唑杂质种类整理列表
《美国药典》(usp40)中西洛他唑质量标准浅析

2019年10月临床医学DOI :10.19347/ki.2096-1413.201930013基金项目:国家自然科学基金项目(No.71603199);陕西省自然科学基础研究计划项目(No.2018JM7083)。
作者简介:蒋玲(1978-),女,汉族,江苏徐州人,高级工程师,硕士。
研究方向:药剂学。
*通讯作者:毕学苑,E -mail:vickeymu@.西洛他唑由日本大冢制药公司开发,1999年获得FDA 注册批准。
西洛他唑不仅可抑制血小板聚集,防止血栓形成和血管闭塞[1],还可降低皮层下梗死患者血浆炎症因子水平[2]。
因此,控制西洛他唑的质量对临床用药意义重大。
本研究就《美国药典》(USP40)收载的西洛他唑质量标准,与《中国药典》2015版二部对比,旨在更好地控制西洛他唑的质量,现报道如下。
1方法比较1.1定义按干燥品计算,含西洛他唑应为98.0%~102.0%。
与《中国药典》2015版二部相同。
1.2包装与储存密闭容器中室温储存。
USP40规定了储存温度,《中国药典》2015版二部中规定为密封保存,未要求储存温度。
1.3鉴别1.3.1红外光谱法。
供试品与对照品红外光谱一致。
与《中国药典》2015版二部相同。
红外光谱法特征性强、测定快速、试样用量少、操作简便、分析灵敏度高。
两国药典均采用此法,均可准确对西洛他唑鉴别。
1.3.2液相色谱法。
供试品溶液和对照品溶液主峰的保留时间一致。
与《中国药典》2015版二部相同。
液相色谱法广泛应用于药物的鉴别,由于保留时间与组分的结构和性质有关,是定性的参数,保留时间一致,表示药物和对照品一致。
两国药典均采用此法,均可准确对西洛他唑鉴别。
1.4干燥失重USP40中规定为110℃下干燥3h ,减失重量不得超过0.3%。
《中国药典》2015版二部中规定为105℃干燥至恒重,减失重量不得超过0.5%。
干燥失重的测定准确与否影响着化学结构的判断和含量测定的结果[3],因此,限度越严格,对于含量测定的影响越小。
西洛他唑杂质汇总
项目报批 纯度高于98%
西洛他唑杂质4 Cilostazol Impurity 4
N/A
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
扬信医药代理各品种杂质对照品:舒更葡糖钠杂质,达托霉素杂质,依维莫司杂质,他克莫司杂质,阿奇霉素杂质,克拉维酸钾杂质, 红霉素杂质,克拉霉素杂质,林可霉素杂质,罗红霉素杂质,克林霉素杂质,恩曲他滨杂质,艾地那非杂质,瑞卢戈西洛他唑杂质2 Cilostazol Impurity 2
N/A
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
西洛他唑杂质3 Cilostazol Impurity 3 1796891-27-4
10mg 25mg 50mg 100mg 更大规格请咨询
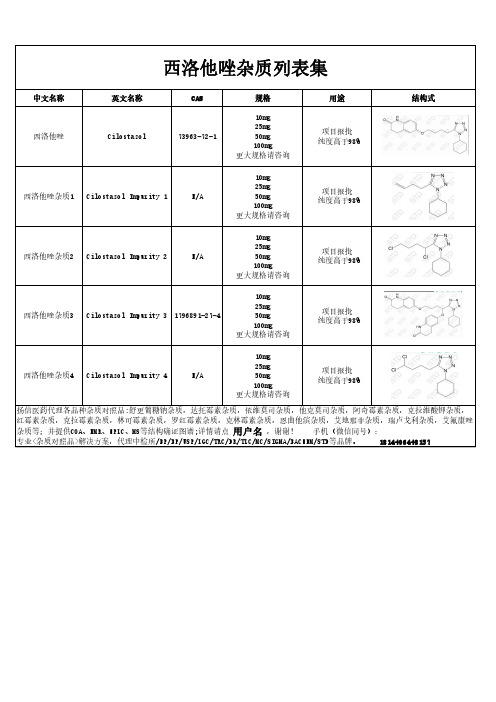
西洛他唑杂质列表集
中文名称 西洛他唑
英文名称 Cilostazol
CAS 73963-72-1
规格
10mg 25mg 50mg 100mg 更大规格请咨询
用途
项目报批 纯度高于98%
结构式
西洛他唑杂质1 Cilostazol Impurity 1
N/A
10mg 25mg 50mg 100mg 更大规格请咨询
杂质等;并提供COA、NMR、HPLC、MS等结构确证图谱;详情请点 用户名 ,谢谢! 手机(微信同号):
专业<杂质对照品>解决方案,代理中检所/EP/BP/USP/LGC/TRC/DR/TLC/MC/SIGMA/BACHEM/STD等品牌。 1814+064+3157
西洛他唑学习资料(1)

各型磷酸二酯酶的分布及作用特点
PDE类 型
PDE I
PDE II
PDE III
PDE IV PDE V
亚型
A、B、C三 种不同基因
编码
A1、A2和A3
A、B不同基 因产物
A、B、C、 D不同基因产
物 2个立体异构
体
生物效应及作用
PDEIA和PDE1B主要水解 cGMP;PDE1C同时水解 cAMP和cGMP
西洛他唑 — 抗血小板聚集药物
从各型PDE的分布以及作用特点看,西洛他 唑专一性抑制PDE III,基本药效功能为抗血小 板聚集。
高选择性磷酸二酯酶抑制剂
基础研究表明,西洛他唑对磷酸二酯酶III(PDE III)具有高度选择性的抑制作用。
此外,对磷酸二酯酶 IV有很弱的抑制作用,而 其他型磷酸二酯酶几乎没有作用。
* 组内治疗前后P<0.05;#组间治疗前后变化程度P<0.05 高妍等.中华内分泌代谢杂志.1999.15(3)
显著改善下肢动脉闭塞
David L et al., Circulation, 1998, 98:678-686
西洛他唑对下肢溃疡
5例患者患有外周动脉疾病和不愈小腿溃疡 不适合行血管重建手术 西洛他唑100mg po bid 结果:溃疡愈合5/5;静息痛缓解3/5
临床常用抗血小板药
环氧化酶阻断剂药物:阿司匹林 干扰ADP介导的血小板活化药:
噻氯匹啶(抵克力得) 氯吡格雷(波立维) 磷酸二脂酶抑制剂: 西洛他唑 潘生丁 血小板纤维蛋白原受体拮抗剂 :阿昔单抗
更安全的抗血小板药物 ——西洛他唑片
西洛他唑的历史回顾
1988
1980
日本大冢在日本申请专利
药物杂质列表
Dithianonimpurity2
二氰蒽醌杂质2
N/A
10mg-25mg-50mg-100mg
≥95%
Dithianonimpurity3
二氰蒽醌杂质3
N/A
10mg-25urity4
二氰蒽醌杂质4
21634-42-4
10mg-25mg-50mg-100mg
氟氯西林钠杂质
N/A
10mg-25mg-50mg-100mg
≥95%
Arginine
精氨酸
7200-25-1
10mg-25mg-50mg-100mg
≥95%
Arginineimpurity1
精氨酸杂质1
N/A
10mg-25mg-50mg-100mg
≥95%
Arginineimpurity2
精氨酸杂质2
天津药明康德新药开发有限公司杂质研究中心提供。
Spectinomycin ImpurityF
大观霉素杂质F
N/A
10mg-25mg-50mg-100mg
≥95%
pleuromulin
截短侧耳素
125-65-5
10mg-25mg-50mg-100mg
≥95%
Pleuromulinimpurity
截短侧耳素杂质
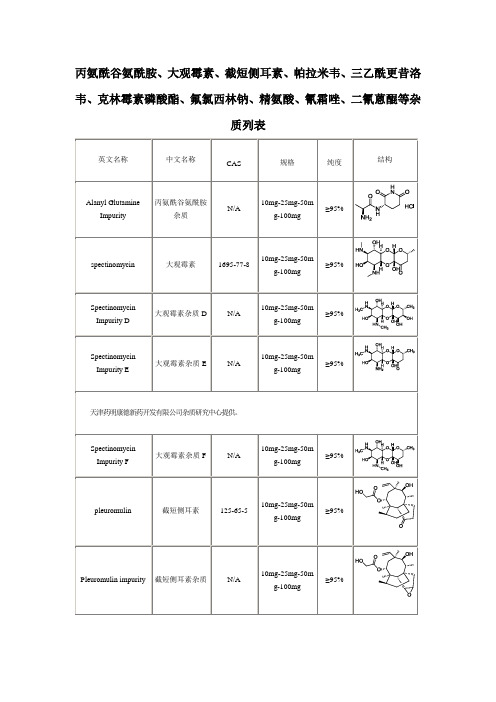
丙氨酰谷氨酰胺、大观霉素、截短侧耳素、帕拉米韦、三乙酰更昔洛韦、克林霉素磷酸酯、氟氯西林钠、精氨酸、氰霜唑、二氰蒽醌等杂质列表
英文名称
中文名称
CAS
规格
纯度
结构
Alanyl GlutamineImpurity
丙氨酰谷氨酰胺杂质
N/A
10mg-25mg-50mg-100mg
多西他赛杂质整理总结文档

多西他赛杂质7(多西他赛EP杂质G)Docetaxel Impurity 7(Docetaxel EP Impurity G)32427D 125354-16-710mg-25mg-50mg-100mg 多西他赛杂质8Docetaxel Impurity 832428D N/A10mg-25mg-50mg-100mg多西他赛杂质9Docetaxel Impurity 932429D N/A10mg-25mg-50mg-100mg多西他赛杂质10Docetaxel Impurity 10324210DN/A10mg-25mg-50mg-100mg多西他赛杂质11Docetaxel Impurity 11324211DN/A10mg-25mg-50mg-100mg多西他赛杂质12Docetaxel Impurity 12324212DN/A10mg-25mg-50mg-100mg多西他赛杂质13(2-苯甲酰-2-戊烯基多西他赛)DocetaxelImpurity 13(2-Debenzoyl-2-pentenoylDocetaxel)324213D 1412898-66-810mg-25mg-50mg-100mg多西他赛杂质14Docetaxel Impurity 14324214DN/A10mg-25mg-50mg-100mgImpurity 15D 250mg-100mg多西他赛杂质16DocetaxelImpurity 16324216DN/A10mg-25mg-50mg-100mg多西他赛杂质17Docetaxel Impurity 17324217D 145533-34-210mg-25mg-50mg-100mg多西他赛杂质18DocetaxelImpurity 18324218D 208406-86-410mg-25mg-50mg-100mg多西他赛杂质19DocetaxelImpurity 19324219DN/A10mg-25mg-50mg-100mg多西他赛杂质20Docetaxel Impurity 20324220D 172018-16-510mg-25mg-50mg-100mg多西他赛杂质21DocetaxelImpurity 21324221D 92950-45-310mg-25mg-50mg-100mg多西他赛杂质22DocetaxelImpurity 22324222D 151636-94-110mg-25mg-50mg-100mgImpurity 23D 150mg-100mg多西他赛杂质24DocetaxelImpurity 24324224DN/A10mg-25mg-50mg-100mg多西他赛杂质25Docetaxel Impurity 25324225D 110258-92-910mg-25mg-50mg-100mg多西他赛杂质26DocetaxelImpurity 26324226D 114915-19-410mg-25mg-50mg-100mg多西他赛杂质27DocetaxelImpurity 27324227DN/A10mg-25mg-50mg-100mg多西他赛杂质28Docetaxel Impurity 28324228DN/A10mg-25mg-50mg-100mg多西他赛杂质29Docetaxel Impurity 29324229DN/A10mg-25mg-50mg-100mg多西他赛杂质30Docetaxel Impurity 30324230DN/A10mg-25mg-50mg-100mgImpurity 31D50mg-100mg多西他赛杂质32Docetaxel Impurity 32324232DN/A10mg-25mg-50mg-100mg多西他赛杂质33Docetaxel Impurity 33324233DN/A10mg-25mg-50mg-100mg多西他赛杂质34Docetaxel Impurity 34324234DN/A10mg-25mg-50mg-100mg多西他赛杂质35Docetaxel Impurity 35324235D 1354900-65-410mg-25mg-50mg-100mg多西他赛杂质36Docetaxel Impurity 36324236D 1095547-98-010mg-25mg-50mg-100mg多西他赛杂质37Docetaxel Impurity 37324237D 1095547-96-810mg-25mg-50mg-100mg多西他赛杂质38Docetaxel Impurity 38324238DN/A10mg-25mg-50mg-100mgImpurity 39D50mg-100mg多西他赛杂质40Docetaxel Impurity 40324240D 133524-69-310mg-25mg-50mg-100mg多西他赛杂质41DocetaxelImpurity 41324241DN/A10mg-25mg-50mg-100mg多西他赛杂质42Docetaxel Impurity 42324242DN/A10mg-25mg-50mg-100mg多西他赛杂质43Docetaxel Impurity 43324243D 154306-81-710mg-25mg-50mg-100mg多西他赛杂质44DocetaxelImpurity 44324244D 147058-27-310mg-25mg-50mg-100mg多西他赛杂质45DocetaxelImpurity 45324245D 154428-10-110mg-25mg-50mg-100mg多西他赛杂质46DocetaxelImpurity 46324246D 157240-36-310mg-25mg-50mg-100mgImpurity 47D 58-250mg-100mg多西他赛杂质48Docetaxel Impurity 48324248D 201856-57-710mg-25mg-50mg-100mg多西他赛杂质49DocetaxelImpurity 49324249D 133577-33-010mg-25mg-50mg-100mg多西他赛杂质50DocetaxelImpurity 50324250DN/A10mg-25mg-50mg-100mg多西他赛杂质51Docetaxel Impurity 51324251D119-52-810mg-25mg-50mg-100mg多西他赛杂质52Docetaxel Impurity 52324252DN/A10mg-25mg-50mg-100mg多西他赛杂质53Docetaxel Impurity 53324253D 165173-47-710mg-25mg-50mg-100mg多西他赛杂质54DocetaxelImpurity 54324254DN/A10mg-25mg-50mg-100mg。
RP-HPLC法测定西洛他唑中的有关物质

RP-HPLC法测定西洛他唑中的有关物质摘要】目的用反相高效液相色谱法(RP-HPLC)检测西洛他唑原料中有关物质。
方法采用十八烷基硅烷键合硅胶柱(250mm×4.6µm)kromasil,梯度洗脱,DAD-UV检测器。
结果西洛他唑主峰与各杂质峰分离度好。
结论本方法简单、快速、专属性好、灵敏度高。
【关键词】西洛他唑反相高效液相色谱法有关物质峰纯度【中图分类号】R927 【文献标识码】B 【文章编号】2095-1752(2012)20-0274-02西洛他唑是第一个批准用于间歇性跛行的药物,于1998年在日本上市,1999年5月获美国FDA批准上市。
西洛他唑是喹啉类衍生物,通过抑制细胞的磷酸二酯酶(特别是对PDEⅢ的抑制)来治疗稳定性间歇性跛行。
西洛他唑和它的代谢产物是cAMP-PDEⅢ抑制剂。
抑制磷酸二酯酶活性和阻碍cAMP降解(和转化)导致cAMP在血小板和血管内上升,抑制了血小板聚集和使血管扩张,防止血栓形成和血管阻塞,从而有效的达到治疗目的。
1 仪器与试药1.1 仪器日本岛津LC-2010高效液相色谱系统; SPD-M20A光电二级管阵列检测器;LC-solution工作站;XS105S型电子天平(瑞士梅特勒-托利多公司)。
1.2 试药西洛他唑(重庆康乐制药厂,含量99.54%,批号1101001);西洛他唑对照品(中国药品生物制品检定所,批号:10063-200301)。
乙腈为色谱纯(TEDIA公司);水为自制蒸馏水;盐酸,氢氧化钠,双氧水,分析纯(汕头市西陇化工厂);2 方法与结果2.1 色谱条件色谱柱:kromasilC18(4.6mm×250mm);流动相A为乙腈;流动相B为水,流速1.0ml/min;DAD-UV检测器;进样量20µl,柱温25℃,线性梯度洗脱程序见下表:时间(分钟)流动相A(%) 流动相B(%) 洗脱0-6 25 75 恒流6.5-10 25→5075→50梯度混合10-25 50 50 恒流25-25.1 50→2550→75梯度混合25.1-40 25 75 重新平衡2.2 专属性研究取本品约100mg,置100ml量瓶中,加1mol˙L盐酸溶液10ml,室温条件下放置2小时,用相应碱中和,加流动相溶解并稀释至刻度,摇匀,滤过作为强酸破坏样品;取本品约100mg,置100ml量瓶中,加1mol˙L氢氧化钠溶液5ml,室温条件下放置2小时,用相应酸中和,加流动相溶解并稀释至刻度,摇匀,滤过作为强碱破坏样品;取本品约1g,置于蒸发皿中,放入170℃烘箱中,放置15分钟,取适量加流动相溶解并稀释至刻度,摇匀,滤过作为高温破坏样品;取本品约100mg,在4500±500Lx强光照射2h,加流动相溶解并稀释至刻度,摇匀,滤过作为强光破坏样品;取本品约100mg,置100ml量瓶,加10ml30%的过氧化氢溶液,室温条件下放置2小时;加流动相溶解并稀释至刻度,摇匀,滤过作为氧化破坏样品,取各条件下破坏样品,高效液相色谱-二极管阵列检测器进样测定,进样量为20μl,记录色谱图,结果见图1,结果表明上述色谱系统与测定方法能使西洛他唑的热、酸、碱、氧化和光破坏试验降解产物色谱峰与主峰获得良好的基线分离,二极管阵列检测器进行峰纯度测定,阈值为0.9999,可认为色谱峰为单一成分。
莫西沙星相关杂质
相关杂质整理列表中文名英文名CAS 号规格纯度结构式莫西沙星杂质1MoxifloxacinImpurity 194242-51-010mg-25mg-50mg-100mg ≥99%莫西沙星杂质3MoxifloxacinImpurity 3172602-83-410mg-25mg-50mg-100mg ≥99%莫西沙星杂质4MoxifloxacinImpurity 4452092-31-810mg-25mg-50mg-100mg ≥99%莫西沙星杂质5MoxifloxacinImpurity 51329836-33-010mg-25mg-50mg-100mg ≥99%莫西沙星杂质6MoxifloxacinImpurity 6151213-15-910mg-25mg-50mg-100mg ≥99%莫西沙星杂质7MoxifloxacinImpurity 71029364-73-510mg-25mg-50mg-100mg ≥99%莫西沙星杂质8(莫西沙星EP 杂质C)Moxifloxacin Impurity 8(MoxifloxacinEP Impurity C)1029364-75-710mg-25mg-50mg-100mg ≥99%莫西沙星杂质9MoxifloxacinImpurity 91029364-77-910mg-25mg-50mg-100mg ≥99%莫西沙星杂质10MoxifloxacinImpurity 101292904-74-510mg-25mg-50mg-100mg ≥99%莫西沙星杂质11MoxifloxacinImpurity 11268545-13-710mg-25mg-50mg-100mg ≥99%莫西沙星杂质12MoxifloxacinImpurity 12139693-52-010mg-25mg-50mg-100mg ≥99%莫西沙星杂质13MoxifloxacinImpurity 13112811-71-910mg-25mg-50mg-100mg ≥99%莫西沙星杂质15MoxifloxacinImpurity 15147459-51-6&151213-42-210mg-25mg-50mg-100mg ≥99%莫西沙星杂质16MoxifloxacinImpurity 16154093-72-810mg-25mg-50mg-100mg ≥99%莫西沙星杂质17(莫西沙星USPRC F)Moxifloxacin Impurity 17(Moxifloxacin USP RC F )1350716-67-410mg-25mg-50mg-100mg ≥99%莫西沙星杂质18MoxifloxacinImpurity 18112811-72-010mg-25mg-50mg-100mg ≥99%莫西沙星杂质19MoxifloxacinImpurity 19112811-70-810mg-25mg-50mg-100mg ≥99%莫西沙星杂质20MoxifloxacinImpurity 2029124-57-010mg-25mg-50mg-100mg ≥99%莫西沙星杂质21MoxifloxacinImpurity 21128740-13-610mg-25mg-50mg-100mg ≥99%莫西沙星杂质22MoxifloxacinImpurity 22128740-14-710mg-25mg-50mg-100mg ≥99%莫西沙星杂质23MoxifloxacinImpurity 2318184-75-310mg-25mg-50mg-100mg ≥99%莫西沙星杂质26MoxifloxacinImpurity 261322062-57-610mg-25mg-50mg-100mg ≥99%莫西沙星杂质27MoxifloxacinImpurity 27172426-88-910mg-25mg-50mg-100mg ≥99%莫西沙星杂质29MoxifloxacinImpurity 29169533-55-510mg-25mg-50mg-100mg ≥99%莫西沙星杂质30MoxifloxacinImpurity 30169533-56-6&158060-81-210mg-25mg-50mg-100mg ≥99%莫西沙星杂质31MoxifloxacinImpurity 31112811-66-210mg-25mg-50mg-100mg ≥99%莫西沙星杂质32MoxifloxacinImpurity 321117-37-910mg-25mg-50mg-100mg ≥99%莫西沙星杂质34MoxifloxacinImpurity 34721970-35-010mg-25mg-50mg-100mg ≥99%莫西沙星杂质35MoxifloxacinImpurity 351403836-23-610mg-25mg-50mg-100mg ≥99%莫西沙星杂质36MoxifloxacinImpurity 361797982-51-410mg-25mg-50mg-100mg ≥99%莫西沙星杂质39MoxifloxacinImpurity 39151213-45-510mg-25mg-50mg-100mg ≥99%莫西沙星杂质40MoxifloxacinImpurity 40151213-40-010mg-25mg-50mg-100mg ≥99%莫西沙星杂质41MoxifloxacinImpurity 41161594-54-310mg-25mg-50mg-100mg ≥99%莫西沙星杂质42MoxifloxacinImpurity 42112811-65-110mg-25mg-50mg-100mg ≥99%莫西沙星杂质43MoxifloxacinImpurity 43765-30-010mg-25mg-50mg-100mg ≥99%莫西沙星杂质46MoxifloxacinImpurity 461932499-97-210mg-25mg-50mg-100mg ≥99%莫西沙星杂质51MoxifloxacinImpurity 511395056-41-310mg-25mg-50mg-100mg ≥99%莫西沙星杂质57MoxifloxacinImpurity 57151213-39-710mg-25mg-50mg-100mg ≥99%莫西沙星杂质62MoxifloxacinImpurity 62855661-74-410mg-25mg-50mg-100mg ≥99%莫西沙星杂质67MoxifloxacinImpurity 671430075-14-110mg-25mg-50mg-100mg ≥99%莫西沙星杂质68MoxifloxacinImpurity 682085709-73-310mg-25mg-50mg-100mg ≥99%莫西沙星杂质69MoxifloxacinImpurity 691430075-08-310mg-25mg-50mg-100mg ≥99%莫西沙星杂质71MoxifloxacinImpurity 711467586-86-210mg-25mg-50mg-100mg ≥99%莫西沙星杂质75MoxifloxacinImpurity 75141290-02-010mg-25mg-50mg-100mg ≥99%莫西沙星杂质78MoxifloxacinImpurity 781571-13-710mg-25mg-50mg-100mg ≥99%莫西沙星杂质79MoxifloxacinImpurity 79652-11-910mg-25mg-50mg-100mg ≥99%莫西沙星杂质80MoxifloxacinImpurity 80133492-64-510mg-25mg-50mg-100mg ≥99%莫西沙星杂质81MoxifloxacinImpurity 8156113-42-910mg-25mg-50mg-100mg ≥99%莫西沙星杂质82MoxifloxacinImpurity 82652-03-910mg-25mg-50mg-100mg ≥99%莫西沙星杂质83MoxifloxacinImpurity 831201-31-610mg-25mg-50mg-100mg ≥99%莫西沙星杂质84MoxifloxacinImpurity 84551-62-210mg-25mg-50mg-100mg ≥99%莫西沙星杂质85MoxifloxacinImpurity 85116751-24-710mg-25mg-50mg-100mg ≥99%莫西沙星杂质86MoxifloxacinImpurity 8694695-48-410mg-25mg-50mg-100mg ≥99%莫西沙星杂质92MoxifloxacinImpurity 92557-66-410mg-25mg-50mg-100mg ≥99%莫西沙星杂质93MoxifloxacinImpurity 93109966-30-510mg-25mg-50mg-100mg ≥99%莫西沙星杂质96MoxifloxacinImpurity96112811-68-410mg-25mg-50mg-100mg≥99%湖北扬信医药科技有限公司经营上万种杂质对照品(优势供应硫酸羟氯喹杂质、硝苯地平杂质、沙丁胺醇杂质、达格列净杂质、厄贝沙坦杂质、阿莫西林克拉维酸钾杂质、利伐沙班杂质、阿托伐他汀钙杂质、西格列汀杂质、利格列汀杂质等),并代理销售中检所、STD、LGC、TLC、EP、USP、TRC等多个品牌产品,提供上万种标准品对照品,真诚为您服务。
西洛他唑片体内生物等效性研究
西洛他唑片体内生物等效性研究张惠【摘要】目的:对两种国产西洛他唑片进行生物等效性研究。
方法:用自身前后对照方法,20例健康男性受试者随机分组,单次口服参比制剂或受试制剂各100mg,60h 内间断采血样;采用高效液相色谱法测定血浆中药物浓度,计算药动学参数。
结果:2种西洛他唑片在人体内药时曲线符合二室模型,主要动力学参数 Tmax 分别为3.25±0.85、3.35±0.81h;Cmax 分别为876.70±276.48、823.79±242.37ng/ml;AUC0~t分别为11137.31±2847.19、10981.44±2475.94(ng·h)/ml,AUC0~∞分别为11974.78±3076.05、11939.44± 2998.14(ng·h)/ml,T1/2分别为11.07±5.87、10.23±8.48h;两种制剂的主要药动学参数 Cmax、AUC0~t经对数转换后进行方差分析及双单侧 t 检验,并计算90%置信区间,表明两种制剂生物等效,受试制剂西洛他唑片的人体相对生物利用度为(101.3±24.6)%。
结论:试验和参比制剂具有生物等效。
%Objective To evaluate the bioequivalence of two formulations cilostazol tables in healthy volunteers.Methods 100mg Test preparation and reference preparation were given to 20 healthy male volunteers in randomized two -way crossover design for the pharmacokinetic and relative bioavailability study.Plasma concentration of cilostazol were determined by RP -HPLC.Results The con-centration-curve in vivo oftwo formulations cilostazol tables in healthy volunteers.The main pharmacokinetic parameters of the two prep-aration were :Tmax 3.25±0.85 and 3.35 ±0.81h,Cmax 876.70 ±276.48 and 823.79±242.37ng/ml,AUC0 ~t 11137.31 ± 2847.19 and 10981.44±2475.94ng·h/ml.AUC0 ~∞11974.78 ±3076.05 and 11939.44±2998.14ng·h/ml,T1 /2(Ke)11.07 ±5.87and 10.23 ±8.48h,respectively.The mean relative bioavailability of test preparation vs reference preparation were (101.3 ±24.6)%.Conclusion The results of statistical analysis shows that the reference and the test tablets were bioequivalent.【期刊名称】《中国民族民间医药》【年(卷),期】2015(000)002【总页数】3页(P6-7,9)【关键词】西洛他唑;生物等效性;高效液相色谱【作者】张惠【作者单位】海南医学院附属医院,海南海口 570102【正文语种】中文【中图分类】R969.1西洛他唑(Cilostazol)为抗血小板药,通过抑制血小板及血管平滑肌内磷酸二酯酶活性,从而增加血小板及平滑肌内cAMP浓度,发挥抗血小板作用及血管扩张作用.主要用于治疗由动脉粥样硬化、大动脉炎、血栓闭塞性脉管炎、糖尿病所致的慢性动脉闭塞症.西洛他唑能改善肢体缺血所引起的慢性溃疡、疼痛、发冷及间歇跛行,并可用作上述疾病外科治疗(如血管成形术、血管移植术、交感神经切除术)后的补充治疗以缓解症状.本试验以浙江大家制药有限公司的西洛他唑片作为参比剂,考察海南绿岛制药有限公司生产的西洛他唑片的药动学,作出生物等效性评价.1. 1受试者资料受试者选择20名男性健康受试者,体重指数19. 2~24.0kg/m2,年龄19~26岁.所有受试者均通过健康体格检查,实验室检查(血常规、肝功能、肾功能、心电图等)均属正常,精神状态良好.在试验期1个月内未服用过任何其他药物,且在试验期1个月内禁忌烟酒.所有受试者均签署知情同意书,并经本基地伦理委员会审批同意.1. 2 药品及试剂西洛他唑片(每片50mg,批号: 101201,海南绿岛制药有限公司);参比制剂(R):西洛他唑片(每片50mg,批号: 120403P,浙江大家制药有限公司);西洛他唑(批号: 100363-200301,中国药品生物制品检定所);地西泮(批号: 171225-200903,中国药品生物制品检定所).乙腈(色谱纯,美国Fisher公司);甲醇(色谱纯,美国Fisher公司);其余试剂均为分析纯.1. 3给药方案20例受试者随机分成2组,每组10例,按2×2交叉试验方案设计,两期研究间的清洗期为14d.参比制剂或受试制剂,经药物清除期(2周)后交换给药.在服药前禁食12h,次晨空腹口服100mg参比制剂(R)或受试制剂(T),统一饮水250ml,服药后2h内不喝水,不吃食物,至给药后4h给予统一低脂标准餐.1. 4血样采集分别于给药前(0h)及给药后0. 5、1、2、3、4、6、8、10、12、24、36、48、60h各取静脉血4ml,血样采集后,于3000r/min离心10min,分离出血浆约2. 5ml,立即分装置EP管中于-20℃低温保存待测.1. 5 样品测定1. 5. 1色谱条件色谱系统Agilent 1200型系列高效液相色谱仪(包括四元梯度泵、在线脱气机、自动进样器、柱温箱、化学工作站);色谱柱: Agilent Eclipse XDB-C18(4. 6×150mm,5μm);柱温: 35℃;流动相:乙腈-30mM乙酸铵水溶液(45∶55);流速: 0. 5ml/min;检测波长: 254nm.在此色谱条件下,西洛他唑的出峰时间约为9min,内标物地西泮的出峰时间约为16min,两个峰之间分离良好,血浆中无内源性物质干扰分离,见图1.1. 5. 2血样预处理冷冻血浆在室温下融化,在涡旋器上涡旋约20s.吸取0. 6ml 血浆,置10ml离心管中,加入内标液(22. 2μg/ml)15μl,漩涡混匀,加乙酸乙酯4ml,涡旋混合2min,3500r/min离心5min.精密吸取上层有机相于40℃水浴氮气吹干,残渣用甲醇100μl溶解,取15μl进样.记录色谱图,内标法以峰面积定量.1. 5. 3标准曲线制备精密称取西洛他唑对照品10. 3mg置于100ml容量瓶中,加甲醇定容至刻度得103μg/ml标准储备液,精密称取内标物地西泮11. 09mg置于100mL容量瓶中,加甲醇定容至刻度得110. 9 μg·ml-1储备液,再用甲醇稀释得22. 2μg/ml的内标液.取健康人空白血浆10ml若干份,分别加入西洛他唑标准储备液使其浓度分别为25. 75、51. 5、103. 0、206. 0、515. 0、1030. 0、2060. 0ng/ml的标准含药血浆.按“1. 5. 2”项下操作,同时制备空白样品,进行HPLC分析,记录色谱图,计算西洛他唑峰面积As和内标峰面积Ai的比值.以比值(= As/Ai)对血药浓度C作权重回归计算,权重系数w = 1/C2,线性范围为25. 75~2060. 0 ng/ml(r = 0. 9995),最小可定量浓度为25. 75ng/ml(S/N >10).1. 5. 4方法学评价配制低、中、高3种浓度(51. 5、206、1030ng/ml)的标准血样,按“1. 5. 2”项处理后进样,同时以相应浓度对照品溶液直接进样,将两组峰面积进行比较计算萃取回收率.另配制低、中、高3种浓度(51. 5、206、1030ng/ml)的标准血样,相应方法处理后进样,由标准曲线计算出浓度,将所得的浓度与已知加人浓度相比,计算相对回收率及日内、日间精密度.结果见表1. 1. 6数据处理以实测值计算Cmax、Tmax;以末端相血药浓度的对数值对时间进行回归,求得斜率Ke及T1/2,运用梯形法计算曲线下面积AUC0~t、AUC0~∞= AUC0~t+ ct/Ke.两种制剂的主要药动学参数Cmax,AUC0~t经对数转换后进行方差分析,在α=0. 05水平进行双单侧t检验,按受试制剂AUC0~t在参比制剂80%~125%,Cmax在75%~133%内判定标准,考察两制剂是否具有生物等效性.2. 1药动学参数20例健康志愿者单剂量口服西洛他唑参比与受试制剂100mg 平均药-时曲线见图2,主要药动学参数见表2.2. 2生物等效性两种制剂间和给药次序间无显著差别,AUC0→T、AUC0→∞在不同给药周期间有显著差异,Cmax在不同给药周期间无显著差异,双单侧t检验的统计参数th 和tl两药均大于单侧t(0. 05,18)(1. 75).试验制剂和参比制剂中西洛他唑的Tmax值经Wilcoxon检验,不同制剂间无显著差异(Z =-0. 587,P = 0. 557).按照生物等效性判定标准,认为两种制剂生物等效.分析结果见表3.2. 3临床观察受试者空腹单剂量口服100mg西洛他唑片后,一般情况良好,整个试验过程中,无明显不良反应发生.本试验建立高效液相色谱法测定人血浆中西洛他唑的浓度,并使用液–液萃取法处理血浆样品,使内源性杂质与西洛他唑很好地分离.该方法操作简便、灵敏度佳、特异性高、重现性好,适于西洛他唑药动学及生物等效性研究.20名受试者口服西洛他唑受试制剂与参比制剂后,主要药动学参数经统计学检验无显著性差异,说明两种制剂的吸收、分布过程基本相似.经计算受试制剂的平均相对生物利用度为(101. 3±24. 6)%;经生物等效性统计分析,均表明两种不同厂家生产的西洛他唑片具有生物等效性.【相关文献】[1]吴友良.市售不同批次西洛他唑片人体药动学参数比较[J].中国药房,2011,38(22): 3590-3592.[2]乔海灵,胡玉容,贾琳静,等.西洛他唑片在健康人体的药代动力学和生物等效性[J].中国临床药理学杂志,200,20(6): 426-429.[3]史美甫,郭涛,李明,等.精编临床用药必备[M].北京:中国科学技术出版社,2003: 772.[4]Woo SK,Kang WK,Kwon KI.Pharmacokinetic and pharmacodyamic modeling of theantiplatelet and cardiovascular effects of cilostazol in healthy humans [J].Clin Pharmacol Ther,2002,71(4): 246-252.。
氯雷他定相关杂质
相关杂质整理列表中文名英文名CAS 号规格纯度结构式氯雷他定杂质1(氯雷他定EP 杂质A)LoratadineImpurity 1(Loratadine EP ImpurityA)133284-74-910mg-25mg-50mg-100mg ≥99%氯雷他定杂质2(氯雷他定EP 杂质B)LoratadineImpurity2(LoratadineEP Impurity B)31251-41-910mg-25mg-50mg-100mg ≥99%氯雷他定杂质3(氯雷他定EP 杂质C)Loratadine Impurity 3(LoratadineEP Impurity C)165739-83-310mg-25mg-50mg-100mg ≥99%氯雷他定杂质4(氯雷他定EP 杂质D)LoratadineImpurity 4(Loratadine EP ImpurityD)100643-71-810mg-25mg-50mg-100mg ≥99%氯雷他定杂质5(氯雷他定EP 杂质E)Loratadine Impurity 5(LoratadineEP Impurity E)170727-59-010mg-25mg-50mg-100mg ≥99%氯雷他定杂质6(氯雷他定EP 杂质F)Loratadine Impurity 6(LoratadineEP Impurity F)125743-80-810mg-25mg-50mg-100mg ≥99%氯雷他定杂质7(氯雷他定EP 杂质G)LoratadineImpurity 7(Loratadine EP ImpurityG)(USP-B)38092-89-610mg-25mg-50mg-100mg ≥99%氯雷他定杂质8(氯雷他定EP 杂质H)LoratadineImpurity 8(Loratadine EP ImpurityH)29976-53-210mg-25mg-50mg-100mg ≥99%氯雷他定杂质10LoratadineImpurity 10119770-60-410mg-25mg-50mg-100mg ≥99%氯雷他定杂质11LoratadineImpurity 11117796-52-810mg-25mg-50mg-100mg ≥99%氯雷他定杂质12LoratadineImpurity 12117810-61-410mg-25mg-50mg-100mg ≥99%氯雷他定杂质13LoratadineImpurity 13165739-62-810mg-25mg-50mg-100mg ≥99%氯雷他定杂质14LoratadineImpurity14(USP-D)38089-93-910mg-25mg-50mg-100mg ≥99%氯雷他定杂质15LoratadineImpurity15(USP-E)133330-60-610mg-25mg-50mg-100mg ≥99%氯雷他定杂质16LoratadineImpurity 16119410-08-110mg-25mg-50mg-100mg ≥99%氯雷他定杂质18LoratadineImpurity 1831255-57-910mg-25mg-50mg-100mg ≥99%氯雷他定杂质19LoratadineImpurity 19109537-11-310mg-25mg-50mg-100mg ≥99%氯雷他定杂质20LoratadineImpurity 201346602-19-410mg-25mg-50mg-100mg ≥99%氯雷他定杂质21LoratadineImpurity 211346605-16-010mg-25mg-50mg-100mg ≥99%氯雷他定杂质23LoratadineImpurity 23609806-40-810mg-25mg-50mg-100mg ≥99%氯雷他定杂质24LoratadineImpurity 24183483-15-010mg-25mg-50mg-100mg ≥99%氯雷他定杂质25LoratadineImpurity 25609806-39-510mg-25mg-50mg-100mg ≥99%氯雷他定杂质26LoratadineImpurity 26165739-64-010mg-25mg-50mg-100mg ≥99%氯雷他定杂质27LoratadineImpurity 27591-22-010mg-25mg-50mg-100mg ≥99%氯雷他定杂质28LoratadineImpurity 281073332-71-410mg-25mg-50mg-100mg ≥99%氯雷他定杂质30LoratadineImpurity 30133330-56-010mg-25mg-50mg-100mg ≥99%氯雷他定杂质31LoratadineImpurity 315570-77-410mg-25mg-50mg-100mg ≥99%氯雷他定杂质33LoratadineImpurity 33169253-13-810mg-25mg-50mg-100mg ≥99%SS湖北扬信医药科技有限公司经营上万种杂质对照品(优势供应硫酸羟氯喹杂质、硝苯地平杂质、沙丁胺醇杂质、达格列净杂质、厄贝沙坦杂质、阿莫西林克拉维酸钾杂质、利伐沙班杂质、阿托伐他汀钙杂质、西格列汀杂质、利格列汀杂质等),并代理销售中检所、STD 、LGC 、TLC 、EP 、USP 、TRC 等多个品牌产品,提供上万种标准品对照品,真诚为您服务。
西洛他唑片Cilostazol-详细说明书与重点
西洛他唑片Cilostazol【警示语】因服用本药可能会使心律增加而发生心绞痛,要特别注意对心绞痛症状(胸痛)等的观察和问诊。
在日本完成的脑梗死后预付复发的试验中,有患者出现长时间血压心律积(pressure rate product)明显升高,此外试验组出现心绞痛的发生率为1.16%(6/516),安慰组则无发生(0/518)。
【成份】本品主要成份为西洛他唑,其化学名称为:6-[4-(1-环已基-1H-戊四唑(5')丁氧基)3,4-二氢-1H-喹诺酮(2')分子式:C20H27N5O2化学结构式:分子量:369.46【性状】本品为白色片。
【适应症】1.改善由于慢性动脉闭塞症引起的溃疡、肢痛、冷感及间歇性跛行等缺血性症状。
2.预防脑梗死复发(心源性脑梗死除外)。
【规格】50mg。
【用法用量】通常,成人每次口服西洛他唑片0.1g(2片),1天2次。
另外,可根据年龄、症状适当增减。
【不良反应】1.严重不良反应(1)有时会发生充血性心衰、心肌梗死、心绞痛、室性心动过速,发生率不明。
发现异常时,应停止给药,并进行适当处理。
(2)出血:有发生脑出血等颅内出血(初期症状:头痛、恶心?呕吐、意识障碍、半身不遂)的可能,发生率不明。
有这些症状时应停止给药并进行适当处理。
有发生肺出血(发生率不明)、消化道出血、鼻出血、眼底出血(0.1%以下)等的可能。
有这些症状时应停止给药并进行适当处理。
(3)有发生全血细胞减少、粒细胞缺乏症(发生率不明)、血小板减少(0.1%以下)的可能,应充分注意观察,发现异常时应停止给药并进行适当处理。
(4)间质性肺炎(发生率不明):有时出现伴随发热、咳嗽、呼吸困难、胸部X线异常、嗜酸性粒细胞增多的间质性肺炎。
有上述症状时,应停止给药,并进行给予肾上腺皮质激素等的适当处理。
(5)肝功能障碍(0.1~5%以下)、黄疸(发生率不明):因为有发生AST(GOT)、ALT(GPT)、Al-P、LDH等升高和黄疸等,应充分注意观察,发现异常时应停止给药并进行适当处理。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
西洛他唑杂质列表
[中文名]:西洛他唑
英文名称:Cilostazol
CAS No.: 73963-72-1
分子式: C20H27N5O2
规格:10mg-25mg-50mg-100mg
用途:项目报批纯度高于99.89%
[中文名] 西洛他唑杂质1
英文名:Cilostazol Impurity 1
CAS No.: N/A
分子式:C29H34N6O4
规格:10mg-25mg-50mg-100mg
用途:项目报批纯度高于99.89%
湖北扬信医药(现货)供应各种杂质对照品:泊沙康唑杂质、替卡格雷杂质、依折麦布杂质、索拉菲尼相关杂质、索非布韦杂质、氨氯地平杂质、Q2-853-78-6-052马来酸氯苯那敏杂质、头孢克肟杂质、瑞舒伐他汀杂质、瑞格列奈杂质等;
代理中检所/EP/BP/USP/LGC/TRC/DR/TLC/MC/SIGMA/BACHEM等品牌
湖北扬信医药专注各种杂质对照品、原研制剂
用途:项目报批并提供COA、NMR、HPLC、MS等图谱。
详情请点击用户名
[中文名] 西洛他唑杂质2
英文名:Cilostazol Impurity 2
CAS No.: N/A
分子式:C20H29N5O3
规格:10mg-25mg-50mg-100mg
用途:项目报批纯度高于99.89%
[中文名] 西洛他唑相关化合物C
英文名:Cilostazol related compound C
CAS No.: 865792-18-3
分子式:C31H45N9O2
规格:10mg-25mg-50mg-100mg
用途:项目报批纯度高于99.89%
[中文名] OPC-13213
英文名:OPC-13213
CAS No.: 87153-04-6
分子式:C20H27N5O3
规格:10mg-25mg-50mg-100mg
用途:项目报批纯度高于99.89%。
