高中化学离子共存的知识点归纳及~高考题 人教版
《高中化学离子共存知识点总结》

《高中化学离子共存知识点总结》离子共存是化学中一个极为重要的概念。
许多物质在自然界或者工业生产过程中都会存在离子共存的情况,因此了解离子共存的知识点对于化学学科来说是非常重要的。
本文将总结高中化学中离子共存的知识点,帮助学生深入了解离子共存相关的知识。
1. 离子共存的定义离子共存是指两种或以上的离子在同一溶液中存在,并且彼此相互影响的现象。
它是很常见的一种现象,它可以对溶液中的化学反应、物质的结构和性质产生很大的影响。
2. 离子共存对于溶解度的影响离子共存对于溶解度的影响非常显著。
通常来说,在同一溶液中存在几种离子时,它们之间会产生一定程度的相互作用,这将会影响物质的溶解度。
其中,最常见的影响是当有两种或多种离子共存时,它们会共同影响物质的活度,从而影响物质的溶解度。
当阴离子和阳离子共存于同一溶液中时,会产生“类盐结构”。
这种结构中,阴离子和阳离子之间的相互作用会导致化合物的颜色发生变化。
基于这种现象,我们可以通过阴离子和阳离子共存来实现某些颜色的控制或调节。
离子共存可以对于化学反应的速率和平衡产生影响。
一般来说,当有两种或多种离子共存时,它们之间会产生一定程度的相互作用,从而影响化学反应的速率和平衡。
这可以通过改变离子的浓度以及相对的反应速率来实现。
5. 过量的离子共存可能会导致沉淀的形成当溶液中某些离子的浓度极高时,会出现过量的离子共存情况。
此时,这些离子将超过其饱和浓度,导致其沉淀并从溶液中分离出来。
这在实际应用中需要特别注意,因为过量的离子共存可能对实验或工业过程产生不利的影响。
6. 针对离子共存的实验策略针对离子共存进行实验时,有几个不同的策略可以帮助我们实现预期的结果。
其中,最重要的策略是将溶液中含有的离子作为反应物,然后逐一地研究它们之间的相互作用。
在这个过程中,通常会使用一些定量的方法,例如浓度法、滴定法等,以便准确地测定溶液中不同离子的浓度。
高中化学离子共存知识点归纳

高中化学离子共存知识点归纳
①离子共存定律:在水溶液中,相似的离子不可共存,而大多数异质
的离子能够共存;
②离子共存的几种方式:(1)强相互作用:离子之间通过电荷的相
互作用使得相邻的离子相互吸引,形成离子对。
(2)离子偶联:当离子
之间产生特定的作用力时,他们可以结合成离子偶联物。
(3)离子排斥:由离子的量子势阻碍,形成离子排斥,使相似离子在空间上分布不均匀。
③离子共存在生物体内的应用:离子共存原理是调节细胞电位、生理
反应、酸碱平衡、能量转运、催化反应等的重要依据,对生命的运作至关
重要。
离子共存知识点归纳高中

离子共存必考知识归纳1.所有的弱酸根离子:CH3COO-、F-、ClO-、AlO₂ ̄、SiO₃²¯、CN-与H+都不能大量共存。
2.酸式弱酸根离子如HCO₃ ̄、HS-、HSO₃ˉ-既不能与OH-大量共存,又不能与H+大量共存。
3.有沉淀生成包括有微溶物生成的离子不能大量共存,如Ba2+、Ca2+、Ag+等不能与SO₄²¯、CO₃²¯等大量共存,Mg2+不能与OH-、CO₃²ˉ大量共存。
4.一些容易发生水解的离子,在溶液中的存在是有条件的。
如AlO₂¯、S2-、CO₃²¯、C6H5O-等必须在碱性条件下才能在溶液中存在;如Fe2+、Al3+、Cu2+等必须在酸性条件下才能在溶液中存在;Fe3+必须在酸性较强的条件下才能在溶液中存在(常温下,pH=7时不能存在)。
5.能发生氧化还原反应的离子不能大量共存。
如S2-、HS-、SO₃²¯、I-和Fe3+不能大量共存;MnO₄¯、(NO₃¯、H﹢)、ClO-与S2-、HS-、SO₃²¯、HSO₃¯、I-、Fe2+等不能大量共存;SO₃²¯和S2-在碱性条件下可以共存,但在酸性条件下则由于发生2S2-+SO₃²¯+6H+===3S↓+3H₂O反应不能共存;H+与S₂O₃²¯不能大量共存。
6.溶液中能发生络合反应的离子不能大量共存。
如Fe3+与SCN-不能大量共存。
7.审题时应注意题中给出的附加条件。
(1)加入铝粉后放出可燃性气体的溶液、由水电离出的c(H+)或c(OH-)=1×10-10mol·L-1的溶液都有两种可能:酸溶液或碱溶液。
(2)无色溶液则没有MnO₄ ̄、Fe3+、Fe2+、Cu2+等有色离子。
澄清溶液即没有沉淀,与无色溶液不同。
高考化学必考知识点总结离子方程式、离子共存问题

高考化学必考知识点总结离子方程式、离子共存问题高考化学必考知识点总结------离子方程式、离子共存问题化学如同物理一样皆为自然科学的根底科学。
查字典化学网为大家推荐了高考化学必考知识点,请大家仔细阅读,希望你喜欢。
离子共存问题离子在溶液中能否大量共存,涉及到离子的性质及溶液酸碱性等综合知识。
凡能使溶液中因反响发生使有关离子浓度显著改变的均不能大量共存。
如生成难溶、难电离、气体物质或能转变成其它种类的离子(包括氧化一复原反响).一般可从以下几方面考虑1.弱碱阳离子只存在于酸性较强的溶液中.如Fe3+、Al3+、Zn2+、Cu2+、NH4+、Ag+ 等均与OH-不能大量共存.2.弱酸阴离子只存在于碱性溶液中。
如CH3COO-、F-、CO32-、SO32-、S2-、PO43-、 AlO2-均与H+不能大量共存.3.弱酸的酸式阴离子在酸性较强或碱性较强的溶液中均不能大量共存.它们遇强酸(H+)会生成弱酸分子;遇强碱(OH-)生成正盐和水. 如:HSO3-、HCO3-、HS-、H2PO4-、HPO42-等4.假设阴、阳离子能相互结合生成难溶或微溶性的盐,那么不能大量共存.如:Ba2+、Ca2+与CO32-、SO32-、 PO43-、SO42-等;Ag+与Cl-、Br-、I- 等;5.假设阴、阳离子能发生氧化一复原反响那么不能大量共存.如:Fe3+与I-、S2-;MnO4-(H+)与I-、Br-、Cl-、S2-、SO32-、Fe2+等;NO3-(H+)与上述阴离子;S2-、SO32-、H+如:Fe3+和SCN-等离子方程式正误判断常见错误原因1.离子方程式书写的根本规律要求:(写、拆、删、查四个步骤来写)(1)合事实:离子反响要符合客观事实,不可臆造产物及反响。
(2)式正确:化学式与离子符号使用正确合理。
(3)号实际:(4)两守恒:两边原子数、电荷数必须守恒(氧化复原反响离子方程式中氧化剂得电子总数与复原剂失电子总数要相等)。
高考化学考点突破:离子共存
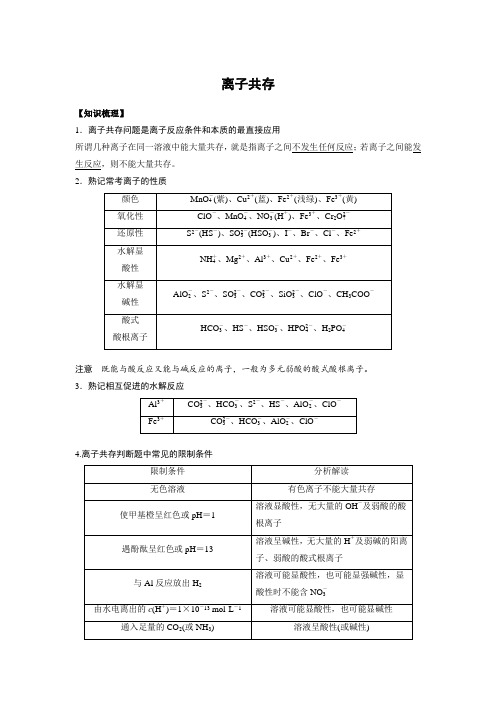
离子共存【知识梳理】1.离子共存问题是离子反应条件和本质的最直接应用所谓几种离子在同一溶液中能大量共存,就是指离子之间不发生任何反应;若离子之间能发生反应,则不能大量共存。
2.熟记常考离子的性质注意既能与酸反应又能与碱反应的离子,一般为多元弱酸的酸式酸根离子。
3.熟记相互促进的水解反应4.离子共存判断题中常见的限制条件深度思考指出下列离子组不能共存的原因。
(1)Na+、OH-、SO2-4、Fe3+_________________________________________________________________________________________________________________________。
(2)K+、Mg2+、I-、ClO-___________________________________________________________________________________________________________________________。
(3)含有大量Fe3+的溶液:Na+、SCN-、Cl-、I-_______________________________________________________________________________________________________。
(4)含有大量NO-3的溶液:H+、Fe2+、Cl-、SO2-4______________________________________________________________________________________________________。
(5)常温下,pH=12的溶液:K+、Cl-、SO2-3、SiO2-3、Ca2+_____________________。
(6)c(H+)=0.1 mol·L-1的溶液:Na+、NH+4、SO2-4、S2O2-3_______________________。
高三化学《离子共存问题》知识点总结

高三化学《离子共存问题》知识点总结高三化学《离子共存问题》知识点总结一.“无色透明”条件型若题目限定溶液“无色”,则不含有色离子,即Fe2+(浅绿色)、Fe3+(黄色)、Cu2+(蓝色)、MnO4-(紫色)等离子。
若“透明”,则溶液不形成混浊或沉淀(与溶液有无颜色无关)。
如Ag+与Cl-、Br-、I-、SO42-;Ca2+与CO32-、SO42-;Ba2+与CO32-、SO32-、SO42-等在水溶液中会发生反应,有混浊或明显的沉淀生成,它们不能大量共存。
例1.某无色透明的溶液中,下列各组离子能大量共存的是A.H+、Cl-、Ba2+、CO32-B.Ag+、I-、K+、NO3-C.K+、OH-、Cl-、Na+D.Fe3+、Cl-、NO3-、Na+解析:正确选项应满足无色透明和能大量共存两个条件。
答案为C项。
二.“酸性”条件型常见的叙述有强酸性溶液、PH=1的溶液、能使PH试纸变红的溶液、紫色石蕊试液呈红色的溶液、甲基橙呈红色的溶液、加入镁粉能放出氢气的溶液等。
若题目中限定溶液呈酸性,则溶液中有H+存在,其中不能大量含有OH-、弱酸根离子(如CO32-、SO32-、S2-、F-、ClO-、CH3COO-、PO43-、AlO2-、SiO32-等)以及弱酸的酸式根离子(如HCO3-、HSO3-、HS-、HPO42-、H2PO4-等)。
例2.在pH=1的溶液中,可以大量共存的离子是A.K+、Na+、SO42-、SO32-B.NH4+、Mg2+、SO42-、Cl-C.Na+、K+、HCO3-、Cl-D.K+、Na+、AlO2-、NO3-解析:正确选项应满足pH=1(有大量H+存在)和可以大量共存两个条件。
答案为B项。
三.“碱性”条件型常见的叙述有强碱性溶液、PH=14的溶液、能使PH试纸变蓝的溶液、红色石蕊试纸变蓝的溶液、酚酞呈红色的溶液、甲基橙呈黄色的溶液、加入铝粉反应后生成AlO2-的溶液、既能溶解Al(OH)3又能溶解H2SiO3的溶液等。
高考化学之离子共存知识点

高考化学之离子共存知识点一、离子能否大量共存的判断方法多种离子能否大量共存于同一溶液中,归纳起来就是四点:一色、二性、三特殊、四反应。
1.一色即溶液颜色,若限定为无色溶液,则Cu2+(蓝色)、Fe3+(棕黄色)、Fe2+(浅绿色)、MnO4—(紫色)等有色离子不能存在。
2.二性即溶液的酸性和碱性。
在强酸性溶液中,OH−及弱酸阴离子(如CO32—、SO32—、CH3COO−等)均不能大量存在;在强碱性溶液中,H+及弱碱阳离子(如NH4+、Al3+、Mg2+、Fe3+等)均不能大量存在;弱酸的酸式酸根离子(如HCO3—、HSO3—等)在强酸性和强碱性溶液中均不能大量存在。
3.三特殊即三种特殊情况:①AlO2—与HCO3—不能大量共存:AlO2—+HCO3—+H2O==Al(OH)3↓+CO32—;②“NO3—+H+”组合具有强氧化性,能与SO32—、Fe2+、I−等发生氧化还原反应,而这一种组合较为隐蔽,不易被察觉;③NH4+与CH3COO −、CO2—,Mg2+与HCO3—等组合中,虽然两组离子都能水解3且水解相互促进,但总的水解程度仍很小,它们在溶液中能大量共存。
4.四反应即离子间通常能发生的四种类型的反应,能相互反应的离子显然不能大量共存。
①生成沉淀、气体、弱电解质的反应,如Ba2+与SO42—、NH4+与OH−、H+与CH3COO−等;②氧化还原反应,如Fe3+与I−、NO3—(H+)与Fe2+、MnO4—((H+)与Br−等;③双水解反应,如Al3+与HCO3—、Al3+与AlO2—等;④络合反应,如Fe3+与SCN−等。
二、在离子共存问题上,常常设置一些“陷阱”,做题时应引起注意。
1.警惕“颜色陷阱”若限定溶液无色,则Cu2+、Fe3+、Fe2+、CrO42-、MnO4-等有色离子不能大量存在。
2.警惕溶液酸、碱性的几种表示方法(1)表示酸性溶液的是①pH<7或c(H+)>c(OH-)或c(OH -)=10-(8~14)mol·L-1(25 ℃);②能使pH试纸显红色的溶液;③能使甲基橙显红色或橙色的溶液;④能使紫色石蕊溶液显红色的溶液。
高中化学离子共存知识点总结(完整版)

高中化学离子共存知识点总结高中化学离子共存知识点总结!AlO2-、ClO-等不能大量共存。
4.溶液中能发生络合反应的离子不能大量共存。
如Fe2+、Fe3+与SCN-不能大量共存;Fe3+与不能大量共存。
5、审题时应注意题中给出的附加条件。
①酸性溶液、碱性溶液、能在加入铝粉后放出可燃气体的溶液、由水电离出的H+或OH-=1×10-10molL的溶液等。
②有色离子MnO4-,Fe3+,Fe2+,Cu2+,Fe2+。
③MnO4-,NO3-等在酸性条件下具有强氧化性。
④S2O32-在酸性条件下发生氧化还原反应:S2O32-+2H+=S↓+SO2↑+H2O⑤注意题目要求“大量共存”还是“不能大量共存”。
6、审题时还应特别注意以下几点:注意溶液的酸性对离子间发生氧化还原反应的影响。
如:Fe2+与NO3-能共存,但在强酸性条件下不能共存;MnO4-与Cl-在强酸性条件下也不能共存;S2-与SO32-在钠、钾盐时可共存,但在酸性条件下则不能共存。
酸式盐的含氢弱酸根离子不能与强碱、强酸共存。
如HCO3-+OH-=CO32-+H2O;HCO3-+H+=CO2↑+H2OAlO2-、ClO-等不能大量共存。
4.溶液中能发生络合反应的离子不能大量共存。
如Fe2+、Fe3+与SCN-不能大量共存;Fe3+与不能大量共存。
5、审题时应注意题中给出的附加条件。
①酸性溶液、碱性溶液、能在加入铝粉后放出可燃气体的溶液、由水电离出的H+或OH-=1×10-10molL的溶液等。
②有色离子MnO4-,Fe3+,Fe2+,Cu2+,Fe2+。
③MnO4-,NO3-等在酸性条件下具有强氧化性。
④S2O32-在酸性条件下发生氧化还原反应:S2O32-+2H+=S↓+SO2↑+H2O⑤注意题目要求“大量共存”还是“不能大量共存”。
6、审题时还应特别注意以下几点:注意溶液的酸性对离子间发生氧化还原反应的影响。
如:Fe2+与NO3-能共存,但在强酸性条件下不能共存;MnO4-与Cl-在强酸性条件下也不能共存;S2-与SO32-在钠、钾盐时可共存,但在酸性条件下则不能共存。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、溶液酸碱性的判断
1、当c(H+)>c(OH-)时,酸性;当c(H+)=c(OH-)时,中性;当c(H+)<c(OH-)时,碱性。
2、通常情况下,c(H+)>>10-7mol/L强酸性;c(H+)=10-7mol/L呈中性;c(H+)<<10-7mol/L强碱性。
3、通常情况下pH>>7(pH=13)强碱性;pH=7中性;pH<<7(pH=1)强酸性。
4、溶液温度100℃,pH>6碱性;pH=6中性;pH<6酸性。
5、当c(H+)水=c(OH-)水=1*10-n<1*10-7mol/L,(n>>7),可能是强酸溶液pH=14-n, 可能是强碱溶液pH=n 。
6、酸性溶液:①甲基橙呈红色的溶液,甲基橙呈橙色的溶液;②紫色石蕊呈红色的溶液;③甲基红呈红色的溶液, 甲基红呈橙色的溶液。
7、碱性溶液:①紫色石蕊试剂呈蓝色的溶液;②酚酞试剂呈粉红色的溶液,酚酞试剂呈红色的溶液。
二、溶液的酸碱性对离子共存的影响
1、强酸性条件下发生复分解反应不能共存的离子有:
①与H+反应产生气体:CO-23、HCO-3、S2-、HS-、SO-23、HSO-3、S2O-23。
②与H+反应产生沉淀:AlO-2、SiO-23、C6H5O- 、S2O-23。
、H2PO-4、HPO-4、OH-、CN-、CH3COO-、HC2O-4。
③与H+反应产生弱酸或水:ClO- 、F-、PO-3
4
2、强酸性条件下发生氧化还原反应不能共存的离子有:
①在大量H+存在下,NO-3和I-(或Fe2+)反应。
②在大量H+存在下,MnO-4和Cl-(或Br-或I-或Fe2+)反应。
③在大量H+存在下,IO-3和I-;ClO-和Cl-;ClO-3和Cl-;BrO-3和Br-反应。
3、强碱性条件下发生复分解反应不能共存的离子有:
①与OH-反应产生气体:NH+4。
②与OH-反应产生沉淀:Mg2+、Al3+、Fe2+、Fe3+、Cu2+、Ag+。
③与OH-发生中和反应:HCO-3、HS-、HSO-3、H2PO-4、HPO-4、H+ 。
三、盐溶液与盐溶液反应而不能共存的离子有:
1、发生双水解反应而不能共存的离子有:①产生Al(OH)3沉淀的离子组:Al3+和AlO-
2、Al3+和CO-23(或HCO-3);Al3+和S2-。
②产生Fe(OH)3沉淀的离子组:Fe3+和AlO-2、Fe3+和CO-23(或HCO-3) 。
2、发生氧化还原反应而不能大量共存:①ClO-和S2-(或SO-23或I-);②Fe3+和S2-(或I-)。
3、发生复分解反应而不能共存的离子有:①产生硫酸盐沉淀的离子组:SO-24和Ba2+(或Pb2+、Ag+、Ca2+);②产生盐酸盐沉淀的离子组:Cl-和Ag+;③产生碳酸盐沉淀的离子组:CO-23和Ca2+或Ba2+。
4、发生络合反应而不能大量共存的离子有:Fe3+和SCN-
四、无色溶液中不能大量存在的离子有:Fe3+(黄色)、Fe2+(浅绿色)、MnO-4(紫色)、Cu2+(蓝色)、CrO-24(橙色)、Cr3+(绿色)。
1.(08年全国I 卷)在溶液中加入足量Na 2O 2后仍能大量共存的离子组是
A .NH +4、Ba 2+、Cl -、NO 3-
B .K +、AlO -2、Cl -、SO -24
C .Ca 2+、Mg 2+
、NO -3、HCO -3 D .Na +、Cl -、CO -23、SO -23 2.(08年重庆理综)下列各组离子在给定条件下能大量共存的是
A .在pH =1溶液中:NH +4、K +
、ClO -、Cl - B .有SO -24存在的溶液中:Na +、Mg 2+、Ca 2+、I
- C .有NO -3存在的强酸性溶液中:NH +4、Ba 2+、Fe 2+、Br -
D .在c (H +) =1.0×10—13 mol·L -1的溶液中:Na +、S 2-、AlO -2、SO -23
3.(08年广东理基)下列各组离子一定能大量共存的是
A .在含有大量[Al(OH)4]- 溶液中NH +4、Na +、Cl -、H +
B .在强碱溶液中 Na +、K +、CO -23、NO -3
C .在pH =12的溶液中 NH +4、Na +、SO -24、Cl -
D .在c (H +)=0.1 mol·L -1的溶液中K +、I -、Cl -
、NO -3 4.(08年江苏化学)在下列溶液中,各组离子一定能够大量共存的是
A .使酚酞试液变红的溶液: Na +、Cl -、SO -24 、Fe 3+
B .使紫色石蕊试液变红的溶液:Fe 2+、Mg 2+、NO 3-、Cl -
C .c (H +)=10-12 mol·L -1的溶液:K +、Ba 2+、Cl -、Br -
D .碳酸氢钠溶液:K +、SO -24 、Cl -、H +
5.(08年海南化学)在pH =13的无色溶液中,可以大量共存的一组离子是
A .NH +4、NO -3 、K +、SO -24
B .CO -23、NO -3、HCO -3、Na +
C .Na +、ClO -、AlO -2、NO 3-
D .CrO -24、K +、Na +、SO -24 6.(07年江苏卷)向存在大量Na +、Cl -的溶液中通入足量的NH 3后,该溶液中还可能大量存在的离于组是
A
.K +、B r -O 2 7.(07年海南化学卷)在pH = 1时,可大量共存且形成无色溶液的一组离子或分子是 A
.C a 2+、C H 3
C O C .HClO 、Ba 2+、Na + 、Cl -
D .K +、Cl -、Al 3+、SO 32 - 8.(07年北京卷理综)在由水电离产生的H +浓度为1×10
-13 mol/L 的溶液中,一定能大量共存的离子组是
= 1 \* G
= 4
\*
A .①③
B .③⑤
C .③④
D .②⑤ 习题答案:1、B, 2、D, 3、B, 4、C, 5、C, 6、A, 7、A, 8、B 。
