乙二胺四乙酸二钠水溶液的紫外吸收
氨氮、硝酸氮、亚硝酸氮测定方法总结
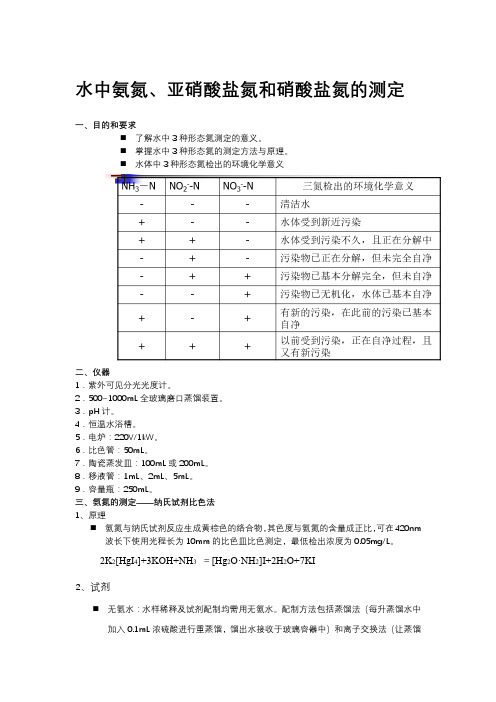
水中氨氮、亚硝酸盐氮和硝酸盐氮的测定一、目的和要求⏹了解水中3种形态氮测定的意义。
⏹掌握水中3种形态氮的测定方法与原理。
⏹水体中3种形态氮检出的环境化学意义二、仪器1.紫外可见分光光度计。
2.500~1000mL全玻璃磨口蒸馏装置。
3.pH计。
4.恒温水浴槽。
5.电炉:220V/1kW。
6.比色管:50mL。
7.陶瓷蒸发皿:100mL或200mL。
8.移液管:1mL、2mL、5mL。
9.容量瓶:250mL。
三、氨氮的测定——纳氏试剂比色法1、原理⏹氨氮与纳氏试剂反应生成黄棕色的络合物,其色度与氨氮的含量成正比,可在420nm波长下使用光程长为10mm的比色皿比色测定,最低检出浓度为0.05mg/L。
2K2[HgI4]+3KOH+NH3=[Hg2O·NH2]I+2H2O+7KI2、试剂⏹无氨水:水样稀释及试剂配制均需用无氨水。
配制方法包括蒸馏法(每升蒸馏水中加入0.1mL浓硫酸进行重蒸馏,馏出水接收于玻璃容器中)和离子交换法(让蒸馏水通过强酸型阳离子交换树脂柱来制备)。
⏹磷酸盐缓冲液(pH为7.4):称取14.3g磷酸二氢钾和68.8g磷酸氢二钾,溶于水中并稀释至1000mL,配制后用pH计测定其pH值,并用磷酸二氢钾或磷酸氢二钾调节pH为7.4。
⏹吸收液:2%硼酸或0.01mol/L硫酸。
⏹纳氏试剂:碘化汞-碘化钾-氢氧化钠。
称取16g氢氧化钠溶于50mL水中,冷却至室温。
称取7g碘化钾和10g碘化汞,溶于水中,然后将此溶液在搅拌下,缓慢加入到氢氧化钠溶液中,并稀释至100mL。
贮存于棕色瓶内,用橡皮塞塞紧,于暗处存放,有效期可达一年。
⏹50%酒石酸钾钠溶液:称取50g酒石酸钾钠溶于100mL水中,加热煮沸,以驱除氨,充分冷却后稀释至100mL。
⏹氨氮标准溶液:CN=1mg/mL。
称取3.819g无水氯化铵(于100~105℃下干燥2h)溶于无氨水中,转入1000mL容量瓶内,用无氨水稀释至刻度,摇匀,准确吸取该溶液10.00mL于1000mL容量瓶内,用无氨水稀释至刻度,其浓度为10ug/mL。
edta紫外吸收波长

edta紫外吸收波长
摘要:
1.引言
2.什么是EDTA
3.EDTA 的紫外吸收波长
4.EDTA 在实际应用中的紫外吸收波长
5.总结
正文:
【引言】
EDTA(乙二胺四乙酸二钠)是一种多功能的螯合剂,广泛应用于化工、食品、医药等行业。
在分析化学中,EDTA 的紫外吸收波长是一个重要的参数,可以用于定量分析。
【什么是EDTA】
乙二胺四乙酸二钠(简称EDTA)是一种多功能的螯合剂,其化学名为乙二胺四乙酸二钠盐。
EDTA 具有良好的螯合性能,能与多种金属离子形成稳定的螯合物。
【EDTA 的紫外吸收波长】
EDTA 在紫外光区域有一定的吸收,其吸收波长主要集中在200-
400nm。
EDTA 的紫外吸收波长与其结构、金属离子的配位环境等因素有关。
在实际应用中,EDTA 的紫外吸收波长可以用于定量分析,通过测量EDTA 在不同波长下的吸光度,可以推算出样品中金属离子的浓度。
【EDTA 在实际应用中的紫外吸收波长】
在实际应用中,EDTA 的紫外吸收波长常用于分析金属离子的浓度。
例如,在食品分析中,可以通过测量EDTA 与金属离子形成的螯合物在特定波长下的吸光度,推算出食品中金属离子的含量。
此外,EDTA 的紫外吸收波长还可以用于环境监测、生物医学等领域。
【总结】
总的来说,EDTA 的紫外吸收波长是一个重要的参数,对于分析化学、食品、环境监测等领域具有重要的应用价值。
清洗剂中有机助剂的分类和基本知识

清洗剂中有机助剂的分类和基本知识清洗剂中还要加入各种有机助剂,尽管其用量比无机助剂小,但在洗涤过程所发挥的作用却并不亚于无机助剂。
1.氨三乙酸钠又称氨基三乙酸,英文缩写NTA。
分子式为WCl^COO-Na)3-H20,白色粉状结晶。
典型乙酸氨气味。
相对密度1.782。
25乞时在水中的溶解度为48.4%,1%水溶液的pH值为10.6~11.0。
能螯合溶液中的钙、镁等多价金属离子,生成易溶的具有强结合力的螯合物。
具有良好的缓冲作用、反絮凝作用和去污作用。
对皮肤和眼睛有刺激。
作为部分三聚磷酸钠的代用品,对水的软化能力大大超过三聚磷酸钠。
因此,在规定的pH值范围内,氨三乙酸钠与阴离子表面活性剂或非离子表面活性剂复配,都能使合成清洗剂获得优良的洗涤性能。
2.乙二胺四乙酸二钠别名EDTA二钠盐,白色结晶粉末。
溶于水,几乎不溶于乙醇。
是一种重要的金属络合剂,用于络合金属离子和分离金属离子。
可作为磷酸盐的代用品,能提高合成清洗剂的泡沫稳定性,但提高合成清洗剂去污力的程度不如三聚磷酸钠。
在清洗剂中的主要作用是作金属离子螯合剂,有助于保持液体清洗剂的透明度,但与合成清洗剂中的香料不相容。
3.柠檬酸钠别名柠檬酸三钠、枸椽酸钠,化学组成为Na3C6H5O7-2H2O,白色晶体或粒状粉末,于150乞失去全部结晶水,大于150乞则分解。
易溶于水,难溶于乙醇,无毒,易被微生物降解,其微生物降解性和安全性在有机助剂中为最佳,但成本较高,对重金属离子的螯合力低,一般只限用于液体清洗剂中。
柠檬酸钠对提高清洗剂去污力的效果较小,但与阴离子表面活性剂复配,具有一定的去污性能,尤其对棉纤维和合成纤维的织物洗涤效果更好。
4.聚段酸钠聚赧酸钠属于聚短酸盐的一种,为丙烯酸与聚丙烯酸或马来酸的共聚物。
聚段酸钠能与钙离子整合,具有钙皂分散性和阻止碳酸钙沉积的优点。
如使用含有52%碳酸钠和4%聚梭酸钠的清洗剂,在100硬度的水中,于25乞时,能阻止碳酸钙的沉积;而在200硬度的此,含有碳酸钠和聚赧酸钠的清洗剂,能与含有碳酸钠、硅酸钠、硫酸钠、阴离子表面活性剂和非离子表面活性剂的合成清洗剂的洗涤性能相似。
乙二胺四乙酸二钠钙盐做基肥

乙二胺四乙酸二钠钙盐做基肥乙二胺四乙酸二钠钙盐是一种重要的化学物质,它在农业生产中起着重要的作用。
它可以作为一种基肥,广泛应用于农业生产中,可以提高土壤肥力,增加农作物产量,改良土壤结构,促进作物生长,提高作物品质,减少化肥的使用量,保护环境等方面发挥着重要的作用。
本文将从该化学物质的性质、用途和作用机制等方面进行介绍,以便更好地了解乙二胺四乙酸二钠钙盐作为基肥的应用价值。
首先,我们来了解一下乙二胺四乙酸二钠钙盐的性质。
乙二胺四乙酸二钠钙盐是一种白色结晶性粉末,溶于水,微溶于醇和醚,不溶于酮类溶剂。
它的分子式为(C10H12N2O8CaNa2),分子量为374.27,密度为1.15g/cm3。
由于其溶解度高,可以迅速溶解于水中,使其成为一种易于施用的肥料。
其次,乙二胺四乙酸二钠钙盐在农业生产中的用途很广泛。
它可以用于作为基肥施用在各种作物上,如水稻、小麦、玉米、豆类、果树等。
它可以作为有机肥的补充,为土壤提供植物所需的养分,提高土壤肥力,增加土壤肥力之间的相互作用,并使植物更好地吸收养分。
乙二胺四乙酸二钠钙盐作为基肥,可以为植物提供全面的营养。
它含有多种植物所需的微量元素,如钙、镁、硼等,可以促进植物生长,增加作物产量。
此外,钙元素可以增加作物的抗病能力,提高作物的抗逆性,促进作物的健康生长。
其次,乙二胺四乙酸二钠钙盐还可以改良土壤结构。
它可以改善土壤的通透性和保水性,改善土壤的肥力,增加土壤的肥力,提高土壤的养分含量,减少土壤的酸碱度,改良土壤结构,增加土壤有机质的含量,提高土壤的肥力,使土壤适合作物的生长。
此外,乙二胺四乙酸二钠钙盐还可以起到减少化肥使用量的作用。
它可以与化肥混合施用,减少施肥量,提高化肥利用率,降低施肥成本,减少对环境的污染,保护生态环境。
总之,乙二胺四乙酸二钠钙盐作为一种基肥,在农业生产中起着重要的作用。
它可以提高土壤肥力,增加农作物产量,改良土壤结构,促进作物生长,提高作物的品质,减少化肥的使用量,保护环境等方面发挥着重要的作用。
乙二胺四乙酸二钠盐二水化合物

乙二胺四乙酸二钠盐二水化合物乙二胺四乙酸二钠盐二水化合物,这个名字听上去是不是有点拗口?我跟你说,这东西可不是咱们平常在街边小摊能买到的零食,而是一种化学物质,听起来高大上,但其实它跟咱们的生活息息相关。
想象一下,它就像个全能选手,能在水里游刃有余,帮助咱们身体里的一些金属离子“找工作”。
这家伙一出现,金属离子们就得乖乖听话,没准还会被它收拾得服服帖帖的。
就好比说,一个班里有个特别能干的同学,老师一喊,其他同学都得老老实实的。
可能有人会问,乙二胺四乙酸二钠盐二水化合物到底有什么用呢?别着急,这就来了!它主要是在化学实验室里和医学领域里活跃,尤其是水处理和重金属离子的去除,简直就像是个“清道夫”。
有了它,咱们能喝上更干净的水,吃上更安全的食物,这可是一项功德无量的事业。
想想看,水里那些对我们身体有害的金属,跟个小偷似的,天天潜伏在水里,等着抓人。
乙二胺四乙酸二钠盐二水化合物就是那个“警察”,把这些小偷全抓起来,确保咱们能平平安安的过日子。
而且呀,它在医药方面的贡献也大得不得了。
比如说,医院里有些药物需要用到它,帮助药物更好地被身体吸收,简直就像是个“助攻”,让患者能够更快恢复。
对于一些病症,比如铅中毒,乙二胺四乙酸二钠盐二水化合物更是“救命稻草”。
一旦中毒,医生就会用它来“解救”患者,感觉就像是电影里那些英雄人物,总能在关键时刻拔刀相助。
说起这个,很多人可能对化学并不太感冒,但我告诉你,化学可不是那么无聊的东西。
生活中的很多东西,甚至连你喝的水,吃的食物,都是跟化学有千丝万缕的关系。
乙二胺四乙酸二钠盐二水化合物这个名字虽长,但它的作用可真不小。
它就像那位默默无闻的英雄,虽然不常出现在镁光灯下,却在背后为我们的健康打拼。
作为一个“化学战士”,乙二胺四乙酸二钠盐二水化合物也得有个好“战场”。
环境一旦污染了,它的效果可就打了折扣。
所以,咱们在享受这些化学成果的时候,也得好好保护环境。
不要等到环境出大问题了,再来后悔,那就真是为时已晚了。
乙二胺四乙酸二钠碳点

乙二胺四乙酸二钠碳点1.引言1.1 概述概述乙二胺四乙酸二钠(EDTA-Na4)是一种重要的有机酸盐,具有广泛的应用领域和显著的化学性质。
碳点是一种纳米级的碳材料,具有优异的光电特性和化学活性。
本文将探讨乙二胺四乙酸二钠与碳点的结合优势,并展望可能的研究方向和应用前景。
在本文中,我们将首先介绍乙二胺四乙酸二钠的定义和性质。
乙二胺四乙酸二钠是一种螯合剂,具有良好的络合能力和稳定性。
它可以与多种金属离子形成稳定的络合物,广泛应用于化学、医药、食品等领域。
其结构中的羧基和胺基使其具有强酸性和螯合活性,可用于金属螯合分析和溶剂萃取。
接下来,我们将介绍碳点的特性和应用。
碳点是一种具有纳米级尺寸的碳材料,具有优异的光电特性和化学活性。
由于其较小的颗粒大小和大的比表面积,碳点具有许多独特的物理、化学和光学性质。
碳点被广泛应用于生物医学、能源存储、光电材料等领域,在生物荧光探针、光电传感器、荧光显示等方面表现出良好的应用前景。
最后,我们将探讨乙二胺四乙酸二钠与碳点的结合优势。
乙二胺四乙酸二钠具有良好的络合能力和稳定性,可以有效地螯合和修饰碳点表面。
这种结合不仅可以改变碳点的表面性质和稳定性,还可以调控其光电特性和化学活性。
乙二胺四乙酸二钠修饰的碳点在生物医学、环境监测、光电传感等领域展示出广阔的应用前景。
综上所述,本文将重点讨论乙二胺四乙酸二钠与碳点的结合优势,并展望可能的研究方向和应用前景。
乙二胺四乙酸二钠的优良螯合性和碳点的优异特性相互结合,将为新型功能材料的设计合成和应用提供新的思路和方法。
预计乙二胺四乙酸二钠与碳点的研究将有助于推动纳米材料领域的发展,并在多个领域取得突破性的进展。
1.2文章结构1.2 文章结构本文将围绕乙二胺四乙酸二钠和碳点展开讨论。
文章分为引言、正文和结论三个部分。
在引言部分,我们将概述本文的主题,并阐明研究动机和研究目的。
接下来,我们将详细介绍乙二胺四乙酸二钠的定义和性质,包括其化学结构、物理性质和化学性质。
乙二胺四乙酸二钠滴定液配制与标定操作规程
**有限公司GMP管理文件一、目的:建立乙二胺四醋酸二钠滴定液(0.05mol/L)的配制和标定操作规程,规范该滴定液的配制和标定行为,保证分析结果的准确性。
二、适用范围:适用于乙二胺四醋酸二钠滴定液(0.05mol/L)的配制、标定与管理。
三、依据:《中华人民共和国兽药典》2020年版一部附录。
四、责任者:化验室滴定液配制和标定人员。
五、正文:1. 配制1.1 试剂和溶液1.1.1乙二胺四醋酸二钠(C10H14Na2O8•2H2O),分析纯;1.1.2 纯化水,符合纯化水质量要求,临用加热至沸,冷却至室温。
1.2 仪器和设备1.2.1 实验室常规仪器;1.2.2 电子天平,感量0.1g。
1.3 配制方法称取乙二胺四醋酸二钠38g,加适量的纯化水使溶解成2000ml,摇匀。
2. 标定2.1 试剂和溶液2.1.1 氧化锌,基准试剂;2.1.2 稀盐酸:取盐酸23.4ml加纯化水稀释至100.0ml;2.1.3 纯化水;2.1.4 甲基红的乙醇溶液(0.025%):称取甲基红25mg,加乙醇使溶解并稀释成100ml;2.1.5 氨试液:取浓氨溶液40ml,加水使成100ml;2.1.6 氨-氯化铵缓冲液(pH10.0):取氯化铵5.4g,加水20ml溶解后,加浓氨溶液35ml,再加水稀释至100ml;2.1.7 铬黑T指示剂。
2.2 仪器和设备2.2.1 实验室常规仪器;2.2.2 高温箱形电炉;2.2.3 分析天平,感量0.01mg 。
2.3 标定方法取于约800℃灼烧至恒重的基准氧化锌0.12g ,精密称定,加稀盐酸3ml 使溶解,加水25ml ,加0.025%甲基红的乙醇溶液1滴,滴加氨试液至溶液显微黄色,加水25ml 与氨-氯化铵缓冲液(pH10.0)10ml ,再加铬黑T 指示剂少量,用本液滴定至溶液由紫色变为纯蓝色,并将滴定的结果用空白试验校正。
每1ml 乙二胺四醋酸二钠滴定液(0.05mol/L )相当于4.069mg 的氧化锌。
乙二胺四乙酸二钠(EDTA)标准溶液配制标定
乙二胺四乙酸二钠(EDTA)标准溶液配制标定各浓度EDTA标准滴定溶液的配制按表1所示,称取乙二胺四乙酸二钠二水物(C10H14N2O8Na2· 2H2O)溶于足够量的水中,稀释至1L,贮存在聚乙烯容器内。
表 1 称取EDTA质量氧化锌基准溶液按表2所示,称取已于800℃灼烧1h的基准氧化锌置于100mL烧杯中,用少量水湿润,滴加盐酸溶液(1+1)至氧化锌溶解,移入250mL量瓶中,稀释至刻度,混匀。
表 2标定所需氧化锌质量标定氨-氯化铵缓冲溶液(pH≈10)1、称取54g氯化铵溶于水,加350mL氨水,稀释至1L。
2、称取26、7g氯化铵溶于水,加36mL氨水,稀释至1L铬黑T指示液(5g/L)称取0、50g铬黑T与4、5g氯化羟胺,溶于乙醇中,用乙醇稀释至100mL,贮存于棕色瓶中。
可保持数月不变质。
标定时,用单标线吸管吸取25mL氧化锌基准溶液于250mL锥形瓶中,加75mL水,用氨水(1+1)中与至溶液pH7~8(溶液出现微混浊),加10mL氨-氯化铵缓冲溶液,5滴铬黑T指示液,用EDTA溶液滴定至溶液由紫红色变成纯蓝色为终点。
计算乙二胺四乙酸二钠标准滴定溶液浓度按式(1)计算:c(EDTA)=m/0、08138×V (1)式乙二胺四乙酸二钠标准滴定溶液之物质的量浓度,mol/L ;中:c(EDTA)──m──25、0mL氧化锌基准溶液中所含氧化锌的质量,g;V──滴定用去乙二胺四乙酸二钠溶液的实际体积,mL;0、08138──与1、00mL乙二胺四乙酸二钠标准滴定溶液〔c( EDTA) = 1、000mol/L〕相当的以克表示的氧化锌的质量。
精密度做五次平行测定,取平行测定的算术平均值为测定结果。
五次平行测定的极差,应小于表3规定的容许差r。
表3EDTA标准滴定溶液标定的容许差稳定性乙二胺四乙酸二钠标准滴定溶液每月重新标定一次。
来自: http://hi、baidu、com/576477481/blog/item/d61b8e5615d649163a2935bc、html。
2020版《中国药典》乙二胺四醋酸二钠滴定液配制与标定操作规程
一、目的:建立乙二胺四醋酸二钠滴定液(0.05mol/L)的配制与标定标准操作规程,规定了乙二胺四醋酸二钠滴定液(0.05mol/L)的配制、标定方法与要求 。
二、范围:适用于乙二胺四醋酸二钠滴定液(0.05mol/L)的配制、标定操作。
三、职责:化验室对实施本规程负责四、内容:1、仪器与用具:马弗炉、电子天平(万分之一)、坩锅、锥形瓶(250m1)、滴定管(50m1、A 级)、取样勺、量筒(50ml)、刻度管(5ml 、10ml )、量筒(100ml 、250m1) 。
2、试药与试液:2.1乙二胺四醋酸二钠(AR)2.2氧化锌(基准试剂)2.3稀盐酸(见EK/SOP-QC8001试液配制操作规程)2.4 0.025%甲基红的乙醇溶液(见EK/SOP-QC8003指示剂与指示液配制操作规程)2.5氨试液(见EK/SOP-QC8001试液配制操作规程)2.6氨-氯化铵缓冲液(pH10.0)(见EK/SOP-QC8002缓冲液配制操作规程)2.7铬黑T 指示剂(见EK/SOP-QC8003指示剂与指示液配制操作规程)3、配制:3.1分子式:C 10H 14N 2Na 2O 8·2H 2O 分子量:372.243.2欲配浓度:18.61g →1000ml3.3取乙二胺四醋酸二钠19g ,加适量的冷水使溶解成1000ml ,摇匀。
4、标定与复标:4.1操作方法:取于约800℃灼烧至恒重的基准氧化锌0.12g ,精密称定,加稀盐酸3ml 使溶解,加水25ml ,加0.025%甲基红的乙醇溶液1滴,滴加氨试液至溶液显微黄色,加水25ml 与氨-氯化铵缓冲液(pH10.0)10ml,再加铬黑T 指示剂少量,用本液滴定至溶液由紫色变为纯蓝色,并将滴定的结果用空白试验校正。
每1ml 乙二胺四醋酸二钠滴定液(0.05mol/L )相当于4.069mg 的氧化锌。
根据本液的消耗量与氧化锌的取用量,算出本液的浓度,即得。
工作场所空气有毒物质测定无机化合物
一氧化氮和二氧化氮的盐酸萘乙二胺分光光度法仪器:具塞比色管10ml吸收液:将50ml冰乙酸(GR)加入900ml水中,摇匀;加入5g对氨基苯磺酸,搅拌溶解后,加入0.05g盐酸萘乙二胺,溶解后,用水稀释至1000ml,为贮备液。
置于棕色瓶中于冰箱内保存,可稳定1个月。
临用前,取4份此液与1份水混合。
吸收液在使用过程中应避免日光直接照射。
氧化氮标准溶液:准确称取0.1500g亚硝酸钠(于105℃干燥2h,GR),溶于水,定量转移入1000ml容量瓶中,稀释至刻度。
此液为0.10mg/ml标准贮备液。
置于冰箱内可保存1个月。
临用前,用水稀释成5ug/ml氧化氮标准溶液。
标准曲线的绘制:取7只具塞比色管,分别加入0.00、0.05、0.10、0.20、0.30、0.50、0.70ml标准溶液,各加水至1.0ml,加入4.0ml吸收液,配成0.00、0.25、0.50、1.00、1.50、2.50、3.50ug氧化氮标准系列。
将各标准管摇匀后,放置15min;在540波长下测量吸光度。
以吸光度均值对氧化氮含量(ug)绘制标准曲线。
氨的纳氏试剂分光光度法仪器:具塞比色管10ml试剂:浓硫酸吸收液:将26.6ml浓硫酸缓缓加入1000ml水中。
纳氏试剂:溶解17g氯化汞于300ml水中;另溶解35g碘化钾于100ml水中;将前液慢慢加入后液中至生成红色沉淀为止。
加入600ml氢氧化钠溶液(200g/L)和剩余的氯化汞溶液,混匀。
贮存于棕色瓶中,于暗处处置数日,取出上清液置于另一棕色瓶中,用胶塞塞紧,避光保存。
标准溶液:准确称取0.3879g硫酸铵(于80℃干燥1h),溶于吸收液中,定量转入100ml容量瓶中,用吸收液稀释至刻度。
此溶液为1.0mg/ml氨标准贮备液。
临用前,用吸收液稀释成20.0ug/ml氨标准溶液。
标准曲线的绘制:取7只具塞比色管,分别加入0.00、0.10、0.30、0.50、0.70、0.90、1.20ml氨标准溶液,各加吸收液至10.00ml,配成0.0、2.0、6.0、10.0、14.0、18.0、5、24.0ug氨标准系列。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
乙二胺四乙酸二钠水溶液的紫外吸收
乙二胺四乙酸二钠(简称EDTA二钠)是一种常用于分析化学和工业生产中的配位试剂。
它具有优异的电子构型和多性质,因此在溶液中的紫外吸收特性备受关注。
EDTA二钠的分子结构含有多个羧酸基团和两个乙二胺配体,它们与金属离子形成稳定的络合物。
溶液中的EDTA-金属络合物能够吸收紫外光,产生特定的吸收峰。
这一现象为我们在化学研究和实验中提供了重要的分析工具。
在紫外吸收光谱图中,EDTA二钠溶液展示了一个明显的吸收峰,其最大吸收波长位于230-250纳米之间。
这个吸收峰的强度与EDTA二钠的浓度成正比。
因此,通过分析紫外吸收光谱,我们可以根据吸收峰的强度来确定EDTA二钠溶液的浓度。
同时,EDTA二钠的紫外吸收谱还可以用于监测金属离子的存在和浓度。
当金属离子存在于EDTA二钠溶液中时,它们会与EDTA形成络合物。
这些络合物在紫外光照射下也会表现出吸收峰。
通过测量吸收峰的强度变化,我们可以推断金属离子的浓度。
它的紫外吸收特性还能用于研究和分析其他化学物质。
例如,我们可以通过测量不同溶液的吸收峰来确定不同物质的浓度。
此外,EDTA二钠还可以与一些有机染料形成稳定的络合物,这些络合物的上转换效率较高,因此在光学材料和荧光探针等领域具有广泛的应用前景。
总之,EDTA二钠的紫外吸收特性对于分析、监测和研究各类化学
物质具有重要意义。
在实验和工业生产中,通过测定吸收峰的强度,
我们能够准确地确定EDTA二钠的浓度以及其他金属离子的存在和浓度。
这为我们提供了一种便捷、准确的分析方法,为化学研究和应用提供
了重要的支持。
