大学无机化学分子结构共57页
合集下载
无机化学第六版第二章 分子结构

2.spd型杂化 能量相近的(n 1)d与ns、np轨道 或ns、np与nd轨道组合成新的dsp或spd型杂化轨
道的过程可统称为spd型杂化。
杂化类型 杂化轨道数
空间构型
dsp2
sp3d d2sp3 或sp3d2
4
5
6
正方形 三角双锥 正八面体
10:01
30
(二)等性杂化与不等性杂化:
原子轨道的杂化可分为等性和不等性杂化两类。
10:01
33
N原子:2s22p3 ,有3个单电子,可形成3个共价键
2p 2s
孤对电子
杂化
孤电子对占据的杂化轨道,不参与成键,电子 云密集在中心原子周围,s轨道成分相对增大,其余 3个杂化轨道p成分相对增大。
产生不等性杂化的原因:参与杂化的原子轨 道中电子数目多于轨道数目,出现孤电子对。
10:01
10:01
13
10:01
14
例如:N2分子的形成, N:1s22s2 2pX12pY12pZ1
10:01
15
σ键与π键的区别
1)σ键重叠程度大,键牢固,可单独存在;π 键电子云较松散,不稳定,只能与σ键共存。 2)以共价键结合的两原子间只能有一个σ键, 但可以有多个π键
单键:σ键 双键:σ+π 叁键:σ+π+π
(2)同一周期中电子层结构相同的阳离子的半径, 随离子的电荷数的增加而减小;而阴离子的半径 随离子的电荷数减小而增大。
(3)同一主族元素的离子半径自上而下随核电荷 数的增加而增大。
(4)相邻主族左上方和右下方两元素的阳离子半 径相近。
10:00
4
(三)离子的电子组态
离子的电子层组态有以下几种: (1)2 电子组态:离子只有 2 个电子,外层电子组态 为 1s2。 (2)8 电子组态:离子的最外电子层有 8 个电子,外
大学无机化学课件分子结构
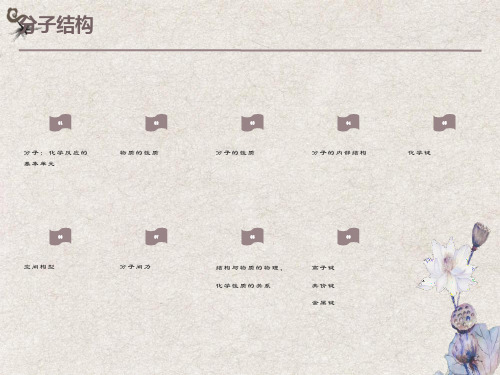
π对称:绕 x 轴旋转180°,形状不变,ψ符号改变。例如:原子轨道pz,py,dxy,dxz,dyz为π对称。
(3) 原子轨道线性组合的类型
例如: A+B→AB
Ⅱ
Ⅱ
Ⅰ
-成键 -反键
① s – s 重叠
1s 原子轨道
1s 原子轨道
分子轨道
s1s *
s1s
②s – p 重叠
p – p 重 叠
③具有方向性:轨道最大重叠的方向。
8.2.2 共价键的类型
(1)σ键:两原子的成键轨道沿键轴(或两核间的连线)的方向,以“头碰头”的方式发生轨道重叠,轨道重叠部分是沿着键轴呈圆柱型对称,这样形成的共价键叫σ键。
+
+
x
+
+
x
—
+
+
x
—
—
s-s
px-s
px- px
(2)π键:两个原子轨道沿键轴的方向,通过键轴的一个平面侧面,以“肩并肩”的方式发生轨道重叠,轨道重叠部分垂直于键轴呈镜面反对称,在键轴上下对称的电子云密度最大,这样形成的共价键叫π键。
价键理论
01
共价键的类型
02
杂化轨道理论
03
价层电子互斥理论(自学)
04
分子轨道理论
05
键参数
06
8.2 共价键
共价键: 分子中原子间通过共用电子对结合而成 的化学键
H· + ·H = H:H
:Cl· + ·Cl: = :Cl:Cl:
:N· + ·N: = :N N:
④ 杂化轨道成键时,满足原子轨道最大重叠原理
⑤杂化轨道成键时,满足化学键间最小排斥原理。
(4) 小结:p226,表9-5
无机化学 第六章 分子结构

随堂练习:
2.请应用现代价键理论合理地解释乙炔的成键情况,有几个σ
键?几个π 键?
HC≡CH
乙炔
随堂练习:
3.试用杂化轨道理论解释下面问题: (1) NH3、H2O 的键角为什么比 CH4 小?CO2 的键角为何是
180°?乙烯为何取120 °的键角?
(2)在 sp2 和 sp 杂化轨道中,是否也存在不等性杂化? 各举一例! 例如 SO2 和 CO
新轨道叫杂化轨道。
(线性组合)
(2)杂化轨道的数目等于参加杂化的原子轨道的数(遵循原则)
二、杂化轨道理论
1.杂化轨道理论基本要点
(3)杂化轨道在空间的伸展方向是尽可能取最大夹角,一般取对称
形,这样排斥力最小,形成的分子体才系稳定(数学理想建模)
杂化轨道的数目 理想模型 空间的最佳排布
直线型 正三角型 正四面体
一、价键理论(电子配对理论)VB法 3.共价键的特征 a.饱和性
基态原子的未成对电子数是一定的,因此它能形成的共价 键数 也是一定的。 3p 例如:N : 1S22S22P3
N: 1s 2s
3个单电子
2Px
2Py 2Pz
NH3分子的成键过程
一、价键理论(电子配对理论)VB法 3.共价键的特征: b.方向性
bonds (C).The hybride orbital considered were sp,sp2,sp3.
Bonds where the electron density is symmetrical about the bond axis are called sigma (σ) bonds; bonds in which the electron density is not symmetrical about the bond axis are called pi(π)bonds .
无机化学第九章 分子结构

1/ 2 cos 1 1 1/ 2
180
ο
2. spd型杂化
• sp3d杂化
PCl5(g)的几何构型为三角双锥。
P: 3s23p3
3p
3d
激发
3p
3d
3s
sp3d杂化
3s
sp3d
sp3d杂化
• sp3d2杂化
SF6的几何构型为八面体。 S: 3s23p4
3p
3d
3p
3d
3
I 属于AX2L3型离子,几何构型为直 线形。
3
思考题:
解释NO2+, O3, SnCl3-, OF2, ICl3, I3-, XeF5+, ICl4- 等离子或分子的空间构型,并
指出其中心原子的轨道杂化方式。
分子 或离子 NO2+ O3
价层 电子对 2(直线型) 3(平面三角形)
孤对 电子对 0 1
第九章
§9.1 §9.2 §9.3
分子结构
Lewis理论 价键理论 杂化轨道理论
§9.4
§9.5
价层电子对互斥理论
分子轨道理论
§9.6
键参数
化学键:分子或晶体中相邻原子(或离 子)之间强烈的吸引作用。 化学键种类:共价键、离子键、金属键。
共价键理论:
Lewis理论(1916年)
价键理论(1927年, 1930年)
a,b—原子轨道,
c1,c2 —系数
Ⅰ :成键分子轨道;Ⅱ:反键分子轨道。
3. 原子轨道组合方式不同,将分子 轨道分为σ轨道与π轨道。
* • s轨道与s轨道线性组合成 s 和 s
节面
* s
s
s
s
180
ο
2. spd型杂化
• sp3d杂化
PCl5(g)的几何构型为三角双锥。
P: 3s23p3
3p
3d
激发
3p
3d
3s
sp3d杂化
3s
sp3d
sp3d杂化
• sp3d2杂化
SF6的几何构型为八面体。 S: 3s23p4
3p
3d
3p
3d
3
I 属于AX2L3型离子,几何构型为直 线形。
3
思考题:
解释NO2+, O3, SnCl3-, OF2, ICl3, I3-, XeF5+, ICl4- 等离子或分子的空间构型,并
指出其中心原子的轨道杂化方式。
分子 或离子 NO2+ O3
价层 电子对 2(直线型) 3(平面三角形)
孤对 电子对 0 1
第九章
§9.1 §9.2 §9.3
分子结构
Lewis理论 价键理论 杂化轨道理论
§9.4
§9.5
价层电子对互斥理论
分子轨道理论
§9.6
键参数
化学键:分子或晶体中相邻原子(或离 子)之间强烈的吸引作用。 化学键种类:共价键、离子键、金属键。
共价键理论:
Lewis理论(1916年)
价键理论(1927年, 1930年)
a,b—原子轨道,
c1,c2 —系数
Ⅰ :成键分子轨道;Ⅱ:反键分子轨道。
3. 原子轨道组合方式不同,将分子 轨道分为σ轨道与π轨道。
* • s轨道与s轨道线性组合成 s 和 s
节面
* s
s
s
s
无机化学 分子结构PPT课件

●原子轨道为什么需要杂化?
●如何求得杂化轨道的对称轴间的夹角?
28
1.基本要点
(1)杂化 (Hybrid) 能量相近,类型不同的同一中心原
子轨道可以混合起来,重新组成一组新 的能量相同,类型相同的轨道。
(2)杂化轨道 (Hybrid Orbital)
n个能量相近,类型不同的原子轨道 可以组成n个能量相同,类型相同的杂化
范畴: pz-pz 重叠 py-py 重叠
25
特征:原子轨道以“肩并肩”的形式发生轨道重叠。
特点:电子云没有集中在两核间连线,所以,
π键重叠程度小于σ键, π键不及σ键
稳定。 举例:N2: 1s22s22p3
1s22s22p3
2px12py12pz1 2px12py12pz1
结论:(1)共价单键为σ键,π键几乎总是与σ键
● 具有饱和性(是指每种元素的原子能提供用于形成 共价键的轨道数是一定的)
例如: H Cl H OH NN
● 具有方向性(是因为每种元素的原子能提供用于形 成共价键的轨道是具有一定的方向)
18
共价键的类型
1. σ键
定义:两原子轨道沿键轴(两核间联 线)进行同号重叠而形成的共 价键称σ键。
范畴:
s~s
第二章 分子结构
(Structure of Molecule) 价键理论
价层电子对互斥理论
分子轨道理论
键参数
1
2-1路易斯结构式
路易斯用元素符号之间的小黑点表示分子中各原子 的键合关系,代表一对键电子的一对小黑点亦可用“- ”代替。路易斯结构式能够简洁地表达单质和化合物的 成键状况,其基本书写步骤如下:
空间构型:平面三角形 键 角:120
38
●如何求得杂化轨道的对称轴间的夹角?
28
1.基本要点
(1)杂化 (Hybrid) 能量相近,类型不同的同一中心原
子轨道可以混合起来,重新组成一组新 的能量相同,类型相同的轨道。
(2)杂化轨道 (Hybrid Orbital)
n个能量相近,类型不同的原子轨道 可以组成n个能量相同,类型相同的杂化
范畴: pz-pz 重叠 py-py 重叠
25
特征:原子轨道以“肩并肩”的形式发生轨道重叠。
特点:电子云没有集中在两核间连线,所以,
π键重叠程度小于σ键, π键不及σ键
稳定。 举例:N2: 1s22s22p3
1s22s22p3
2px12py12pz1 2px12py12pz1
结论:(1)共价单键为σ键,π键几乎总是与σ键
● 具有饱和性(是指每种元素的原子能提供用于形成 共价键的轨道数是一定的)
例如: H Cl H OH NN
● 具有方向性(是因为每种元素的原子能提供用于形 成共价键的轨道是具有一定的方向)
18
共价键的类型
1. σ键
定义:两原子轨道沿键轴(两核间联 线)进行同号重叠而形成的共 价键称σ键。
范畴:
s~s
第二章 分子结构
(Structure of Molecule) 价键理论
价层电子对互斥理论
分子轨道理论
键参数
1
2-1路易斯结构式
路易斯用元素符号之间的小黑点表示分子中各原子 的键合关系,代表一对键电子的一对小黑点亦可用“- ”代替。路易斯结构式能够简洁地表达单质和化合物的 成键状况,其基本书写步骤如下:
空间构型:平面三角形 键 角:120
38
大学无机化学分子结构

·· K·+ :Cl· →
K+[:C··l:]-
··
··
定义:正负离子间的静电吸引力叫做离子键。
特点:既没有方向性, 也不具饱和性。
NaCl 晶体
1.1 离子键的形成条件
1. 元素的电负性差比较大
X > 1.7,发生电子转移,产生正、负离子,形成离子键;
X < 1.7,不发生电子转移,形成共价键。(X > 1.7 ,实 际上是指离子键的成分大于 50 %)
第二章 分子结构
序言:
• 原子怎样结合成为分子? 化学键
• 离子键
Link
共价键
金属键
• 分子的形状? - 分子构型
–价电子对互斥理论
• 分子怎样组成物质材料?-分子间作用力
• 固体材料的结构?
-晶体结构
-无定型结构
化学键: 分子中原子间的强烈作用。
第一节 离子键
离子键及其特点
离子键及其特点· :
一、经典的共价键理论(G.N. Lewis, 1916, 美国) 1. 要点:
共价分子中的原子都有形成稀有气体电子结构(8 电子稳定结构)的趋势,求得自身的稳定。
原子通过共用电子对形成化学键。
——共价键
“-”单键 “=”双键“ ”三键,价键结构式如:NN
Lewis 的贡献,在于提出了一种不同于离子键的新的 键型,解释了电负性比较小的元素之间原子的成键事实。
1.2 离子键的特征
离子键的实质是静电引力 F q1 q2 / r 2,影响 离子键强度的因素有:离子的电荷 q 、离子的电子 层构型和离子半径 r (离子的三个重要特征) 。
第二节 共价键
针对一些非金属单质或电负性相差不大的元素间 形成的化合物中各原子之间的化学键。
大学无机化学《分子结构》 ppt课件
19
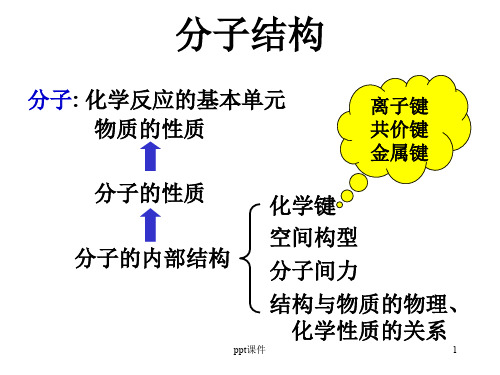
sp3杂化轨道示意图
CH4分子的空间结构
ppt课件
20
④ sp3d2杂化 1 ns + 3 np + 2 nd 6 sp3d2 六个sp3d2杂化轨道指向正八面体的六个顶点 sp3d2杂化轨道间的夹角 = 180或90
ppt课件
21
3p 3s
激发态
激发
SF6分子形成
杂化
3d
sp3d2杂化态
② 杂化前后轨道数目不变。
③ 杂化轨道可分为等性和不等性杂化轨道。 采用sp3杂化轨道成键的分子,其空间构型可 能为四面体型,V型或者三角锥型。
③ 单电子键 (如 H2+p)p,t课O件 2具有磁性
6
1927年, Heitler 和 London 应用量子力学研究 H2分子结构, 初步解答了共价键的本质.
1930年, Pauling 和 Slater 等发展出现代价键 理论(电子配对理论)、杂化轨道理论、 价层电子对互斥理论
1932年, 美国化学家密立根和德国化学家洪特 提出分子轨道理论
ppt课件
10
8.2.2 共价键的类型
(1)σ键:两原子的成键轨道沿键轴(或两 核间的连线)的方向,以“头碰头”的方式 发生轨道重叠,轨道重叠部分是沿着键轴呈 圆柱型对称,这样形成的共价键叫σ键。
++
x
s-s
—
++
x
px-s
—
++
—
x
ppt课件
px- px
11
(2)π键:两个原子轨道沿键轴的方向,通过键轴的
另一方有空轨道。
例:NH
4
H
HNH
H
BF4
CO
药学大一无机化学分子结构PPT课件
c. 离子的电子层结构
原子究竟能形成何种电子层构型的离子, 除决定于原子本身的性质和电子层构型本身 的稳定性外,还与其相作用的其它原子或分 子有关。
一般简单的负离子( F-、Cl-、O2-)等,其 最外层都具有稳定的8电子结构。
第17页/共95页
对正离子情况复杂得多。 ①、2电子构型: Li+,Be2+ ②、8电子构型: Na+,Mg2+ ③、18电子构型: Zn2+,Hg2+ ,Cu+,Ag+ ④、18+2电子构型: Pb2+,Sn2+ ⑤、9-17电子构型: Fe2+, Cr3+ ,Mn2+ 等。 离子的电子构型不同,其离子间的作用力不同。
xx px
++
绕键轴旋转
键轴
z
180°
++
第39页/共95页
例: N2 分子中两个原子各有三个单电子
px py pz
沿 z 轴成键时, px 与 px “ 头碰头” 形成一个 键 。此时, pz 和 pz , py 和 py 以 “ 肩并肩 ” 形式重叠,形成两个 键。
N2 分子的 3 键中,有 1 个 键, 2 个 键 。
第3页/共95页
1、离子键及其特点:
Na· +
·· :Cl·→
Na +[:C··l:]-
定义:正负离子间··的静电吸引·力· 叫做离子键。
特点:既没有方向性,也不具饱和性。
NaCl 晶体
第4页/共95页
离子键理论的基本要点:
a.活泼金属原子失去最外层电子,形成稳定电子结 构的带正电的子; b.活泼非金属原子得到电子,形成稳定电子结构的 带负电的离子; c.正、负离子之间由于静电引力作用而形成稳定的 结合体。
