尿葡萄糖定性检测试剂盒(改良班氏法)
尿糖的定性检测-尿糖定性试验
尿糖的定性检测
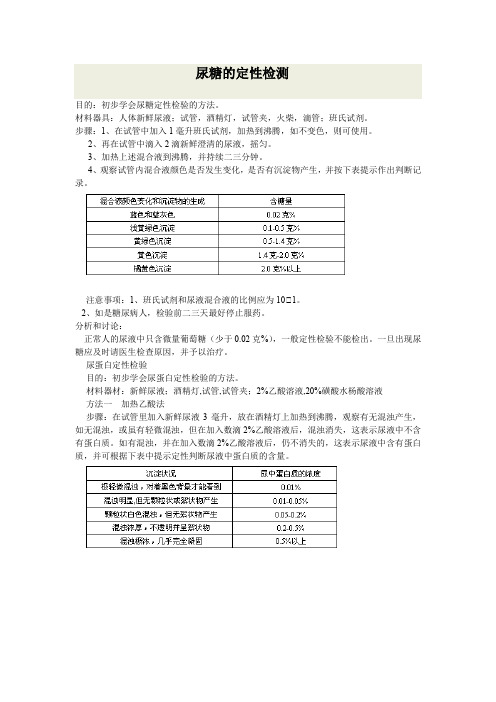
目的:初步学会尿糖定性检验的方法。
材料器具:人体新鲜尿液;试管,酒精灯,试管夹,火柴,滴管;班氏试剂。
步骤:1、在试管中加入1毫升班氏试剂,加热到沸腾,如不变色,则可使用。
2、再在试管中滴入2滴新鲜澄清的尿液,摇匀。
3、加热上述混合液到沸腾,并持续二三分钟。
4、观察试管内混合液颜色是否发生变化,是否有沉淀物产生,并按下表提示作出判断记录。
注意事项:1、班氏试剂和尿液混合液的比例应为10∶1。
2、如是糖尿病人,检验前二三天最好停止服药。
分析和讨论:
正常人的尿液中只含微量葡萄糖(少于0.02克%),一般定性检验不能检出。
一旦出现尿糖应及时请医生检查原因,并予以治疗。
尿蛋白定性检验
目的:初步学会尿蛋白定性检验的方法。
材料器材:新鲜尿液;酒精灯,试管,试管夹;2%乙酸溶液,20%磺酸水杨酸溶液
方法一加热乙酸法
步骤:在试管里加入新鲜尿液3毫升,放在酒精灯上加热到沸腾,观察有无混浊产生,如无混浊,或虽有轻微混浊,但在加入数滴2%乙酸溶液后,混浊消失,这表示尿液中不含有蛋白质。
如有混浊,并在加入数滴2%乙酸溶液后,仍不消失的,这表示尿液中含有蛋白质,并可根据下表中提示定性判断尿液中蛋白质的含量。
尿糖测定的实验报告

一、实验目的1. 了解尿糖测定的原理和方法。
2. 掌握尿糖定性检测的操作步骤。
3. 通过实验,判断尿液中是否含有糖分。
二、实验原理尿糖测定是利用葡萄糖的还原性,在碱性条件下将硫酸铜还原为氧化亚铜,从而产生颜色变化。
根据颜色深浅可以判断尿液中糖分的含量。
三、实验仪器和试剂1. 仪器:试管、试管架、酒精灯、滴管、移液管、显微镜等。
2. 试剂:班氏试剂、氢氧化钠溶液、尿液样本、硫酸铜溶液、标准葡萄糖溶液等。
四、实验步骤1. 标准曲线的制作(1)取5个试管,分别编号为1-5。
(2)向每个试管中加入0.5ml的标准葡萄糖溶液。
(3)向每个试管中加入1.0ml的班氏试剂。
(4)将试管放入水浴中加热,观察颜色变化。
(5)记录每个试管中溶液的颜色变化,绘制标准曲线。
2. 尿糖定性检测(1)取一个试管,加入2ml尿液样本。
(2)向试管中加入1.0ml班氏试剂。
(3)将试管放入水浴中加热,观察颜色变化。
(4)将加热后的溶液与标准曲线进行比对,判断尿液中是否含有糖分。
五、实验结果与分析1. 标准曲线的制作标准曲线如图所示,根据溶液颜色变化,可以判断尿液中糖分的含量。
2. 尿糖定性检测实验结果显示,尿液样本加热后溶液颜色与标准曲线相比,颜色略深,说明尿液样本中可能含有糖分。
六、实验讨论1. 实验过程中,应注意加热温度和时间,以确保实验结果的准确性。
2. 尿糖测定结果受多种因素影响,如尿液样本的浓度、试剂的纯度等,因此实验结果仅供参考。
3. 若尿液样本中糖分含量较高,可能提示患有糖尿病等疾病,需进一步检查确认。
七、实验总结通过本次实验,我们掌握了尿糖测定的原理和方法,了解了尿糖检测在临床医学中的重要性。
在实验过程中,我们学会了如何操作仪器和试剂,提高了实验技能。
同时,我们也认识到了实验过程中应注意的问题,为今后类似实验打下了基础。
实验报告完毕。
尿糖的检测实验报告

一、实验目的1. 了解尿液中糖分的存在情况。
2. 掌握尿糖的定性检测方法。
3. 学习班氏法检测尿糖的原理和操作步骤。
二、实验原理尿糖检测是通过检测尿液中葡萄糖的含量来评估机体糖代谢状况的一种方法。
葡萄糖是人体代谢过程中产生的主要糖类物质,正常情况下,肾脏会将多余的葡萄糖重吸收,因此尿液中葡萄糖含量极低。
当血糖浓度升高,超过肾脏的重吸收阈值时,多余的葡萄糖会随尿液排出体外,形成尿糖。
班氏法检测尿糖的原理是:葡萄糖分子中含有醛基,在碱性条件下,葡萄糖可以将试剂中的蓝色硫酸铜还原成黄色的氢氧化亚铜,并进一步与班氏试剂中的酒石酸钾钠反应生成红色氧化亚铜沉淀,从而判断尿液中是否存在葡萄糖。
三、实验仪器和试剂1. 仪器:离心机、移液器、试管、试管架、酒精灯、石棉网、加热板等。
2. 试剂:尿液样本、班氏试剂(含硫酸铜、酒石酸钾钠、氢氧化钠)、盐酸、蒸馏水等。
四、实验步骤1. 尿液样本准备:取适量尿液样本,离心后取上清液备用。
2. 班氏试剂准备:将班氏试剂中的硫酸铜、酒石酸钾钠、氢氧化钠按比例混合,配制成班氏试剂。
3. 尿糖检测:a. 取三个试管,分别标记为A、B、C。
b. 在A、B、C试管中分别加入等量的尿液样本。
c. 在每个试管中加入2滴班氏试剂。
d. 将试管放入水浴中加热,保持沸腾状态5分钟。
e. 观察试管中颜色变化,记录结果。
五、实验结果与分析1. 结果:- A试管:出现红色沉淀。
- B试管:出现淡红色沉淀。
- C试管:无沉淀。
2. 分析:- A试管中出现红色沉淀,说明尿液样本中葡萄糖含量较高。
- B试管中出现淡红色沉淀,说明尿液样本中葡萄糖含量较低。
- C试管中无沉淀,说明尿液样本中不含葡萄糖。
六、实验结论1. 通过本次实验,成功掌握了尿糖的定性检测方法。
2. 班氏法检测尿糖操作简便、结果准确,适用于临床诊断。
3. 实验结果表明,尿液样本中葡萄糖含量与检测结果呈正相关。
七、实验注意事项1. 实验过程中注意操作规范,避免污染。
测定尿糖原理的班氏法解析

测定尿糖原理的班氏法解析测定尿糖是人体健康监测的重要指标之一。
尿糖的测定方法众多,其中班氏法是常用的一种。
本文将介绍班氏法的原理和操作步骤,以及其在尿糖测定中的应用和局限性。
班氏法是利用酚作为还原剂与硫酸铜(Fehling液)反应,生成红色的氧化铜沉淀,进而定量测定尿液中的糖分含量。
该方法的原理基于尿液中的还原性物质(如葡萄糖、果糖等)能与酚一起氧化,生成对应的酚醛酸,同时将硫酸铜还原为氧化铜沉淀。
而尿液中没有还原性物质时,硫酸铜会保持蓝色。
接下来,让我们逐步解析班氏法的操作步骤。
我们需要准备班氏试剂,它是由Fehling A液和Fehling B液组成的。
Fehling A液含有硫酸铜和硝酸铜,Fehling B液含有碱式酱油盐和酚。
接下来,我们将尿液样品与班氏试剂混合,并进行加热。
在加热的过程中,如果尿液中含有还原性物质,它们将与酚一起氧化,生成红色的氧化铜沉淀。
这种沉淀的形成可以用肉眼观察到。
我们需要注意一个重要的步骤,就是控制加热的时间和温度。
如果加热时间太短或温度过低,尿液中的还原性物质可能没有完全氧化,导致实验结果偏低。
相反,如果加热时间太长或温度过高,还原性物质可能过度氧化,导致实验结果偏高。
完成反应后,我们可以通过比色法来定量测定尿液中的糖分含量。
可以利用分光光度计来测量生成的氧化铜沉淀的吸光度,然后与已知浓度的糖溶液进行比较,从而确定尿液中的糖分含量。
然而,班氏法也存在一些局限性。
该方法只能定性和定量测定还原性糖分,对非还原性糖分的测定效果较差。
班氏法对其他物质的干扰比较敏感,如某些药物和尿液中存在的其他化合物。
在使用班氏法测定尿糖时,需要注意样品的处理和准备,以确保准确性和可靠性。
班氏法是一种常用的测定尿糖的方法,其原理是利用酚作为还原剂与硫酸铜反应,从而测定尿液中的糖分含量。
然而,该方法也存在一定的局限性。
对于准确的尿糖测定,我们建议结合其他方法和技术,以获得更全面、准确和可靠的结果。
家兔糖定性实验报告(3篇)

第1篇一、实验目的1. 了解家兔肾脏对葡萄糖的重吸收功能。
2. 掌握糖定性实验的操作方法及原理。
3. 分析实验结果,验证肾小管对葡萄糖的重吸收作用。
二、实验原理人体内葡萄糖通过肾小球滤过,但大部分葡萄糖在肾小管中被重吸收。
本实验通过静脉注射葡萄糖,观察尿液的变化,来判断肾小管对葡萄糖的重吸收功能。
实验原理如下:1. 正常情况下,尿液中的葡萄糖含量极低,糖定性实验结果为阴性。
2. 当静脉注射葡萄糖后,血液中的葡萄糖浓度升高,超过肾糖阈(约180mg/dL),肾小管无法将所有葡萄糖重吸收,导致尿液中的葡萄糖含量增加。
3. 葡萄糖含有醛基,具有还原性。
将尿液加热煮沸后,葡萄糖会将班氏试剂中的硫酸铜还原为氧化亚铜,使试剂由蓝色变为砖红色。
三、实验材料1. 实验动物:家兔2. 实验器材:注射器、酒精棉球、手术刀、手术剪、镊子、试管、班氏试剂、蒸馏水、葡萄糖溶液、试管架、酒精灯、加热器3. 实验试剂:班氏试剂、葡萄糖溶液、蒸馏水四、实验步骤1. 家兔处死:使用注射器抽取10ml空气,迅速注入家兔耳缘静脉。
观察家兔反应,确认其已死亡。
2. 解剖家兔:打开家兔腹腔,暴露肾脏。
剪开肾包膜,取出肾脏。
3. 肾脏处理:将肾脏放入生理盐水中洗净,去除血污。
将肾脏置于解剖盘上,用手术刀和镊子将肾小球、肾小管等组织分离。
4. 肾小管收集:将肾小管放入试管中,加入少量蒸馏水,用玻璃棒轻轻搅拌,使肾小管内容物充分溶解。
5. 葡萄糖注射:将家兔静脉注射葡萄糖溶液,注射剂量为1g/kg体重。
6. 尿液收集:收集家兔尿液,放入另一支试管中。
7. 糖定性实验:将尿液和肾小管内容物分别加入两支试管中,分别加入班氏试剂。
将试管放入加热器中加热煮沸,观察颜色变化。
五、实验结果1. 尿液:加热煮沸后,尿液变为砖红色,说明尿液中含有葡萄糖。
2. 肾小管内容物:加热煮沸后,肾小管内容物颜色无明显变化,说明肾小管对葡萄糖的重吸收功能正常。
六、实验分析1. 本实验结果表明,家兔肾脏具有对葡萄糖的重吸收功能。
班氏试剂鉴定葡萄糖

班氏试剂鉴定葡萄糖篇一:班氏试剂的配制与鉴定结果班氏试剂的配置取无水硫酸铜,溶于100ml热水中,冷却后稀释到150ml,取柠檬酸钠173g,无水碳酸钠100g和600ml水共热,溶后冷却并加水至850ml,再将冷却的150ml 硫酸铜倾入即可。
鉴定糖尿的结果沸水浴加热后的现象葡萄糖含量(g/dl)透明蓝色无加热时无变化,仅冷却后有少量沉淀微量,约以下加热1分钟后即出现少量黄绿色沉淀少量,约-1加热10-15秒后即出现土黄色沉淀中量,约1-2加热时很快出现多量砖红色沉淀大量,约2以上班氏试剂与斐林试剂比较:首先,两者的配方不一样。
斐林试剂主要由质量浓度为0.1gmL-1的NaOH溶液和质量浓度为0.05gmL-1的CuSO4溶液配制而成。
其中0.1gmL-1的NaOH溶液称为斐林试剂甲,gmL-1的CuSO4溶液称为斐林试剂乙。
而班氏试剂的配方为:①400mL水中加85g柠檬酸钠和50g 无水碳酸钠;②50mL加热的水中加入无水硫酸铜,制成CuO4溶液;③把CuSO4溶液倒入柠檬酸钠?Na2CO3溶液中,边加边搅,如产生沉淀可滤去。
其次,两者在反应原理上略有差别。
利用斐林试剂鉴定时,斐林试剂甲和斐林试剂乙直接反应产生Cu(OH)2,Cu(OH)2和可溶性还原糖反应产生砖红色沉淀。
而班氏试剂中Cu(OH)2的产生却是这样的:柠檬酸钠和碳酸钠均为强碱弱酸盐,在水中它们均可水解产生OH-,与柠檬酸钠?Na2CO3溶液和CuSO4溶液混合时,Cu2+和OH-结合,生成Cu(OH)2,Cu(OH)2与葡萄糖中的醛基反应产生砖红色沉淀。
第三,两种试剂的保存方式不同。
斐林试剂甲和斐林试剂乙可强烈反应产生Cu(OH)2,Cu(OH)2很容易沉淀析出,因此斐林试剂一般为现用现配;而班氏试剂的配方中,柠檬酸钠?Na2CO3为一对缓冲物质,产生的OH-数量有限,与CuSO4溶液混合后产生的Cu(OH)2浓度相对较低,不易析出,因此该试剂可长期保存。
尿液化学(一)

加尿液 加氯化钙 离心取上清液 加Ehrlicn试剂 观察反应
尿液 1m l 磺基水杨酸试剂 1~2滴 立即观察结果
尿液蛋白质定性(磺基水杨酸法)
尿液蛋白质定性(干化学法)
【原理】利用指示剂的蛋白质误差原理,在PH3.2的条件下, 酸碱指示剂(溴酚蓝)产生的阴离子与带阳离子的蛋白质结合 生成复合物,引起指示剂进一步电离,当超越缓冲范围时,指 示剂发生颜色改变,颜色的深浅与蛋白质含量成正比。 【评价】 1. 试带对白蛋白敏感,对球蛋白的灵敏度仅为白蛋白的1/100~ 1/50,容易漏检本周氏蛋白 2. 试带法不适用于肾脏疾病的疗效观察及预后判断 3. 采用单克隆抗体技术的试带检测白蛋白可排除其他蛋白质的干 扰。基于考马斯亮蓝等染料结合蛋白质的原理,国外已研发一 种新型蛋白质试带,对白、球、本周氏同样灵敏。 4. 操作影响:试带浸渍时间过长,反应颜色变深,反之。
尿液蛋白质定性(磺基水杨酸法)
【原理】在略低于蛋白质等电点的酸性环境下,磺基水杨酸根离子 与蛋白质氨基酸阳离子结合,形成不溶性蛋折盐而沉淀。沉淀量或 溶液浑浊程度,可反映蛋白质的含量,为定性或半定量检查方法。 【评价】简便、敏感,清蛋白、球蛋白、本周氏蛋白均可检出,曾 为CCCLS推荐为参考方法,便干扰因素多,有些药物(大剂量的庆 大、青霉素)及盐类结晶可致假阳性。而大剂量的奎宁、磺胺等药 物使尿液呈碱性(PH>9),造成尿蛋白呈假阴性 【灵敏度】达50mg/L 【操作】
班氏法实验报告(3篇)

第1篇实验目的:1. 学习并掌握班氏法测定葡萄糖含量的原理和方法。
2. 了解班氏试剂的配制和保存方法。
3. 培养实验操作技能,提高分析能力。
实验原理:班氏法是一种常用的比色法,用于测定葡萄糖含量。
该法基于葡萄糖在碱性条件下与铜离子反应生成红色的氧化亚铜沉淀,通过比色测定沉淀物的颜色深浅,从而计算出葡萄糖的含量。
实验仪器与试剂:1. 仪器:分析天平、滴定管、移液管、锥形瓶、烧杯、试管、酒精灯、温度计、比色计等。
2. 试剂:班氏试剂、葡萄糖标准溶液、硫酸铜溶液、氢氧化钠溶液、盐酸、蒸馏水等。
实验步骤:1. 班氏试剂的配制:- 称取1.5g硫酸铜,加入50mL蒸馏水溶解;- 称取0.1g氢氧化钠,加入50mL蒸馏水溶解;- 将硫酸铜溶液和氢氧化钠溶液混合,充分搅拌;- 将混合液煮沸5分钟,冷却后备用。
2. 葡萄糖标准溶液的配制:- 称取1.0g葡萄糖,加入100mL蒸馏水溶解;- 将溶液转移至1000mL容量瓶中,用蒸馏水定容至刻度;- 配制浓度为0.1mg/mL的葡萄糖标准溶液。
3. 样品处理:- 称取适量样品,加入少量蒸馏水溶解;- 将溶液转移至100mL容量瓶中,用蒸馏水定容至刻度。
4. 测定:- 取5mL葡萄糖标准溶液和5mL样品溶液分别置于锥形瓶中;- 加入5mL班氏试剂,充分混合;- 将锥形瓶置于水浴中,加热至沸腾,保持5分钟;- 冷却至室温,用比色计测定溶液的吸光度。
5. 计算:- 根据标准曲线或标准方法,计算样品中葡萄糖的含量。
实验结果:1. 标准曲线:以葡萄糖浓度为横坐标,吸光度为纵坐标,绘制标准曲线。
2. 样品测定:根据标准曲线,计算样品中葡萄糖的含量。
实验讨论:1. 实验过程中,班氏试剂的配制和保存对实验结果有较大影响,应严格按照操作规程进行。
2. 样品处理过程中,应避免样品污染,保证实验结果的准确性。
3. 实验过程中,应注意控制水浴温度,避免加热过度导致实验结果偏差。
结论:通过本次实验,掌握了班氏法测定葡萄糖含量的原理和方法,提高了实验操作技能和分析能力。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
尿葡萄糖定性检测试剂盒(改良班氏法)
简介:
班氏试剂(Benedict's Reagent)又称本氏液、本尼迪克特试剂、本尼迪克试剂、本尼迪克试液或本尼迪特试剂,是一种浅蓝色化学试剂。
Leagene 尿葡萄糖定性检测试剂盒(改良班氏法)采用改良班氏试剂进行检测,其原理是含有醛基的葡萄糖在高热和强碱条件下,能将溶液中蓝色将的Cu 2+还原为Cu +,后者与碱性物质(非OH 根)结合转变为,变成黄色至砖红色的氧化亚铜(Cu 2O)沉淀。
该试剂盒主要用于定性检测人、动物尿液中葡萄糖含量。
该试剂盒仅用于科研领域,不宜用于临床诊断或其他用途。
组成:
操作步骤(仅供参考):
1、 取尿葡萄糖定性试剂置于试管中,加热煮沸,若不变色则可进行下列实验,否则应弃用。
2、 加入新鲜尿液,煮沸,冷却后观察结果。
结果判断:
参考区间:阴性(含糖量0.1~1mmol/L)。
当血糖>8.88mmol/L 超过肾糖阈,可出现尿糖阳性。
注意事项:
1、 在酒精灯上加热煮沸,时间不得少于1min 。
编号 名称 TC0455 100T Storage 尿葡萄糖定性试剂 100ml RT 使用说明书 1份 阴性(-)
不变色,如有较高磷酸盐可呈蓝色浑浊。
可疑(±)
冷却后呈绿色,但无沉淀(含糖量<6mmol/L) 阳性(+)
呈黄绿色混浊,管底有少量黄色沉淀(含糖量6~28mmol/L) (2+)
煮沸1min 呈绿色混浊,有较多黄色沉淀(含糖量28~55mmol/L) (3+)
煮沸15s 呈黄土色沉淀(含糖量55~110mmol/L) (4+) 煮沸时即呈大量砖红色混浊,并迅速沉淀,上清液无色(含糖量>110mmol/L)
2、应在煮沸后自然冷却,不应用冷水使其变冷。
3、当含有大量尿酸盐时,应把尿液置于冰箱中待盐类下沉后,取上清做实验。
4、当含有大量铵盐时,应加入过量的碱并煮沸几分钟再做实验。
5、链霉素、维生素C、水合氯醛、葡萄糖醛酸化合物课程假阳性反应;大黄、黄连等可呈
假阳性反应。
6、为了您的安全和健康,请穿实验服并戴一次性手套操作。
有效期:12个月有效。
相关:
编号名称
CC0007 磷酸缓冲盐溶液(10×PBS,无钙镁)
CS0001 ACK红细胞裂解液(ACK Lysis Buffer)
DC0032 Masson三色染色液
DF0135 多聚甲醛溶液(4% PFA)
NR0001 DEPC处理水(0.1%)
PW0082 丽春红S染色液(1×Ponceau S)。
