乙醇气相脱水制乙烯动力学实验
乙醇脱水制乙烯
3、反应进行10分钟后,正式开始实验。放出反应器 下吸收瓶中的液体,并记下此时湿式流量计的读数 ,然后关闭吸收瓶上的放液活塞,开始实验。每隔 10分钟记录湿式流量计读数,并记录反应温度等 实验条件。
实验内容 实验目的 仪器药品 实验原理 实验步骤
数据处理
资料仅供参考,不当之处,请联系改正。
乙醇脱水制乙烯
(2)进料速率为1.0mL.min-1时的样品色谱分析数据
分析次数 I
II
峰号 项目
1
2
3
1
2
3
保留时间 /min
峰面积 /uv.s
峰面积百 分比/%
实验内容 实验目的 仪器药品 实验原理 实验步骤
数据处理
资料仅供参考,不当之处,请联系改正。
乙醇脱水制乙烯
工艺流程
实验内容 实验目的 仪器药品 实验原理 实验步骤
数据处理
资料仅供参考,不当之处,请联系改正。
乙醇脱水制乙烯
实验原理
❖ 乙醇脱水生成乙烯和乙醚,是一个吸热、分子数 增不变的可逆反应。提高反应温度、降低反应压 力,都能提高反应转化率。乙醇脱水可生成乙烯 和乙醚,但高温有利于乙烯的生成,较低温度时 主要生成乙醚,有人解释这大概是因为反应过程 中生成的碳正离子比较活泼,尤其在高温,它的 存在寿命更短,来不及与乙醇相遇时已经失去质 子变成乙烯。而在较低温度时,碳正离子存在时 间长些,与乙醇分子相遇的机率增多,生成乙醚。 有人认为在生成产物的决定步骤中,生成乙烯要 断裂C-H键,需要的活化能较高,所以要在高温才 有乙烯的生成。
乙醇脱水制乙烯反应器应用与操作乙醇脱水制乙烯实验目的实验原理实验内容数据处理仪器药品实验步骤实验内容一实验目的二实验仪器和药品三实验原理四实验步骤五实验数据记录及处理乙醇脱水制乙烯实验目的实验目的实验原理实验内容数据处理仪器药品实验步骤?掌握乙醇脱水实验的反应过程和反应机理特点了解针对不同目的产物的反应条件对正副反应的影响规律和生成的过程
化学实验报告制取乙烯(3篇)

第1篇实验名称:制取乙烯实验日期:2023年X月X日实验目的:1. 学习实验室制取乙烯的方法。
2. 掌握乙醇脱水反应的原理和操作步骤。
3. 了解反应条件对产物的影响。
4. 培养实验操作技能和安全意识。
实验原理:乙醇在浓硫酸的催化作用下,加热至170℃左右时,会发生消去反应,生成乙烯和水。
反应方程式如下:\[ C_2H_5OH \xrightarrow{H_2SO_4, 170℃} C_2H_4 + H_2O \]实验仪器与试剂:1. 仪器:酒精灯、试管、试管夹、烧杯、铁架台、导管、集气瓶、橡胶塞、玻璃片、温度计。
2. 试剂:无水乙醇、浓硫酸、碎瓷片。
实验步骤:1. 取一支干燥的试管,加入约5ml无水乙醇。
2. 慢慢加入浓硫酸,边加边振荡,使混合液均匀。
3. 在试管中加入少量碎瓷片,防止暴沸。
4. 用橡胶塞密封试管,插入温度计,温度计的水银球应位于液面以下。
5. 将试管固定在铁架台上,用酒精灯加热,控制温度在170℃左右。
6. 观察反应现象,当观察到有气体产生时,将导管插入集气瓶中,收集乙烯气体。
7. 实验结束后,关闭酒精灯,将试管中的液体倒入烧杯中,用水冲洗试管。
8. 将收集到的乙烯气体用点燃的火柴检验,观察火焰的颜色和声音。
实验现象:1. 加热过程中,试管内出现大量气泡,表明有气体产生。
2. 集气瓶中收集到的气体,用火柴点燃,火焰明亮,伴有“嘭”的一声,表明气体为乙烯。
实验结果:1. 成功制取乙烯气体。
2. 实验过程中,温度控制在170℃左右,反应现象明显。
实验分析:1. 本实验成功制取了乙烯气体,验证了乙醇在浓硫酸催化下加热至170℃左右可以发生消去反应生成乙烯。
2. 实验过程中,温度对反应有重要影响,温度过高或过低都会影响产物的生成。
3. 实验过程中,应注意安全操作,避免发生意外。
实验总结:1. 本实验学习了实验室制取乙烯的方法,掌握了乙醇脱水反应的原理和操作步骤。
2. 通过实验,了解了反应条件对产物的影响,培养了实验操作技能和安全意识。
乙醇气相脱水制乙烯动力学(内循环无梯度)
3.300
气 81.57 1.465 16.46 0.08825 0.408
液
16.24
83.5
0.6000
318.5
气 89.78 2.065
液
48.81
7.098
0.1551 51.09
0.984 0.9600
气 90.18 2.298 7.109 0.3243
1.440
液
56.59
43.02
1.570
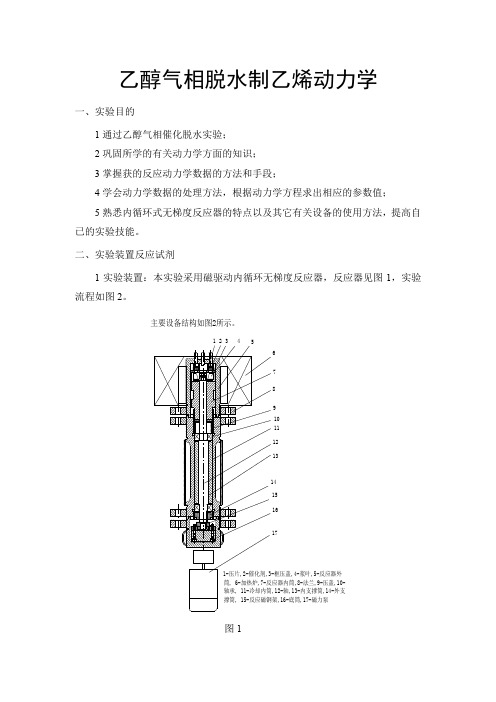
水,乙醇,乙醚的摩尔数分别为 0.0134,0.0151,0.0041 质量计算;乙烯质量=原子量×摩尔数=32×0.0087=0.2795 水和乙醇,乙醚的质量分别为 0.2407,0.6975,0.3030 合计为:0.0087+0.2407+0.6975+0.303=1.5206 与乙醇进料量基本平衡。
六、讨论 1、本次实验用来巩固所学的有关动力学的知识,由实验证明该反应器是本
征反应。 2、本次实验在操作过程中,另取了 4 个点,得一直线。 3、由实验结果可以看出,升高反应温度,乙醇气相脱水制乙烯反应有利于
生成乙烯,不利于生成乙醚。最佳反应温度在 350℃左右。
95.98
46.45 0.03515
69.50 24.59 2.155 3.766
96.62
66.36 0.01675
59.08 38.42 0.7433 1.763
98.67
64.13 0.03238
54.62 43.76 0.4146 1.198
99.24
60.84 0.04605
CA
0.0002080 0.0001580 0.0001230 0.0004320 0.0002540 0.0002310 0.001462 0.0005890 0.0005340 0.0004270 0.0001470 0.00008210
乙醇气固相催化制备乙烯实验报告

化工专业实验报告实验六乙醇气固催化脱水制乙烯姓名:XXX学号:XXXXXX班级:同组人:一实验目的1、掌握乙醇脱水实验的反应过程、实验流程和操作。
2、掌握乙醇气相脱水操作条件对产物收率的影响,学会获取稳定的工艺条件的方法。
3、了解固定床反应器的构造、原理和使用方法,学习反应器的正常操作和安装。
4、学习气相色谱在线分析的方法和定性、定量分析,学习如何手动进样分析液体成分。
了解气相色谱的原理和构造,掌握色谱的正常使用和分析条件选择。
5、学习微量泵的使用方法,学会使用湿式流量计测量流体流量。
二、实验原理乙醇脱水属于平行反应,即可进行分子内脱水生成乙烯,又可进行分子间脱水生成乙醚。
一般而言,较低的温度有利于生成乙醚,因此该复合反应条件改变,脱水机理也有不同。
采用浓硫酸、氧化铝和分子筛催化剂可以有下列反应过程产生:浓硫酸:2C2H5-OH C2H5OC2H5+H2O(140℃)C2H5OH C2H4+H2O(170℃)氧化铝:C2H5OH C2H4+H2O(360℃)分子筛:C2H5OH C2H4+H2O(300℃)随着温度升高,反应可得到足够多的乙烯转化,而乙醚的生成量较少。
乙烯是世界上产量最大的化学产品之一,乙烯工业是石油化工产业的核心,乙烯产品占石化产品的70%以上,在国民经济中占有重要的地位。
世界上已将乙烯产品作为衡量一个国家石油化工生产水平的重要标志之一。
主要用于制聚乙烯、聚氯乙烯、醋酸、高级醇等,还可用来催熟水果。
三、实验装置及流程图6-1 固定床反应装置实物图 VAVV 57151683TCITITCI-控温热电偶;TI-测温热电偶;PI-压力计; K-调节阀;V-截止阀;VA-调节阀;VB-安全阀;1-气体钢瓶;2-钢瓶减压阀;3-稳压阀;4-干燥器;5-过滤器;6-质量流量控制器;7,7'-取样器;8-预热炉;9-预热器;10-反应炉;11-固定床反应器;12-汽液分离器;13-冷凝器; 14-尾液收集器;15-转子流量计;16-湿式流量计; 17-加料罐;18-液体泵;PI9104TCI TCITCI6137'141812111217KPIVV57151683TCITI TCI-控温热电偶;TI-测温热电偶;PI-压力计; K-调节阀;V-截止阀;VA-调节阀;VB-安全阀;1-气体钢瓶;2-钢瓶减压阀;3-稳压阀;4-干燥器;5-过滤器;6-质量流量控制器;7,7'-取样器;8-预热炉;9-预热器;10-反应炉;11-固定床反应器;12-汽液分离器;13-冷凝器; 14-尾液收集器;15-转子流量计;16-湿式流量计; 17-加料罐;18-液体泵;PI9104TCI TCITCI6137'14181111217K PI图6-2 乙醇气固催化制备乙烯实验流程图本实验选用固定床反应器,凡是流体通过不动的固体物料所形成的床层而进行反应的装置都称作固定床反应器。
实验三 乙醇脱水

实验三乙醇脱水实验三乙醇气相脱水制乙烯反应动力学(本实验学时:7×1)实验室小型管式炉加热固定床、流化床催化反应装置是有机化工、精细化工、石油化工等部门的主要设备,尤其在反应工程、催化工程及化工工艺专业中使用相当广泛。
本实验是在固定床和流化床反应器中,进行乙醇气相脱水制乙烯,测定反应动力学参数。
固定床反应器内填充有固定不动的固体催化剂,床外面用管式炉加热提供反应所需温度,反应物料以气相形式自上而下通过床层,在催化剂表面进行化学反应。
流化床反应器内装填有可以运动的催化剂层,是一种沸腾床反应器。
反应物料以气相形式自下而上通过催化剂层,当气速达到一定值后进入流化状态。
反应器内设有档板、过滤器、丝网和瓷环(气体分布器)等内部构件,反应器上段有扩大段。
反应器外有管式加热炉,以保证得到良好的流化状态和所需的温度条件。
反应动力学描述了化学反应速度与各种因素如浓度、温度、压力、催化剂等之间的定量关系。
动力学在反应过程开发和反应器设计过程中起着重要的作用。
它也是反应工程学科的重要组成部分。
在实验室中,乙醇脱水是制备纯净乙烯的最简单方法。
常用的催化剂有:浓硫酸液相反应,反应温度约170℃。
三氧化二铝气-固相反应,反应温度约360℃。
分子筛催化剂气-固相反应,反应温度约300℃。
其中,分子筛催化剂的突出优点是乙烯收率高,反应温度较低。
故选用分子筛作为本实验的催化剂。
一、实验目的1、巩固所学有关反应动力学方面的知识。
2、掌握获得反应动力学数据的手段和方法。
3、学会实验数据的处理方法,并能根据动力学方程求出相关的动力学参数值。
4、熟悉固定床和流化床反应器的特点及多功能催化反应装置的结构和使用方法,提高自身实验技能。
二、实验原理乙醇脱水属于平行反应。
既可以进行分子内脱水生成乙烯,又可以进行分子间脱水生成乙醚。
一般而言,较高的温度有利于生成乙烯,而较低的温度有利于生成乙醚。
因此,对于乙醇脱水这样一个复合反应,随着反应条件的变化,脱水过程的机理也会有所不同。
乙醇脱水反应动力学参数测定实验讲义

三、实验装置及流程
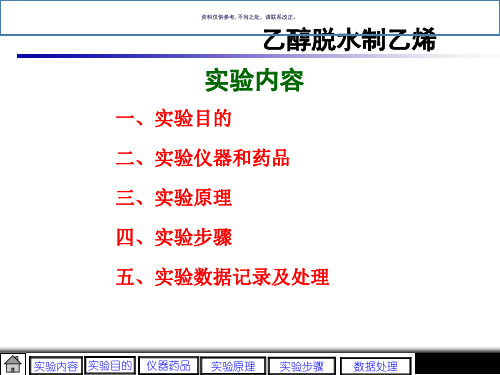
采用磁驱动内循环无梯度反应器,实验流程如图 1,反应器见图 2。
TT—热电偶,PI—压力计,1—钢瓶,2—稳压阀,3—调节阀,4—转子流量计,5—预热器,6— 预热炉,7—反应器,8—反应炉,9—冷凝器,10—尾液收集器,11—六通阀,12—马达 图 1 内循环无梯度乙醇脱水实验装置
2、数据处理
表 2 数据处理表 实 验 号 1 反应 温度 /℃ 245 乙醇进 料量 /(ml/mi n) 2 4 6 2 270 2 4 6 3 312 2 4 6 产物摩尔数组成 乙烯 0.064 0.025 0.056 0.515 0.549 0.504 0.544 0.523 0.454 水 0.321 0.281 0.221 0.195 0.152 0.229 0.309 0.333 0.305 乙醇 0.602 0.667 0.712 0.265 0.258 0.235 0.145 0.144 0.240 乙醚 0.013 0.027 6 0.011 0.025 0.041 0.032 0.003 0 0.006 乙醇转 化率 0.1301 0.1073 0.099 0.6807 0.7098 0.7073 0.7910 0.7841 0.6601 乙烯 收率 0.092 5 0.033 5 0.070 9 0.620 5 0.617 5 0.627 6 0.782 7 0.784 1 0.643 1 V/(mol · min1 -1 g ) 0.0010 0.0008 0.0024 0.0071 0.0141 0.0646 0.0090 0.0179 0.0221 C/(L/m ol) 0.0141 6 0.0156 9 0.0167 5 0.0059 5 0.0057 9 0.0052 7 0.0030 2 0.0030 0 0.0050 0 2.9801 1.1933 K/( L1 · min1 -1 g ) 0.0706 2
乙醇脱水制乙烯

实验内容 实验目的 仪器药品 实验原理 实验步骤
数据处理
资料仅供参考,不当之处,请联系改正。
乙醇脱水制乙烯
(2)进料速率为1.0mL.min-1时的样品色谱分析数据
分析次数 I
II
峰号 项目
1
2
3
1
2
3
保留时间 /min
峰面积 /uv.s
峰面积百 分比/%
实验内容 实验目的 仪器药品 实验原理 实验步骤
❖ A.B.ФPOOT研究了在Al2O3上乙醇脱水的动力学 ,导出了一级反应速度方程式:
v0
ln 1 1y
+v0y
其中:v0—乙醇的加料速度(毫克分子/分) y—乙醇转化率(%)
实验内容 实验目的 仪器药品 实验原理 实验步骤
数据处理
资料仅供参考,不当之处,请联系改正。
乙醇脱水制乙烯
实验步骤
1、打开装置总电源将反应器加热温度设定为280℃ ,预热器温度设定为150℃。
实验日期: 年 月 日 时间: 1、标准溶液的配制及其色谱分析 (1)标准溶液配制数据记录表
室温: ℃
物质
水(H2O) 无水乙醇(C2H5OH) 无水乙醚((CH3)2O)
质量/g
质量百分含 量/%
实验内容 实验目的 仪器药品 实验原理 实验步骤
数据处理
资料仅供参考,不当之处,请联系改正。
乙醇脱水制乙烯
/g
重/g
样品质量/g
实验内容 实验目的 仪器药品 实验原理 实验步骤
数据处理
资料仅供参考,不当之处,请联系改正。
乙醇脱水制乙烯
4、样品色谱分析数据记录表 (1)进料速率为0.5mL.min-1时的样品色谱分析数据
乙醇气相脱水制备乙烯动力学

实验三乙醇气相脱水制乙烯反应动力学(简易无梯度内循环)反应动力学描述了化学反应速度与各种因素如浓度、温度、压力、催化剂等之间的定量关系。
动力学在反应过程开发和反应器设计过程中起着重要的作用。
它也是反映工程学科的重要组成部分。
其中,分子筛催化剂的突出优点是乙烯收率高,反应温度较低。
故选用分子筛作为本实验的催化剂。
一.实验目的1.巩固所学有关反应动力学方面的知识。
2.掌握获得反应动力学数据的手段和方法。
3.熟悉内循环式无剃度反应器的特点及其它有关设备的使用方法,提高实验技能。
二.实验原理乙醇脱水属于平行反应,既可以进行分子内脱水生成乙烯,又可以进行分子间脱水生成乙醚。
一般而言,较高的温度有利于生成乙烯,而较低的温度有利于生成乙醚。
因此,对于乙醇脱水这样一个复合反应,随着反应条件的变化,脱水过程的机理也会有所不同。
借鉴前人在这方面所做的工作,将乙醇在分子筛催化剂作用下的脱水过程描述成:2C2H5OH→C2H5OC2H5+H2OC2H5OH→C2H4+H2O三.装置、流程及试剂1.装置本实验装置由三部分构成。
第一部分是由微量进料泵、氢气钢瓶、汽化器和取样六通阀组成的进料系统。
第二部分是反应系统,它是由一台内循环式无剃度反应器、温度控制器和显示仪表组成。
反应器的结构如图5-1所示。
图5-1无梯度反应器结构图1-直流电机;2-磁钢固定片;3-磁钢;4-上法兰;5-磁钢;6-磁钢固定片;7-轴承;8-密封垫片;9-冷却水夹套;10-反应器上部;11-轴承;12-密封垫片;13-密封垫片;14-反应器下部;15-旋转轴:16-反应器外壁;17-旋转叶片;18-催化剂及固定框;19-加热电炉;20-热电偶套管;21-进气口;22-出气口第三部分是取样和分析系统。
包括取样六通阀、产品收集器和在线气相色谱仪。
整套实验装置安装在一个实验柜中,操作方便。
2.流程实验流程见图5-2图5-2实验流程简图1-微量进料泵;2-氢气钢瓶;3-记录仪;4-气相色谱仪;5-汽化器;6-六通阀;7-冷凝器;8-温度控制仪;9-反应器;10-电机调速器;11-数字化温度显示器;12-恒温阀箱;13-色谱处理器3.试剂和催化剂:无水乙醇,优级纯;分子筛催化剂,60~80目,重3.0克。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化工专业实验报告
实验名称:乙醇气相脱水制乙烯动力学实验学院:化学工程学院
专业:化学工程与工艺
班级:化工、班
姓名:、学号、
同组者姓名:
指导教师:杨春风
日期:2012年3月8日
一、实验目的
1.巩固所学的有关动力学方面的知识。
2.掌握获得反应动力学数据的方法和手段。
3.学会动力学数据的处理方法,根据动力学方程求出相应的参数值。
4.熟悉内循环式无梯度反应器的特点以及其它有关设备的使用方法,提高自己的实验技能。
二、实验原理
乙醇属于平行反应。
既可以进行分子内脱水生成乙烯,又可以进行分子间脱水生成乙醚。
一般而言,较高的温度有利于生成乙烯,而较低的温度有利于生成乙醚。
因此,对于乙醇脱水这样一个复合反应,随着反应条件的变化,脱水过程的机理也会有所不同。
借鉴前人在这方面做的工作,将乙醇在分子筛催化剂作用下的脱水过程描述成:
2C
2H
5
OH→C
2
H
5
OC
2
H
5
+H
2
O
C 2H
5
OH→C
2
H
4
+H
2
O
三、实验装置及流程
实验装置:无梯度反应器
试剂和催化剂:无水乙醇,优级纯;分子筛催化剂,重3.0克。
内循环无梯度反应色谱实验装置流程示意图
四、实验步骤
开始实验之前,需熟悉流程中所有设备、仪器、仪表的性能及使用方法。
然后才可按实验步骤进行实验。
1.打开H2钢瓶使柱前压达到0.5kg/cm2确认色谱检测中截气通过后启动色谱,柱温110℃,气化室130℃,检测室温达到120℃,待温度稳定后,打开热导池—微电流放大器开关,桥电流至100mA。
2.在色谱仪升温的同时,开启阀恒温箱加热器升温至110℃,开启保温加热器升温至150℃。
3.打开反应器温度控制器开关,升温,同时向反应器冷却水夹套通冷却水。
4.打开微量泵,以小流量向气化器内通原料乙醇。
5.用阀箱内旋转六通阀取样分析尾气组成,记录色谱处理的浓度值。
6.在260-360℃之间选两个温度,改变三次进料速度,测定各种条件下的数据。
五、原始实验数据(附页)
六、实验数据记录及处理
乙醇密度:0.79g/ml 进料速度:0.3ml/min 乙醇进料质量:3.0g
计算说明:
乙醇的转化率=反应掉的乙醇摩尔数/原料中乙醇的摩尔数
乙烯的收率=生成乙烯的摩尔数/原料中乙醇的摩尔数
乙醇的进料速度=乙醇液的体积流量×0.79(乙醇的密度)/46(乙醇的分子量)乙烯的生成速度=(乙醇进料速度×乙烯的收率)/[催化剂用量(g)] mol/(g·h)反应器内乙醇的浓度:C A=P A/(R·T)
式中P A为乙醇的分压;反应的总压为0.1Mpa。
所以可将反应器内的混合气视为理想气体。
生成乙烯的反应步骤的速率常数k可以通过下式求出:
k =r/C A
由阿仑尼乌斯方程k=k0exp(-E/RT),将lnk对1/T作图,即可求出k0和E。
由第一组数据:
ρ(乙醇)=0.79g/ml t=5min m总(乙醇)=0.79×0.3×5=1.185g
n总(乙醇)=1.185/46=0.0258mol m(乙烯)=1.185-1.18=0.005g
n(乙烯)=0.005/28=1.786×10-4mol
由第一组数据:乙醇的转化率=0.00015/0.0258=5.814×10-3
乙烯的收率=1.786×10-4/0.0258=6.922×10-3
乙醇的进料速度=0.3×0.79/46=5.15×10-3mol/min=0.309 mol/h
乙烯的生成速率=(0.309×6.922×10-3)=2.139×10-3 mol/(g·h)
反应器内乙醇的浓度:C A=P A/(R·T)
0.1:P A =0.0258:0.02565 P A=0.0994MPa
C A=P A/(R·T)=0.0994×106/(8.3145*462.35)=25.86mol/m3=0.02586mol/L
生成乙烯的反应步骤的速率常数k可以通过下式求出:
K =r/C A=2.139×10-3 /0.02586=0.0827L/(g·h)
同理可得如下:
由阿仑尼乌斯方程k=k0exp(-E/RT),将lnK对1/T作图,即可求出k0和E。
以lnK为纵坐标,1/T为横坐标作图如下:
Y A x i s T i t l e
X Axis Title
由k=k 0exp(-E/RT)得,
lnk=lnk 0-E/(R·T),由图中可知:-E/R=-7.912,lnk 0=15.378 解得:E=65.784kJ/mol ,k 0=4.771×106 L/(g·h)
七、实验结论
根据实验过程记录的数据,计算分析后得到的lnk 对1/T 的图可以看出,基本成线性关系。
在实验误差允许的范围内,实验得到的数据准确。
通过实验我们了解到用无梯度反应器测定化学反应动力学的优点是反应器进口浓度物料循环,使累计的转化率较高,但起缺点是进料浓度和出口浓度有较大的差值,因此对组成分析没有过苛要求和出口浓度十分接近,反应器内不存在浓度梯度和温度梯度。
八、思考题
1. 用无梯度反应器测定化学反应动力学的优、缺点是什么?
答:反应器进口浓度物料循环,使累计的转化率较高,进料浓度和出口浓度有较大的差值,因此对组成分析没有过苛要求和出口浓度十分接近,反应器内不存在浓度梯度和温度梯度。
2. 要证明测定的本证动力学数据,还需要补充哪些实验内容?
答:还需要补充热量传递,质量传递,动量传递等内容,加上前面的反应,即三传一反是化学动力学的本证特性。
