大鼠灌胃给药标准操作规程
腹腔注射灌胃实验报告

1. 掌握腹腔注射和灌胃的操作方法;2. 了解腹腔注射和灌胃的优缺点;3. 掌握实验动物的基本操作技术。
二、实验材料1. 实验动物:大鼠(体重约200-300g);2. 实验药品:生理盐水、葡萄糖、抗生素等;3. 实验器材:注射器、针头、酒精棉球、镊子、剪刀、解剖盘、剪刀、纱布等;4. 实验环境:实验室。
三、实验方法1. 腹腔注射实验(1)准备工作:将实验动物固定在解剖盘上,用酒精棉球消毒实验动物腹部皮肤。
(2)注射操作:左手抓取大鼠腹部皮肤,右手持注射器,针头斜向上,沿腹中线方向进针,进入腹腔后回抽无血液,缓慢注入药物。
(3)注射完毕,用纱布覆盖注射部位,观察动物反应。
2. 灌胃实验(1)准备工作:将实验动物固定在解剖盘上,用酒精棉球消毒实验动物口腔及咽部皮肤。
(2)灌胃操作:左手抓住大鼠头部,右手持注射器,针头沿一侧口角进针,紧贴咽后壁,头后仰以便伸直消化道,缓慢注入药物。
(3)注射完毕,用纱布覆盖注射部位,观察动物反应。
四、实验结果1. 腹腔注射实验:注射过程中,大鼠无不良反应,注射完毕后,动物精神状态良好。
2. 灌胃实验:注射过程中,大鼠无明显不适,注射完毕后,动物精神状态良好。
1. 腹腔注射和灌胃是两种常见的实验动物给药方式,各有优缺点。
2. 腹腔注射的优点是操作简便,药物吸收迅速,但可能引起动物应激反应,且部分药物不适宜腹腔注射。
3. 灌胃的优点是给药量准确,适用于多种药物,但操作过程中可能损伤动物,且药物吸收速度较慢。
4. 在实验过程中,应严格遵守操作规程,确保动物安全。
六、实验结论1. 通过本次实验,掌握了腹腔注射和灌胃的操作方法。
2. 了解腹腔注射和灌胃的优缺点,为今后的实验研究提供参考。
3. 提高了实验动物的基本操作技能,为科研工作奠定基础。
大鼠小鼠给药标准操作规程

目的规范实验人员进行大、小鼠给药的操作程序。
适用范围适用于对大、小鼠的给药操作。
职责.1 管理人员负责监督、管理;.2 实验动物中心技术员负责指导、教学;.3 实验人员选择合适的给药方法,并严格遵守本规程。
规程.1 大小鼠常用的给药方法有:灌胃给药、皮内注射、皮下注射、腹腔注射、尾静脉注射、肌肉注射。
.2 灌胃给药操作规程(如图).2.1 灌胃针、注射器规格的选择.2.1.1 小鼠:灌胃针针长 5-7cm,直径 0.9-1.5mm,1mL 注射器.2.1.2 大鼠:灌胃针针长 6-8cm,直径 1-2mm,2.5-5mL 注射器.2.2 将灌胃针与注射器连接好并吸入一定量药液放置一旁备用;.2.3 左手保定实验动物,使之身体呈垂直或略向后仰,颈部拉直。
.2.4 右手持灌胃器,沿体壁用灌胃针测量口角至最后肋骨之间的长度,作为插入灌胃针的深度。
然后经口角插入口腔,与食管呈一直线,轻轻转动针头,刺激动物的吞咽,再将灌胃针沿上颚壁缓慢插入食管,小鼠插入深度约为2-3cm,大鼠插入深度约为 3-4cm,通过食管的膈肌部位时略有抵抗感。
.2.5 如动物正常呼吸且无异常挣扎行为,即可注入受试物。
如遇阻力应抽出灌胃针重新插入。
.2.6 剂量:小鼠约为 0.1-0.3ml/10g 体重,大鼠约为 1-2ml/100g 体重。
.2.7 注意事项:灌胃时需要先了解食道和气管的结构避免误插进入气管4.3 皮内注射操作规程(如图).3.1 注射部位:选实验动物颈背部皮肤或小鼠腋下约 1cm 处皮肤;.3.2 提前剪毛,常规消毒注射部位的皮肤,注射针头与皮肤呈 15-30°角刺入皮肤浅层,向上挑起并稍刺入,将药液注入皮内。
.3.3 注射后皮肤隆起一白色小皮丘,皮肤上毛孔变大。
.3.4 剂量:小鼠不超过 0.05ml/次,大鼠不超过 0.1ml/次。
.4 皮下注射操作规程(如图).4.1 注射部位:选实验动物颈背部皮下;.4.2 常规消毒注射部位的皮肤,用注射针头取一锐角角度刺入皮下;.4.3 将针头轻轻左右摆动,易摆动表示已刺入皮下,再轻轻抽吸,如无回血,可缓慢地将药物注入皮下。
小鼠大鼠灌胃实验报告

一、实验目的本实验旨在通过灌胃法对小鼠和大鼠进行药物给药,以观察药物在小鼠和大鼠体内的吸收、分布和代谢情况,并探讨不同给药途径对药物效果的影响。
二、实验材料1. 实验动物:昆明小鼠10只(体重20-25g),雄性大鼠5只(体重200-250g)。
2. 实验药物:某药物溶液(浓度1mg/ml)。
3. 实验仪器:电子天平、灌胃器、注射器、计时器、解剖显微镜、组织切片机等。
4. 实验试剂:生理盐水、盐酸、乙醇等。
三、实验方法1. 实验动物分组:将小鼠和大鼠随机分为实验组和对照组,每组5只。
2. 给药方法:实验组采用灌胃法给药,对照组采用生理盐水灌胃作为对照。
- 小鼠灌胃:左手抓取小鼠,使其头部略低,右手持灌胃器,将灌胃针头从口角插入,沿咽后壁缓慢推进至食道,注入药物溶液。
- 大鼠灌胃:左手抓取大鼠,使其头部略低,右手持灌胃器,将灌胃针头从口角插入,沿咽后壁缓慢推进至食道,注入药物溶液。
3. 观察指标:- 观察实验组和对照组小鼠和大鼠的精神状态、活动能力、进食情况等。
- 在给药后1小时、2小时、4小时、6小时、8小时分别采集实验组和对照组小鼠和大鼠的血液,检测药物浓度。
- 在给药后24小时处死实验组和对照组小鼠和大鼠,解剖观察其器官组织变化。
四、实验结果1. 实验组小鼠和大鼠在给药后,精神状态、活动能力、进食情况与对照组无明显差异。
2. 在给药后1小时、2小时、4小时、6小时、8小时,实验组小鼠和大鼠的血液药物浓度逐渐升高,至4小时时达到峰值,随后逐渐降低。
3. 在给药后24小时处死实验组和对照组小鼠和大鼠,解剖观察发现,实验组小鼠和大鼠的器官组织无明显病变。
五、实验讨论1. 灌胃法是一种常用的给药途径,适用于小鼠和大鼠等实验动物。
2. 本实验结果表明,灌胃法能够有效地将药物输送至小鼠和大鼠体内,使药物在体内达到有效浓度。
3. 在进行灌胃实验时,应注意事项:- 严格掌握灌胃技巧,避免损伤动物食道。
- 控制灌胃剂量,避免药物过量。
大鼠灌胃实验报告

一、实验目的本实验旨在探究灌胃方法在动物实验中的应用效果,通过对大鼠进行灌胃实验,观察灌胃给药对大鼠生理指标、血液指标和病理组织学的影响,评估灌胃方法的可靠性和安全性。
二、实验材料1. 实验动物:SPF级SD大鼠,体重180-220g,雌雄各半。
2. 实验药物:已知药物,剂量为10mg/kg。
3. 试剂与仪器:灌胃针、注射器、电子天平、血液分析仪、病理切片机、显微镜等。
三、实验方法1. 将SD大鼠随机分为实验组和对照组,每组10只。
2. 实验组大鼠通过灌胃途径给予已知药物,剂量为10mg/kg,对照组大鼠给予等体积的生理盐水。
3. 灌胃操作:将大鼠固定在实验台上,用灌胃针将药物缓慢注入大鼠口腔,直至药物完全进入消化道。
4. 给药后,观察大鼠的生理指标、血液指标和病理组织学变化。
5. 实验结束后,对大鼠进行解剖,采集相关组织样本,进行病理切片和显微镜观察。
四、实验结果1. 生理指标:实验组大鼠在给药后出现轻微的呕吐、腹泻等症状,但症状持续时间为1-2天,未出现死亡现象。
对照组大鼠生理指标无明显变化。
2. 血液指标:实验组大鼠给药后血液白细胞计数、红细胞计数、血红蛋白浓度等指标无明显变化,与对照组相比无统计学差异。
3. 病理组织学观察:实验组大鼠胃黏膜、小肠黏膜、肝脏、肾脏等器官组织无明显病变,与对照组相比无统计学差异。
五、讨论与分析1. 灌胃方法是一种常用的动物实验给药途径,具有操作简便、给药剂量准确、对动物生理影响较小的特点。
2. 本实验结果显示,灌胃给药对大鼠生理指标、血液指标和病理组织学影响较小,说明灌胃方法在本实验中具有较高的可靠性和安全性。
3. 然而,灌胃方法也存在一定的局限性,如给药剂量难以精确控制、药物吸收速度较慢等。
在实际应用中,应根据实验目的和动物种类选择合适的给药途径。
六、结论本实验结果表明,灌胃方法在大鼠实验中具有较高的可靠性和安全性,可用于动物实验的给药途径。
在后续实验中,可根据具体实验目的和动物种类,选择合适的灌胃方法,以获得准确的实验结果。
介绍一种简便的大鼠灌胃方法_符路娣

表2两组治愈病例主要临床症状起效时间比较组别犬数发热腹痛里急后重脓血便腹部压痛治疗组230.85?0.32*1.10?0.41*1.08?0.36*1.13?0.451.51?0.47*对照组141.31?0.271.70?0.731.76?0.721.17?0.572.05?0.72注:与对照组比较*p<0.01表3两组治愈病例主要临床症状消失时间比较组别犬数发热腹痛里急后重脓血便腹部压痛治疗组231.97?0.75*3.10?1.02*2.79?1.05*2.87?1.113.16?1.17*对照组142.69?1.193.89?1.333.93?1.193.92?1.094.41?1.35注:与对照组比较*p<0.014小结犬的急性菌痢临床施治中,随着致病菌群的不断变化,耐药菌株的增长,给治疗带来一定的困难。
特别是基层兽医站无实验室,条件差,全凭目观和经验,无法对大便进行细菌培养,给用药带来了一定困难。
盲目滥用抗生素,而导致菌群失调,迁延不愈,给广大养殖户增加了支出,浪费了财力、物力、人力,造成不应有的损失。
而用中药治疗常可取得良好的疗效。
自拟葛根芩连汤中,主药葛根味甘平有解肌清热、升清止痢功用;黄芩、黄连则味苦、性寒、清热燥湿,抗菌消炎,除里急后重症;木香理气开胃、行止泻;马齿苋清热解毒止痢;茯苓、泽泻,渗湿利水、健脾和中;金银花清热解毒;甘草清热解毒、补中、调和诸药。
诸药相合,共奏清热解毒,燥湿坚阴止痢之功。
现代药理研究认为:葛根、黄芩、黄连、马齿苋对痢疾杆菌有较强的抑制作用,同时,葛根芩连汤有提高机体免疫力,增强小肠黏膜绒毛上皮细胞功能的作用。
文章编号:1003-8655(2006)03-0036-01中草药治疗宠物犬腹胀病赵沛林(山东省无棣县畜牧局2519007)中图分类号:S858.292文献标识码:B宠物犬的腹胀病,是由饲养管理不善或饲料品质低劣、变质等引起的一种原发或继发性疾病,临床比较多见。
动物实验操作
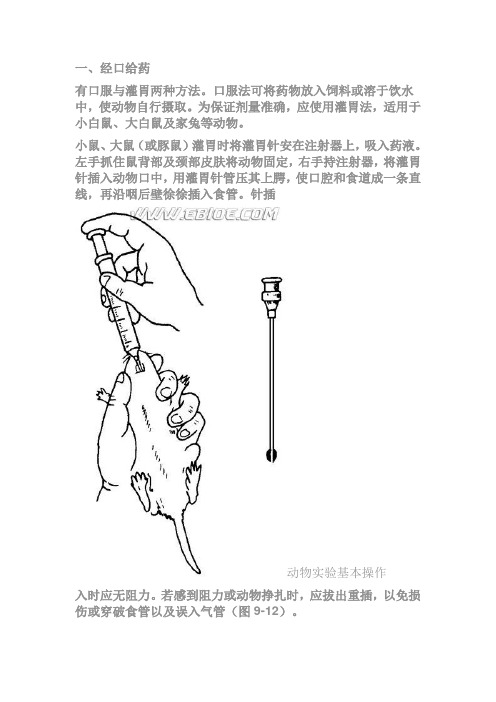
一、经口给药有口服与灌胃两种方法。
口服法可将药物放入饲料或溶于饮水中,使动物自行摄取。
为保证剂量准确,应使用灌胃法,适用于小白鼠、大白鼠及家兔等动物。
小鼠、大鼠(或豚鼠)灌胃时将灌胃针安在注射器上,吸入药液。
左手抓住鼠背部及颈部皮肤将动物固定,右手持注射器,将灌胃针插入动物口中,用灌胃针管压其上腭,使口腔和食道成一条直线,再沿咽后壁徐徐插入食管。
针插动物实验基本操作入时应无阻力。
若感到阻力或动物挣扎时,应拔出重插,以免损伤或穿破食管以及误入气管(图9-12)。
一般当灌胃针插入小鼠3~4cm,大鼠或豚鼠4~6cm后可将药物注入。
常用的灌胃量小鼠为0.2~1ml,大鼠1~4ml,豚鼠为1~5ml。
二、腹腔注射常用于大鼠或小鼠给药。
用左手捕捉固定动物,使腹部向上,鼠头略低于尾部,右手将注射针头自下腹部靠近腹白线的两侧刺入皮下,使针头向前推0.5~1.0cm,再以45°角穿过腹肌,缓缓注入药液。
为避免伤及内脏,可使动物处于头低位,使内脏移向上腹(图9-15)。
若实验动物为家兔,进针部位为下腹部的腹白线离开1cm处。
三、毛细管法小鼠内眦取血(眼眶静脉丛采血)左手拇指及食指紧紧握住小鼠颈部,压迫颈部两侧使眶后静脉丛充血,但用力要恰当,防止动物窒息死亡。
右手持玻璃毛细管从右眼或左眼以45度角插入结膜,再轻轻向眼底部方向刺入,刺入深度为2-3mm,轻轻旋转毛细管以划破静脉丛,让血液顺毛细管流出,接收入事先准备的容器中。
若遇阻力稍后调整角度后再刺入,如穿刺恰当,血液能自然流入毛细管内。
得到血后,即除去颈部压力,拔出毛细管,用干棉球或纱布轻压眼球止血。
数分钟后可在同一穿刺孔重复取血。
小鼠一次可采得血0.2-0.3ml。
注:实验前先将毛细管浸泡过肝素后烘干使用即可。
大、小鼠的抓取保定及灌胃操作规程
大、小鼠的抓取保定及灌胃操作规程
一、大小鼠的抓取保定
(1)先用右手抓取鼠尾提起。
(2)置于鼠笼或实验台向后拉。
(3)在鼠向前爬行时,用左手拇指和食指抓住大、小鼠的两耳和颈部皮肤。
(4)将鼠体置于左手心中,把后肢拉直。
(5)以无名指按住鼠尾,小指按住后腿即可;如果大鼠体积太大,可由第二个人协助固定后肢。
二、大小鼠的灌胃
(1)将针尖圆滑的灌胃针接在注射器上,吸入药液。
(2)一只手抓住鼠背部及颈部皮肤将动物抓取固定;体位为头高尾低(头高位)。
(3)另一只手持注射器,将灌胃针从动物嘴部侧面插入动物口中。
(4)然后轻轻摆正灌胃针并沿口腔顶壁和咽后壁徐徐插入食道,针插入时应无阻力;若感到阻力或动物挣扎时,应立即停止进针或将针拔出,以免损伤或穿破食道以及误入气管。
(5)一般当灌胃针插入小鼠3~4 cm,大鼠或豚鼠4~6 cm后轻轻回抽一下,见有胃液可将药物注入。
(6)用输血针头或小号腰穿针头,将其尖端斜面磨平,用焊锡在针尖周围焊一圆头,即成灌胃针,或购买现成的灌胃针。
常用的灌胃量小鼠为0.2~1 mL,大鼠1~4 mL,豚鼠为1~5 mL。
综述:大鼠灌胃给药方法——修改版
综述:实验大鼠灌胃给药方法简介徐意摘要:本文主要介绍了几种大鼠经口灌胃给药的方法。
并介绍各年龄段等方面大鼠(删)在灌胃中注意事项。
关键词:大鼠;灌胃;给药。
随着科学(医学)技术的发展,动物实验已成为医学实验研究的基本方法。
根据实验目的、实验动物的种类及药物剂量的不同,需对实验动物实施不同的给药方法。
经口灌胃给药方法是一种重要的给药途径。
[1]灌胃给药能够准确掌握给药剂量、控制给药时间,在营养学和药物学动物实验中有重要意义。
在此,作者根据操作经验,对各实验动物灌胃方法加以改良,并用于实验操作中,关于大鼠的灌胃方法介绍如下。
1 大鼠解剖生理特点: [2]SD大鼠与Wistar大鼠的解剖生理特点相似:①腔粘膜幼嫩,易受损伤引起出血。
②咽喉部神经反射较差,自我保护能力差。
药液溢出时极易呛入肺内而致死。
③管长,自口角至责门为5.5士0.5cm。
④解剖位置低,常达腹中部甚至腹下部。
胃的外形似蚕豆状,胃底部和幽门部均高于责门部。
责门括约肌紧张度较低,灌胃时药液易外溢。
⑤胃内容积为0.6士0.2ml,但胃内常常是积满汁液,压力较大,也是药液易于外溢的原因。
2 特制灌胃管的制作(与题无关)2.1软质灌胃器的制作选取临床用小儿头皮针(带针座)塑管一段。
放置60°C左右热水中浸泡2~3min,取出后迅速将其拉长,使该塑管变细,直径约为1mm。
剪取带针座的一段长约6cm,再将游离端磨光滑即成。
最后连干注射器上备用。
2.2硬质灌胃器的制作取12号普通注射针头,首先用粗锉刀把针头锉掉,然后用细锉刀把锉掉部位锉平、锉光、再用沙纸磨平。
加工成有一定弧度,针体长约5 cm并连接1 ml注射器,即成大鼠灌胃器。
灌胃时在针头处套上长2 cm 硅胶管,比针头稍微长0.1 cm,太长容易被动物咬掉。
以防灌胃时损伤动物食道。
另外在锉针头时或加工弧度时用力要均匀,否则就会把针管弄扁,以影响通畅。
3 大鼠(固定)保定操作[1~3] (文献要标注到具体的位置)3.1清醒大鼠的保定大鼠在未受到强烈刺激情况下性情虽较温顺,但捕捉时也要提防被其咬伤或抓伤手指,因此需要戴手套捕捉。
实验动物的给药途径和方法及药量计算方法
实验动物的给药途径和方法及药量计算方法一、经口给药法(一)灌胃法此法给药剂量准确,是借灌胃器将药物直接灌到动物胃内的一种常用给药法。
1、鼠类:鼠类的灌胃器由特殊的灌胃针构成。
左手固定鼠,右手持灌胃器,将灌胃针从鼠的右U角中,插入口中,沿咽后壁慢慢插入食道,使其前端到达膈肌位置,灌胃針插入时应无阻力,如有阻力或动物挣扎则应退针或将针拔出,以免损伤、穿破食道或误入气管。
2、兔、犬等:灌胃一般要借助于开口器、灌胃管进行。
先将动物固定,再将开口器固定于上下门齿之间。
然后将灌胃管(常用导尿管代替)从开口器的小孔插入动物口中,沿咽后壁而进入食道。
插入后应检查灌胃管是否确实插入食道。
可将灌胃管外开口放入盛水的烧杯中,若无气泡产生,表明灌胃管被正确插入胃中,未误入气管。
此时将注射器与灌胃管相连,注入药液。
(二)口服法口服给药是把药物混入饲料或溶干饮水中让动物自由摄取。
此法优点是简单方便,缺点是剂量不能保证准确,且动物个体间服药量差异较大。
大动物在给予片剂、丸剂、胶囊剂时,可将药物用镊子或手指送到舌根部,迅速关闭口腔,将头部稍稍抬高,使其自然吞咽。
二、注射给药法(一)皮下注射皮卜注射一般选取皮下组织疏松的部位,大鼠、小鼠和豚鼠可在颈后肩胛问、腹部两侧作皮下注射;家兔可在背部或耳根部作皮卜注射;猫、犬则在大腿外侧作皮下注射。
皮下注射用左手拇指和食指轻轻提起动物皮肤,右手持注射器,使针头水平刺入皮下。
推送药液时注射部位隆起。
拨针时,以手指捏住针刺部位,可防止药液外漏。
(二)肌肉注射肌肉注射一般选肌肉发达,无大血管通过的部位。
大鼠、小鼠、豚鼠可注射大腿外侧肌肉;家兔可在腰椎旁的肌肉、臀部或股部肌肉注射;犬等大型动物选臀部注射。
注射时针头宜斜刺迅速人肌肉,回抽针栓如无回血,即可注射。
(三)腹腔注射给大鼠、小鼠进行腹腔注射时,以左手固定动物,使腹部向上,为避免伤及内脏,应尽量使动物头处于低位,使内脏移向上腹,右手持注射器从下腹两侧向头方刺入皮下,针头稍向前,再将注射器沿45角斜向穿过腹肌进入腹腔,此时有落空感,回抽无回血或尿液,即可注入药液。
大小鼠给药基本操作-精品文档
腹腔注射给药
左手抓取并固定好动物,使腹部朝上,头
略低于鼠尾。75%酒精消毒腹部,右手持注射 器将针头在下腹腹白线稍偏左/右位置从下腹
朝头方向平行刺入皮下,进针3-5mm,再使针
头与皮肤呈45°角穿过腹肌,到达腹腔时有落 空感。然后固定针头,回抽无血液、肠液、尿
皮内注射给药
局部去除被毛,消毒后,用皮试针头紧贴皮肤皮层刺入 皮内,然后再向上挑起再稍刺入,即可注射药物。注射时会 感到有很大的阻力。注射后可见皮肤表面鼓起以白色小丘。
注射完毕停留5min在拔出针头,一免药液漏出。
注射量:
小鼠:≤0.05mL
大鼠:≤ 0.1mL
液后,便可缓缓推入药液。
注射量: 小鼠:0.1-0.2mL/10g体重; 大鼠:1.0-2.0mL/100g体重。
肌肉注射给药
肌肉注射相对皮下和腹腔注射用得较少。
当注射不溶于水而混悬于油或其它溶剂中的药
物时,常采用肌肉注射。动物肌肉注射应选择 肌肉发达,无大血管经过的部位。注射前应用 75%酒精消毒注射部位。 注射量: 小鼠:0.1mL/10g体重;
实验大、小鼠给药基本操作
小胖纸 2019年5月16日
xy-room.taobao
实验大、小鼠灌胃给药
实验大、小鼠注射给药
实验大、小鼠灌胃给药
一般可以从市场上面买到,实 在没有的话,可以用12号的针头,
剪去针尖,用砂纸将头端磨平,也
可以用。但是买的灌胃针头的头端 用锡或者适宜的方法处理了针头的
锐口,自己用砂纸不可能将所有的
大鼠:0.5mL/100g体重。
皮下注射给药
消毒注射部位(背部或前肢
腋下),注射时,左手拇指和食 指轻捏动物皮肤形成皱褶,右手
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
北京伽拓医药研究有限公司
JAT BioDiscovery Co., Ltd.
大鼠灌胃给药的标准操作规程
编号:SOP.QA.001.00
起草:熊伟日期:
修订:日期:
审核:日期:
批准:日期:
生效日期:拷贝号:
分发部门:部门待最终确定后补齐,昭衍和康龙化成的sop用后销毁,协和建昊的SOP交到我处!
大鼠灌胃给药的标准操作规程
1.目的
规范大鼠灌胃给药的具体操作,良好使用实验动物,保持实验质量的稳定性,合理控制因操作引起的实验误差,以确保实验的可靠性和准确性。
2.范围
适用于本机构实验大鼠灌胃给药的操作人员。
3.内容
3.1准备工作
3.1.1核对实验方案,按照实验计划规定时间准时进行灌胃给药。
3.1.2从供试品管理部领取受试物,核对专题名称和剂量。
3.1.3若操作在SPF级动物房进行,按照动物房的更衣SOP进行更衣,按人流路径行走,进入操作动物房。
3.2操作程序
3.2.1从笼内将大鼠取出,放在饲养盒的盒盖(或表面粗糙的物体)上,根据体表标记或者RFID识别动物编号。
3.2.2操作者用合适规格的灌胃注射器抽取所需受试物的剂量,排空注射器内的空气,放在操作台上或者交给辅助人员。
3.2.3操作者用一只手的拇指和中指从背侧伸入大鼠腋下,固定大鼠的手翻转,将大鼠头朝上,腹面对着操作者,同时食指抵住顶骨,确保食道平直。
3.2.4另一只手拿起准备好的灌胃注射器,大致定好灌胃针头应插到胃内后的位置。
3.2.5将灌胃针头由大鼠左侧口角,顺着上颚后壁插入咽部,轻轻移动灌胃针头前端,沿着平行于动物的纵轴,进入食道,没有抵触感,把灌胃针头插入胃部。
3.2.6若感到阻力或者动物挣扎时,应立即停止进针或将针拔出,稍作安抚后重新进行灌胃操作,以免损伤或穿破大鼠食道以及误入气管。
3.2.7将灌胃针头插入胃内后,稳定推动针芯,慢慢注入受试物。
3.3给药后程序
3.3.1在完成每只大鼠灌胃操作后,应立即填写“给药记录表”上相应内容,在完成该批大鼠灌胃操作后,必须立即在“给药记录表”上签名和注明日期,并作好核
查。
3.3.2仔细观察每只动物情况,检查是否有迟发的异常情况。
3.3.3核对各类标签指标、用药量以及记录,防止发生漏给药和错给药的情况。
3.3.4将剩余受试物及盛装受试物的容器交还供试品管理部。
3.3.5由项目负责人将“给药记录表”放入课题档案。
3.4注意事项
3.4.1开始给药之前,必须核对实验方案,确定不同剂量组的动物编号。
3.4.2除实验方案中另有规定外,各组的给药顺序应先雄后雌,先低剂量后高剂量,按照下列分组顺序给药:雄性对照,雌性对照,雄性低剂量,雌性低剂量,雄性中剂量,雌性中剂量,雄性高剂量,雌性高剂量等。
3.4.3 应根据灌胃大鼠的大小和操作人的习惯选择直杆或弯头的灌胃针头;使用前应仔细检查灌胃针头处有无缺痕或锋利之感。
一般应选择头部较圆且光滑的针头使用。
3.4.4每只大鼠在给药后,放回原来的笼具时应特别注意核对编号、性别等,盖好笼盖,观察大鼠是否出现与给药前明显不同状态。
3.4.5在进行不同剂量组给药时,必须用生理盐水清洗灌胃针头及注射器或更换注射器。
3.4.6受试物的标签、给药动物笼具标签、实验方案、时间设计和剂量水平都必须一一加以核对。
3.4.7根据GLP的实验要求对实验操作进行核查。
4.编制依据
[1]药物非临床研究质量管理规范
[2] 药物非临床研究质量管理规范认证标准
[3] 药物毒理学实验方法与技术
5.变更记载
版本号批准日期生效日期变更原因及目的。
