《选修四》电化学基础
人教高中化学选修4课件:第4章 电化学基础

练习:把a、b、c、d四块金属浸入稀硫酸中,用
导线两两相连组成原电池。若
a、b相连时,a为负极;
a >b
c、d相连时,电流由d到c;
c>d
a、c相连时,c极产生大量气泡,
a>c
b、d相连时,溶液中的阳离子向b极移动。
d>b
则四种金属的活泼性顺序为: a>c > d > b 。
原电池原理应用:
(2)比较反应速率 当形成原电池之后,反应速率加快,如实验室制H2时, 纯Zn反应不如粗Zn跟酸作用的速率快。
负极
e-
正极
A
Zn-
Cu
Zn2+
负极
H+ H+ SO42-
阳离子
阴离子
正极
组成原电池的条件
1.内部条件:能自发进行氧化还原反应 2.外部条件:
(1)有两种活泼性不同的金属(或一种是 非金属单质或金属氧化物)作电极。 (2)电极材料均插入电解质溶液中。 (3)两极相连形成闭合电路。
两极一液成回路,氧化还原是中心
负极(Zn):Zn-2e-=Zn2+(氧化反应) 正极(Pt或C):2Fe3++2e-=2Fe2+(还原反应)
ZnCl2溶液
FeCl3溶液
负极(Zn):Zn-2e-=Zn2+(氧化反应) 正极(Pt或C):2Fe3++2e-=2Fe2+(还原反应)
2.依据氧化还原反应: 2Ag+(aq)+Cu(s)==Cu2+(aq)+2Ag(s)设计的原 电池如图所示。
盐桥制法:1)将热的琼胶溶液倒入U形管中(注意不要产生裂隙),
将冷却后的U形管浸泡在KCl或NH4NO3的饱和溶液中即可。2)将 KCl或NH4NO3的饱和溶液装入U形管,用棉花都住管口即可。
人教版高中化学选修4第4章电化学基础ppt课件

成才之路 ·高中新课程 ·学习指导 ·人教版 ·化学 ·选修④
最新学习可编辑资料 Latest learning materials
感谢大家观看
最新资料可自行编辑修改,供参考,感谢大家的支持。谢谢 The latest information can be edited and modified for
第四章 电化学基础
有关电化学的知识是无机化学中很重要的知识,它既涉及 到理论知识,又与元素化合物知识密切相关。
燃料电池公共汽车
化学能与其它形式的能量可以相互转换,而且严格遵守能 量守恒定律。化学能和电能通过一定的装置也可以相互转换, 从能量转换角度看,电化学反应过程(包括装置)可分两类:一 是化学能转换为电能,二是电能转换为化学能。通过化学能和 电能之间的相互转换,能够使我们对氧化还原反应的认识及化 学反应中能量变化的认识更加深刻。
reference. Thank you for your support. thank you
第四章 电化学基础
(完整word版)高中化学原电池知识点总结
(完满word 版)高中化学原电池知识点总结 1 / 1
选修四 第四章 电化学基础
第一节 原电池
1.定义:把化学能转变成电能的装置
2.实质:一个能自觉进行的氧化还原反应。
3.构成条件:
( 1)两个活性不同样的金属(其中一种可以为非金属,即作导体用)作电极。
( 2)两电极插入电解质溶液中。
( 3)形成闭合回路。
(两电极外线用导线连接,可以接用电器。
)
( 4)自觉地发生氧化还原反应
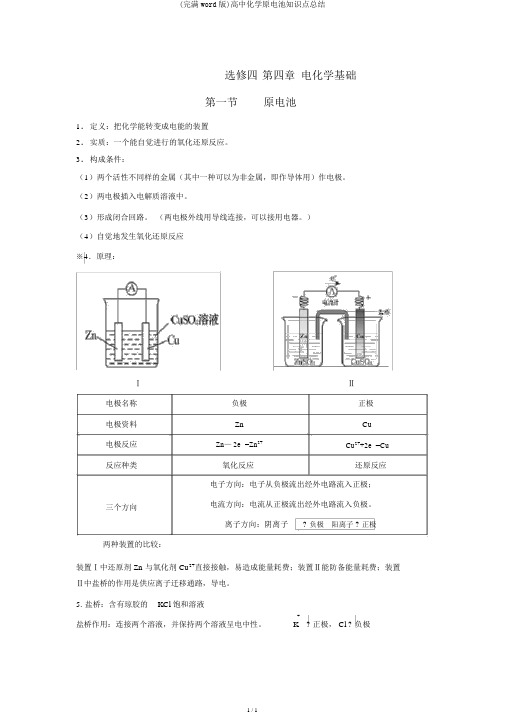
※ 4.原理:
Ⅰ
Ⅱ 电极名称
负极 正极 电极资料
Zn Cu 电极反应
Zn — 2e - =Zn 2+ Cu 2++2e - =Cu 反应种类
氧化反应 还原反应 电子方向:电子从负极流出经外电路流入正极;
三个方向 电流方向:电流从正极流出经外电路流入负极。
离子方向:阴离子
? 负极 阳离子 ? 正极 两种装置的比较:
装置Ⅰ中还原剂 Zn 与氧化剂 Cu 2+直接接触,易造成能量耗费;装置Ⅱ能防备能量耗费;装置Ⅱ中盐桥的作用是供应离子迁移通路,导电。
5. 盐桥:含有琼胶的 KCl 饱和溶液
盐桥作用:连接两个溶液,并保持两个溶液呈电中性。
+ - ? 负极
K ? 正极, Cl。
电化学知识点总结 选修4 人教版

电化学知识点总结选修4 人教版电化学是研究电动力学和化学反应之间的关系的科学,它既包含了电学,又包含了化学。
电化学的基本概念和原理是理解电池、电解和电沉积过程的基础,对于了解蓄电池、金属电沉积、电解制氢和电解制氧等实际应用也具有重要意义。
下面将对电化学的几个重要知识点进行总结。
1. 电化学电池:电化学电池是将化学能转化为电能或将电能转化为化学能的装置。
它由两个电极(即正极和负极)和电解质组成。
正极是电子的流出处,负极是电子的流入处。
电化学电池可以分为原电池和电解池。
原电池可继续工作,能将化学能转化为电能,如干电池;电解池则将电能转化为化学能,是通过电解反应进行的。
2. 电势:电势是描述电池正极与负极之间电压差的物理量,单位为伏特(V)。
在电化学反应中,正极具有较高的电势,而负极具有较低的电势。
电势差可以通过测量两个电极之间的电压差来确定。
3. 氧化还原反应:氧化还原反应是指电子从一种物质转移到另一种物质的化学反应。
氧化是指物质失去电子,而还原是指物质获得电子。
在电化学反应中,氧化与还原同时进行,被氧化的物质是还原剂,而被还原的物质是氧化剂。
4. 电解质溶液:电解质溶液是指在溶液中存在可导电的离子种类。
电解质溶液可以分为强电解质溶液和弱电解质溶液。
强电解质溶液中,离子完全离解,能够导电;而弱电解质溶液中,离子只有一部分离解,导电能力较弱。
5. 离子迁移:在电化学反应中,离子在电场力的作用下沿着电场方向移动,这就是离子迁移。
离子在迁移中的速度与电场强度和离子浓度有关,通常用电导率来衡量离子迁移的能力。
6. 电沉积:电沉积是指通过电解反应将金属离子还原成纯金属的过程。
电沉积具有选择性,可以控制金属的沉积位置、形状和厚度。
电镀是电沉积的一种实际应用,通过电解反应在物体表面沉积一层金属覆盖层,起到防腐和装饰的作用。
7. 电解质溶液的电导性:电解质溶液的电导性是指电流通过该溶液时的导电能力。
电解质溶液的电导性和电解质的浓度、温度、离子迁移速率等因素有关。
化学:第四章《电化学基础》课件(新人教版选修4)

√
Zn Cu
B
H2SO4
C
H 2SO 4
Fe Cu
Zn Cu
D √
NaCl溶液
Zn
Cu
E √
F
Cu 2SO4 CuSO4
M
酒精
NaCl溶液
N
H2SO4 H2SO4
武宁一中化学教研组
8
例2. 在盛有稀H2SO4的烧杯中放入用 导线连接的锌片和铜片,下列叙述正 D) 确的是( (A)正极附近的SO42 -离子浓度逐渐增大 (B)电子通过导线由铜片流向锌片 (C)正极有O2逸出 (D)铜片上有H2逸出
正极:
PbO2 + 4H+ + SO42- + 2e - = PbSO4 + 2H2O 总反应式为: 当向外提供0.5mol电子时,消耗硫酸的 物质的量为 0.5mol
武宁一中化学教研组
Pb + PbO2 + 2H2SO4 =2PbSO4 + 2H2O
26
补:2. 铅蓄电池
阳极: PbSO4 + 2H2O - 2e - = PbO2 + 4H+ + SO42阴极: PbSO4 + 2e - = Pb + SO42总反应
21
练习:
宇宙飞船上使用的氢氧燃料电池,其电池反应 为2H2+O2=2H2O,电解质溶液为KOH,反应 保持在高温下,使H2O蒸发,正确叙述正确的 是:( BD ) A.H2为正极反应物,O2为负极反应物 B.电极反应(正极): O2+2H2O+4e- = 4OHC.电极反应(负极): 2H2+4OH- + 4e- = 4H2O D.负极发生氧化反应,正极发生还原反应
人教版选修四第四章、电化学基础 期末基础知识复习及训练(含答案)

人教版高二化学必修四第四章、电化学基础期末基础知识复习及训练(含答案)基础知识点整理一、原电池基本概念理解。
1、原电池的概念:把化学能直接转化为电能的装置叫做原电池。
2、化学电池的分类:常见的原电池可以分为三类:(1)一次电池:常见一次电池:碱性锌锰电池、锌银电池、锂电池等;(2)二次电池:放电后可以再充电使活性物质获得再生,可以多次重复使用,又叫充电电池或蓄电池;(3)燃料电池:是使燃料与氧化剂反应直接产生电流的一种原电池。
3、原电池的电极反应:以锌铜原电池为例:负极:氧化反应:Zn-2e=Zn2+(较活泼金属)正极:还原反应:2H++2e=H2↑(较不活泼金属)总反应式:Zn+2H+=Zn2++H2↑4、常见原电池的电极反应总结。
⑴干电池(属于一次电池)①结构:锌筒、填满MnO2的石墨、溶有NH4Cl的糊状物。
②电极反应负极:Zn-2e-=Zn2+正极:2NH4++2e-=2NH3+H2NH3和H2被Zn2+、MnO2吸收:MnO2+H2=MnO+H2O,Zn2++4NH3=Zn(NH3)42+⑵铅蓄电池(属于二次电池、可充电电池)①结构:铅板、填满PbO2的铅板、稀H2SO4。
②A.放电反应负极: Pb-2e-+ SO42- = PbSO4正极: PbO2 +2e-+4H+ + SO42- = PbSO4 + 2H2OB.充电反应:阴极:PbSO4 +2e-= Pb+ SO42-阳极:PbSO4 -2e- + 2H2O = PbO2 +4H+ + SO42-===总反应式:Pb + PbO 2 + 2H2SO4放电充电2PbSO4 + 2H2O5、典型例题分析。
例题1、原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。
下列说法中正确的是( )A.(1)(2)中Mg作负极,(3)(4)中Fe作负极B.(2)中Mg作正极,电极反应式为6H2O+6e-===6OH-+3H2↑C.(3)中Fe作负极,电极反应式为Fe-2e-===Fe2+D.(4)中Cu作正极,电极反应式为2H++2e-===H2↑答案:B解析:(1)中Mg作负极;(2)中Al作负极;(3)中铜作负极;(4)是铁的吸氧腐蚀,Fe作负极。
选修四 电化学基础知识点总结202-11-20

选修四电化学基础知识点总结202-11-20 选修四电化学基础知识点总结202*-11-20选修四电化学基础知识点总结202*-11-201原电池及其应用1.1原电池原理1.1.1原电池装置构成①两个活泼性不同的电极;②电解质溶液或熔融的电解质[说明]原电池的两极分别称为正极和负极。
两极中相对活泼(易失电子)的作为负极,相对不活泼的为正极。
负极应要能与电解质溶液发生自发的氧化反应。
当两电极材料均插入电解质溶液中并将两极相连构成闭合电路,原电池装置才能发生电化反应产生电流。
1.1.2原电池发电原理及电极反应将铜片和锌片平行地插入稀硫酸溶液中,则构成了原电池。
若将两极用导线相连,则有电流产生。
“发电”的原理说明如下:由于锌比铜活泼,易失电子,Zn为负极,Cu则为正极。
两极相连后,Zn自发失去2++电子,不断“溶解”,形成Zn进入溶液。
锌片失去的电子沿外电路到达铜片,此时溶液中阳离子H在铜2--+片表面获得电子,形成H2逸出。
与此同时溶液中的阴离子(SO4,OH)移向负极,阳离子(H)移向正极(电池内部离子的迁移是由化学势所推动的,即非电场力做功完成)。
由于电池工作时,电子能自发地从负极经外电路流向正极,在电池内部,溶液中离子能自发地迁移,这样电池就向外提供电能,发电了。
电极反应式表示如下-2+负极(Zn)Zn2e=Zn(负极发生失电子的氧化反应,流出电子)+-正极(Cu)2H+2e=H2↑(正极发生得电子的还原反应,流进电子)+2+ 总反应式Zn+2H=Zn+H2↑从上分析可知此例正极材料本身并无参与电极反应,仅起作导体作用而已。
因此,正极材料若换为活泼性比锌差的导体为电极(如石墨),效果一样。
1.2原电池的应用主要有两方面:其一,利用原电池自发进行的氧化还原反应,开发化学电源;其二,抑制原电池反应发生,应用于金属腐蚀的防护。
1.2.1常见的化学电源①锌-锰干电池正极-石墨棒,负极-锌筒,电解质-淀粉湖-NH4Cl与碳粉、MnO2的混合物。
高中化学 第四章《电化学基础》 新人教版选修4

2.原电池工作原理(以锌铜原电池为例)
装 置 示 意 图 现 锌片逐__渐__溶__解__,铜片上有红___色__物__质__沉__积__, 象 电流表指针发生_偏__转_____
电极 电极名称 得失电子 电子流向 反应类型
电极反应式
总反应式
Zn电极
Cu电极
负极
正极
失电子
得电子
流出
流入
氧化反应
还原反应
解析:选C。判断原电池正负极,除考虑活 泼性还要注意电解质溶液对正负极的影响。 对于稀硫酸来说,镁是比铝更活泼的金属; 但对于氢氧化钠溶液来说,铝是比镁更活泼 的金属,所以A池中镁是负极,B池中铝是负 极,B对;
A池中电极反应为Mg-2e-===Mg2+,A 对;B池中电子流向为Al―→Mg,C项错。 A池中正极2H++2e-===H2↑,随着反应进 行,c(H+)减少,pH增大,D对。
二、原电池的设计 1.依据 理论上,能自发进行的__氧__化__还__原__反__应____均 能设计成原电池。 2.实际设计时应注意的几个方面 (1)外电路
负极(还__原__性__较__强___的物质)―失 导―线e→- 正极(能__导__电__ 的物质) (2)内电 路 将两极浸入 _电__解__质___溶液 中,并通过 _阴__、__阳__ 离子的定向运动而 形成内电路。
原电池原理的应用
探究导引2为什么锌与稀硫酸反应时,加入少 量CuSO4,会使反应速率加快? 提示:锌与稀硫酸反应时,加入少量CuSO4, Cu2+被锌置换出来,生成的单质Cu附着在锌 的表面,此时会发生原电池反应,锌为负极, 使反应速率加快。
要点归纳
1.加快氧化还原反应的速率 在金属与酸溶液的置换反应中,通过形成原电 池而使反应速率加快。 2.比较金属活动性的强弱
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《选修四》第四章电化学基础
1. 下列各变化中属于原电池反应的是()
A.在空气中金属铝表面迅速氧化形成保护层
B.镀锌铁表面有划损时,也能阻止铁被氧化
C.红热的铁丝与冷水接触,表面形成蓝黑色保护层
D.浓硝酸比稀硝酸更能氧化金属铜
2. 对外加电流的保护中,下列叙述正确的是()
A. 被保护的金属与电源的正极相连
B. 被保护的金属与电源的负极相连
C. 在被保护的金属表面上发生氧化反应
D. 被保护的金属表面上不发生氧化反应,也不发生还原反应
3. 在某电解质溶液里,用M和N作电极,通电一段时间后,发现M极质量减小,N极质量增大,符合这一情况的是()
A. 电解质溶液是稀硫酸
B. 金属M是阳极,金属N是阴极
C. M和N都是石墨电极
D. M是阴极,N是阳极
4. 已知蓄电池在充电时作电解池,放电时作原电池。
铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“—”。
关于标有“+”
的接线柱,下列说法中正确
..的是()
A.充电时作阳极,放电时作负极 B.充电时作阳极,放电时作正极
C.充电时作阴极,放电时作负极 D.充电时作阴极,放电时
作正极
5. 化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确..
的是( ) A .电解饱和食盐水时,阳极的电极反应式为:2Cl - -2e -==Cl 2 ↑
B .氢氧燃料电池的负极反应式:O 2 + 2H 2O + 4e - == 4OH -
C .粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu -2e - == Cu 2+
D .钢铁发生电化学腐蚀的正极反应式:Fe -2e - == Fe 2+
6.铁棒与石墨棒用导线连接后浸入0.01mol?L -1的食盐溶液中,可能出现的现象是( )
A. 铁棒附近产生OH -
B. 铁棒逐渐被腐蚀
C. 石墨棒上放出Cl 2
D. 石墨棒上放出O 2
7. 下面有关电化学的图示,完全正确的是( )
8. 用两根铂丝作电极插入KOH 溶液中,再分别向两极通入甲烷气体和氧气,可形成燃料电池,该电池放电时的总反应为:CH 4+2KOH+2O 2==K 2CO 3+3H 2O ,下列说法错误的是( )
A. 通甲烷的一极为负极,通氧气的一极为正极
B. 放电时通入氧气的一极附近溶液的pH 升高
C. 放电一段时间后,KOH 的物质的量不发生变化
D. 通甲烷的电极反应式是:CH 4+10OH --8e -==CO 32-+7H 2O
9.镍镉(Ni-Cd )可充电电池在现代生活中有广泛应用。
已知某镍镉电池的电解质溶液为KOH 溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H 2O 放电
Cd(OH)2 + 2Ni(OH)2 有关该电池的说法正确的是( )
A.充电时阳极反应:Ni(OH)2-e- + OH- == NiOOH + H2O
B.充电过程是化学能转化为电能的过程
C.放电时负极附近溶液的碱性不变
D.放电时电解质溶液中的OH-向正极移动
10. 用惰性电极电解100mL饱和食盐水,一段时间后,在阴极得到112mL H
2
(标准状况),此时电解质溶液(体积变化忽略不计)的pH为 ( )
A. 13
B. 12
C. 8
D. 1
11. 用两支惰性电极插入500mL AgNO
3
溶液中,通电电解。
当电解液的pH从6.0变为3.0时(电解时阴极没有氢气放出,且电解液在前后体积变化可以忽略),电极上析出的质量大约是()
A. 27mg
B. 54 mg
C. 108 mg
D. 216 mg
12. 在1LK
2SO
4
和CuSO
4
的混合溶液中,c(SO
4
2-)=2.0 mol·L-1,用石墨作电极电
解此溶液,当通电一段时间后,两极均收集到22.4L(标准状况)气体,则原溶液中K+的物质的量浓度为()
A. 2.0 mol·L-1
B. 1.5 mol·L-1
C. 1.0 mol·L-1
D. 0.5 mol·L-1
13.右图为以惰性电极进行电解:
(1)写出B、C、D各电极上的电极反应式和总反应方程式:
A:________________________________,
B:________________________________,
总反应方程式:________________________;
C:________________________________,
D:________________________________,
总反应方程式:___________________________;
(2)在A、B、C、D各电极上析出生成物的物质的量比为__________________。
14. 如图A 直流电源,B为浸透饱和氯化钠溶液和酚酞试液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
(1)电源A上的a为________极;
(2)滤纸B上发生的总化学方程式为
___________________;
(3)欲在电槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为________________,电极f上发生的反应为______________________________,槽中放的镀液可以是________或________(只要求填两种电解质溶液)。
15.电解原理在化学工业中有广泛应用。
右图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。
请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,则电解池中X极上的电极反应为___________________________,在X极附近观察到的现象是:__________________
(2)Y电极上的电极反应式是_________,检验该电极反应产物的方法是:____________________________________
(3)如果用电解方法精炼粗铜,电解液a选用CuSO
4
溶液,则X电极的材料是_________,电极反应式是__________________,Y电极的材料是_________,电极反应式是__________________
参考答案
1-5 BBBBA 6-12 BDCAABA
13.(1)Cu2++2e-== Cu 2Cl-2e-=Cl
2↑ CuCl
2
电解 Cu+ Cl
2
↑
4Ag++4e-== 4Ag 4OH--4e-== 2H
2O+O
2
↑ 4AgNO
3
+2H
2
O== 4Ag+O
2
↑+4HNO
3
(2)2:2:4:1
14.(1)正(2)2NaCl+2H
2O电解H
2
↑+Cl
2
↑+2NaOH
(3)Zn—2e-===Zn2+ Zn2++2e-===Zn ZnSO
4溶液或ZnCl
2
溶液
15.(1)2H++2e-==H
2
↑ 有气泡,溶液变红
(2)2Cl-—2e-==Cl
2
↑把湿润的淀粉KI试纸放在Y极附近,试纸变蓝,说明
Y极产物为Cl
2
(3)纯铜 Cu2++2e-==Cu 粗铜 Cu-2e-==Cu2+。
