个人设计菌株传代记录
菌种传代记录

菌种名称
菌种代数
传代传代次数
传代数量
传代人
传代结束日期
保存温度
培养时间(小时)
传代步骤:
1、在无菌条件下,将经复活后的菌种置于洁净工作台面。
2、点燃酒精灯,在火焰旁的上部空间操作。
3、灼烧接种环,环进入试管的部分,在通过火焰灼烧。灼烧时,把环置于酒精灯的外焰上,灼烧完毕将环稍冷片刻再进行操作。
7、先将灼烧过的接种环插入菌种管内,先接触无菌苔生长的培养基上,如有熔印则表明接种环未冷却,能烫死细菌。一定待冷后,再从斜面上挑取菌苔少许。取出时接种环不能通过火焰,应在火焰旁迅速插入接种管,在斜面上轻轻划线接种。划线时先由下而上划一直线后,再由下而上划曲线。操作过程应迅速,勿使菌苔沾至管壁或管口。
8、当接种完毕,立即将管口通过火焰灭菌,右手到火焰旁塞上棉塞,不要将管口离开火焰旁去迎接右手的棉塞。最后将接种环灼烧灭菌放置原处,再把可能未塞紧的棉塞塞紧,即可进行培养。
9、每支菌种需标明菌株编号、传代次数、菌种名称、接种日期、有效期、接种人。
10、将接种好的培养基放置培养箱中(按照菌种说明书所规定的时间和温度要求培养),观察菌种生长情况。
传代管编号:________________________________
________________________________
________________________________
________________________________
4、菌种管与接种管持在左手,菌种管在前,接种管在后。应斜持试管呈45°角,使试管斜面向上。
5、以右手在火焰旁转动两管的棉塞,以便接种易于拔取。再以右手持接种环的柄端,把接种环在火焰上烧灼。顶端的环必须烧红,以彻底灭菌。
菌株致泻大肠埃希菌传代记录

菌株致泻大肠埃希菌传代记录标题:学术研究与探索:菌株致泻大肠埃希菌传代记录导语:近年来,由菌株致泻的大肠埃希菌(Escherichia coli)引起了广泛的关注和研究。
这些致病菌对人类健康构成了严重威胁,因此科学家们对其传递和演化过程进行了深入研究。
本文将基于这些研究成果,从不同角度探讨菌株致泻大肠埃希菌的传代记录。
一、病原学背景(1)对菌株致泻大肠埃希菌的定义和特点的介绍菌株致泻大肠埃希菌是指对宿主产生肠道感染并引起泻泄症状的一类致病菌。
它们在肠道中繁殖,产生毒素和附着因子,从而破坏宿主的肠道组织,并导致腹泻、腹痛和发热等症状。
(2)菌株致泻大肠埃希菌的传递途径和发展趋势研究表明,菌株致泻大肠埃希菌可以通过食物、水源和接触传播等多种途径感染人体。
随着全球化和人类活动的增加,其传播的范围不断扩大,形成了全球性的公共卫生问题。
了解其传递途径和发展趋势,有助于制定预防和控制措施,减少感染的风险。
二、菌株传代过程的研究(1)临床样本的分离和鉴定研究人员通过采集病例和样本,利用分子生物学方法对人体和环境中的菌株进行鉴定。
通过对不同时间和地点分离的菌株进行比较,可以了解其传递路径和演化过程。
(2)菌株的基因分析和比较利用高通量测序技术和生物信息学分析,研究者可以对不同菌株的基因进行全面的比较。
这些研究揭示了菌株间的遗传关系、演化轨迹以及与菌株致病性相关的基因。
(3)实验室模型和动物传代试验通过实验室模型和动物传代试验,研究人员可以模拟菌株在不同宿主中的传递和适应过程。
这些实验为了解菌株传代规律和适应性变化提供了重要手段。
三、病原菌菌株的公共卫生意义(1)疫苗的开发与预防策略的制定通过对菌株的传代记录和基因分析,可以寻找到共有的抗原或毒力因子,从而为疫苗的开发提供理论依据。
对传播途径和环境因素的研究,也有助于制定针对菌株致病大肠埃希菌的预防策略。
(2)全球监测和溯源有效的全球监测和溯源机制对于控制菌株致泻大肠埃希菌的传播和爆发至关重要。
菌种传代步骤

菌种传代步骤嘿,咱今儿就来讲讲菌种传代步骤这档子事儿哈!你可别小瞧了这小小的菌种,那可是好多实验、生产的重要基础呢!先来说说准备工作吧,就好比咱要出门得先收拾好东西一样。
得把各种需要的工具、培养基啥的都准备齐全咯,少了一样都不行,这就跟战士上战场没带枪似的。
然后呢,咱得把菌种从原来的地方小心翼翼地取出来。
这可得轻点儿,就像抱小婴儿似的,可不敢粗鲁。
把它放到准备好的培养基上,这就像给它找了个新家。
接着就是培养啦!让菌种在这新家里舒舒服服地待着,给它合适的温度、湿度,就跟咱人得待在舒服的环境里一样。
看着它一点点长大、繁殖,嘿,那感觉还挺奇妙呢!等它长到一定程度了,咱就得给它来个“分家”。
把它分成一小份一小份的,这可不能马虎,得均匀分好,不然有的长得壮,有的长得弱,那可不行。
再把这些分好的小菌种放到新的培养基里,让它们继续成长、繁衍。
这就好比接力赛,一棒接一棒,不能掉链子。
你说这菌种传代是不是挺有意思?就像养宠物似的,得精心照料。
要是哪个环节出了错,那可就麻烦咯!好比盖房子,基础没打好,那房子能结实吗?咱再想想,要是没有正确的菌种传代步骤,那好多研究、生产不都得乱套啦?所以啊,可别小看了这些步骤,每个都重要得很呢!在这个过程中,咱得时刻保持警惕,不能有一点马虎。
就跟走钢丝似的,得小心翼翼,一步一个脚印。
而且啊,不同的菌种可能还有一些特殊的要求呢,这就得咱更加仔细地去了解、去掌握。
不能一概而论,得具体问题具体分析。
总之呢,菌种传代步骤看似简单,实则暗藏玄机。
咱得认真对待,才能让这些小菌种发挥出大作用!你说是不是这个理儿?。
菌株领用记录

菌株领用记录
菌株领用记录应该包括以下内容:
1. 领用日期:记录菌株被领用的具体日期。
2. 领用人:记录菌株是由谁领用的,应该包括领用人的姓名、部门、职位等信息。
3. 菌株编号:记录被领用菌株的编号,以便追踪和管理。
4. 领用数量:记录被领用菌株的数量,包括种类和规格等。
5. 用途:记录被领用菌株的具体用途,如实验、生产等。
6. 归还日期:如果领用人需要将菌株归还,则记录归还的日期。
7. 归还数量:记录归还菌株的数量,以确保数量一致。
8. 备注:记录其他需要说明的事项,如特殊要求、注意事项等。
以上是一份简单的菌株领用记录表格,具体格式可以根据实际需要进行调整。
菌株交接记录

菌株交接记录菌株交接记录工作的总结范文,如果你不会写作,可以参考一下。
菌种分离和复壮工作已经进行了四年多,在这期间我们积累了很多有关菌种分离与复壮的经验教训,特别值得回味、总结和思考。
我站是一个较大型的技术服务机构,每年需向各省市(自治区)提供十几个乃至几十个菌种。
其中有数百份因复壮失败而报废处理,还有一小部分虽然复壮成功但也只能算做是临床试用,绝非生产性品种。
由此看来,培养基及配制过程对菌种复壮起着决定性作用。
在工作实践中我体会到:在从事原种、原液和一级种的生产时应注意以下几点问题;1.选择合适的菌株来源这里所说的“合适”,既指性状表现良好、遗传稳定性强、生长速度快、繁殖力高、经济效益明显等,又包括外界环境和人工管理适宜等方面。
2.正确掌握和使用新鲜培养基为保证有充足的营养物质,供给细胞分裂所必须的氧气和养料,防止代谢产物增加,从而抑制菌丝生长,通常把这类菌株称为“活化株”。
3.合理采用复壮措施根据菌种遗传特性和当前存在的主要问题,选取相应的手段来消除或减轻病害,以达到预期目标。
例如当发现多数担子孢子或菌丝出现畸形,即往往有不同程度的退化时,便可以针对不同情况,先后采用添加磷酸二氢钾、调整氮源、补充微量元素、深层分离、直接倒平板扩大接种等办法予以解决。
4.注重综合分析和协调进行人员、设备、器材、资金和信息五个因素的综合分析和协调,才能有助于创造最佳的生产条件。
对于那些条件比较好的地方要求更为严格,不允许带入任何杂菌,否则会导致所谓“霉变”,影响制种产量和质量,甚至可能造成全军覆没。
在近三年的工作中我亲身感受到菌种复壮难度之大超乎想象,必须立足长远,多花费精力、财力和物力,千万不能急功近利。
对于一些有希望、有潜力、长势喜人的优秀种质,应该继续加强研究并探索规律,促使它们尽早投入生产。
诚然,作为技术服务单位的菌种室有责任为各省(市、自治区)提供更多更优秀的菌种,同时还必须承担国家赋予的为农业科研服务的职责。
菌种传代、接受和使用记录
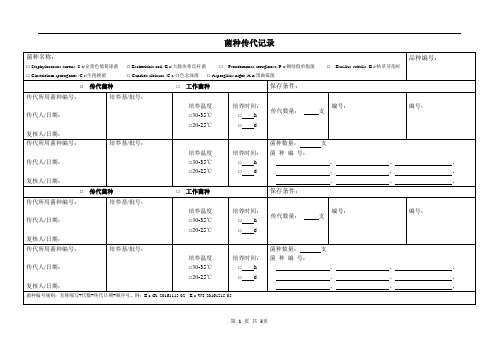
菌种名称:
□Staphylococcus aureus /S.a/金黄色葡萄球菌□Escherichia coli /E.c/大肠埃希氏杆菌□Pseudomonas aeruginosa /P.a/铜绿假单胞菌□Bacillus subtilis /B.s/枯草芽孢杆
□Clostridium sporogenes /C.s/生孢梭菌□Candida albicans /C.a/白色念珠菌□Aspergillus niger /A.n/黑曲霉菌
菌种编号:
、、、
、、、
、、、
□传代菌种□工作菌种
保存条件:
传代所用菌种编号:
传代人/日期:
复核人/日期:
培养基/批号:
培养温度
□30-35℃
□20-25℃
培养时间:
□h
□d
传代数量:支
编号:
编号:
传代所用菌种编号:
传代人/日期:
复核人/日期:
培养基/批号:
培养温度
□30-35℃
□20-25℃
培养时间:
保存温度
有效期
复核人/日期
使用人/日期
用途
复核人/日期
备注
□ -20 ℃ □ 2-8 ℃
□ -20 ℃ □ 2-8 ℃
□ -20 ℃ □ 2-8 ℃
□ -20 ℃ □ 2-8 ℃
□ -20 ℃ □ 2-8 ℃
□ -20 ℃ □ 2-8 ℃
工作菌种接受和使用登记
菌种名称:
□Staphylococcus aureus/S.a/金黄色葡萄球菌□Escherichia coli/E.c/大肠埃希氏杆菌□Pseudomonas aeruginosa/P.a/铜绿假单胞菌□Bacillus subtilis/B.s/枯草芽孢杆
检定菌种接收、传代记录(附表1-7)
用途 用于 20220301 批次产品初始污 染菌阳性对照菌 用于洁净区环境监测沉降菌阳 性对照菌 用于菌悬液的制备
文件编号:
废弃菌种(物品)销毁记录
日期 被处理菌种(物品)名 销毁原因 处理方式
销毁人 销毁监督人
备注:废弃菌种要标明编号、数量(支)
表码: 接收日期
名称
代号
编号
标准菌株库存记录 数量 代次
来源
检查情况 保存条件 接收人Biblioteka 备注:表码: 接收日期
名称
编号
检定菌种接收记录
数量 代次
来源
检查情况 保存条件 接收人
备注:
表码: 菌种名称
传代前菌种代次 传代前菌种状态
检定菌种传代记录
大肠埃希菌
0代 正常
菌种代号
传代前菌种保存方 法
传代数量
备注
表码: 日期
检定菌种观察记录
塞子是否
冰箱温度(℃)
是否染菌
松动
处理措施
记录人
文件编号: 菌种名称及编号
鉴定原因
菌落形态
检定菌种鉴定记录 开始鉴定日期
革兰氏染色
鉴定 项目
显微镜下形态
典型生化特征 鉴定结果:
备注:
操作人:
复核人:
文件编号: 领用日期 菌种名称
检定菌种使用登记台账
菌种编号
数量
使用人
CMCC(B)44102
冷藏>-30℃ 1支
传代日期
2022.3.1
编号
E.c-G1-220301-01
传代用菌种
□工作用菌种
培养基信息 生产批号:
胰酪大豆胨琼脂培养基(TSA)
生产日期:
支原体菌株传代记录
操作步骤
完成情况
4.1 生物安全柜提前开启紫外灯消毒 30 分钟,培养基经高压蒸汽灭菌,待到 45℃以下。
完成
4.2 将培养基分装,每支试管 8mL,加入 2mL 灭能血清,混匀。
完成
4.3 将支原体从微生物培养箱取出,观察支原体培养基颜色变化,当肺炎支原体培养基颜色由橘 完成
红色变成橘黄色,表明支原体生长旺盛,可以传代,当口腔支原体培养基颜色由橘黄色变成橘
管架内,放入微生物培养箱培养。
操作人/日期:
复核人/日期:
红色,表明支原体生长旺盛,可以传代,
4.4 将支原体试管喷洒酒精,擦拭干净后,放入生物安全柜内,用混匀仪混匀。
完成
4.5 若为肺炎支原体用 1.0mL 菌液,加入到支原体肉汤培养基中,混匀。做好标记,放入试管架 完成
内,放入微生物培养箱培养。
4.5 若为口腔支原体用 1.0mL 菌液,加入精氨酸支原体肉汤培养基中,混匀,做好标记,放入试 完成
1.菌株信息 菌株名称
菌株编号
菌株代次
菌株批号
操作人/日期
2.主要试剂、耗材信息 名称
批号
有效期至
使用量
灭能小牛血清
精氨酸支原体肉汤培养基
支原体肉汤培养基
10 mL 刻度移液管 3.主要设备信息
设备名称
编号
校准有效期至
生物安全柜
电动移液器
高压蒸汽灭菌器Βιβλιοθήκη 微生物恒温培养箱移液器
4.操作流程
1000uL 无菌枪头
细菌传代实验报告
实验报告:细菌传代实验一、实验目的1. 掌握细菌传代培养的基本原理和方法。
2. 了解细菌在传代过程中形态、生长曲线和生理特性的变化。
3. 掌握细菌纯种分离和接种技术。
二、实验原理细菌传代培养是指将已经培养好的细菌接种到新的培养基中,使细菌在适宜的环境中继续生长繁殖的过程。
通过传代培养,可以保证细菌的纯种,同时观察细菌在传代过程中的生长曲线和生理特性变化。
三、实验材料1. 菌种:大肠杆菌(Escherichia coli)2. 培养基:LB培养基、固体LB培养基3. 仪器:超净工作台、接种环、酒精灯、培养皿、恒温培养箱、显微镜、计数器等四、实验方法1. 制备LB培养基:按照实验要求配制LB培养基,分装于培养皿中,待凝固后备用。
2. 细菌接种:将活化的大肠杆菌菌种接种于LB培养基中,置于37℃恒温培养箱中培养。
3. 观察生长情况:在培养过程中,每隔一定时间观察细菌的生长情况,记录菌落形态、颜色等。
4. 传代培养:将生长良好的菌液按1:100的比例接种于新的LB培养基中,重复以上步骤。
5. 细菌纯种分离:取一定量的菌液,涂布于固体LB培养基上,置于37℃恒温培养箱中培养。
6. 观察纯种分离效果:观察菌落形态、颜色等,判断是否为纯种。
7. 计算生长曲线:通过观察不同代数的细菌生长情况,绘制生长曲线。
8. 生理生化特性观察:通过观察不同代数的细菌在固体培养基上的生长情况,分析其生理生化特性。
五、实验结果1. 细菌生长曲线第一代:菌落呈圆形、光滑、湿润,颜色为白色。
第二代:菌落较第一代略小,表面略粗糙,颜色略淡。
第三代:菌落继续缩小,表面粗糙,颜色较淡。
2. 细菌纯种分离效果通过涂布培养,观察菌落形态、颜色等,发现第三代细菌菌落为纯种。
3. 细菌生理生化特性通过观察不同代数的细菌在固体培养基上的生长情况,发现第一代细菌生长旺盛,菌落呈圆形、光滑、湿润,颜色为白色;第二代细菌生长速度略慢,菌落较第一代略小,表面略粗糙,颜色略淡;第三代细菌生长速度进一步减慢,菌落继续缩小,表面粗糙,颜色较淡。
细菌菌株保存和传代程序
细菌菌株保存和传代程序
本文档描述了细菌菌株的保存和传代程序。
保持菌株的纯度和可行性对于科研工作的进行至关重要。
保存程序
1. 菌株选择: 选择合适的细菌菌株进行保存。
确保菌株具有所需的特性,并且无任何污染。
2. 菌株培养: 在含有适当培养基和添加适当抗生素的培养皿中培养细菌菌株。
确保正确的菌株转接和培养条件。
3. 菌株冷冻: 使用含有甘油或DMSO的培养基冷冻保存菌株。
将菌株移植到含有冷冻保护剂的培养基中,然后迅速冷冻至-80°C 或更低的温度。
4. 菌株标签: 对冷冻保存的每个菌株进行正确标记,包括菌株名称、保存日期和其他重要信息。
传代程序
1. 选择菌株: 从冷冻保存中选择所需菌株,并进行解冻。
2. 菌株培养: 将解冻的菌株转移到含有适当培养基的培养皿中。
根据需要添加适当的抗生素。
3. 菌株传代: 在培养皿中选择一个单独的菌落,并将其转移至
新的培养皿中。
确保每次传代使用无菌操作。
4. 检测菌株纯度: 每次传代后,使用适当的方法检测菌株的纯度,例如菌落PCR或进行生理生化测试。
5. 记录菌株信息: 记录每次传代的日期和传代次数,以跟踪菌
株的使用情况和变化。
注意事项
- 保持无菌操作: 在操作培养菌株时,始终使用无菌技术和设备,以避免菌株污染。
- 定期检查菌株: 对保存的菌株进行定期检查,并尽可能定期进行传代以保持其新鲜度和活性。
- 数据备份: 对于重要菌株,建议制作并保存冷冻保存和传代记录的备份。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
革兰氏阴性杆菌
/
无杂菌
合格
高超燎
JP-20181030
-D1-3
2018.12.25
JP-20181225
-D2-1(2)
菌落凸起、圆形不透明
革兰氏阳性球菌
血浆凝固酶阳性
无杂菌
合格
高超燎
BP-20181030
-D1-3
2018.12.25
BP-20181225
-D2-1(2)
/
无杂菌
合格高超燎酿酒酵母A NhomakorabeaCC9763
2018.10.30
JM-20181030
-D1-1(2)
奶油色菌落
阳性球菌
/
无杂菌
合格
高超燎
移接前
菌株编号
移接日期
移接后
菌株编号
生长特征
染色形态
生化鉴定
纯度检查
结论
操作人员
备注
DC-20181030
-D1-3
2018.12.25
DC-20181225
-D2-1(2)
高超燎
M-20181030
-D1-2
2019.1.16
M-20190116
-D2-1(2)
黑色孢子
孢子为球形呈黑色
/
无杂菌
合格
高超燎
JM-20181030
-D1-2
2019.1.16
JM-20190116
-D2-1(2)
奶油色菌落
阳性球菌
/
无杂菌
合格
高超燎
菌落凸起、圆形不透明
革兰氏阳性球菌
徐江凝固酶阴性
无杂菌
合格
高超燎
SM-20181030
-D1-3
2018.12.25
SM-20181225
-D2-1(2)
/
革兰氏阴性杆菌
生化试剂鉴定盒符合沙门氏菌检定要求
无杂菌
合格
高超燎
移接前
菌株编号
移接日期
移接后
菌株编号
生长特征
染色形态
生化鉴定
纯度检查
结论
操作人员
SM-20181030
-D1-1(2、3)
/
革兰氏阴性杆菌
/
无杂菌
合格
高超燎
福氏志贺氏菌
CMCC(B)5127
2018.10.30
ZH-20181030
-D1-1(2)
/
革兰氏阴性杆菌
/
无杂菌
合格
高超燎
黑曲霉
ATCC16404
2018.10.30
M-20181030
-D1-1(2)
黑色孢子
孢子为球形呈黑色
备注
DC-20181225
-D2-1
2019.1.16
DC-20190116
-D3-1(2)
菌落凸起、圆形、湿润、乳白色
革兰氏阴性杆菌
/
无杂菌
合格
高超燎
JP-20181225
-D2-1
2019.1.16
JP-20190116
-D3-1(2)
菌落凸起、圆形不透明
革兰氏阳性球菌
血浆凝固酶阳性
无杂菌
合格
高超燎
BP-20181225
-D2-1
2019.1.16
BP-20190116
-D3-1(2)
菌落凸起、圆形不透明
革兰氏阳性球菌
血浆凝固酶阴性
无杂菌
合格
高超燎
SM-20181225
-D2-1
2019.1.16
SM-20190116
-D3-1(2)
/
革兰氏阴性杆菌
生化试剂鉴定盒符合沙门氏菌检定要求
无杂菌
合格
-D1-1(2、3)
菌落凸起、圆形不透明
革兰氏阳性球菌
血浆凝固酶阳性
无杂菌
合格
高超燎
表皮葡萄球菌
CMCC(B)26069
2018.10.30
BP-20181030
-D1-1(2、3)
菌落凸起、圆形不透明
革兰氏阳性球菌
徐江凝固酶阴性
无杂菌
合格
高超燎
伤寒沙门氏菌
CMCC(B)50071
2018.10.30
移接前
菌株编号
移接日期
移接后
菌株编号
生长特征
染色形态
生化鉴定
纯度检查
结论
操作人员
备注
大肠埃希氏菌
ATCC25922
2018.10.30
DC-20181030
-D1-1(2、3)
菌落凸起、圆形、湿润、乳白色
革兰氏阴性杆菌
/
无杂菌
合格
高超燎
金黄色葡萄球菌
ATCC25923
2018.10.30
JP-20181030
