【三维设计】(教师用书)高考化学总复习“点、面、线”备考全攻略 第11章 化学与资源开发利用章末知识整合
【三维设计】(人教通用版)高考化学一轮总复习 第十一章 有机化学基础

第十一章有机化学基础考点一烃的组成、结构与性质1.(2013·新课标全国Ⅱ理综,6分)下列叙述中,错误的是( )A.苯与浓硝酸、浓硫酸共热并保持55~60℃反应生成硝基苯B.苯乙烯在合适条件下催化加氢可生成乙基环己烷C.乙烯与溴的四氯化碳溶液反应生成1,2二溴乙烷D.甲苯与氯气在光照下反应主要生成2,4二氯甲苯解析:选 D 本题考查有机化合物,意在考查考生对有机物性质的分析和判断能力。
①BaCl2BaSO4和BaCO3的K sq相差不大,当溶液中存在大量CO2-3时,BaSO4(s)会部分转化为BaCO3(s) ②H2、Cl22NaClO3+4HCl===2ClO2↑+Cl2↑+2NaCl+2H2O2.(2013·福建理综,6分)下列关于有机化合物的说法正确的是( )A.乙酸和乙酸乙酯可用Na2CO3溶液加以区别B.戊烷(C5H12)有两种同分异构体C.乙烯、聚氯乙烯和苯分子中均含有碳碳双键D.糖类、油脂和蛋白质均可发生水解反应解析:选A 本题考查有机化合物知识,意在考查考生的识记能力和知识的运用能力。
乙酸与碳酸钠溶液反应放出二氧化碳气体,乙酸乙酯与碳酸钠不反应,不溶于碳酸钠溶液,在碳酸钠溶液的上层,A项正确;戊烷有正戊烷、异戊烷和新戊烷三种同分异构体,B项错误;聚氯乙烯和苯分子中不含有碳碳双键,C项错误;单糖不能水解,D项错误。
3.(2013·重庆理综,6分)有机物X和Y可作为“分子伞”给药载体的伞面和中心支撑架(未表示出原子或原子团的空间排列)。
X(C24H40O5)H2NCH2CH2CH2NHCH2CH2CH2CH2NH2Y下列叙述错误的是( )A.1 mol X在浓硫酸作用下发生消去反应,最多生成3 mol H2OB.1 mol Y发生类似酯化的反应,最多消耗2 mol XC.X与足量HBr反应,所得有机物的分子式为C24H37O2Br3D.Y和癸烷的分子链均呈锯齿形,但Y的极性较强解析:选B 本题考查有机物的结构与性质,意在考查考生对有机化学知识的掌握情况。
【三维设计】(教师用书)高考化学总复习“点、面、线”备考全攻略 第9章 电化学基础章末知识整合与命题热

10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为________极; ②电极b上发生的电极反应为_______________________; ③列式计算电极b上生成的气体在标准状况下的体积: ④电极c的质量变化是________g;
⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其
第五步:析。根据电极反应式分析电极、电解质溶液的变化,
并进行有关计算。
[角度一] 下图所示装置中,甲、乙、丙三个 烧杯依次分别盛放100 g 5.00%的NaOH溶液、足量的CuSO4溶 液和100 g 10.00%的K2SO4溶液,电极均为石墨电极。
(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为
O2-由正极向负极移动。若以质子交换膜为电解质,则传导
介质为H+,则正极反应为O2+4H++4e-===2H2O。 答案:B
解答电解问题的五步分析法:
第一步:看。先看清楚电极材料,对于惰性电极如石墨、
铂等,不参加阳极的氧化反应;对于铜、银等活泼电极, 阳极参与电极反应。 第二步:离。写出溶液中所有的电离方程式,包括水的电 离方程式。
A.电池放电时,甲醇在负极上发生氧化反应 B.以固体氧化物为电解质的电池放电时,氧离子由负极移
向正极
C.以质子交换膜为电解质的电池放电时,正极的反应为: O2+4H++4e-===2H2O D.电池的总反应是:2CH3OH+3O2===2CO2+4H2O
解析:甲醇在负极发生氧化反应,O2在正极发生还原反应, 总反应方程式为 2CH3OH+ 3O2===2CO2+4H2O。若以固体 氧化物为电解质,则传导介质为 O2- ,正极反应为 O2 + 4e- ===2O2-,负极反应为CH3OH+3O2--6e-===CO2+2H2O,
《三维设计》高考化学(人教版)复习教师用书:第十一章 物质结构与性质(选修3) Word版含答案
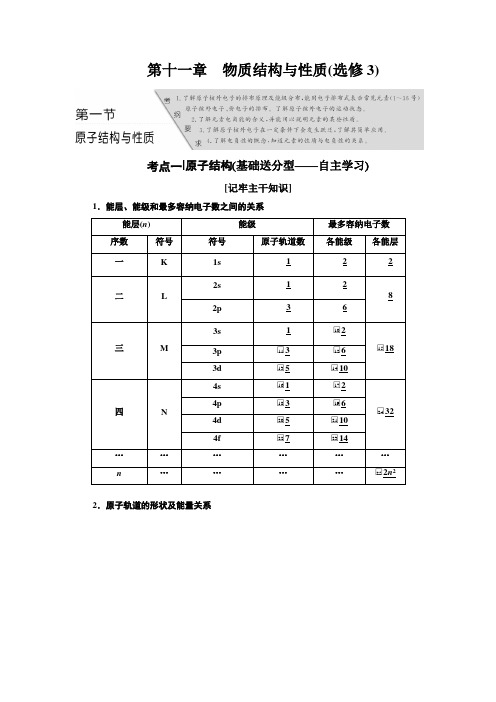
第十一章物质结构与性质(选修3)考点一|原子结构(基础送分型——自主学习)[记牢主干知识]1.能层、能级和最多容纳电子数之间的关系能层(n) 能级最多容纳电子数序数符号符号原子轨道数各能级各能层一K 1s 1 2 2二L 2s 1 28 2p 3 6三M 3s 1 □102□1518 3p □113 □1263d □135 □1410四N 4s □161 □172□2432 4p □183 □1964d □205 □21104f □227 □2314………………n…………□252n2 2.原子轨道的形状及能量关系⎩⎪⎪⎪⎪⎪⎨⎪⎪⎪⎪⎪⎧ 轨道形状⎩⎪⎨⎪⎧s 电子的原子轨道呈球形对称p 电子的原子轨道呈哑铃形各能级上的原子轨道数目⎩⎪⎨⎪⎧s 能级 1 个p 能级 3 个d 能级5个f 能级7个……能量关系⎩⎪⎨⎪⎧①相同能层上原子轨道能量的高低:n s <n p < n d <n f②形状相同的原子轨道能量的高低:1s <2s <3s <4s ……③同一能层内形状相同而伸展方向不同的原子轨道的能量相等,如2p x 、2p y、2p z轨道的能量相等3.基态原子核外电子排布 (1)基态原子核外电子排布三原则[注意] 当能量相同的原子轨道在全满(p 6、d 10、f 14)、半满(p 3、d 5、f 7)、全空(p 0、d 0、f 0)时体系的能量最低,如24Cr 的电子排布式为[Ar]3d 54s 1,29Cu 的电子排布式为[Ar]3d 104s 1。
(2)基态原子核外电子在原子轨道上的填充顺序——构造原理绝大多数元素的原子核外电子的排布遵循如图所示的排布顺序,人们把它称为构造原理。
它是书写基态原子核外电子排布式的依据。
原 子 轨 道(3)基态原子核外电子排布的表示方法表示方法以硫原子为例电子排布式1s22s22p63s23p4简化电子排布式[Ne]3s23p4电子排布图(或轨道表示式)价电子排布式3s23p4(1)原子的状态①基态原子:处于最低能量的原子。
【三维设计】高考化学一轮复习 第十一章 专题大看台 实战场 新人教版

【三维设计】高考化学一轮复习第十一章专题大看台实战
场新人教版
1.(2010·上海高考)下列做法不能体现低碳生活的是( )
A.减少食物加工过程
B.注意节约用电
C.尽量购买本地的当季食物
D.大量使用薪柴为燃料
解析:薪柴燃烧时会产生大量CO2,大量使用薪柴为燃料,不能体现低碳生活.
答案:D
2.(2010·天津高考)以节能减排为基础的低碳经济是保持社会可持续发展的战略举措.下列做法违背发展低碳经济的是( )
A.发展氢能和太阳能
B.限制塑料制品的使用
C.提高原子利用率,发展绿色化学
D.尽量用纯液态有机物代替水作溶剂
解析:氢能和太阳能都属于清洁能源,能够起到节能减排作用,A项正确.塑料制品是石油化工产品,消耗大量的化石燃料,限制其使用可以实现社会的可持续发展,B项正确.绿色化学的目标是达到100%的原子利用率,实现零排放,C项正确.液态有机物作为溶剂,不仅浪费资源,而且容易造成环境污染,D项不正确.
答案:D
3.(2011·苏州模拟)近年来,全球气候变暖对人类生存和发展带来了严峻的挑战,在此背景下,“新能源”、“低碳”、“节能减排”、“吃干榨尽”等概念愈来愈受到人们的重视.下列有关说法不.正确的是( )
A.太阳能、地热能、生物质能和核聚变能均属于“新能源”
B.“低碳”是指采用含碳量低的烃类化合物作为燃料
C.右图甲烷经氯甲烷化合成低碳烯烃途径体现了“节能减排”
思想
D.让煤变成合成气,把煤“吃干榨尽”,实现了煤的清洁、高效利用
解析:“低碳”的实质是指能源高效利用,清洁能源开发,追求“绿色”.
答案:B。
高中三维设计一轮复习化学通用版课件:第十一章 第一板块 1.2 分子结构与性质(42张PPT)

目 录
01
共价键
02 分子的立体构型
03 分子间作用力与分子性质
知识点 一 共价键
1.共价键
(1)共价键的本质与特征
①本质:两原子之间形成 共用电子对 。
②特征:具有方向性和饱和 性。
(2)共价键的分类
分类依据
类型及特点
形成共价键的原子 σ 键 原子轨道“_头__碰__头__”重叠
长相等,键角是 120°;若 NH3 分子是三角锥形结构,三个
N—H 键键长相等,键角为 107.3°,C 项正确。
4.向盛有硫酸铜溶液的试管中滴加氨水,先生成难溶物,继续滴
加氨水,难溶物溶解,得到深蓝色透明溶液。下列对此现象的
说法正确的是
()
A.反应后溶液中不存在任何沉淀,所以反应前后 Cu2+的浓度
(5)氢键 ①形成:已经与电负性很 大 的原子形成共价键的氢原子 (该氢原子几乎为祼露的质子)与另一个电负性 很大 的原子之 间的作用力,称为氢键。 ②表示方法:A—H…B—(A、B 是电负性很大的原子, 一般为 N、O、F 三种元素;A、B 可以相同,也可以不同。) ③特征:具有方向性和饱和性。 ④分类:氢键包括 分子内 氢键和 分子间 氢键两种。 ⑤分子间氢键对物质性质的影响:主要表现为使物质的 熔、沸点 升高 ,对电离和溶解度等产生影响。
分子立 体构型
实例
键角
2
2
0
直线形 _直__线__形 BeCl2 180°
3
3
0
平__面__三 ___角_形 三角形
BF3
120°
2
1
_V__形 SnBr2 105°
4
0
正__四__面 __体 __形 CH4 109°28′
2019年1月高考化学一轮复习三维设计学案第十一章 物质结构与性质(选修③)
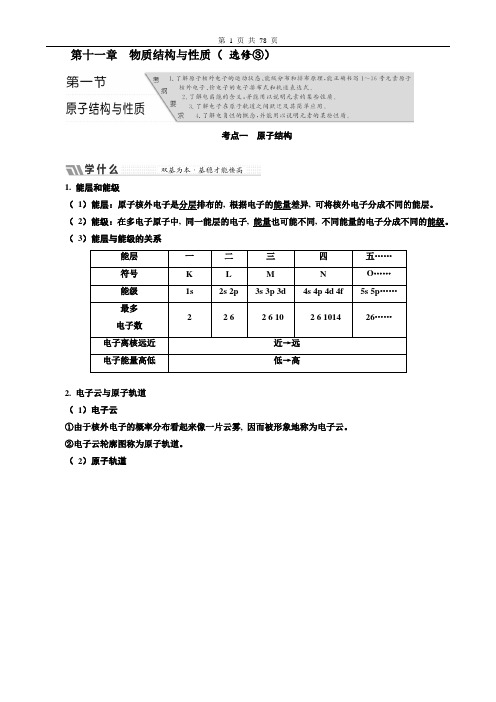
第十一章物质结构与性质(选修③)考点一原子结构1. 能层和能级(1)能层:原子核外电子是分层排布的, 根据电子的能量差异, 可将核外电子分成不同的能层。
(2)能级:在多电子原子中, 同一能层的电子, 能量也可能不同, 不同能量的电子分成不同的能级。
(3)能层与能级的关系能层一二三四五……符号K L M N O……能级1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p……最多2 2 6 2 6 10 2 6 1014 26……电子数电子离核远近近→远电子能量高低低→高2. 电子云与原子轨道(1)电子云①由于核外电子的概率分布看起来像一片云雾, 因而被形象地称为电子云。
②电子云轮廓图称为原子轨道。
(2)原子轨道原子轨道⎩⎪⎪⎪⎪⎪⎨⎪⎪⎪⎪⎪⎧轨道形状⎩⎪⎨⎪⎧s电子的原子轨道呈球形对称p电子的原子轨道呈哑铃形各能级上的原子轨道数目⎩⎪⎨⎪⎧s能级1个p能级3个d能级5个f能级7个……能量关系⎩⎪⎨⎪⎧①相同能层上原子轨道能量的高低:n s<n p<n d<n f②形状相同的原子轨道能量的高低:1s<2s<3s<4s……③同一能层内形状相同而伸展方向不同的原子轨道的能量相等,如2p x、2p y、2p z轨道的能量相等3. 基态原子核外电子排布(1)排布原则[注意]当能量相同的原子轨道在全满(p6、d10、f14)、半满(p3、d5、f7)、全空(p0、d0、f0)时原子的能量最低, 如24Cr的电子排布式为[Ar]3d54s1,29Cu的电子排布式为[Ar]3d104s1。
(2)填充顺序——构造原理绝大多数元素的原子核外电子的排布遵循如图所示的排布顺序, 人们把它称为构造原理。
它是书写基态原子核外电子排布式的依据。
(3)基态原子核外电子排布的表示方法①电子排布式a. 用数字在能级符号的右上角标明该能级上排布的电子数, 这就是电子排布式, 例如K:1s22s22p63s23p64s1。
【三维设计】2015高考化学(人教通用)一轮配套课件第11章 第4节 生命中的基础有机化学物质(共43张PPT)
分子式均为 C12H22O11 都能发生 水解反应
是否含醛基
不同点 水解产物
否
葡萄糖和果糖
是
葡萄糖
相互关系
互为同分异构体
4.淀粉与纤维素 (1)相似点: ①都属于天然 高分子化合物 ,属于多糖,分子式都表示
为 (C6H10O5)n 。 ②都能发生 水解 反应,反应的化学方程式分别为:
酸或酶 (C6H 10O5n+nH2O―――→nC6H12O6;
(
)
3.(2011· 上海高考)某物质的结构为 质的叙述正确的是 ( )
,关于该物
A.一定条件下与氢气反应可以生成硬脂酸甘油酯 B.一定条件下与氢气反应可以生成软脂酸甘油酯 C.与氢氧化钠溶液混合加热能得到肥皂的主要成分 D.与其互为同分异构且完全水解后产物相同的油脂有三种
1.解析:天然油脂均为混合物,不含其他杂质的天然油脂也属 于混合物;液态油脂含有不饱和烃基,能使溴水褪色;油脂 的烃基饱和程度越大,熔点越高。 答案:A
4.化学性质 (1)油脂的氢化(油脂的硬化)
经硬化制得的油脂叫人造脂肪,也称硬化油。 如油酸甘油酯与 H2 发生加成反应的化学方程式为:
。
(2)水解反应
①酸性条件下,如硬脂酸甘油酯水解反应的化学方程式为:
。 ②碱性条件下(即皂化反应),如硬脂酸甘油酯在 NaOH 溶
液中发生水解反应的化学方程式为:
2.解析:制备生物柴油的动植物油脂及短链醇可以再生,A 项 正确;生物柴油为不同酯类组成的混合物,B 项正确;动植 物油脂为高级脂肪酸的甘油酯,不是高分子化合物,C 项错 误;“地沟油”中含有油脂,可以用于制备生物柴油,D 项 正确。 答案:C
3.解析:从其结构简式可以看出,该物质属于油脂,且相应的高 级脂肪酸各不相同,因此选项 A、B 均不正确,而选项 C 正 确;与其互为同分异构且完全水解后产物相同的油脂有两种。 选项 D 不正确。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1.对社会热点的关注,如对环境的治理、新能源和新材料 的开发、诺贝尔奖相关成果„„ 2.要掌握一些重要的名词术语,如富营养化、光化学烟雾、 酸雨、温室效应、一级能源、二级能源等。
[角度一] 近年来,全球气候变暖给人类的生存和发展带 来了严峻的挑战,在此背景下,“新能源”、“低碳”、 “节能减排”、“吃干榨尽”等概念愈来愈受到人们的重
解析 :溶液中存在 Mg2 、 HCO 3 ,过滤后得到的沉淀应是
+ -
MgCO3,再煅烧生成 MgO。溶液中存在 Na 、Cl
+
-
2- 、SO4 等,
故只需检验滤液中是否存在这些离子即可。 硫酸钠的溶解度随 温度的变化比较大,而氯化钠的溶解度随温度的变化比较小, 因而应先析出硫酸钠,再蒸发结晶得到氯化钠。
- Cl-、SO2 4 )为原料制取高纯氧化镁的工艺流程如图所示:
(1)下表是反应温度对产品质量的影响情况:
温度/℃ 30 40 50 97.86 60 99.13 70 99.01
MgO质量分数/% 97.75 97.56
由此可知,由A煅烧生成MgO最适宜的温度为________,
原因是________________________________________。
答案:(1)60℃ (2)MgCO3
此温度下产品中 MgO 的质量分数最高
取最后一次洗涤液,加入少量盐酸酸化的
BaCl2 溶液,若无沉淀生成则已洗涤干净 (3)硫酸钠 氯化钠
高温H2O↑
解析:电解水法制取氢气会消耗大量的电能,不符合节能
要求;有节制地开采煤和石油等矿物资源,综合利用资源、
废旧塑料的回收利用,均符合节能减排要求。 答案:A
化工流程类试题选取的材料新、背景新,生产流程图 复杂,但问题设置比较简单。考生答题时不要力求把生产流 程图中每个细节都弄清楚,只需把握以下几条: 第一步,读懂工艺流程图,抓住物质流入、流出的方向,挖
掘反应条件及记录重要数据;
第二步,联系相关化学原理。即每步涉及的化学反应
或实验方法,涉及的化学原理如水解平衡原理等,还
要联系中学实验方法等; 第三步,在上述两步基础上,结合要回答的问题,分 析、判断得出正确答案。
[角度一] 海水是巨大的资源宝库,从海水中提取食盐和溴
的过程如下:
(1)请列举海水淡化的两种方法:__________、_________。 (2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、 ________、________或H2、________。
视。下列有关说法不正确的是 .
(
)
A.太阳能、地热能、生物质能和核聚变能均属于“新能源” B.“低碳”是指采用含碳量低的烃类作为燃料 C.右图甲烷经一氯甲烷生成低碳烯烃的 途径体现了“节能减排”思想 D.让煤变成合成气,把煤“吃干榨尽”,实现了煤的清洁、 高效利用
解析:低碳”实质上是指能源高效利用、清洁能源开发、追
答案:(1)蒸馏法、电渗析法、离子交换法及其他合理答案中的 任意两种 (2)Cl2 NaOH NaClO
(3)富集溴元素
- - (4)Br2+SO2+2H2O===4H++SO2 + 2Br 4
强酸对设备的严重腐蚀
[角度二]
(2011· 衡水模拟)氧化镁主要用于制备陶瓷和耐火
材料,医药上可用作抗酸剂。以卤水(主要含 Mg2+、Na+、
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目
的为__________________________________。 (4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应 的离子方程式为___________________, 由此反应可知,除环境保护外,在工业生产中应解决的主要
问题是_______________________________________。
解析:(1)海水淡化的常见方法有:蒸馏法、离子交换法、电渗 析 法 等 。 (2) 电 解 NaCl 溶 液 的 化 学 方 程 式 为 : 2NaCl + 电解 2H2O=====2NaOH+H2↑+Cl2↑,电解槽中若有阳离子交换 膜,则得到的产品是:NaOH、H2、Cl2;电解槽中若无阳离子 交换膜,产品中的 Cl2 与 NaOH 会发生反应生成 NaClO,得到 的产品是:H2、NaClO。(3)步骤Ⅰ中的 Br2 的浓度很小,多次 用 SO2 反复吸收,最终用 Cl2 处理,则可获得大量的工业溴。 (4)由于溴具有强氧化性可以氧化 SO2,生成 H2SO4,因此要注 意酸对设备的腐蚀问题。
(2)A的主要成分是________(填化学式),确定A已洗涤干净 的操作和现象是________________。 (3)物质B和C的主要成分分别是________、_______(写 名称)。
(4)写出碱式碳酸镁生成MgO的化学方程式:
_______________________________________________。
求绿色化学的问题,因此B错。 答案: B
[角度二]
节能减排与我们的生活息息相关,参与节能减排是
每一位公民应尽的义务。下列举措不符合这一要求的是
( )
A.为推广氢能的使用,工业上可采用电解水法制取大量氢气 B.将石油裂化、裂解,综合利用石油资源 C.有节制地开采煤、石油、天然气等矿物资源
D.将某些废旧塑料熔化后再成型
