无机合成与制备考题
无机物制备型实验综合题(解析版)-2025年高考化学

无机物制备型实验综合题建议完成时间:120分钟选择题:精选0题实际完成时间:分钟非选择题:精选12题1.(2025·河北·一模)氨基磺酸(H2NSO3H)是一种无味、无毒的固体强酸,可用于制备金属清洗剂等,微溶于乙醇,260℃时分解,溶于水时存在反应:H2O+H2NSO3H=NH4HSO4。
实验室用羟胺(NH2OH)和SO2反应制备氨基磺酸。
已知:NH2OH性质不稳定,室温下同时吸收水蒸气和CO2时迅速分解,加热时爆炸。
实验室常用亚硫酸钠粉末与75%硫酸制备SO2,根据下列装置回答相关问题:(1)仪器X名称为。
(2)气流从左至右,导管接口连接顺序为a→(装置可以重复使用)。
(3)实验过程中,先旋开(填“A”或“C”)装置的分液漏斗活塞,后旋开另一个活塞,其目的是。
(4)D装置可以用下列装置替代的是(填标号)。
a.盛装饱和食盐水的洗气瓶 b.盛装品红溶液的洗气瓶c.盛装碱石灰的U形管 d.盛装五氧化二磷的U形管(5)下列说法正确的是(填标号)。
a.C装置应采用热水浴控制温度b.本实验应在通风橱中进行c.实验完毕后,采用分液操作分离C装置中的混合物d.A装置中用饱和亚硫酸钠溶液替代亚硫酸钠粉末可以加快化学反应速率(6)产品纯度测定。
取w g氨基磺酸溶于蒸馏水配制成100mL溶液,准确量取25.00mL配制溶液于锥形瓶中,滴加几滴甲基橙溶液,用cmol⋅L-1标准NaOH溶液滴定至终点,消耗NaOH溶液的体积为V mL。
产品纯度为(用含w、c、V的代数式表示)。
若选用酚酞溶液作指示剂;测得结果(填“偏高”“偏低”或“无影响”)。
【答案】(1)三颈烧瓶(2)f→g→d→e→f→g→b(3)A将装置中的空气排尽(4)d(5)b(6)38.8cvw%偏高【详解】(1)根据仪器构造,可知仪器X的名称是三颈烧瓶;(2)依题意,必须先制备干燥的二氧化硫,否则产品会混有杂质硫酸氢铵。
用氢氧化钠溶液吸收尾气,要防止氢氧化钠溶液中的水蒸气入装置C,故装置排序为a→f→g→d→e→f→g→b;(3)装置C中反应之前要排尽装置内CO2、水蒸气,即先旋开装置A中分液漏斗活塞,利用SO2将装置中空气排尽;(4)装置D中浓硫酸用于干燥SO2,吸收水,可选择装有五氧化二磷的U型管来替代装置D,a、b不能吸收水,c与SO2反应;故选d;(5)a.依题意,羟胺加热时会发生爆炸,a项错误;b.本实验有SO2产生,应在通风橱中进行,b项正确;c.氨基磺酸微溶于乙醇,采用过滤操作分离,c项错误;d.若用饱和亚硫酸钠溶液替代亚硫酸钠粉末,则相当于把浓硫酸稀释,不能加快反应速率,d项错误;故选b;(6)氨基磺酸(H2NSO3H)是一元强酸,与NaOH反应化学方程式为H2NSO3H+NaOH=H2NSO3Na+H2O,根据比例关系,产品纯度为c×v×10-3×10025×97w×100%=38.8cvw%;若用酚酞作指示剂,消耗氢氧化钠溶液增多,测得结果偏高。
全国卷第一道大题 无机化合物的制备
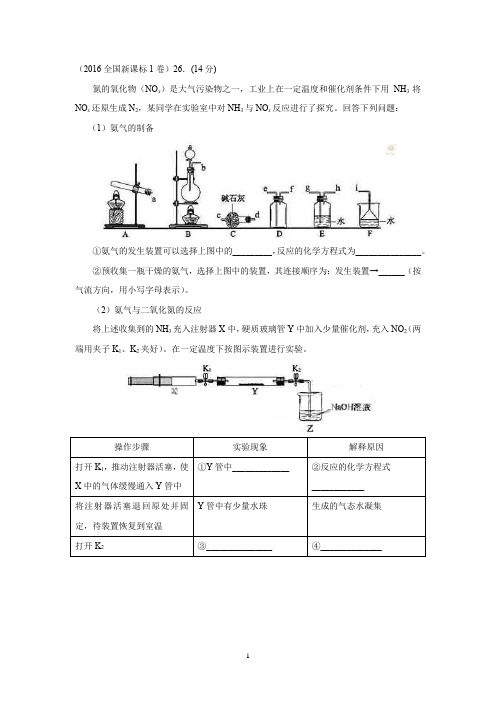
(2016全国新课标1卷)26.(14分)氮的氧化物(NO x)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NO x还原生成N2,某同学在实验室中对NH3与NO x反应进行了探究。
回答下列问题:(1)氨气的制备①氨气的发生装置可以选择上图中的_________,反应的化学方程式为_______________。
②预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→______(按气流方向,用小写字母表示)。
(2)氨气与二氧化氮的反应将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。
在一定温度下按图示装置进行实验。
(2016高考全国新课标Ⅲ卷)26.(14分)过氧化钙微溶于水,溶于酸,可作分析试剂、医用防腐剂、消毒剂。
.以下是一种制备过氧化钙的实验方法。
回答下列问题:(一)碳酸钙的制备(1)步骤①加入氨水的目的是_______。
小火煮沸的作用是使沉淀颗粒长大,有利于____。
(2)右图是某学生的过滤操作示意图,其操作不规范的是______(填标号)。
a.漏斗末端颈尖未紧靠烧杯壁b.玻璃棒用作引流c.将滤纸湿润,使其紧贴漏斗壁d.滤纸边缘高出漏斗e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度(二)过氧化钙的制备(3)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,此时溶液呈____性(填“酸”、“碱”或“中”)。
将溶液煮沸,趁热过滤。
将溶液煮沸的作用是___________。
(4)步骤③中反应的化学方程式为________,该反应需要在冰浴下进行,原因是_________。
(5)将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是_______。
(6)制备过氧化钙的另一种方法是:将石灰石煅烧后,直接加入双氧水反应,过滤后可得到过氧化钙产品。
该工艺方法的优点是______,产品的缺点是_______。
2016无机材料合成与制备试卷A
中南林业科技大学课程考试试卷课程名称: 无机材料合成与制备;试卷编号: A 卷;考试时间:100分钟一、是非题(1分×10=20分,选全对或全错,计零分)1微波有很强的穿透力,微波加热时能深入到样品内部,其燃烧波首先从样品的表面向内部传播,最终完成微波烧结。
( × ) 2插层反应的特征是,要有一定的结构开放性,能允许外来原子或离子易于扩散进或逸出。
( √ ) 3用五个9纯度的晶体Se ,在氩气下(0.8ml/s),球与金属质量比在10的条件下球磨5h 就转变成非晶Se 。
( √ )4大块非晶合金的制备思路是均匀形核的推迟和非均匀形核的避免。
( √ )5磁控溅射可显著地提高溅射速率,可控制二次电子的运动,避免高能粒子对衬底的轰击,降低衬底温度,但靶材的利用率不高,一般低于40%。
( √ )6直接凝固成型是依靠有机单体交联形成高聚物,温度诱导絮凝成型是依靠分散剂的分散特性。
( × ) 7 Au 衬底上长Pb 单晶膜一般是薄膜的层状生长模式,在Si 表面沉积Bi 、Ag 一般是薄膜的层岛生长模式。
( √ )8反应温度低于200℃的固相反应为低热固相反应,反应温度介于200~600℃之间的固相反应为中热固相反应,反应温度高于600℃的固相反应为高热固相反应。
( × )9水热与溶剂热合成的体系一般处于非理想非平衡状态,在高温高压条件下,水或其它溶剂处于亚临界或超临界状态,反应活性提高。
( √ )10为了减少污染和节约用水,镉黄颜料的工业生产采用低热固相反应法,即镉盐和硫化钠的固态混合物在球磨机中球磨2~4小时。
( √ )11时间-温度-结晶的“3T 曲线”头部的顶点对应了析出晶体体积分数为 10-6时的最短时间。
( √ ) 12分子束外延是以蒸镀为基础的超薄层材料生长新技术,是超真空(10-8Pa)条件下的精控蒸发技术。
( √ ) 13沉积温度较高,原子的扩散得以进行得比较充分,形态T 和形态3型的生长称为高温热激活型生长。
无机合成与制备考题

《无机合成与制备化学》期末考试试卷B( 2008 —— 2009 学年第二学期)(闭卷 120 分钟)学号姓名专业年级重修标记□一、填空题(每空2分,共40分)1.固相反应与液相反应的主要差别可归为以下几点:;;等。
P672. 溶胶-凝胶合成过程为:分子态→聚合体→溶胶→凝胶→晶态或非晶态。
P103. 低温下的气体分离方法主要有:;;等。
P1054. 在高温高压水热体系中,水的性质将产生下列变化:。
蒸汽压变高;密度变低;表面张力变低;粘度变低;离子积变高。
P 1315. 目前用于光化学合成的光源主要是汞灯光源,依据汞灯中汞蒸气的压强,汞灯有三种类型。
(低压汞灯,中压汞灯和高压汞灯)。
P2406.由于石墨和金刚石都是由碳元素构成的,高压高温作用使它们发生了同素异型相转变,金刚石是石墨通过静高压高温直接合成值得的P1747.从溶液中生长晶体的最关键因素是控制溶液的过饱和度,其手段有改变温度,移去溶剂,控制化学反应等方式。
8. 表面与界面效应、小尺寸效应、量子尺寸效应及宏观量子隧道效应是纳米微粒与纳米固体的基本特性。
二、选择题 (只选1个正确答案,填在横线处,每题2分,共20分)1. 由于液氧、液氮、液氩的沸点比较接近,因此,用于贮存它们的贮槽基本相同,通常用 。
(A) 杜瓦瓶 (B )冷阱 (C)反应釜2.CVD 装置通常可以由气源控制部件、 、沉积控温部件、真空排气和压强控制部件等部分组成。
(A) MPCVD 反应器 (B )沉积反应室 (C) 金属蒸发器3. 该反应属于 。
(A) 光敏化反应 (B )光取代反应 (C) 光异构化反应4.可以通过静高压高温直接合成的是 。
(A) 富勒烯 (B ) 金刚石 (C) 巴基球5. 产生富勒烯笼外配合物的反应主要有四种,其中金属加成到富勒烯的连接六元环的烯式C-C 键上,形成 。
(A) η2-配位络合物 (B )μ2-配位络合物 (C) μ2- C60配位络合物6.下图为 装置示意图。
无机物的制备综合实验题

无机物的制备综合实验题1.物质制备流程2.气体发生装置(1)设计原则:根据制备原理(化学方程式)、反应物状态和反应所需条件、制取气体的量等因素来设计反应装置。
(2)气体发生装置的基本类型制取装置可用来制取的气体反应原理固+固――→△气O 22KClO 3=====MnO 2△2KCl +3O 2↑ NH 32NH 4Cl +Ca(OH)2=====△CaCl 2+2NH 3↑+2H 2O固+液――→△气Cl 2MnO 2+4HCl(浓)=====△MnCl 2+Cl 2↑+2H 2OHClNaCl +H 2SO 4(浓)=====△NaHSO 4+HCl ↑固(块状)+液―→气H 22H ++Zn===H 2↑+Zn 2+CO 2 CaCO 3+2HCl===CaCl 2+CO 2↑+H 2O固+液―→气 O 2、H 2、CO 2、NH 3、Cl 2、SO 2 O 2:H 2O 2与MnO 2 H 2:Zn 与稀硫酸CO 2:CaCO 3与稀盐酸 NH 3:浓氨水与CaO Cl 2:浓盐酸与KMnO 4 SO 2:亚硫酸钠与硫酸3.气体的净化(干燥)装置(1)设计原则:根据主要气体及杂质气体的性质差异来选择除杂试剂及除杂装置。
(2)除杂装置基本类型装置示意图适用范围试剂与杂质气体反应,与主要气体不反应;装置③用固体吸收还原性或氧化性杂质气体杂质气体被冷却后变为液体,主要气体不变为液体(3)吸收剂的选择选择吸收剂应根据被提纯气体的性质和杂质的性质而确定,一般情况如下:①易溶于水的气体杂质可用水来吸收;②酸性杂质可用碱性物质吸收;③碱性杂质可用酸性物质吸收;④水为杂质时,可用干燥剂来吸收;⑤能与杂质发生反应生成沉淀(或可溶物)的物质也可作为吸收剂。
4.尾气处理装置的选择a装置用于吸收溶解或反应速率不是很快的气体,如用NaOH溶液吸收Cl2、CO2等。
b装置用于收集少量气体。
c、d装置用于吸收极易溶且溶解很快的气体,如HCl、HBr、NH3等;其中d装置吸收量少。
无机物的制备

无机化合物制备流程题
3以1 000 kg含氧化铝36%的铝土矿为原料制取Al2(SO4)3;需消耗质量分数98%的 硫酸(密度1 84 g·cm-3)_____5_7_5_4L(保留一位小数); (4)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若 欲使制得的铵明矾和硫酸铝的物质的量之比为1∶1,则投料时铝土矿中的Al2O3 和H2SO4的物质的量之比为3_∶__1_0____。
请回答下列问题:
1__固__体_A_a_的lO__化2-_+_学__式C_O_为_2__+__S__2_i_HO____22_O___=_;Ⅲ=_=_中_H_通C__O入__3-足_+_量_A_C_l(_OO_2_H气__)体3_↓;发生反应的离子方程式为
(2)由Ⅴ制取铵明矾溶液的化学方程式为_A__l2_O_3_+__4_H__2S_O__4_+__2_N_H__3=_=__=________ _2_N__H_4_A_l_S_O__42_+__3_H__2O___,从铵明矾溶液中获得铵明矾晶体的实验操作依次为 (填操作名称蒸)发__浓__缩_____ 冷却结晶、过滤洗涤。
无机化合物制备流程题
③灼烧 焙烧、煅烧:改变结构;使一些物质能溶解,并使
一些杂质高温下氧化、分解
④控制反应条件的方法
2分离提纯阶段的常见考点
①调pH值除杂
a控制溶液的酸碱性使其某些金属离子形成氢氧化物沉淀
例如:已知下列物质开始沉淀和沉淀完全时的pH如下表所示
物质
开始沉淀
沉淀完全
Fe(OH)3
27
37
无机化合物制备流程题
4根据实验以及工业生产的实验要求;从下表中得出的最佳工艺条件为 ___B_____(填序号);
无机合成与制备化学题目

无机合成与制备化学题目一、填空题1.合成反应中常用作为反应能否进行的依据, 一般当其值在范围内时,表明可用于合成反应。
2.温度是沸石合成中重要的因素之一,高水含量的沸石一般要求,而低水含量的沸石一般要求。
3.碱金属与液氨反应后生成溶液。
该反应速率一般很慢,通常需要作为催化剂。
4.除水干燥剂的作用方式有和两种。
沸石分子筛属于型干燥剂,与其他脱水剂相比,其优点是。
5.固相化合物的合成反应中,其反应速度与产物层的厚度成比,为缩短反应时间,通常将阳离子制成,这种方法也叫做合成法。
6.金属簇合物与一般多核化合物的区别在于和。
7.合成反应中常用的调节反应速率的手段有,,,和。
8.使用干冰作为低温源时,为了提高致冷效果,需加入一些,常用的有。
9.高温固相合成反应中,1000℃以上的电热材料不能选用。
在实验室中通常是用法来制备的。
10.O311.在合成具有强还原性的特殊低价态化合物时,对溶剂和气氛的要求很高,这种要求一般是和,这是由于的原因。
12.用水热法合成Na-Si-Al-O 分子筛时,产物的孔径与有关,一般在时孔径较大。
13.化学气相沉积是利用在气相或气固界面上反应生成的技术。
14.一些物质本身在高温下会气化分解然后在沉积反应器稍冷的地方反应沉积生成等形式的产物。
15.金属有机化合物通常指含有的化合物,在许多方面B、Si、P和As元素有机化学类似于相关的金属有机化学。
16.主族金属和碳键的形成可大致分类为:、、、。
17.离子迁移产生的微波能损失与被解离的、和有关,并受离子与溶剂分子之间相互作用的影响。
18.获得等离子体的方法和途径是多种多样的,微波等离子体是靠的办法获得的。
19.在合成配位化合物时,加入辅助配体的作用主要有:,。
20.由三氯化铬与乙酰丙酮水溶液合成配合物时,在反应液中加入尿素的目的是。
21.分子筛表面具有,因而对极性分子有很大的亲和力。
22.延伸固体按连续的化学键作用的空间分布可分为___________、___________、___________。
无机合成与制备化学习题

无机合成与制备化学习题一,填空题1.等离子体中主要基元反应过程包括、、、。
2.主族金属有机化合物中金属利用ns和np轨道形成构型,由于不同,同周期两端元素易形成,非金属或类金属则形成。
3.纳米粒子呈现出许多奇异的特性,目前归结于,,,四方面效应。
4.根据固体中连续的化学键作用的分布范围,可将固体分为和两种。
5.制备各种各样的稀土固体材料,常采用和两种方式。
6.固相化学反应种类繁多,经研究发现低热固相化学具有,,,和等独有的规律。
7.真空泵通常采用,,和四个参量来表征其工作特性。
8.高压一般是指压力在0.1-500GPa或者500GPa以上的压力,根据压力作用的时间可将高压分为和两类。
9.金属有机配合物可采用,,,和等光化学反应进行合成。
10.高温是无机合成的重要手段,实验室中常采用,,等获得高温。
11.金属有机化合物通常指含有的化合物,可分为和两类。
12.凡是有固相参与的化学反应都可称为固相反应。
固相反应可分为,,,和四个阶段。
13.化学转移反应中常采用,和等作为传输剂。
14.光化学反应中反应物分子需要吸收的光子才能激发到激发态,所以光化学反应的比热反应的强。
15.1946年由于发明超高压装置和在高压物理学领域的突出贡献获得第四十六届物理学奖。
16.晶体的形成是在一定条件下发生的物质相变过程,它可分为和生长两个阶段。
17.粉体的表面修饰和改性常采用,,,和来改变粒子表面的物理化学性质。
18.实际上,沸石的晶体结构并不十分完美,普遍存在和,这两种缺陷可以在合成中得到控制。
19.按反应历程划分,沸石生长过程可以分为,和几个阶段,但在实际情况下这几个阶段并没有十分清楚的界限,是相互重叠的。
20.高温是无机合成的重要手段,为了进行高温无机合成,就需要、、等一些符合不同要求的产生高温的设备和手段。
21.低温技术的发展对推动许多尖端科学技术与学科的发展起到重要作用,在实验室中常采用等作为低温热源。
22.光化学反应的初级反应过程是反应分子吸收光子被激发的过程,其速率只与有关,与无关,表现为零级反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《无机合成与制备化学》
期末考试试卷B ( 2008 —— 2009 学年第 二 学期)
(闭卷 120 分钟)
学号 姓名 专业 年级 重修标记 □
一、填空题(每空2分,共40分)
1.固相反应与液相反应的主要差别可归为以下几点 : ; ; 等。
P67
2. 溶胶-凝胶合成过程为:分子态→聚合体→ 溶胶 → 凝胶→ 晶态或非晶态。
P10
3. 低温下的气体分离方法主要有: ; ; 等。
P105
4. 在高温高压水热体系中,水的性质将产生下列变化: 。
蒸汽压变高;密度变低;表面张力变低;粘度变低;离子积变高。
P 131
5. 目前用于光化学合成的光源主要是汞灯光源,依据汞灯中汞蒸气的压强,汞灯有三种类型 。
(低压汞灯,中压汞灯和高压汞灯)。
P240
6.由于石墨和金刚石都是由碳元素构成的,高压高温作用使它们发生了同素异型相转变,金刚石是石墨通过静高压高温直接合成值得的P174
7.从溶液中生长晶体的最关键因素是控制溶液的 过饱和度 ,其手段有改变温度,移去溶剂,控制化学反应等方式。
8. 表面与界面效应、 小尺寸效应 、量子尺寸效应及宏观量子隧道效应是纳米微粒与纳米固体的基本特性。
二、选择题 (只选1个正确答案,填在横线处,每题2分,共20分)
1. 由于液氧、液氮、液氩的沸点比较接近,因此,用于贮存它们的贮槽基本相同,通常用 。
(A) 杜瓦瓶 (B )冷阱 (C)反应釜
2.CVD 装置通常可以由气源控制部件、 、沉积控温部件、真空排气和压强控制部件等部分组成。
(A) MPCVD 反应器 (B )沉积反应室 (C) 金属蒸发器
3. 该反应属于 。
(A) 光敏化反应 (B )光取代反应 (C) 光异构化反应
4.可以通过静高压高温直接合成的是 。
(A) 富勒烯 (B ) 金刚石 (C) 巴基球
5. 产生富勒烯笼外配合物的反应主要有四种,其中金属加成到富勒烯的连接六元环的烯式C-C 键上,形成 。
(A) η2-配位络合物 (B )μ2-配位络合物 (C) μ2- C
60配位络合物
6.下图为 装置示意图。
22222222[()()][()()]hv cis Ru bipy H O trans Ru bipy H O ++
-←−→-
(A)化学转移反应制备Fe3O4单晶(B)微波等离子体合成金刚石反应
(C) 金属蒸汽法制备Co2(PF3)8反应装置
7.金属为导体,但纳米金属微粒在低温下会呈现绝缘性,这是引起的。
(A) 光电效应(B)量子尺寸效应 (C) 压电效应
8. 分子筛的主要特色在于这些晶体物质具有具有孔状或笼状的结构。
分子筛在工业上的应用主要表现为优越的和催化性能。
(A)吸附性能(B)磁学性能 (C) 化学稳定性
9.符号Mx@Cn所表示的是。
(A)(B) (C)
三、名词解释(每题2.5分,共10分)
1.化学转移反应;
2.光敏化反应;P252 ;
3.压电效应
4.纳米材料
四、简答题(每题5分共30分)
1. 化学气相沉积法有哪些类型?该法对反应体系有哪些要求? P259
2.微波加热和加速反应的机理是什么。
3.获得和测量真空的设备和仪表有哪些?
4.溶胶-凝胶(sol-gel)合成技术具有哪些优点P44,说明溶胶-凝胶(sol-gel)法的原理和基本步骤。
5. 简述影响固相反应速率的主要因素P38
6.碳素存在哪几种不同晶体形态?在结构上各有何特点?。
