有机化学课件
《有机化学》第二版全册教材完整课件

与金属反应
卤代烃可与金属镁、锌等反应生成相应的有 机金属化合物。
醇的结构和命名
醇的通式
R-OH,其中R为烷基。
命名规则
选择含有羟基的最长碳链作为主链,将羟基作为取代基进行编号,并注明羟基 的位置。
醇的物理性质
密度比水小。
能与水以任意比例互溶。
低级醇为无色液体,高级 醇为白色固体。
稠环芳烃的命名
以共用碳原子数最少的苯环 为母体进行命名,如萘、蒽 等。
稠环芳烃的结构
具有多个共轭的苯环结构, 稳定性较高。
稠环芳烃的物理性质
稠环芳烃的外观
通常为无色或淡黄色固体,具有特殊的气味 。
稠环芳烃的溶解性
不溶于水,易溶于有机溶剂如乙醇、乙醚等 。
稠环芳烃的熔沸点
随着分子量的增加和共轭体系的扩大,熔沸 点逐渐升高。
物理性质各异,多为无色或淡黄色液体或固体 具有不同的气味和溶解性
羧酸衍生物的化学性质
酰卤易水解生成羧酸和卤 化氢
酯在酸性或碱性条件下可 发生水解反应生成羧酸和 醇
酸酐易水解生成羧酸
酰胺在酸性或碱性条件下 可发生水解反应生成羧酸 和胺
谢谢聆听
在空气中完全燃烧生成二氧化碳和水。
03 烯烃和炔烃
烯烃的结构和命名
烯烃的通式
CnH2n,其中n≥2
烯烃的结构
含有一个或多个碳-碳双键的烃
烯烃的命名
选取含有双键的最长碳链作为主 链,从靠近双键的一端开始编号 ,双键的位置用阿拉伯数字表示 ,并用“烯”字结尾
烯烃的物理性质
常温下的状态
随着分子量的增加,由气态逐渐过渡到液态、固态
稠环芳烃的化学性质
有机化学课件

定义
烷烃是一类仅由碳和氢两种元素组成 的有机化合物,分子中的碳原子都以 单键相连,其余的价键均用于与氢原 子结合,达到“饱和”。
命名
根据碳链的长度,分别称为甲烷、乙 烷、丙烷等。对于含有支链的烷烃, 采用“基数命名法”,并标注支链位 置。
性质
烷烃具有较低的沸点、熔点和密度, 不溶于水,化学性质相对稳定,主要 发生取代反应。
醛、酮、醌
醌的分类和命名
醌是含有两个羰基的六元环状化合物,根据取代基的不同 ,醌可分为苯醌和萘醌等。醌的命名遵循系统命名法。
醌的物理性质
醌通常为固体,颜色较深,具有特殊的气味。
醌的化学性质
醌具有较高的化学稳定性,可发生亲电取代反应和亲核加 成反应等。
羧酸及其衍生物
羧酸的分类和命名
羧酸是羧基与氢原子和一个烃基相连的化合物,根据烃 基的不同,羧酸可分为脂肪酸和芳香酸。羧酸的命名遵 循系统命名法。
胺的化学性质
胺类化合物具有碱性,可以与 酸反应生成盐;同时胺类化合 物还具有还原性,可以被氧化
剂氧化。
重氮和偶氮化合物
重氮化合物的定义和性质
重氮化合物是一类含有重氮基(-N=N-)的有机化合物,具有不稳定 性,容易发生分解反应。
偶氮化合物的定义和性质
偶氮化合物是一类含有偶氮基(-N=N-)的有机化合物,通常为有色 物质,具有良好的染色性能。
醚的化学性质
醚可发生开裂反应、氧化反应等,其反应活性受氧原子和烃基结 构的影响。
醛、酮、醌
醛的分类和命名
醛是羰基与氢原子和一个烃基相连的化合物,根据烃基的不同, 醛可分为脂肪醛和芳香醛。醛的命名遵循系统命名法。
醛的物理性质
醛的沸点、熔点和密度等物理性质与烃类相似,但受羰基影响,其 性质有所差异。
有机化学课件
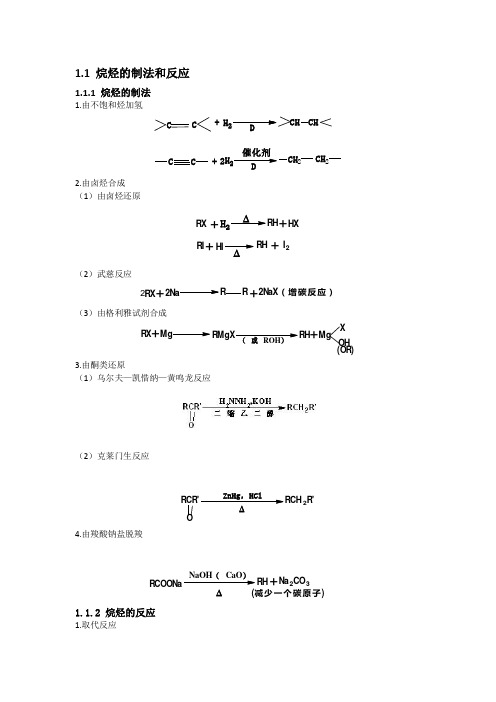
1.1 烷烃的制法和反应1.1.1 烷烃的制法1.由不饱和烃加氢C C+H 2CHCHCC+H 22D DCH 2CH 22.由卤烃合成 (1)由卤烃还原RX+H 2RHHX +RI HI+∆RH +I 2∆(2)武慈反应R X2+2N aRR2N aX (增碳反应)+ (3)由格利雅试剂合成RX+MgRMgX(或ROH )RH +MgX OH (OR)3.由酮类还原(1)乌尔夫—凯惜纳—黄鸣龙反应(2)克莱门生反应RCR'O2R'4.由羧酸钠盐脱羧NaOH (CaO )∆RH +Na 2CO 3(减少一个碳原子)1.1.2 烷烃的反应1.取代反应RH +X2光RX +HX (反应活性3'H>2'H>1'H>CH 4)例CH 3CH 2CH 3Cl 2光CH 3CH CH 3Cl+CH 3CH 2CH 2Cl(57%)(43%)2.氧化反应 (1)完全氧化CH 4+2O CO 2+2H 2O +热能(2)部分氧化RCH 2CH 2O 2,锰盐RCOOH +R'COOH (可制肥皂)4CH 4+O 21500C CH CH+2CO +7H 2O(3)裂化反应CH 3CH 2CH 2CH 3C H 2CH 2+C H 3CH 3+CH 3CH 2CH=CH 2+H 2+CH 4+CH 2CH 3(4)异构化反应CH 3CH 2CH 2CH 3AlBr 3 HBrCH 3CHCH 3CH 320%80%1.2 烯烃的制法和反应1.2.1烯烃的制法1 烷烃脱氢C C H H催化剂∆-H2C C (适合于简单烯烃,通常得混合物)CH3CH2CH2CH3Pt,500C CH3CH2CH=CH2+CH3CH3HH+CH3CH3H H+CH2=CHCH=CH2+H22.卤烷脱卤化氢C CX碱,热-HXC CHHHCl(CH3)3CO-K+3.醇脱水4.霍夫曼消除5.由炔烃加氢6.魏梯希反应1.2.2烯烃的反应1.烯烃的亲电加成(2)加水直接水合间接水合以上都符合马氏规律硼氢化-氧化反应(3)加卤素(4)加次卤酸2.烯烃的催化氢化CH3CH2H2,Pt CH3CH2CH33与碳烯加成CC+CC CC (X,Y=H,Cl,Br,I 或COOEt)+CHCl 3(CH 3)3COK+Cl4烯烃的氧化(1) 烯烃的环氧化C C+21O2CC OCH 2CH 2+21O 2O环氧丙烷C C+RCOOH C C O+RCOHCH 3CH CH 2+CH3OCH 2H 3CHCO+CH 3COOH(2) 高锰酸钾氧化C C稀KMnO OH C C (或OsO 4,H 2O 2)RCHCH KMnO R CO +CO 2+H 2OCH 3CH 2CH CH 2KMnO CH 3CH 2C O+CO 2+H 2OCR O+CR'OHORC RR C R'KMnOCH 3CHCCH 3CH 3KMnO 4CH 3COHO+CH 3CH 3O5烯烃的臭氧化反应C RR C R'+O 3OO COC RRR'H H 2ORO +CR'H ORCH 3CHCH CH 32Zn ,H 2OCH 3CHO +CH 3CH 3O6聚合反应nCH 2CH2>100℃,100MPaCH 2CH 2nn>100nCH 3CH CH 2烷基铝-三氧化钛50℃,1MPaCH3CH 2n7烯烃的a 氢原子反应(1) 卤代C Ha 氢+X 2C X+HX(或NBS)+NBSBr(2) 氧化烯烃的a氢易被氧化,在不同条件下,得到不同产物:CH 3CHCH 2+O 2CuO 370℃CH 2CHCHOCH 3CH CH 2+23O 磷钼酸铋 0.7~1.4MPa CH 2CHCOOHCH 3CHCH 2+NH 3+23O 2磷钼酸铋470℃2CHCN +3H 2O1.3 炔烃的制法和反应1.3.1 炔烃的制法1.金属炔化合物与卤烷反应RCC -Na ++R'XS N 2RCCR'+X -(1。
有机化学课件徐寿昌全精品PPT

根据IUPAC命名法,烷烃的命名基于其碳原 子数和结构。直链烷烃称为正烷烃,带有支 链的称为异烷烃。
物理性质
化学性质
烷烃通常为无色、无味、非极性的气体或液 体,不溶于水,易溶于有机溶剂。
烷烃的主要化学反应包括燃烧、卤化、裂化 等。
烯烃
定义与通式
烯烃是含有至少一个碳碳双键的 烃类化合物,通式为CnH2n。
机理
通常通过离子型或自由基型机理进行,与取 代反应和加成反应密切相关。
实例
乙醇在浓硫酸存在下发生消除反应,生成乙 烯和水。
重排反应
01
定义
有机分子中原子或基团的位置发生 重新排列的反应。
机理
通常涉及碳正离子、碳负离子或自 由基等中间体的形成和重排。
03
02
种类
频哪醇重排、贝克曼重排、霍夫曼 重排等。
有机化合物分类及命名
分类
按照碳架分类、按照官能团分类、按 照性质分类等。
命名
系统命名法、普通命名法、衍生物命名 法等,遵循IUPAC命名规则。
有机化学发展历史
早期历史
从天然有机物的提取和利用开始,如糖、油脂、染料等。
现代发展
合成有机化学的兴起,如塑料、橡胶、药物等人工合成有机物 的广泛应用。
有机化学在现实生活中的应用
物理性质
芳香烃通常为无色或淡黄色的液体或固体, 具有特殊的芳香气味,不溶于水,易溶于 有机溶剂。
命名与结构
芳香烃的命名基于其苯环数和取代基的种 类和位置。苯环是芳香烃的核心结构,具 有特殊的稳定性和芳香性。
化学性质
芳香烃的主要化学反应包括取代、加成、 氧化等。由于苯环的稳定性,芳香烃通常 比脂肪烃更难发生化学反应。
实例
有机化学概述课件

有机化学概述课件一、引言有机化学是研究碳原子与氢原子及其它元素原子之间化学键形成、断裂及转化的科学。
作为一门重要的自然科学学科,有机化学在生命科学、材料科学、环境科学等领域具有广泛的应用。
本课件旨在概述有机化学的基本概念、研究对象、研究方法及发展趋势,为初学者提供一个全面的有机化学知识框架。
二、有机化学基本概念1. 有机化合物:含有碳元素的化合物称为有机化合物,简称有机物。
有机化合物在自然界中广泛存在,如蛋白质、脂肪、糖类等生物大分子,以及石油、天然气等化石燃料。
2. 无机化合物:不含碳元素的化合物称为无机化合物。
无机化合物包括酸、碱、盐、氧化物等,如硫酸、氢氧化钠、氯化钠、二氧化碳等。
3. 同分异构体:分子式相同、结构不同的有机化合物互为同分异构体。
同分异构体的存在使得有机化学具有丰富的化学性质和反应类型。
4. 手性:手性是指分子或离子不能与其镜像重合的性质。
手性分子广泛存在于生物体内,如氨基酸、糖类等,手性对生物活性、药效等方面具有重要影响。
三、有机化学研究对象1. 碳骨架:碳原子之间通过共价键连接形成碳骨架,碳骨架分为链状和环状两种类型。
链状碳骨架包括直链和支链,环状碳骨架包括脂环和芳香环。
2. 官能团:官能团是有机化合物中具有特定化学性质的原子或原子团。
常见的官能团有羟基、羰基、羧基、氨基、卤素等。
官能团的种类和位置决定了有机化合物的性质和反应。
3. 有机反应:有机反应是有机化合物在一定条件下发生化学变化的过程。
有机反应类型繁多,包括加成反应、消除反应、取代反应、氧化还原反应等。
4. 生物大分子:生物大分子是有机化合物的重要组成部分,包括蛋白质、核酸、多糖等。
生物大分子的研究对揭示生命现象具有重要意义。
四、有机化学研究方法1. 提取与分离:从天然产物中提取有机化合物,并通过柱色谱、薄层色谱等方法进行分离纯化。
2. 结构鉴定:利用核磁共振、红外光谱、质谱等分析手段确定有机化合物的结构。
3. 合成方法:有机合成是有机化学的核心内容,包括经典有机合成、有机催化、不对称合成等。
有机化学(课件PPT)

一、烃 (一)有机物概述
1、有机化合物:指含碳元素的化合物,简称有机物 。(但CO、CO2、碳酸盐、金属碳化物等由于组 成、性质与无机物相似,属于无机物)
2、有机物的主要特点:熔点低、易燃、不易导电, 难溶于水,易溶于酒精、汽油、苯等有机溶剂。 有机反应比较复杂,反应速率慢,一般需加热和 使用催化剂,常伴有付反应,因而所得产品往往 是混合物。
3、乙烯的化学性质 (1)、加成反应:
有机物分子中双键或三键两端的碳原子于其 他原子或原子团直接结合生成新的化合物的反应
CH2=CH2+H2
CH3CH3
CH2=CH2+Br2 → CH2BrCH2Br
CH2=CH2+H2O
催化剂
→
CH3CH2OH
CH2=CH2+HCl → CH3CH2Cl
(2).氧化反应:
B.氧化反应:
C 4 2 H O 2 点 C 燃 2 2 O H 2 O
。 注意:先验纯再点燃
C.分解反应:
C4H 高 温 C 2 H 2
D.取代反应: 有机物分子里的某些原子或原子团被其他原子
或原子团所代替的反应。
C4 H C 2 l光 C3 C H H l Cl
3、有机物种类繁多的主要原因: 碳原子能与其他原子形成四个共价键,且碳原子 之间也能互相成键
(二)甲烷及烷烃 1、甲烷的结构、性质 (1)结构:分子式:CH4, 正四面体键角为109°28´, 非极性分子。 (2)物理性质:无色、无味的气体极难溶于水,密度 比空气轻 (3)化学性质:在通常情况下甲烷比较稳定跟强酸、 强碱或强氧化剂等一般不反应。 A.甲烷不能使溴水、酸性高锰酸钾褪色
现象:燃烧火焰明亮且有大量黑烟。
有机化学ppt课件完整版
重排反应通常发生在含有不稳 定结构或官能团的化合物中, 需要加热或加入催化剂。在重 排过程中,分子的骨架结构可 能发生变化。
重排反应在有机合成中具有重 要的应用价值,可以用于合成 具有特定结构或官能团的有机 化合物。同时,重排反应也是 研究有机化合物结构和性质的 重要手段之一。
08
有机化学在生活中的应 用
定义
特点
加成反应在有机合成中具有重要的应用价值,可以用 于合成各种烯烃、醇、醛、酮等有机化合物。
应用
加成反应通常发生在分子中的不饱和键上,需要一定 的反应条件和催化剂。
消除反应
定义
消除反应是指有机化合物分子中 失去一个小分子(如水、卤化氢
等),形成不饱和键的反应。
种类
包括脱水消除、脱卤化氢消除、 热消除等。
反应。此外,醇还可以与酸反应生成酯,是重要的有机合成原料。
酚类化合物结构与性质
结构特点 酚类化合物的分子中含有苯环和羟基(-OH)官能团,通 式为Ar-OH,其中Ar为苯基或其衍生物。
物理性质 酚类化合物一般为无色或淡黄色的固体或液体,具有特殊 的气味和较强的毒性。酚的熔点和沸点较高,易溶于有机 溶剂。
化学性质
03
可发生加成、氧化、还原等反应,如与氢气加成生成醇,被弱
氧化剂氧化成酸。
酮类化合物结构与性质
结构特点
羰基(C=O)两侧连接烃基或芳基,无双键性质。
物理性质
沸点较高、难溶于水、易溶于有机溶剂。
化学性质
主要发生加成和还原反应,如与氢气加成生成醇,被还原剂还原 成仲醇。
醌类化合物结构与性质
结构特点
04
醇、酚、醚类化合物
醇类化合物结构与性质
01
结构特点
高中化学有机化学ppt课件
03有机物主要由碳、氢元素组成,还可能含有氧、氮、硫、磷等元素;无机物则可能包含各种元素。
组成元素有机物分子结构复杂,具有同分异构现象;无机物分子结构相对简单。
结构特点有机物大多具有可燃性、难溶于水、反应速率较慢等性质;无机物性质各异,有些具有与有机物相似的性质。
性质特征有机物与无机物区别古代人们对天然动植物和矿物的利用,如木材、药材、染料等。
萌芽时期18世纪末至19世纪初,贝采利乌斯等化学家提出有机化学概念,并合成尿素等有机化合物。
创立时期19世纪中后期,合成染料、香料、药物等有机化合物的出现,推动了有机化学的快速发展。
发展时期20世纪以来,随着物理和化学方法的不断进步,有机化学在合成、结构、反应机理等方面取得了巨大成就。
现代时期有机化学发展简史有机化合物分类及命名分类根据碳骨架形状,有机化合物可分为链状化合物和环状化合物;根据官能团类型,可分为烃类、醇类、醛类、酮类、羧酸类等。
命名有机化合物的命名遵循一定的规则和原则,包括选取主链、编号原则、官能团优先顺序等。
常见的命名法有普通命名法、系统命名法和衍生命名法等。
01结构特点碳原子间以单键相连,其余价键被氢原子饱和。
02物理性质随碳原子数增加,沸点、熔点逐渐升高,密度逐渐增大。
03化学性质相对稳定,主要发生取代反应,如卤代反应。
含有一个或多个碳碳双键。
结构特点物理性质化学性质随碳原子数增加,沸点、熔点逐渐升高,密度逐渐增大。
较为活泼,可发生加成反应、氧化反应、聚合反应等。
030201含有一个或多个碳碳三键。
结构特点随碳原子数增加,沸点、熔点逐渐升高,密度逐渐增大。
物理性质非常活泼,可发生加成反应、氧化反应、聚合反应等。
化学性质1 2 3含有苯环或其他芳香环结构。
结构特点具有特殊芳香味,沸点、熔点较高,密度较大。
物理性质相对稳定,可发生取代反应、加成反应等。
化学性质芳香烃结构和性质卤代烃结构和性质卤代烃的分子结构由烃基和卤素原子组成,卤素原子与烃基通过共价键连接。
有机化学PPT课件
目录
• 有机化学简介 • 有机化学基础知识 • 有机化学反应 • 有机化学的应用 • 有机化学的未来发展
01 有机化学简介
有机化学的定义
总结词
有机化学是一门研究有机化合物 的组成、结构、性质、合成和反 应的学科。
详细描述
有机化学主要关注碳氢化合物及 其衍生物,即有机化合物,它们 是构成生命体的基本物质。
将有机化学与计算机科学、数学等学科交叉融合,利用计算机模拟和预测有机化学反应和 分子的性质,为有机化学研究和应用提供新的工具和手段。
THANKS FOR WATCHING
感谢您的观看
有机化学的发展历程
总结词
有机化学的发展经历了从天然有机化学到合成有机化学的演变,并不断推动着 人类社会的进步。
详细描述
早期的有机化学主要研究天然有机物,如动植物体内的化合物。随着科技的发 展,合成有机化学逐渐崛起,人们开始能够合成大量原本自然界不存在的有机 化合物,从而极大地丰富了人类的物质生活。
农业领域
1 2
农药合成
有机化学在农药合成中扮演着关键角色,通过设 计并合成新的农药分子,可以开发出更安全、更 有效的农药。
植物生长调节剂
有机化学也可用于合成植物生长调节剂,通过调 节植物生长代谢,提高作物产量和品质。
3
转基因作物
利用有机化学手段,可以修改作物的基因组,培 育出抗逆性更强、产量更高的转基因作物。
举例
乙醇被氧化生成乙醛。
04 有机化学的应用
医药领域
药物合成
有机化学在药物合成中发挥着重要作用,通过设计并合成新的有 机分子,可以开发出具有治疗作用的创新药物。
药物代谢
有机化学也涉及药物代谢的研究,了解药物在体内的代谢过程有助 于优化药物的疗效和降低副作用。
有机化学ppt课件完整版
有机化学ppt课件完整版目录•绪论•有机化合物的结构与性质•烃类化合物•烃的衍生物•有机合成与反应机理•生物活性有机化合物绪论碳氢化合物研究碳氢化合物(烃)的结构、性质、合成和反应机理。
碳氢化合物的衍生物研究烃的衍生物,如醇、醛、酮、羧酸、酯等有机化合物的结构、性质、合成和反应机理。
生命体系中的有机化合物研究生物体内的氨基酸、蛋白质、核酸、多糖等生命物质的结构、性质和功能。
经典时期19世纪初到20世纪初,以经验规律为指导,通过大量的实验总结出了许多有机化学的基本概念和原理。
萌芽时期从远古时期到18世纪,人们开始使用天然有机物,如木材、植物、动物等。
现代时期20世纪至今,以量子力学和统计力学为基础,发展出了现代有机化学的理论和方法,如分子轨道理论、价键理论、反应机理理论等。
环境领域有机化学在环境保护方面发挥着重要作用,如研究大气污染物、水体污染物的来源和治理方法等。
同时,有机化学也致力于开发环保材料和清洁能源。
材料领域合成纤维、塑料、橡胶等高分子材料广泛应用于服装、家居用品、交通工具等领域。
医药领域合成药物如抗生素、抗癌药物等对于治疗疾病具有重要意义。
同时,天然药物中提取的有效成分也是有机化学的研究对象。
农业领域合成农药和化肥对于提高农作物产量具有重要作用。
此外,生物农药和生物肥料的研发也需要有机化学的支持。
有机化学与生产生活的关系有机化合物的结构与性质碳原子通过四个共价键与其他原子或基团相连,形成复杂的有机分子结构。
碳原子的四价性键的极性空间构型碳原子与其他原子形成的共价键具有不同的极性,影响有机物的物理和化学性质。
有机化合物分子中的原子或基团在空间的排列方式不同,导致同分异构现象的产生。
030201有机化合物的结构特点03同分异构体的性质差异由于结构上的差异,同分异构体在物理性质、化学性质以及生物活性等方面表现出明显的不同。
01构造异构分子式相同但连接方式不同,如正丁烷和异丁烷。
02立体异构分子式相同、连接方式也相同,但空间构型不同,如顺反异构、对映异构等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
32-69-93-130
17
(1)取代基的命名
烃分子中的一个氢原子去掉后剩余的原子团称为基 团或取代基。 (1)烷烃去掉一个氢原子后的原子团叫某烷基
烃(alkynes)
• 烷烃: 烷烃(饱和烃)中, 碳和碳以单键相连, 通式
为CnH2n+2。
C3H8
CH3CH2CH3
32-69-93-130
4
烯烃
• 烯烃的碳链中含有碳碳双键,分子链中只有一个双 键的称为单烯烃,通式为 CnH2n。
• 含有两个双键的称为二烯烃,通式为CnH2n-2。 • 含有多个双键的称为多烯烃。
32-69-93-130
14
(5)“正”(n-)表示直链,“异”(iso-)表示具有(CH3)2CH-结 构的异构体,“新”(neo-)表示具有(CH3)3CCH2-结构的异 构体。
CH3(CH2)4CH3 正己烷
CH3CHCH2CH3 CH3
异戊烷
CH3CHCH2CH2CH3 CH3 CH3
CH3 C CH3 CH3
乙烯 CH2=CH2Fra bibliotek1,3-丁二烯
CH2=CH-CH=CH2
32-69-93-130
5
炔烃
• 炔烃的碳链中含有碳碳叁键,只含有一个叁键
的炔烃通式为CnH2n-2 。
名称 乙炔 丙炔 1-丁炔
分子式
C2H2 C3H4 C4H6
结构简式 CH CH
CH3C CH CH3CH2C CH
双键和叁键称为不饱和键,烯烃和炔烃属于不饱和烃。
21 CH2CH3
H3C CH CH2 34
5 CH CH2 CH3
CH2CH2CH3 6 78
3+5=8
78 CH2CH3
H3C CH CH2 65
4 CH CH2 CH3
CH2CH2CH3 321
4+6=10
32-69-93-130
22
第三步正确书写: 若烷基不止一次地作为支链出 现,应该用中文数字来表示相同烷基的数目,并用阿 拉伯数字指明每个烷基的位置。
n ftp地址: ftp:/// n 校内地址:10.71.33.252
课件上传专用/林旭锋
32-69-93-130
1
有机化学成绩评定(理论课)
项目
分(%)
1. 考勤
5
2. 作业、课堂练习
15
4. 期中考试
10
5. 期末考试
70
32-69-93-130
2
第2章 脂肪烃和脂环烃
23
次序规则
(1) 将各取代基的原子按原子序数大小排列,大者 为较优基团。有机化合物中常见的元素其顺序由大到小排 列如下: I>Br>Cl>S>P>F>O>N>C>D>H
(2)如果两个基团的第一个原子相同,则比较与它相
连的其它原子,比较时,按原子序数排列,先比较
最大的,若仍相同,再依次比较第二、第三个原
表示取代基位次的阿拉伯数字之间要用逗号分 开;阿拉伯数字与汉字之间用“-”半字线分开。
如果有几种不同的烷基连接在母体链上,按次序 规则从小到大的先后次序来命名(IUPAC命名法中取代 基按首位字母顺序排列)。
CH3
CH3CH2CHCHCH3 H3C CH
2,4-二甲基-3-乙基戊烷
CH3
32-69-93-130
1O
CH3
CH
C4O
2O
CH2
1O
CH3
3O CH3
1O
32-69-93-130
13
2.2 脂肪烃的命名
1.普通命名法 ( 1 ) 对 于 十 个 碳 以 内 的 脂 肪 烃 , 碳 数 用 天 干 —— 甲 、 乙 、 丙 、 丁、戊、己、庚、辛、壬、癸表示。 十一个碳及多于十一个碳的用中文数字表示。 (2)饱和烷以“烷”字结尾,相应的碳数放在“烷”字之前。 (3)含有双键的以“烯”字结尾,碳原子数分别放在“烯”之前。 (4)含有叁键的以“炔”字结尾,碳原子数分别放在“炔”字之前。
英文名称:2,3,5-trimethylhexane
32-69-93-130
27
123 4
5
876 5
4
CH3CH2CH2CH CH
CH3 6 CH2
7 CH2
6
78
3
21
CH CHCH3
CH3 CH3
8 CH3
1 确定主链: 有两个等长的最长链。
比侧链数: 一长链有四个侧链,另一长链有二个 侧链,多的优先。
32-69-93-130
9
构造,构造异构,碳架异构体,官能团位置异构
• 分子中各原子的连接方式和顺序称为构造。 • 由于分子中各原子的连接方式和顺序不同产生的异构
称为构造异构(constitutional isomerism)。
• 烷烃中的构造异构都是由于碳的连接顺序不同而产生
的,这样的异构体又称碳架异构体。
• 官能团在碳链中的位置不同所产生的异构,称官能团
位置异构。
32-69-93-130
10
碳架异构体,官能团位置异构都属于构造异构
CH3CH2CH=CHCH3
CH3CH2CH2CH=CH2
CH3CH2C=CH2
2-戊烯
1-戊烯
CH3 2-甲基-1-丁烯
官能团位置异构
骨架异构
构造异构
32-69-93-130
CH3C C 丙炔基
32-69-93-130
19
(4)烷烃中去掉两个氢原子后剩余的基团称为亚基, 从不同碳原子上去掉两个氢原子,应该标明去掉氢原 子的位置。
CH3CH
亚乙基;
CH2CH2
CH2CH2CH2
1,3-亚丙基
1,2-亚乙基
32-69-93-130
20
(2)烷烃的命名
第一步选择主链:
选择最长的连续碳链作为母体结构,称为某烷, 支链作 为取代基(即烷基);
子。如-CH2Cl与-CHF2,第一个均为碳原子,再按 顺序比较与碳相连的其它原子。在—CH2Cl中为—C ( Cl 、 H 、 H ) , 在 —CHF2 中 为 —C ( F、 F、 H) 。 Cl>F,故—CH2Cl>—CHF2。
32-69-93-130
24
(3)含有双键或叁键的基团,可认为连有两个或三 个相同的原子。
异己烷
新戊烷
CH3
CH3 C CH2 CH3 CH3
新己烷
CH3 CH2 CH CH2 正丁烯
CH3 C CH2 CH3
异丁烯
32-69-93-130
15
2. 系统命名法
• 系统命名法是由国际纯化学和应用化学联合会 (International Union of Pure and Applied
Chemistry,简称IUPAC)拟定的世界统一的有 机化合物命名原则,称为IUPAC系统命名法。 • 我国根据这个命名法,结合中文的特点,制定了中 文的命名原则。
11
烷烃的可能构造异构体数目
碳原子数
分子式
名称
可能异构 体的数目
4
C4H10
丁烷
2
8
C8H18
辛烷
18
30
C30H62
三十烷
4111×109
32-69-93-130
12
伯碳(氢)仲碳(氢)叔碳
• 只与一个碳原子相连的称为伯碳(或称一级碳原子),用1°C
表示,伯碳上所连的氢称为伯氢,用1°H表示。
32-69-93-130
16
有机化合物系统命名的基本格式
构型 + 取代基 + 母体
R, S; D, L; Z, E; 顺,反
取代基位置号 + 个数 + 名称 官能团位置号 (有多个取代基时,中文按顺 +名称 序规则确定次序,小的在前。 (没有官能团时 英文按英文字母顺序排列) 不涉及位置号)
iso, neo 参加比较
如果构造式中最长碳链不止一条时,则选择带有最多取 代基的一条为主链,命名时将烷基写在母体名称的前面,称为 某基某烷。
32-69-93-130
21
第二步给定编号:
如果烷基在母体碳链上可因位置不同而引起异构现象时,就 必须对母体碳链进行编号,并用阿拉伯数字指明烷基所连的碳原 子。
编号时,以离取代基最近的一端为1。
CH3
甲基
CH3CH2
乙基
CH3(CH2)16CH2
十八烷基
32-69-93-130
18
(2)烯烃去掉一个氢原子后的基团命名为某烯基
CH2 CH
CH3CH CH
乙烯基 1-丙烯基
CH2 CHCH2
烯丙基
CH2 C
CH3
异丙烯基
(3)炔烃去掉一个氢原子后的基团命名为某炔基
CH C 乙炔基
CH C CH2 炔丙基
32-69-93-130
26
1 23 456
6 54 321 CH3CHCH2CHCHCH3
CH3 H3C CH3
2, 4, 5 2, 3, 5
1 确定主链: 最长链为主链。 2 编 号: 第一行 取代基编号为2, 4, 5;
第二行 取代基编号为2, 3, 5;
3. 命
根据最低系列原则, 用第二行编号。 名: 中文名称:2,3,5-三甲基己烷
2 编 号: 第二行取代基编号2,3,4,5; 第一行取代基编号 4,5,6,7。根据最低系列原则, 选第二行编号
