289个仿制药质量和疗效一致性评价品种批准文号情况表
仿制药质量与疗效一致性评价参比制剂备案与推荐程序用表格汇总
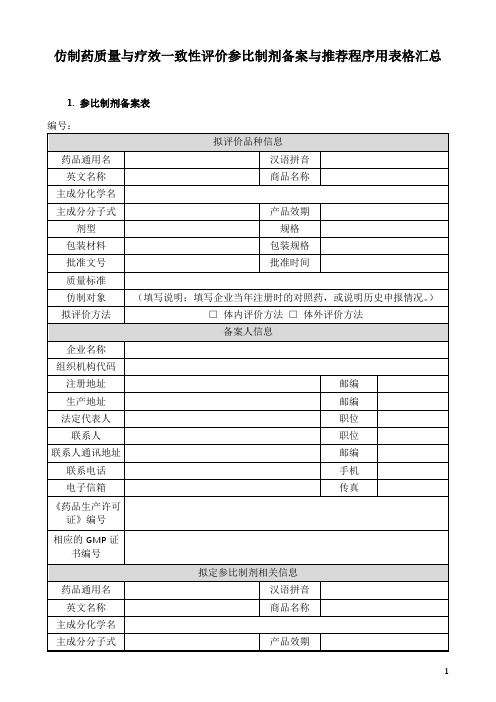
仿制药质量与疗效一致性评价参比制剂备案与推荐程序用表格汇总1. 参比制剂备案表注释:上述表格中事项均需填写,如不能填写,请在表格内说明原因。
2. 参比制剂推荐表注释:上述表格中事项均需填写,如不能填写,请在表格内说明原因。
3. 参比制剂申报表编号:注释:上述表格中事项均需填写,如不能填写,请在表格内说明原因。
综述资料1. 拟评价品种基本信息1.1 通用名称1.2 规格1.3 剂型2. 拟评价品种历史沿革与目前使用情况2.1 品种研发历史2.2 国外使用情况2.3 美国食品药品管理局《经过治疗等效性评价批准的药品》(橙皮书)和日本《医疗用医药品品质情报集》(橙皮书)参比制剂收载情况2.4 国内使用情况3. 拟评价品种国内上市情况3.1 国内该品种批准规格、文号情况3.2 原研产品进口情况3.3 原研地产化产品上市情况3.4 国际公认的同种药物进口情况3.5 国际公认的同种药物地产化产品上市情况4. 参比制剂选择结论5. 其他需要说明的问题6. 参考文献7. 附件(参考文献复印件)原研地产化产品申报口服固体制剂参比制剂资料要求一、原研产品和地产化产品的比较资料1. 品种概述1.1 原研产品和地产化产品历史沿革1.2 原研产品和地产化产品批准及上市情况1.3 原研产品和地产化产品临床信息及不良反应1.4 生物药剂学分类2. 产品比较2.1 处方比较2.1.1 原研产品处方2.1.2 地产化产品首次批准处方2.1.3 原研产品和地产化产品处方比较2.1.4 地产化产品上市后历次处方变更情况说明2.1.5 地产化产品上市后历次处方变更对质量和疗效影响的说明2.2 生产工艺比较2.2.1 原研产品生产工艺2.2.2 地产化产品首次批准生产工艺2.2.3 原研产品和地产化产品生产工艺比较2.2.4 地产化产品上市后历次生产工艺变更情况说明2.2.5 地产化产品上市后历次生产工艺变更对质量和疗效影响的说明2.3 原辅料控制比较2.3.1 原研产品原辅料控制2.3.2 地产化产品原辅料控制2.3.3 原研产品和地产化产品原辅料控制比较2.3.4 地产化产品上市后历次原辅料控制变更情况说明2.3.5 地产化产品上市后历次原辅料控制变更对质量和疗效影响的说明2.4 包装材料比较2.4.1 原研产品包装材料2.4.2 地产化产品包装材料2.4.3 原研产品和地产化产品包装材料比较2.4.4 地产化产品上市后历次包装材料变更情况说明2.4.5 地产化产品上市后历次包装材料变更对质量和疗效影响的说明2.5 质量控制比较2.5.1 原研产品和地产化产品的质量标准比较2.5.2 原研产品和地产化产品的分析方法比较2.5.3 原研产品和地产化产品的批检验报告比较2.5.4 原研产品和地产化产品的杂质谱比较2.6 稳定性比较2.6.1 原研产品稳定性数据2.6.2 地产化产品稳定性数据2.6.3 原研产品和地产化产品稳定性数据比较2.7 体外评价2.7.1 质量一致性评价2.7.1.1 申报产品和原产地产品的关键指标比较(影响一致性评价的关键参数,例如杂质分析、晶型等)2.7.2 申报产品和原产地产品的溶出曲线相似性评价2.7.2.1 体外溶出试验方法建立(含方法学验证)2.7.2.2 不同溶出仪之间结果差异考察2.7.2.3 批内与批间差异考察2.7.2.4 溶出曲线相似性比较结果(与原研产品的比较)3. 临床研究数据(包括生物等效性研究数据)3.1 原研产品临床研究数据3.2 地产化产品首次批准临床研究数据3.3 地产化产品历次注册变更临床研究数据4. 综合评价(原研产品与地产化产品一致性的综合评价)5. 参考文献6. 附件二、一致性评价申报资料(参照仿制药质量和疗效一致性评价申报资料要求提交)。
170825总局关于仿制药质量和疗效一致性评价工作有关事项的公告(2017年第100号)

总局关于仿制药质量和疗效一致性评价工作有关事项的公告(2017年第100号)颁布时间:20170825为做好仿制药质量和疗效一致性评价工作(以下简称一致性评价),现就有关事宜公告如下:一、为便于企业选择参比制剂,国家食品药品监督管理总局将把《关于落实〈国务院办公厅关于开展仿制药质量和疗效一致性评价的意见〉有关事项的公告》(2016年第106号)所附289个品种的原研企业药品列出清单并向社会公布,供企业选择参比制剂时参考。
清单分为已在中国境内上市和未在中国境内上市两类。
建议企业按以下顺序选择其一作为参比制剂备案:(一)原研药品:进口原研药品、经审核确定的原研企业在中国境内生产上市的药品、未进口原研药品;(二)在原研企业停止生产的情况下,可选择美国、日本或欧盟获准上市并获得参比制剂地位的药品。
对国家食品药品监督管理总局已公布的参比制剂,建议企业按照公布的参比制剂开展研究,未备案的无需再备案;对已公布的参比制剂存疑的,可向国家食品药品监督管理总局药品审评中心提出异议并说明理由,国家食品药品监督管理总局召开专家咨询委员会会议公开审议,并公开审议结果。
二、企业报国家食品药品监督管理总局备案的参比制剂全部向社会公开。
对国家食品药品监督管理总局未公布参比制剂的品种,由国家食品药品监督管理总局组织专家咨询委员会讨论后区别情况提出如下指导性意见:(一)可以确认符合参比制剂条件的;(二)存疑的;(三)明显不符合条件的。
对于(二)(三)两种情况是否继续进行研究或重新选择参比制剂,由企业自主决定并承担相应的责任。
三、企业自行从境外采购的参比制剂产品,在提交一致性评价资料时需提供购买凭证、产品包装及说明书等材料,或以其他适当方法证明所用参比制剂是标明企业的产品。
企业发现所使用的参比制剂产品为假冒产品的,应终止正在进行的研究工作,已申报的,应及时向国家食品药品监督管理总局药品审评中心报告并撤回一致性评价申请,视情况免于责任;监管部门发现企业使用的参比制剂产品为假冒产品的,应及时通报相关企业,终止审评审批;已批准上市的要撤销批准文件并向社会公开信息,责成企业作出解释并根据情况立案调查。
仿制药一致性评价289种基药名录

193 194 195 196 197 198 199 200 201 202 203 204 205 206 207 208 209 210 211 212 213 214 215 216 217 218
布洛芬颗粒 富马酸比索洛尔胶囊 枸橼酸铋钾片 华法林钠片 磷酸伯氨喹片 马来酸氨氯地平片 奈韦拉平片 齐多夫定片 双氯芬酸钠缓释胶囊 盐酸吗啡片 佐匹克隆片 法莫替丁胶囊 磷酸可待因片 羟基脲片 石杉碱甲片 头孢呋辛酯胶囊 盐酸左氧氟沙星胶囊 吲达帕胺缓释片 硫唑嘌呤片 阿莫西林克拉维酸钾颗粒 白消安片 布洛芬缓释片 富马酸喹硫平片 硫酸亚铁缓释片 氯化钾颗粒 鞣酸小檗碱片
2018年底前须完成仿制药一致性评价的289种药品名录
序号 1 2 3 4 5 药品通用名称 复方磺胺甲噁唑片 盐酸小檗碱片 诺氟沙星胶囊 甲硝唑片 红霉素肠溶片 规格 100mg:20mg(磺胺甲唑:甲氧苄啶) 400mg:80mg(磺胺甲唑:甲氧苄啶) 每片含盐酸小檗碱30mg 0.1g 0.2g 0.125g(12.5 万单位) 0.25g(25 万单位) 50mg 6 异烟肼片 100mg 300mg 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 利福平胶囊 维生素B6片 维生素B2片 盐酸雷尼替丁胶囊 布洛芬片 对乙酰氨基酚片 头孢氨苄胶囊 马来酸氯苯那敏片 阿司匹林肠溶片 卡托普利片 硝苯地平片 氨茶碱片 头孢拉定胶囊 碳酸氢钠片 阿莫西林胶囊 0.15g 0.3g 10mg 5mg 10mg 0.15g 0.1g 0.2g 0.5g 0.125g 0.25g 每片重0.37g(含马来酸氯苯那敏1mg) 0.3g 12.5mg 25mg 5mg 10mg 0.1g 0.2g 0.25g 0.5g 0.3g 0.5g 0.125g 0.25g
仿制药质量和疗效一致性评价

仿制药质量和疗效一致性评价仿制药质量和疗效一致性评价,是指通过临床试验和化学生物等多个方面的研究来评估仿制药与原研药在质量和疗效上的一致性。
该评价是确保仿制药产品质量和疗效与原研药相近或一致的重要手段,对于保证仿制药的安全性和有效性具有重要意义。
其次,仿制药疗效一致性评价是通过临床试验和生物等研究手段,来评估仿制药与原研药在疗效上的一致性。
临床试验应包括药代动力学、药效学和安全性等多个方面的评价指标,以确保仿制药在药物的吸收、分布、代谢、排泄等方面与原研药的相似性。
同时,还需进行临床试验来评估仿制药在治疗特定疾病时的疗效和安全性。
评价仿制药质量和疗效一致性的主要目的是确保仿制药在临床使用中的安全性和有效性。
如果仿制药与原研药在质量和疗效上存在显著差异,可能会给患者带来潜在风险,降低治疗效果,甚至导致治疗失败。
因此,对于仿制药的质量和疗效进行一致性评价,对于患者用药的安全和疗效至关重要。
为了完成仿制药质量和疗效一致性评价,需要建立完善的评价体系和标准。
评价体系应包括严格的化学分析、生物药剂学和临床试验等多个环节,确保评价结果的客观性和准确性。
评价标准应参考国家和国际药物注册要求,以确保评价结果符合规定的质量和疗效要求。
此外,评价过程中还应加强监管和监督,确保评价的科学性和有效性。
总之,仿制药质量和疗效一致性评价是保证仿制药质量和疗效与原研药相近或一致的重要手段。
通过严格的质量和疗效评价,可以确保仿制药的安全性和有效性,为患者提供高质量的药物治疗。
加强仿制药质量和疗效一致性评价的监管和监督工作,是保证仿制药市场良性竞争和患者用药安全的关键。
仿制药质量和疗效一致性评价品种分类的指导意见

附件仿制药质量和疗效一致性评价品种分类的指导意见(征求意见稿)为了进一步推动仿制药质量和疗效一致性评价(以下简称一致性评价)工作的开展,现对289 品种的分类情况提出如下指导意见:一、原研进口品种。
无需开展一致性评价,经仿制药质量和疗效一致性评价专家委员会审核确定和食品药品监管总局发布后,可选择为参比制剂。
二、原研企业在中国境内生产上市的品种(一)上市前按照与原研药品质量和疗效一致原则申报和审评的, 可列为参比制剂。
由企业在规定时间内,参照《化学药品仿制药口服固体制剂质量和疗效一致性评价申报资料要求(试行)》,向食品药品监管总局一致性评价办公室提交相关资料及证明性文件。
一致性评价办公室安排食品药品监管总局药品审评中心(以下简称药审中心)审核并出具意见,需进行研制现场检查、生产现场检查、临床试验核查的,由药审中心提出,食品药品监管总局食品药品审核查验中心具体实施,并反馈给药审中心。
依据药审中心意见,一致性评价办公室提出审批意见,报食品药品监管总局审核发布。
所提交资料不足以证明与原研药品质量和疗效一致的,可补充相关试验研究。
(二)未按照与原研药品质量和疗效一致原则申报和审评的,需按照有关规定开展一致性评价。
三、进口仿制品种。
上市前按照与原研药品质量和疗效一致原则申报和审评的,按照上述第二条第一款规定的程序执行;上市前未按照与原研药品质量和疗效一致原则申报和审评的,需按有关规定开展一致性评价。
四、国内仿制品种。
上市前按照与原研药品质量和疗效一致原则申报和审评的,按照上述第二条第一款规定的程序执行;未按照与原研药品质量和疗效一致原则申报和审评的,需按照有关规定开展一致性评价。
五、改规格、改剂型、改盐基的仿制品种需按照食品药品监管总局发布的相关指导原则开展一致性评价。
(一)改规格品种。
按照《仿制药质量和疗效一致性评价改规格药品评价一般考虑》(待发布)的要求,对不改变用法、用量、适应症的,且在治疗剂量范围内,药物呈现线性药代动力学特征,以改规格药品和参比制剂以相同剂量给药(单次给药剂量不超过最大给药剂量),进行生物等效性试验;对不满足上述条件的,应参照《仿制药质量和疗效一致性评价临床有效性试验一般考虑》(待发布,以下简称临床有效性试验一般考虑)的要求,开展临床有效性试验研究。
通过(视同通过)质量和疗效一致性评价仿制药(第三批)审
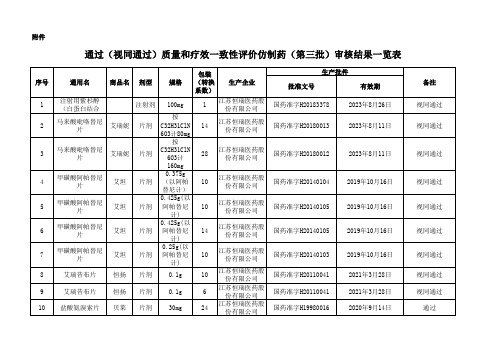
2023年5月22日
视同通过
1
海南普利制药股 份有限公司 石药集团欧意药 业有限公司 广东东阳光药业 有限公司 广东东阳光药业 有限公司
国药准字H20173261
2022年7月25日
通过
46 47 48
1 3 3
国药准字H20183044 国药准字H20183226 国药准字H20183246
2023年2月1日 2023年6月27日 2023年7月5日
56
盐酸舍曲林片
50mg
14
国药准字H20051076
2020年3月12日
通过
57 58 59 60 61 62
盐酸舍曲林片 恩替卡韦胶囊 苯磺酸氨氯地平 片 恩替卡韦分散片 恩替卡韦分散片 恩替卡韦分散片 安内真
50mg 0.5mg 5mg 0.5mg 0.5mg 0.5mg
28 7 21 7 14 28
3
艾瑞妮
片剂
28
国药准字H20180012
2023年8月11日
视同通过
4
艾坦
片剂
10
国药准字H20140104
2019年10月16日
视同通过
5
艾坦
片剂
10
国药准字H20140105
2019年10月16日
视同通过
6
艾坦
片剂
14
国药准字H20140105
2019年10月16日
视同通过
7 8 9 10
艾坦 恒扬 恒扬 贝莱
视同通过 视同通过 视同通过
序号 49 50 51 52 53 54 55
通用名 阿托伐他汀钙片 注射用还原型谷 胱甘肽 注射用还原型谷 胱甘肽 盐酸二甲双胍片 盐酸二甲双胍片 盐酸二甲双胍片 阿莫西林胶囊
仿制药一致性评价289种基药名录

序号 1 2 3 4 5
6
7 8 9 10 11 12 13 14 15 16
17
18
19
20
21
药品通用名称 复方磺胺甲噁唑片
盐酸小檗碱片 诺氟沙星胶囊
甲硝唑片 红霉素肠溶片
异烟肼片
利福平胶囊 维生素B6片 维生素B2片 盐酸雷尼替丁胶囊
布洛芬片 对乙酰氨基酚片 头孢氨苄胶囊 马来酸氯苯那敏片 阿司匹林肠溶片
胶体果胶铋胶囊
50mg(以铋计)
104
磷酸氯喹片
75mg 250mg
105
复方地芬诺酯片
盐酸地芬诺酯2.5mg,硫酸阿托品25μg
106
替硝唑片
0.5g
1mg
107
盐酸哌唑嗪片
2mg
108
口服补液盐散(Ⅰ)
已批准的所有规格
109
吲达帕胺片
2.5mg
110
乳酶生片
0.15g 0.3g
111
盐酸胺碘酮片
86
布洛芬胶囊
87
茶碱缓释片
88
阿奇霉素胶囊
89
螺内酯片
90
阿苯达唑胶囊
91
辛伐他汀片
92
制霉素片
30mg 已批准的所有规格
0.4mg 5mg 0.1g 25mg 5mg 10mg 20mg
0.25g 每袋含0.11g 铋
5mg 0.25g(25 万单位)
0.1g 2mg 4mg 50mg 100mg 0.25g 0.5g 8mg 40mg 10mg 20mg 0.1g 0.2g 0.1g 0.25g(25 万单位) 4mg 12mg 20mg 0.1g 0.2g 10mg 20mg 10 万单位 25 万单位 50 万单位
我国仿制药与原研药的一致性评价-文档

我国仿制药与原研药的一致性评价上海医药集团、华北制药、齐鲁制药等公司闻风而动,但大多数企业对如何开展该“评价”存在很多疑问,比如仿制药一致性评价所需对照品是否都必须采用原研药;国家对未来通过仿制药一致性评价的品种在药品招标、定价等方面有何区别政策;企业目前应如何开展工作等。
本文就仿制药存在的意义、仿制药质量评价和影响仿制药质量的因素,以及国家近期拟开展的仿制药与原研药的一致性评价工作等内容作一阐述,供医药工作者参考。
1仿制药不可或缺1.1 仿制药的定义、意义及市场地位仿制药是指原研药(又叫专利药)专利到期后原研制药企业之外的企业仿制该原研药而生产出的仿制品,又称非专利药。
根据国家食品药品监督XX局,XX局于2007年出台的《药品注册管理办法》,国家规定仿制药应在5 个方面与原研药达到一致,即活性成分、给药途径、剂型、规格、治疗作用。
与原研药相比开发仿制药所需投资少、周期短、见效快,符合我国的国情。
仿制药是全球巨大的社会公共财富,具有价格较低的优势,其在提升医疗服务水平、降低医疗支出、维护广大公众健康等方面具有良好的经济效益和社会效益。
比如我国恒瑞药业生产的多西他赛注射液(艾素)价格仅是原研药(泰素帝)的1/4[1] 。
因此,质量过硬、价格易于接受的仿制药成为众多患者的首选目前,无论是欧美制药发达国家,还是亚洲的一些新兴市场国家,仿制药均已成为药品消费的主流。
2009 年,全球处方药销售额已经突破8 000亿美元,虽然从销售金额上来看,仍然是品牌原研药为主,但从处方药的用量来看,仿制药已经完全占主导,大约为处方药总量的70%[2] 。
美国的药品市场是长期以创新药为主,仿制药为辅的市场,但随着医疗费用上涨,2003 年6 月18日美国FDA发布了“药品专利登记及新药申请(Abbreviated New Drug Application , ANDA停审期的管理规定”,这是促进仿制药发展及使用的新政策,主要为了鼓励仿制药快速面世并合理使用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
25
琥乙红霉素片
201
26
枸橼酸喷托维林片
201
27
醋酸泼尼松片
195
28
盐酸乙胺丁醇片
187
29
头孢氨苄片
181
30
尼群地平片
177
31
磺胺嘧啶片
168
32
地西泮片
166
33
利福平片
152
34
盐酸氯丙嗪片
139
35
卡马西平片
133
36
醋酸地塞米松片
122
37
盐酸二甲双胍片
116
38
盐酸环丙沙星片
15
140
秋水仙碱片
15
141
氟康唑片
14
142
格列吡嗪胶囊
14
144
硫酸亚铁片
14
145
甲巯咪唑片
14
146
枸橼酸他莫昔芬片
13
147
硝酸甘油片
13
148
盐酸苯海索片
13
149
碳酸锂片
13
150
氯雷他定胶囊
13
151
头孢呋辛酯片
13
152
盐酸特拉唑嗪片
13
153
吡嗪酰胺胶囊
12
154
丙戊酸钠片
12
108
39
盐酸异丙嗪片
107
40
盐酸普罗帕酮片
103
41
舒必利片
102
42
阿苯达唑片
102
43
苯妥英钠片
101
44
复方氢氧化铝片
101
45
头孢氨苄颗粒
100
46
葡萄糖酸钙片
99
47
盐酸克林霉素胶囊
98
48
盐酸多西环素片
98
49
甲氧氯普胺片
94
50
氢氯噻嗪片
90
51
阿替洛尔片
87
52
酚酞片
79
53
盐酸雷尼替丁片
26
114
丙硫氧嘧啶片
26
115
盐酸地尔硫䓬片
24
116
盐酸赛庚啶片
23
117
阿莫西林克拉维酸钾片
23
118
甲状腺片
23
119
阿昔洛韦片
22
120
己烯雌酚片
20
121
格列美脲片
20
122
环孢素软胶囊
20
123
阿奇霉素颗粒
19
124
甲硝唑胶囊
19
125
口服补液盐散(Ⅱ)
19
126
苯磺酸氨氯地平片
19
143
8
184
齐多夫定胶囊
8
185
佐匹克隆片
8
186
富马酸喹硫平片
8
187
硫酸吗啡缓释片
8
188
氨苯砜片
7
189
地红霉素肠溶胶囊
7
190
地塞米松片
7
191
多巴丝肼胶囊
7
192
氯化钾缓释片
7
193
尼尔雌醇片
7
194
巯嘌呤片
7
195
盐酸昂丹司琼片
7
196
乙胺嘧啶片
7
197
奈韦拉平片
7
198
劳拉西泮片
7
203
华法林钠片
169
地红霉素肠溶片
10
170
奥美拉唑肠溶片
9
171
利培酮片
9
172
柳氮磺吡啶肠溶片
9
173
蒙脱石散
9
174
盐酸氨溴索片
9
175
乳酸左氧氟沙星片
9
176
腺苷钴胺片
8
177
阿昔洛韦胶囊
8
178
氨茶碱缓释片
8
179
司莫司汀胶囊
8
180
替加氟胶囊
8
181
缬沙坦胶囊
8
182
盐酸二甲双胍肠溶片
8
183
多潘立酮片
马来酸依那普利片
18
127
对氨基水杨酸钠肠溶片
17
128
枸橼酸铋钾胶囊
17
129
氨苯蝶啶片
17
130
阿莫西林片
16
131
布洛芬缓释胶囊
16
132
醋酸甲羟孕酮片
16
133
氯硝西泮片
16
134
吡喹酮片
15
135
别嘌醇片
15
136
红霉素肠溶胶囊
15
137
酒石酸美托洛尔片
15
138
克拉霉素颗粒
15
139
盐酸多塞平片
4
229
阿莫西林克拉维酸钾片(7:1)
4
230
左甲状腺素钠片
4
231
奥美拉唑钠肠溶片
3
232
苯唑西林钠胶囊
3
233
琥乙红霉素胶囊
35
100
利巴韦林片
34
101
口服补液盐散(Ⅰ)
34
102
叶酸片
33
103
醋酸甲萘氢醌片
32
104
法莫替丁片
32
105
磷酸氯喹片
30
106
胶体果胶铋胶囊
29
107
复方地芬诺酯片
29
108
吲达帕胺片
29
109
替硝唑片
28
110
盐酸哌唑嗪片
28
111
盐酸左氧氟沙星胶囊
28
112
乳酶生片
26
113
盐酸胺碘酮片
423
11
布洛芬片
415
12
对乙酰氨基酚片
361
13
头孢氨苄胶囊
348
14
马来酸氯苯那敏片
309
15
阿司匹林肠溶片
309
16
卡托普利片
303
17
氨茶碱片
251
18
硝苯地平片
249
19
头孢拉定胶囊
246
20
碳酸氢钠片
231
21
阿莫西林胶囊
228
22
双氯芬酸钠肠溶片
205
23
双嘧达莫片
204
24
阿司匹林片
289个仿制药质量和疗效一致性评价品种批准文号情况表
(统计时间:2016年5月31日)
序号
品种名称
药品批准文号数量
1
复方磺胺甲噁唑片
895
2
盐酸小檗碱片
773
3
诺氟沙星胶囊
690
4
甲硝唑片
614
5
红霉素肠溶片
599
6
异烟肼片
568
7
利福平胶囊
532
8
维生素B6片
479
9
维生素B2片
464
10
盐酸雷尼替丁胶囊
盐酸左氧氟沙星片
62
70
阿普唑仑片
55
71
格列吡嗪片
55
72
诺氟沙星片
54
73
盐酸苯海拉明片
54
74
消旋山莨菪碱片
54
75
呋塞米片
50
76
盐酸乙胺丁醇胶囊
50
77
阿奇霉素片
50
78
枸橼酸铋钾颗粒
49
79
盐酸氟桂利嗪胶囊
49
80
盐酸金刚烷胺片
43
81
奋乃静片
43
82
氟康唑胶囊
43
83
盐酸环丙沙星胶囊
43
76
54
联苯双酯片
75
55
盐酸普萘洛尔片
75
56
格列本脲片
57
氯氮平片
74
58
奥美拉唑肠溶胶囊
74
59
硫酸阿托品片
72
60
呋喃妥因肠溶片
70
61
吡嗪酰胺片
68
62
克拉霉素胶囊
68
63
硝酸异山梨酯片
66
64
苯巴比妥片
65
65
阿莫西林颗粒
65
66
尼莫地平片
64
67
艾司唑仑片
63
68
复方利血平片
63
69
7
199
阿立哌唑片
6
200
布洛芬颗粒
6
201
富马酸比索洛尔胶囊
6
202
枸橼酸铋钾片
6
204
马来酸氨氯地平片
6
205
齐多夫定片
6
206
双氯芬酸钠缓释胶囊
6
207
盐酸吗啡片
6
208
法莫替丁胶囊
6
209
吲达帕胺缓释片
6
210
硫唑嘌呤片
6
211
硫酸氢氯吡格雷片
6
212
磷酸伯氨喹片
5
213
磷酸可待因片
5
214
155
米非司酮片
12
156
尼莫地平胶囊
12
157
