4-6理想液态混合物
合集下载
第四章,液体混合物与溶液

3. 化学势(chemical potential)
(1)
G G G dG dnB dT p dp n T p ,nB B T , n B B T , p , n
C
当组成不变时,
G dG SdT Vdp dnB n B B T , p ,nC
2.单选题: (1)1molA与 nmol B组成的溶液,体积为0.65 dm3 ,当xB = 0.8 时,A的偏摩尔体积VA=0.090dm3· -1,那么B的偏摩尔VB 为: mol (A) 0.140 dm3· -1 ; mol (B) 0.072 dm3· -1 ; mol (C) 0.028 dm3· -1 ; mol (D) 0.010 dm3· -1 。 mol
ΔG TΔS
1
ΔS2 ΔS1 ΔS 56.25J K
1
ΔG2 ΔG1 ΔG 298.15 56.25J 16.77kJ
(5)化学势与温度的关系
B SB,m T p,nB
4. 恒温下理想气体混合物化学势
(1)单组分纯理想气体
RT dGm Vmdp dp p
T Gm RT ln p
Gm RT ln p C
* (Pg) O (g) p RT dp O (g) RT ln( p / p O ) p O p
B
G T p ,nB T , p ,n
S
C
nB T , p ,n
S
B ,m
C
(3) 等温等压下, 系统内发生相变化或化学变化时, 有
物理化学:第4章_多组分系统热力学_
Vm*,B Vm*,C Vm*,B xC
真实混合物:实曲线
Vm xBVB xCVC VB (VC VB)xC
当混合物组成改变时,两组 分偏摩尔体积随之改变,且二者 变化相互关联。
组成接近某纯组分,其偏摩 尔体积也接近该纯组分摩尔体积。
5. 吉布斯 − 杜亥姆方程
对广度量 X (T , p, nB, nC , nD ,) 求全微分:
dX
X T
p,nB
dT
X p
T ,nB
dp
B
X nB
dnB T , p,nC
恒温、恒压
另一方面,由加和公式
,恒温恒压下求导:
比较两式,得
或
或
吉布斯-杜亥姆方程--在一定温度压力下,当混合物
组成变化时,各组分偏摩尔量变化的相互依赖关系。
➢ 系统中各组分的偏摩尔量并非完全独立,而是相 互依存的。
➢ 例:固体溶解、过饱和溶液析出、…
组分B在α、β两相中迁移达平衡的条件:该组分
在两相中的化学势相等。
➢ 物质总是从其化学势高的相向化学势低的相迁移, 直至物质迁移达平衡时为止,此时系统中每个组分在 其所处的相中的化学势相等。
化学势 判据
② 化学平衡
<0:自发不可逆; =0:平衡、可逆
任一化学反应,假定系统已处于相平衡,
任一组分B在每个相中的化学势都相等: Bα B
B
B
整个系统中B组分物质的量的变化量: dnBα dnB
α
BdnB
B
化学平衡时
平衡条件:与化学反应达到平衡的方式无关。
§4.3 气体组分的化学势
1、纯理想气体的化学势 2、理想气体混合物中任一组分的化学势 3、纯真实气体的化学势 4、真实气体混合物中任一组分的化学势
真实混合物:实曲线
Vm xBVB xCVC VB (VC VB)xC
当混合物组成改变时,两组 分偏摩尔体积随之改变,且二者 变化相互关联。
组成接近某纯组分,其偏摩 尔体积也接近该纯组分摩尔体积。
5. 吉布斯 − 杜亥姆方程
对广度量 X (T , p, nB, nC , nD ,) 求全微分:
dX
X T
p,nB
dT
X p
T ,nB
dp
B
X nB
dnB T , p,nC
恒温、恒压
另一方面,由加和公式
,恒温恒压下求导:
比较两式,得
或
或
吉布斯-杜亥姆方程--在一定温度压力下,当混合物
组成变化时,各组分偏摩尔量变化的相互依赖关系。
➢ 系统中各组分的偏摩尔量并非完全独立,而是相 互依存的。
➢ 例:固体溶解、过饱和溶液析出、…
组分B在α、β两相中迁移达平衡的条件:该组分
在两相中的化学势相等。
➢ 物质总是从其化学势高的相向化学势低的相迁移, 直至物质迁移达平衡时为止,此时系统中每个组分在 其所处的相中的化学势相等。
化学势 判据
② 化学平衡
<0:自发不可逆; =0:平衡、可逆
任一化学反应,假定系统已处于相平衡,
任一组分B在每个相中的化学势都相等: Bα B
B
B
整个系统中B组分物质的量的变化量: dnBα dnB
α
BdnB
B
化学平衡时
平衡条件:与化学反应达到平衡的方式无关。
§4.3 气体组分的化学势
1、纯理想气体的化学势 2、理想气体混合物中任一组分的化学势 3、纯真实气体的化学势 4、真实气体混合物中任一组分的化学势
大学物理化学--第四章

由两种或两种以上物质以分子,原子或离子为 基本单元相互均匀混合而成的均匀系统。
混合物(mixture):对系统中的各组分采用同样 的标准态和研究方法,系统中的各组分是平等的。
溶液(solution): 各组分区分为溶剂(solvent) 和溶质(solute ),并对二者采用不同的标准态和研 究方法;系统中的各组分是不平等的。
偏摩尔量
XB
(
X nB
)T
,
p
,
,下标必须是
nC
T
,
p。, nC
只有广度量才有偏摩尔量(质量除外)。
偏摩尔量是强度量。
偏摩尔量随温度、压力、组成(浓度)变化而变, 与系统的总量无关。
上一内容 下一内容 回主目录
返回
2020/8/23
§4.1 偏摩尔量
偏摩尔量的加和公式
X nB X B
B
它的含义是:在一定温度、压力下,一定组成混合
物理化学电子教案—第四章
多组分系统热力学
上一内容 下一内容 回主目录
返回
2020/8/23
第四章 多组分系统热力学
目录
§4.1 偏摩尔量 §4.2 化学势 §4.3 气体组分的化学势 §4.4 逸度及逸度因子 §4.5 拉乌尔定律和亨利定律 §4.6 理想液态混合物 §4.7 理想稀溶液
§4.8 活度及活度因子 §4.9 稀溶液的依数性
标准态 kb,B ( p p )
实际溶液 pB - bB 关系曲线
pB
O
b
上一内容 下一内容 回主目录
bB
返回
2020/8/23
4.7 理想稀溶液
理想稀溶液中溶质的化学势
B(溶 质)
0 B(溶 质)
混合物(mixture):对系统中的各组分采用同样 的标准态和研究方法,系统中的各组分是平等的。
溶液(solution): 各组分区分为溶剂(solvent) 和溶质(solute ),并对二者采用不同的标准态和研 究方法;系统中的各组分是不平等的。
偏摩尔量
XB
(
X nB
)T
,
p
,
,下标必须是
nC
T
,
p。, nC
只有广度量才有偏摩尔量(质量除外)。
偏摩尔量是强度量。
偏摩尔量随温度、压力、组成(浓度)变化而变, 与系统的总量无关。
上一内容 下一内容 回主目录
返回
2020/8/23
§4.1 偏摩尔量
偏摩尔量的加和公式
X nB X B
B
它的含义是:在一定温度、压力下,一定组成混合
物理化学电子教案—第四章
多组分系统热力学
上一内容 下一内容 回主目录
返回
2020/8/23
第四章 多组分系统热力学
目录
§4.1 偏摩尔量 §4.2 化学势 §4.3 气体组分的化学势 §4.4 逸度及逸度因子 §4.5 拉乌尔定律和亨利定律 §4.6 理想液态混合物 §4.7 理想稀溶液
§4.8 活度及活度因子 §4.9 稀溶液的依数性
标准态 kb,B ( p p )
实际溶液 pB - bB 关系曲线
pB
O
b
上一内容 下一内容 回主目录
bB
返回
2020/8/23
4.7 理想稀溶液
理想稀溶液中溶质的化学势
B(溶 质)
0 B(溶 质)
物理化学 第四章 多组分系统热力学

Vm
T,p一定
V*m,C VC
V*m,B VB
d c· b·
0 B
a xC
C
图4.1.2 二组分液态混合物的 偏摩尔体积示意图
若B,C形成真实液态混合物: 则混合物体积为由V*m,B至V*m,C的曲线。对于任一 组成a时,两组分的偏摩尔体积可用下法表示: 过组成点a所对应的系统体积点d作Vm-xC曲线的 切线,此切线在左右两纵坐标上的截距即分别 为该组成下两组分的偏摩尔体积VB,VC。
B
系统中各广度量的偏摩尔量: 对于多组分系统中的组分B,有: 偏摩尔体积: VB=(ƽV/ƽnB)T,p,n C 偏摩尔热力学能: UB=(ƽU/ƽnB)T,p,n C 偏摩尔焓: HB=(ƽH/ƽnB)T,p,n C 偏摩尔熵: SB=(ƽS/ƽnB)T,p,n C 偏摩尔亥姆霍兹函数:AB=(ƽA/ƽnB)T,p,n C 偏摩尔吉布斯函数: GB=(ƽG/ƽnB)T,p,n
C
几点说明: (1)偏摩尔量为两个广度性质之比,所以为强度 性质; (2)偏摩尔量的定义中明确是在恒温、恒压及系 统组成不变的条件下,偏导数式的下标为T,p 时才是偏摩尔量; (3)同一物质在相同温度、压力但组成不同的多 组分均相系统中,偏摩尔量不同; (4)若系统为单组分系统,则该组分的偏摩尔量 与该组分的摩尔量相等,即: XB=X*B,m
C
=VB (数学知识:二阶偏导与求导的顺序无关) 得证。
4.2化学势 4.2化学势
1.化学势的定义 混合物(或溶液中)组分B的偏摩尔吉布斯函数GB 定义为B的化学势,用符号μB表示:
μB = GB=(ƽG/ƽnB)T,p,n
def
C
对于纯物质,其化学势等于它的摩尔吉布斯函 数。
物理化学第四章 溶液

上一内容 下一内容 回主目录
返回
2012-3-17
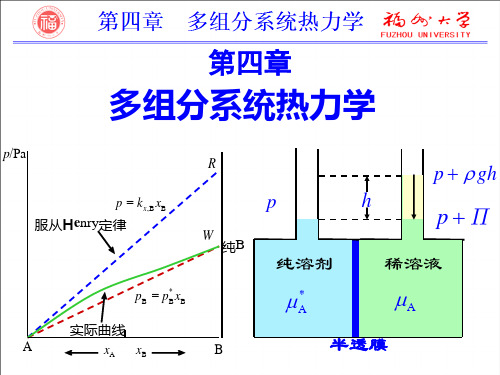
二、亨利定律
稀溶液上挥发性溶质的分压与溶质的摩尔分数成正 比。但比例常数不为pB*(1803年,Henry): pB=kx,B xB 换算浓度可有:pB=kc,B cB /c (c =1mol/L); pB=kb,B bB/b (b =1mol/kg); pB=k%,B[%B] 等。 k称为亨利系数,其值与T、p、溶剂、溶质以及溶液 组成的表示方法有关。 使用亨利定律要求溶质在气、液两相中的存在形态 相同。如水中NH3、HCl不能用,CO2只可近似应用。
∂∆ G ∆ mix S = − mix = − R ∑ nB ln xB ∂T p B
B
∂∆ mix G = 0 ∆ mixV = ∂p T
上一内容 下一内容 回主目录
∆ mix H = ∆ mix G + T ∆ mix S = 0
返回
2012-3-17
上一内容 下一内容 回主目录
返回
2012-3-17
三、偏摩尔量的的几个重要公式
1、集合公式 、 定T定p定组成条件下:
dZ = ∑ Z BdnB
nk
在保持偏摩尔量不变的情况下,对上式积分
Z = Z1 ∫ dn1 + Z 2 ∫ dn2 + ⋅ ⋅ ⋅ + Z k ∫ dnk
0 0 0 n1 n2
= n1 Z1 + n2 Z 2 + ⋅ ⋅ ⋅ + nk Z k
上一内容 下一内容 回主目录
返回
2012-3-17
三、拉乌尔定律与亨利定律的应用
1、用拉乌尔定律测定非挥发性溶质的摩尔质量M 、用拉乌尔定律测定非挥发性溶质的摩尔质量
返回
2012-3-17
二、亨利定律
稀溶液上挥发性溶质的分压与溶质的摩尔分数成正 比。但比例常数不为pB*(1803年,Henry): pB=kx,B xB 换算浓度可有:pB=kc,B cB /c (c =1mol/L); pB=kb,B bB/b (b =1mol/kg); pB=k%,B[%B] 等。 k称为亨利系数,其值与T、p、溶剂、溶质以及溶液 组成的表示方法有关。 使用亨利定律要求溶质在气、液两相中的存在形态 相同。如水中NH3、HCl不能用,CO2只可近似应用。
∂∆ G ∆ mix S = − mix = − R ∑ nB ln xB ∂T p B
B
∂∆ mix G = 0 ∆ mixV = ∂p T
上一内容 下一内容 回主目录
∆ mix H = ∆ mix G + T ∆ mix S = 0
返回
2012-3-17
上一内容 下一内容 回主目录
返回
2012-3-17
三、偏摩尔量的的几个重要公式
1、集合公式 、 定T定p定组成条件下:
dZ = ∑ Z BdnB
nk
在保持偏摩尔量不变的情况下,对上式积分
Z = Z1 ∫ dn1 + Z 2 ∫ dn2 + ⋅ ⋅ ⋅ + Z k ∫ dnk
0 0 0 n1 n2
= n1 Z1 + n2 Z 2 + ⋅ ⋅ ⋅ + nk Z k
上一内容 下一内容 回主目录
返回
2012-3-17
三、拉乌尔定律与亨利定律的应用
1、用拉乌尔定律测定非挥发性溶质的摩尔质量M 、用拉乌尔定律测定非挥发性溶质的摩尔质量
6-2二组分系统理想液态混合物的气—液平衡相图

二组分系统液态互溶情况:
(a)完全互溶
(b)完全不互溶 (c)部分互溶
液态完全互溶系统 p-x、t-x图
理想系统 真实系统
一般正偏差 最大正偏差
一般负偏差 最大负偏差
液态部分互溶系统 t-x图
气相组成介于两液相之间 气相组成位于两液相同侧
液态完全不互溶系统 t-x图
完全互溶系统:理想液态混合物系统气-液平衡相图
1. 压力—组成图
A、B形成理想液态混合物:均符合拉乌尔定律
A组分分压: pA pA* xA pA* 1 xB
B组分分压: pB pB* xB
pA,pB,p和xB均成
气相总压: p pA pB
直线关系
pA* 1 xB pB* xB
pA* pB* pA* xB
液相线:气相总压 p 与液相组成 xB 之间的关系曲线
nL
解: (1) 先确定系统点的总组成
xM
nB nA nB
6 46
0.6
利用
nG (xM yB ) nL (xB xM ) 即 nG (0.6 0.2) nL (0.7 0.6) (1)
nG nL n总 =4+6=10mol (2)
解得
nG =2mol
nL =8mol
(2) 气相中: 甲苯 nB nG yB 2 0.2 0.4mol 苯 nA nG yA 2 0.8 1.6mol
(4)最大负偏差系统
p实际 p理想
且在某一组成范围内比 难挥发组分的饱和蒸气 压还小,实际蒸气总压 出现最小值
液相线
氯仿(A)—丙酮(B)系统
加上气相线:
一般正偏差系统
一般负偏差系统
最大正偏差系统
液相线 气相线
(a)完全互溶
(b)完全不互溶 (c)部分互溶
液态完全互溶系统 p-x、t-x图
理想系统 真实系统
一般正偏差 最大正偏差
一般负偏差 最大负偏差
液态部分互溶系统 t-x图
气相组成介于两液相之间 气相组成位于两液相同侧
液态完全不互溶系统 t-x图
完全互溶系统:理想液态混合物系统气-液平衡相图
1. 压力—组成图
A、B形成理想液态混合物:均符合拉乌尔定律
A组分分压: pA pA* xA pA* 1 xB
B组分分压: pB pB* xB
pA,pB,p和xB均成
气相总压: p pA pB
直线关系
pA* 1 xB pB* xB
pA* pB* pA* xB
液相线:气相总压 p 与液相组成 xB 之间的关系曲线
nL
解: (1) 先确定系统点的总组成
xM
nB nA nB
6 46
0.6
利用
nG (xM yB ) nL (xB xM ) 即 nG (0.6 0.2) nL (0.7 0.6) (1)
nG nL n总 =4+6=10mol (2)
解得
nG =2mol
nL =8mol
(2) 气相中: 甲苯 nB nG yB 2 0.2 0.4mol 苯 nA nG yA 2 0.8 1.6mol
(4)最大负偏差系统
p实际 p理想
且在某一组成范围内比 难挥发组分的饱和蒸气 压还小,实际蒸气总压 出现最小值
液相线
氯仿(A)—丙酮(B)系统
加上气相线:
一般正偏差系统
一般负偏差系统
最大正偏差系统
液相线 气相线
中国石油大学华东物理化学课件溶液4-5
二、理想液态混合物中各组分的化学势 设 (A+B) 理 想 液 态 混 合 物 , 一 定 温 度 、 压 力
下达到气液平衡时:
对A组分 A (l) A (g)
ΘA (T )
RT
ln
pA pΘ
ΘA (T )
RT
ln
pA* xA pΘ
ΘA (T )
RT
ln
pA* pΘ
RT
ln
xA
A* (l) RT ln xA
RT ln xA(2) 2RT ln xB(2) 2RT ln xA(1) 2RT ln xB(1)
8.314
298(ln
1 3
2 ln
2 3
2 ln
1 2
2 ln
1 2
)J
2139.4J
∴ WR G 2139.4J
例4 20℃下,将压力为pΘ的1mol气态NH3溶解到大
量的物质的量之比为 nNH3 : nH2O 1: 21 的溶液中。
例3 在298.15K时,要从下列混合物中分出1mol纯A,试计算 Gibbs自由能的变化值及最少必须做功的值。 (1)大量的A 和B的等物质的量的混合物; (2)含A和B的物质的量各为2mol的混合物。 (p267 7题参考)
解:(1)
大量A和B混合物 T, p一定,G大量A和B混合物
nA : nB 1:1
GΘ m
NH3
Θ NH3
RT ln
pNH3 pΘ
8.314
293
.15
ln
3.6 101 .325
J
8134
J
问 题
0.5mol萘溶于1升苯中形成的溶液,与
0.25mol萘溶于0.5升苯中形成的溶液,二溶液
6-4相平衡-二组分理想液态混合物气液平衡相图
p* A3
p* As
p* B3
p* Bs
x B3 1.0
y B 3 1.0
3.绘图: T—XB线(紫)T—YB线(红)
§6-3二组分理想液态混合物气液平衡相图
四、温度——组成图(T—X图)分析 1.相图静分析:坐标、区、线、点 坐标:T,XB(YB) 区: 下线下边(浅蓝色区)
P=1、液相、F=2 上线上边(灰色区)
第六章 相平衡
§6-!本章基本要求 §6-1 相平衡系统基本概念 §6-2 单组分相平衡 §6-3二组分理想液态混合物气液平衡相图 §6-4二组分真实液态混合物液态完全互溶系统气液平衡相图 *§6-5 精镏原理 §6-6二组分液态部分互溶及完全不互溶系统气液平衡相图 §6-7二组分无中间化合物的凝聚系统相图 §6-8二组分有中间化合物的凝聚系统相图 *§6-9三组分系统相图简介 §6-$本章小结与学习指导
(上册)
第六章就先讲到这里 下节课再见!
LM G
§6-3二组分理想液态混合物气液平衡相图
二、压力——组成图(p—x图)分析 2.相图动分析: 压力不变往液体A中
加入B气体 组成不变改变压力
§6-3二组分理想液态混合物气液平衡相图
三、杠杆规则(物料衡算)
对二组分2相系统(如左下图气液2相):
中间M点称为系统点
L
M点组成XM,B称为系统组成
§6-3二组分理想液态混合物气液平衡相图
前面课程我们讲述了二组份系统的特征 1.描述二组分系统需要的三个独立变量,可以用三维坐标系表
示二组分系统相平衡 。 2.二组分系统若固定一个变量,就可以用二维坐标系表示相平
衡。 3主要讨论:确定温条件下的压力—组成图,确定压条件下的温
4-05理想液态混合物
结论 :对理想液态混合物的混合过程,有:
mixV = 0 mixH = 0 mixS = -RnBlnxB > 0 mixG = RTnBlnxB < 0
理想混合物中各组分B的标准态规定为: 温度为T, 压 力为p下的该组分纯液体。标准化学势 B(l)仅是温度的 函数。
3.理想液态混合物的混合性质
(1)mixV = 0 (2) mixH = 0 VB=Vm (体积不变) HB=Hm (焓不变) (熵增大) (吉布斯函数减少)
(3) mixS = -RnBlnxB > 0 (4) mixG = RTnBlnxB < 0
B( l )
B(l) p
μ B(l)
Vm, B dp p
dGm SmdT VmdP
B(l)
B(l)
V dp RT ln x B
p m,B
p
B(l)
B(l)
RT ln x B
近似为:
B B RT ln xB
(1)mixV = 0
(体积不变)
推导说明如下:
* * V ( n V n V ) ( n V n V 由理想液态混合物中任 mix B 意组分的化学势: B C C B m, B C m,C )
Gx ln B * BB B RT VB p T ,x 对上式在恒温恒组成下对压力求偏导得:
μ * μ B B p p 0 T ,x T
μ * μ B * B 因: V , V B m, B p p T ,x T
* 得 : VB Vm, B
4.6 理想液态混合物
将式(4.5.4)在恒温、恒组成条件下对 T 求偏导数。 在恒温、 求偏导数。 将式 在恒温
∗ ∗ ∂ µB + RT ln xB ∂µB ∂µB = = ∂T + R ln xB ∂T ∂T p , x p, x p, x
µB(l) = µB(g)
∗ pB = pB xB
不大, 若与液体平衡的蒸气压力 p不大,可以看作 不大 是理想气体混合物。则有: 是理想气体混合物。则有:
xB
µB(l)
pB = µB(g) = µB(g) + RT ln p
∗ 因为对理想液态混合物有: 因为对理想液态混合物有:pB = pB xB 代入上式后得
∆ mix S = −nR ∑ xB ln xB
B
其中: 其中:
n = ∑ nB
B
即在恒温、恒压下,由纯液体形成理想液态混合物时混合熵 即在恒温、恒压下,由纯液体形成理想液态混合物时混合熵 的计算公式,其实,与理想气体恒温、 的计算公式,其实,与理想气体恒温、恒压下混合熵的计算公式 是一样的。 是一样的。
∴ ∆ mixG = nRT ∑ xB ln xB
B
因为 xB < 1,所以 ∆mixG < 0 ;因为是恒温恒压非体 , 积功为零,所以过程自发 过程自发。 积功为零,所以过程自发。
∂ µB / T + R ln xB ∂ µB / T ∂ ( µB / T ) = ∂T = ∂T ∂T p , x p, x p, x
G ∂ T H = − 2 T ∂T p
(
)
(
)
已知有: 已知有:
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2. 理想液态混合物中任一组分的化学势:
T
pB pB xB
理想气体混合物
xB
理想液态混合物
根据相平衡判据:
pB pB xB
μ B ( l)
μ B ( pg)
μB(g) RT
ln
pB p
μB(g)
RT
ln
p*B xB p
μB(l) μB(g) RT ln( pB /p ) RT ln xB
nB XB
nB
X m, B
ΔmixG、Δmix S、Δmix H、ΔmixV、ΔmixU
(1)混合吉布斯函数变化:
ΔmixG nB GB nB Gm,B nB B nB Gm,B nB ( μB RTln xB ) nB Gm,B
f* AA
f* BB
f AB
② 各组分分子具有相似的形状和体积 V(A分子)=V(B分子)
严格的理想混合物是不存在的,但某些结构上的异构体 的混合物,可近似认为。
如:
同位素异构体:12CH3I与 13CH3I 紧邻同系物:苯,甲苯 光学异构体:R-(-)-乳酸与R-(+)-乳酸 结构异构体: o- 二甲苯与 p-二甲苯(对、邻)
B(纯 l,T, p )
μB (l)
B(纯 l, T, p )
μ
* B
(l)
dB dGB dGm* Vm*dp
B
p p
Vm*
(
B,
l
)dp
p
μ B (l)
μB(l)
Vm, B (l)dp
p
理想液态混合物中组分 B 的化学势与组成的关系为:
p
μB(l) μB(l) RT ln xB Vm*,B(l)dp
mix H 0
ΔmixU 0
ΔmixG RT nBln xB 1.719 kJ
B
mixS R
n ln B
xB
5.764J K1
p
在一般情况下,p 与 p 相差不大,所以可近似写作:
μB(l) μB(l) RT ln xB
μB(l)
μ B(l)
RT ln xB
均为化学势表达式
4. 理想液态混合物的混合性质
在恒温恒压下,形成理想液态混合物的过程中,系统热 力学性质 V,U,H,S,G在混合前后的变化。
定义: Δmix X
μB(l) μB(g) RT ln( pB /p ) RT ln xB
xB=
1
的纯液体 B:
μ* B (l)
μ* B (g)
μB(g)
RT
ln
p*B p
p
B
xB=1
μB(l)
μ B(l)
RT ln xB
液态混合物中组分 B 的标准态:指定温度,p 下的纯液
体。标准化学势为 μB(l)
B
这些结果对于理想气体的恒温、恒压 混合过程完全适用。
理 想
任一组分B的化学势
μB(l)
μ* B(l)
RTlnxB
μB(l)
μ B(l)
RTlnxB
液
态 混
ΔmixV 0 ΔmixH 0
合 物 理想液态混合物
ΔmixS 0 ΔmixG 0
的混合性质
ΔmixU 0 Δmix A 0
nBln xB
已知: G S T p
可得:
mixG T
p
mix S
mix S R
n B
ln
xB
mixS >0
能否作判据?
(3)混合热:
ΔmixG RT nBln xB
B
mixG mix H Tmix S
pB*
pB pC pD
p
T
B
xB 1 B xB
T
B
xB 1
T、p
例 p193 4-12
298K、100kPa下,由各为0.5mol的A和B混 合形成理想液态混合物。 求此混合过程的 ΔmixG、Δmix S、Δmix H、ΔmixV、ΔmixU
解 恒温恒压下,形成理想液态混合物
mixV 0
(5)混合热力学能:
Δmix H ΔmixU Δmix (PV) ΔmixU PΔmixV (6)混合亥姆霍兹函数:
ΔmixU 0
ΔmixG Δmix A Δmix (PV) Δmix A PΔmixV
Δmix A 0
Δmix A ΔmixG RT nBln xB
nBHB
n H B m, B
0
B
B
(4)混合体积:
将 ΔmixG RT nBln xB 在恒温、组成不变的条件下
B
对p 求偏导数:
mixG p
T
0
已知:
G p
T
V
可得:
mix p
G
T
mixV
mixV 0
由G-H公式
(G /T T
)
p
H T2
所以
B
(l,
T
T
)/T
p
得
B (l) T
/
T
p
,
xB
HB T2
HB
H m, B
B
(l)
/
T
T
p
H m, B T2
,得
mix H
§4.6 理想液态混合物
1. 理想液态混合物
定义:
任一组分在全部组成范围内都符合拉乌尔定律的液态混
合物称为理想液态混合物,简称为理想混合物。
pB=pB*xB 微观模型:
拉乌尔定律和亨利定律没有区别
① 同一组分分子之间与不同组分分子之间(二组分系统时
即 B – B、C – C及B – C)的相互作用力相同;
μB
G m, B
nB RTln xB RT nB ln xB
ΔmixG RT nBln xB
B
mixG < 0
能否作判据?
(2)混合熵:
将 ΔmixG RT nBln xB 在恒压、组成不变的条件下
B
对T 求偏导数:
mixG R
T p
mix S R
n B
ln
xB
mix H mixG Tmix S 0
mix H 0
在定压,组成恒定的条件下,将化学势对T求导,得
B (l)/T
T
p, xB
B(l, T
T
)/T
0
p, xB
