初三上册化学所有的化学方程式
化学九年级上册方程式

化学九年级上册方程式
1. 红磷燃烧:红磷这小家伙在氧气里一烧,就变成了五氧化二磷。
方程式是:4P + 5O₂点燃 2P₂O₅。
2. 硫燃烧:硫粉燃烧起来,和氧气结合生成二氧化硫,就像一场火热的约会!方程式:S + O₂点燃 SO₂。
3. 铁在氧气中燃烧:铁可真是个热情的家伙,在氧气里一烧,就变成了四氧化三铁。
方程式:3Fe + 2O₂点燃 Fe₃O₄。
4. 过氧化氢分解制取氧气:过氧化氢在二氧化锰这个“小助手”的帮助下,分解成水和氧气,就像变魔术一样!方程式:2H₂O₂ MnO₂ 2H₂O + O₂↑。
5. 氯酸钾受热分解制取氧气:氯酸钾在加热和二氧化锰的催化下,分解成氯化钾和氧气,努力地为我们产生氧气呢!方程式:2KClO₃加热 2KCl + 3O₂↑。
6. 高锰酸钾受热分解制取氧气:高锰酸钾加热之后,就分解成了锰酸钾、二氧化锰和氧气,这可是个大变身!方程式:2KMnO₄加热 K₂MnO₄ + MnO₂ + O₂↑。
7. 水通电分解:水通上电,就分解成了氢气和氧气,这电的力量可真神奇!方程式:2H₂O 通电 2H₂↑ + O₂↑。
8. 氢气燃烧:氢气和氧气一相遇,燃烧起来就生成了水,真是一场美丽的“结合”。
方程式:2H₂ + O₂点燃 2H₂O。
九年级上册化学化学方程式汇总

九年级上册化学化学方程式汇总化学方程式是化学学习中的重要内容,它用简洁的符号和式子准确地表达了化学反应的本质。
在九年级上册的化学学习中,我们接触到了许多重要的化学方程式,下面就为大家进行汇总。
一、氧气的性质1、红磷在空气中燃烧:4P + 5O₂点燃 2P₂O₅现象:产生大量白烟,放出热量。
2、硫在空气中燃烧:S + O₂点燃 SO₂现象:发出淡蓝色火焰,生成有刺激性气味的气体,放出热量。
硫在氧气中燃烧:S + O₂点燃 SO₂现象:发出明亮的蓝紫色火焰,生成有刺激性气味的气体,放出热量。
3、木炭在氧气中充分燃烧:C + O₂点燃 CO₂现象:发出白光,放出热量,生成能使澄清石灰水变浑浊的气体。
木炭在氧气中不充分燃烧:2C + O₂点燃 2CO4、铁丝在氧气中燃烧:3Fe + 2O₂点燃 Fe₃O₄现象:剧烈燃烧,火星四射,生成黑色固体,放出热量。
二、制取氧气1、过氧化氢分解制取氧气:2H₂O₂ MnO₂ 2H₂O + O₂↑2、氯酸钾受热分解制取氧气:2KClO₃ MnO₂、△ 2KCl +3O₂↑3、高锰酸钾受热分解制取氧气:2KMnO₄△ K₂MnO₄+MnO₂+ O₂↑三、水的电解2H₂O 通电 2H₂↑ + O₂↑现象:电极上有气泡产生,正负极产生的气体体积比约为 1:2 。
四、氢气的性质1、氢气在空气中燃烧:2H₂+ O₂点燃 2H₂O现象:产生淡蓝色火焰,放出热量。
五、碳的化学性质1、碳在氧气中充分燃烧:C + O₂点燃 CO₂2、碳在氧气中不充分燃烧:2C + O₂点燃 2CO3、碳还原氧化铜:C + 2CuO 高温 2Cu + CO₂↑现象:黑色粉末逐渐变成红色,生成能使澄清石灰水变浑浊的气体。
4、碳还原氧化铁:3C + 2Fe₂O₃高温 4Fe + 3CO₂↑六、二氧化碳的制取1、大理石(或石灰石)与稀盐酸反应:CaCO₃+ 2HCl = CaCl₂+ H₂O + CO₂↑2、碳酸钠与稀盐酸反应:Na₂CO₃+ 2HCl = 2NaCl + H₂O +CO₂↑七、二氧化碳的性质1、二氧化碳与水反应:CO₂+ H₂O = H₂CO₃现象:二氧化碳通入紫色石蕊试液,试液变红。
初三上册化学方程式大全

初三上册化学方程式大全一、氧气的性质1、镁在空气中燃烧:2Mg + O₂点燃 2MgO2、铁在氧气中燃烧:3Fe + 2O₂点燃 Fe₃O₄3、铜在空气中受热:2Cu + O₂加热 2CuO4、铝在空气中燃烧:4Al + 3O₂点燃 2Al₂O₃5、氢气中空气中燃烧:2H₂+ O₂点燃 2H₂O6、红磷在空气中燃烧:4P + 5O₂点燃 2P₂O₅7、硫粉在空气中燃烧: S + O₂点燃 SO₂8、碳在氧气中充分燃烧:C + O₂点燃 CO₂9、碳在氧气中不充分燃烧:2C + O₂点燃 2CO二、实验室制氧气1、加热氯酸钾(有少量的二氧化锰):2KClO₃加热 2KCl +3O₂ ↑2、加热高锰酸钾:2KMnO₄加热 K₂MnO₄+ MnO₂+ O₂↑3、过氧化氢在二氧化锰作催化剂条件下分解反应:2H₂O₂二氧化锰 2H₂O + O₂ ↑三、水的性质1、水在直流电的作用下分解:2H₂O 通电 2H₂↑+ O₂ ↑2、生石灰溶于水:CaO + H₂O == Ca(OH)₂四、二氧化碳的性质1、碳在氧气中充分燃烧:C + O₂点燃 CO₂2、二氧化碳通过灼热碳层: C + CO₂高温 2CO3、一氧化碳在氧气中燃烧:2CO + O₂点燃 2CO₂4、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO₂+H₂O === H₂CO₃5、碳酸不稳定而分解:H₂CO₃=== H₂O + CO₂↑6、二氧化碳通入澄清石灰水:Ca(OH)₂+ CO₂==== CaCO₃↓+ H₂O7、大理石与稀盐酸反应(实验室制二氧化碳):CaCO₃+ 2HCl == CaCl₂+ H₂O + CO₂↑五、燃料及其利用1、甲烷在空气中燃烧:CH₄+ 2O₂点燃 CO₂+ 2H₂O2、酒精在空气中燃烧:C₂H₅OH + 3O₂点燃 2CO₂+ 3H₂O这些化学方程式是初三上册化学中的重要知识点,需要同学们熟练掌握和理解。
九年级化学上册常见化学方程式
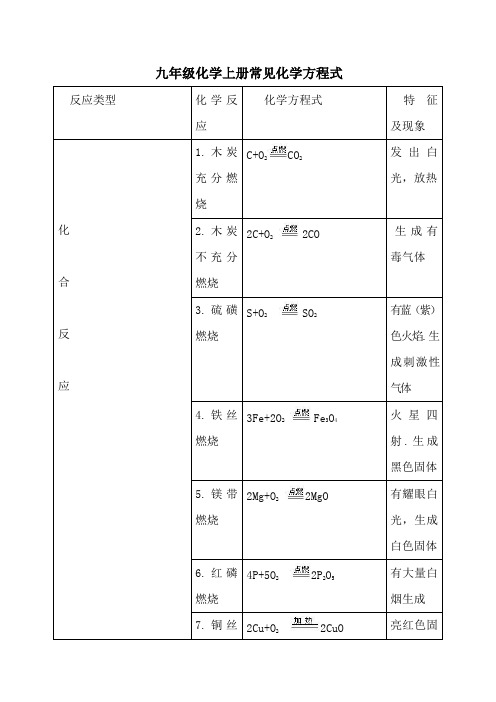
九年级化学上册常见化学方程式反应类型化学反应化学方程式特征及现象化合反应1.木炭充分燃烧C+O2CO2发出白光,放热2.木炭不充分燃烧2C+O2 2CO生成有毒气体3.硫磺燃烧S+O2 SO2有蓝(紫)色火焰.生成刺激性气体4.铁丝燃烧3Fe+2O2 Fe3O4火星四射.生成黑色固体5.镁带燃烧2Mg+O2 2MgO有耀眼白光,生成白色固体6.红磷燃烧4P+5O22P2O5有大量白烟生成7.铜丝2Cu+O22CuO亮红色固在空气中受热体变成黑色固体8.铝丝燃烧4Al+3O22Al2O3火星四射,生成白色固体9.氢气燃烧2H2+O22H2O有淡蓝色火焰10.有毒气体CO 燃烧2CO+O22CO2有蓝色火焰11.CO2和H2O反应CO2+H2O = H2CO3生成物能使石蕊变红12.CO2与C反应CO2+C 2CO所有物质中都含碳元素13.生石灰和水反应CaO+H2O = Ca(OH)2实验室制氢氧化钙,反应放热14.氢气与氯气H2+Cl2 2HCl剧烈燃烧,产生的反应苍白色火焰15.汞与氧气的反应2Hg+O22HgO 银白色液体变成粉红色固体分解反应16.氯酸钾制取氧气2KClO3 2KCl+3O2↑加热固体混合物制取氧气17.过氧化氢制氧气2H2O2 2H2O + O2 ↑常温下固液混合物制取氧气18.高锰酸钾制氧气2KMnO4K2MnO4+MnO2+O2↑加热纯净物制取氧气19.水电解2H2O 2H2↑+O2↑分解产生两种气体单质20.碳酸分解H2CO3= H2O+CO2↑碳酸不稳定21.碳酸钙煅烧CaCO3CaO+CO2↑工业制取二氧化碳22.氧化2HgO 2Hg+O2产生银白汞分解↑色液体金属23.碳酸氢钠受热分解2NaHCO3Na2CO3+CO2↑+H2O干粉灭火器的原理置换反应24.碳还原氧化铜C+2CuO 2Cu+CO2↑黑色固体混合物加热生成红色固体25.碳还原氧化铁3C+2Fe2O3 4Fe+3CO2↑固体混合物反应生黑色固体26.碳还原四氧化三铁2C+Fe3O4 3Fe+2CO2↑黑色固体混合物加热生黑色固体27.镁带与盐酸反应Mg+2HCl == MgCl2 +H2↑该反应放热28.氢气还原氧化铜H2+CuO Cu+H2O单质气体还原氧化铜,生红色原理酸氢盐遇酸生成CO234.苏打与稀盐酸反应Na2CO3+2HCl=2NaCl+H2O+CO2↑泡沫灭火器的原理35.硫酸铜与氢氧化钠反应CuSO4+2NaOH=Cu(OH)2↓+Na2SO4有蓝色沉淀生成其他36.乙醇燃烧C2H5OH+3O22CO2+3H2O 绿色燃料燃烧37.一氧化碳还原氧化铜CO+CuO Cu+CO2化合物的气体还原氧化铜38.一氧化碳还原氧化铁3CO+Fe2O32Fe+3CO2工业用赤铁矿炼铁39.一氧4CO+Fe3O43Fe+4CO2工业用磁化碳还原四氧化三铁铁矿炼铁40.甲烷燃烧CH4+2O2CO2+2H2O有蓝色火焰。
化学九年级上册全部化学方程式

化学九年级上册全部化学方程式1. 镁在空气中燃烧:2Mg + O2 =点燃= 2MgO2. 铁在氧气中燃烧:3Fe + 2O2=点燃= Fe3O43. 铜在空气中受热:2Cu + O2 =加热= 2CuO4. 铝在空气中燃烧:4Al + 3O2 =点燃= 2Al2O35. 氢气中空气中燃烧:2H2 + O2 =点燃= 2H2O6. 红磷在空气中燃烧(研究空气组成的实验):4P + 5O2 =点燃= 2P2O57. 硫粉在空气中燃烧:S + O2 =点燃= SO28. 碳在氧气中充分燃烧:C + O2 =点燃= CO29. 碳在氧气中不充分燃烧:2C + O2 =点燃= 2CO10. 一氧化碳在氧气中燃烧:2CO + O2 =点燃= 2CO211. 甲烷在空气中燃烧:CH4 + 2O2 =点燃=CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 =点燃= 2CO2 + 3H2O13.玻义耳研究空气的成分实验2HgO =加热= Hg+ O2 ↑14.加热高锰酸钾:2KMnO4 =加热= K2MnO4 + MnO2 + O2↑(实验室制氧气原理1)15.过氧化氢在二氧化锰作催化剂条件下分解反应:H2O2 (MnO2催化剂)=2H2O+ O2 ↑(实验室制氧气原理2)16.水在直流电的作用下分解(研究水的组成实验):2H2O =通电= 2H2↑+ O2 ↑17.生石灰溶于水:CaO + H2O == Ca(OH)218.二氧化碳可溶于水:H2O + CO2==H2CO319.镁在空气中燃烧:2Mg + O2 =点燃= 2MgO20.铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu21.氢气还原氧化铜:H2 + CuO =加热= Cu + H2O22. 镁还原氧化铜:Mg + CuO =加热= Cu + MgO23. 碳在氧气中充分燃烧:C + O2 =点燃= CO224.木炭还原氧化铜:C+ 2CuO =高温=2Cu + CO2↑25.焦炭还原氧化铁:3C+ 2Fe2O3 =高温= 4Fe + 3CO2↑26.煤炉的底层:C + O2 =点燃= CO227.煤炉的中层:CO2 + C =高温= 2CO28.煤炉的上部蓝色火焰的产生:2CO + O2 =点燃= 2CO229.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3 + 2HCl == CaCl2 + H2O + CO2↑30.碳酸不稳定而分H2CO3 == H2O + CO2↑31.二氧化碳可溶于水:H2O + CO2== H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3=高温= CaO + CO2↑33.石灰水与二氧化碳反应(鉴别二氧化碳):Ca(OH)2 + CO2 === CaCO3 ↓+ H2O34.一氧化碳还原氧化铜:CO+ CuO =加热= Cu + CO235.一氧化碳的可燃性:2CO + O2 =点燃= 2CO236.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑37.甲烷在空气中燃烧:CH4 + 2O2 =点燃= CO2 + 2H2O38.酒精在空气中燃烧:C2H5OH + 3O2 =点燃= 2CO2 + 3H2O 39.氢气中空气中燃烧:2H2 + O2 =点燃= 2H2O40.镁在空气中燃烧:2Mg + O2 =点燃= 2MgO41.铁在氧气中燃烧:3Fe + 2O2 =点燃= Fe3O442. 铜在空气中受热:2Cu + O2 =加热=2CuO43. 铝在空气中形成氧化膜:4Al + 3O2 = 2Al2O344. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑45. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑46. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑47. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3 H2↑48. 锌和稀盐酸Zn + 2HCl == ZnCl2 + H2↑49. 铁和稀盐酸Fe + 2HCl == FeCl2 + H2↑50. 镁和稀盐酸Mg+ 2HCl == MgCl2 + H2↑51.铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3 H2↑52. 铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu53. 锌和硫酸铜溶液反应:Zn + CuSO4 ==ZnSO4 + Cu54. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 == Cu(NO3)2 + Hg 55.3CO+ 2Fe2O3 高温4Fe + 3CO2↑56. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl ==2FeCl3 + 3H2O57. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 == Fe2(SO4)3 + 3H2O58. 氧化铜和稀盐酸反应:CuO + 2HCl ==CuCl2 + H2O59. 氧化铜和稀硫酸反应:CuO + H2SO4 == CuSO4 + H2O60.盐酸和烧碱起反应:HCl + NaOH == NaCl +H2O61. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 == CaCl2 + 2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 == AlCl3 + 3H2O63. 硫酸和烧碱反应:H2SO4 + 2NaOH == Na2SO4 + 2H2O64.大理石与稀盐酸反应:CaCO3 + 2HCl == CaCl2 + H2O + CO2↑65.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑66.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl== NaCl + H2O + CO2↑67. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 == BaSO4 ↓+ 2HCl 68.苛性钠暴露在空气中变质:2NaOH + CO2 == Na2CO3 + H2O 69.苛性钠吸收二氧化硫气体:2NaOH + SO2 == Na2SO3 + H2O 70.苛性钠吸收三氧化硫气体:2NaOH + SO3 == Na2SO4 + H2O 71.消石灰放在空气中变质:Ca(OH)2 + CO2 == CaCO3 ↓+ H2O72. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 == CaSO3 ↓+ H2O73. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH74. 铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu75.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑碳酸氢钠与稀盐酸反应:NaHCO3 + HCl== NaCl + H2O + CO2↑76. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 == CaCO3↓+ 2NaOH 77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 == AgCl↓+ NaNO3 78.硫酸钠和氯化钡:Na2SO4 + BaCl2 == BaSO4↓+ 2NaCl。
九上化学方程式大全

九上化学方程式大全一、燃烧反应(描述现象要点:光或火焰,放热,生成物的颜色、状、态气味) 1、碳充分燃烧:C+O 2 =点燃CO 2 (基本反应类型:化合反应) (空气中:红热)(氧气中:发出白光,放出热量,产生使石灰水变浑浊的无色气体) 2、碳不充分燃烧:2C+O 2 =点燃2CO (基本反应类型:化合反应) 3、硫燃烧:S+O 2 =点燃SO 2 (基本反应类型:化合反应)(空气中:淡蓝色火焰,放出热量,产生具有刺激气味的气体) (氧气中:蓝紫色火焰,放出热量,产生具有刺激气味的气体) 4、磷燃烧:4P+5O 2 =点燃2P 2O 5 (基本反应类型:化合反应) (产生大量白烟,P 2O 5污染空气) 5、铁燃烧:3Fe+2O 2=点燃Fe 3O 4 (基本反应类型:化合反应)(氧气中:剧烈燃烧,火星四射,放出大量热,生成黑色固体) (瓶底留少量水或细沙,防止溅落的高温熔化物炸裂瓶底。
) 6、镁燃烧:2Mg+O 2=点燃2MgO (基本反应类型:化合反应) (发出耀眼的白光,生成白色固体)7、氢气燃烧:2H 2+O 2 =点燃2H 2O (基本反应类型:化合反应) (产生淡蓝色火焰,干冷烧杯壁有小水株) 8、一氧化碳燃烧:2CO+O 2 =点燃2CO 2 (基本反应类型:化合反应) (产生蓝色火焰,产生使石灰水变浑浊的无色气体) 9、甲烷燃烧:CH 4+2O 2 =点燃CO 2+2H 2O (产生明亮的蓝色火焰) 10、乙醇燃烧: C 2H 5OH+3O 2 =点燃2CO 2+3H 2O 二、常见气体制备方程式 (一)制取氧气1、过氧化氢与二氧化锰混合制氧气:2H 2O 2 =MnO22H 2O + O 2↑ (基本反应类型:分解反应) 2、加热氯酸钾和二氧化锰制备氧气:2KClO 3 =MnO 2 △=2KCl+3O 2↑ (基本反应类型:分解反应) 3、加热高锰酸钾:2KMnO 4 =加热K 2MnO 4 + MnO 2 + O 2↑ (基本反应类型:分解反应) (棉花:防止高锰酸钾粉末堵塞导管)(先撤导管后灭酒精灯:防止水倒流回试管底部而炸裂试管) 4、加热氧化汞:2HgO =加热2Hg+O 2↑ (基本反应类型:分解反应)5、电解水:2H 2O =通电H 2↑+O 2↑ (基本反应类型:分解反应)(电极:正氧负氢;体积比:氢二氧一;质量比:氧八氢一;加入硫酸或氢氧化钠的目的:增强水的导电性) (二)制取二氧化碳1、石灰石跟稀盐酸反应制二氧化碳:CaCO 3 + 2HCl = CaCl 2 + H 2O+ CO 2↑(基本反应类型:复分解反应)2、碳酸不稳定:H 2CO 3 = H 2O+CO 2↑ (基本反应类型:分解反应) 3、高温煅烧石灰石:CaCO 3 =高温 CaO+CO 2↑(CO 2工业制法,基本反应类型:分解反应) (三)制取氢气 1、锌跟稀硫酸反应:Zn + H 2SO 4=ZnSO 4 + H 2↑(实验室制氢气,基本反应类型:置换反应)2、锌跟稀盐酸:Zn + 2HCl=ZnCl2+ H2↑(实验室制氢气,基本反应类型:置换反应)3、镁跟稀盐酸反应:Mg + 2HCl=MgCl2+ H2↑(基本反应类型:置换反应)三、其他方程式1、二氧化碳使澄清石灰水变浑浊(CO2的检验):Ca(OH)2+ CO2=CaCO3↓+ H2O2、二氧化碳溶于水:CO2+H2O = H2CO3 (基本反应类型:化合反应)(CO2通入紫色石蕊试液,试液由紫色变为红色)3、木炭粉跟氧化铜高温共热:C+2CuO=高温2Cu+CO2↑(基本反应类型:置换反应)(黑色粉末逐渐变红,生成能使澄清石灰水变浑浊的气体)4、木炭粉还原氧化铁:3C+2Fe2O3=高温4Fe+3CO2↑(基本反应类型:置换反应)5、一氧化碳还原氧化铜:CO+CuO =加热Cu+CO 2(要有尾气处理装置)6、H 2还原氧化铜:H 2+CuO =加热Cu+H 2O (基本反应类型:置换反应) (反应前先通一段时间气体:排尽装置中的空气或氧气;反应结束后继续通一段时间气体,直至试卷冷却至常温下:防止生成的Cu 重新被氧化成氧化铜)7、一氧化碳还原氧化铁(赤铁矿炼铁): 3CO+Fe 2O 3 =高温2Fe+3CO 28、一氧化碳还原四氧化三铁(磁铁矿炼铁): 4CO+Fe 3O 4=高温3Fe+4CO 2四、金属与盐溶液反应(基本反应类型:置换反应) 1.铁与硫酸铜溶液:Fe + CuSO 4 = Cu + FeSO 4 (湿法冶铜,不能用铁桶盛放硫酸铜溶液原理。
九年级上册所有化学公式

九年级上册所有化学公式一、氧气相关的化学方程式。
1. 镁在空气中燃烧。
- 化学方程式:2Mg + O_2{点燃}{===}2MgO- 现象:发出耀眼的白光,生成白色固体。
2. 铁在氧气中燃烧。
- 化学方程式:3Fe + 2O_2{点燃}{===}Fe_3O_4- 现象:剧烈燃烧,火星四射,生成黑色固体。
3. 铜在空气中受热。
- 化学方程式:2Cu+O_2{}{===}2CuO- 现象:红色固体变为黑色。
4. 铝在空气中氧化。
- 化学方程式:4Al + 3O_2===2Al_2O_3- 现象:铝表面变暗。
5. 氢气在空气中燃烧。
- 化学方程式:2H_2+O_2{点燃}{===}2H_2O- 现象:产生淡蓝色火焰,放出热量。
6. 红磷在空气中燃烧。
- 化学方程式:4P + 5O_2{点燃}{===}2P_2O_5- 现象:产生大量白烟。
7. 硫粉在空气中燃烧。
- 化学方程式:S+O_2{点燃}{===}SO_2- 现象:在空气中发出淡蓝色火焰,在氧气中发出蓝紫色火焰,生成有刺激性气味的气体。
8. 碳在氧气中充分燃烧。
- 化学方程式:C + O_2{点燃}{===}CO_2- 现象:发出白光,放出热量。
9. 碳在氧气中不充分燃烧。
- 化学方程式:2C+O_2{点燃}{===}2CO二、制取氧气的化学方程式。
1. 加热高锰酸钾制取氧气。
- 化学方程式:2KMnO_4{}{===}K_2MnO_4+MnO_2+O_2↑2. 加热氯酸钾和二氧化锰制取氧气。
- 化学方程式:2KClO_3frac{_MnO_2}{}2KCl + 3O_2↑3. 过氧化氢在二氧化锰的催化下分解制取氧气。
- 化学方程式:2H_2O_2frac{_MnO_2}{}2H_2O+O_2↑三、水相关的化学方程式。
1. 水的电解。
- 化学方程式:2H_2O{通电}{===}2H_2↑+O_2↑四、碳和碳的氧化物相关的化学方程式。
1. 木炭还原氧化铜。
初三上册化学方程式总结

初三上册化学方程式总结随着年级的升高,学业任务也越来越繁重。
所以知识更需要整理和总结了。
那么有同学问了初三上册化学方程式有哪些呢?下面是由小编为大家整理的“初三上册化学方程式总结”,仅供参考,欢迎大家阅读。
初三上册化学方程式总结一、物质与氧气的反应:1. 镁在空气中燃烧:2Mg + O2 点燃 2MgO2. 铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O43. 铜在空气中受热:2Cu + O2 加热 2CuO4. 铝在空气中燃烧:4Al + 3O2 点燃 2Al2O35. 氢气中空气中燃烧:2H2 + O2 点燃 2H2O6. 红磷在空气中燃烧:4P + 5O2 点燃 2P2O57. 硫粉在空气中燃烧: S + O2 点燃 SO28. 碳在氧气中充分燃烧:C + O2 点燃 CO29. 碳在氧气中不充分燃烧:2C + O2 点燃 2CO10. 一氧化碳在氧气中燃烧:2CO + O2 点燃 2CO211. 甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O二.分解反应:13. 水在直流电的作用下分解:2H2O 通电2H2↑+ O2 ↑14. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl + 3O2 ↑15. 加热高锰酸钾:2KMnO4 加热K2MnO4 + MnO2 + O2↑16. 碳酸不稳定而分解:H2CO3 === H2O + CO2↑17. 高温煅烧石灰石:CaCO3 高温CaO + CO2↑三.氧化还原反应:19. 氢气还原氧化铜:H2 + CuO 加热 Cu + H2O20. 木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温4Fe + 3CO2↑22. 焦炭还原四氧化三铁:2C+ Fe3O4 高温3Fe + 2CO2↑23. 一氧化碳还原氧化铜:CO+ CuO 加热 Cu + CO224. 一氧化碳还原氧化铁:3CO+ Fe2O3 高温 2Fe + 3CO225. 一氧化碳还原四氧化三铁:4CO+ Fe3O4 高温 3Fe + 4CO2四、其他反应26 实验室制CO2大理石与稀盐酸反应:CaCO3 + 2HCl === CaCl2 + H2O + CO2↑27. CO2与水反应:H2O + CO2 === H2CO328 检验二氧化碳的方法:Ca(OH)2 + CO2 ==== CaCO3 ↓+ H2O29. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑五.拓展资料元素符号及化学式:元素符号:气态非金属元素:氧 O 氢 H 氯 Cl 氮 N 氟 F固态非金属元素:碳 C 硅 Si 硫 S 磷 P 碘 I金属元素:钙 Ca 铁 Fe 钾 K 钠 Na 镁 Mg 铝 Cl 铜 Cu 锌 Zn 锰Mn银 Ag 汞 Hg 钡 Ba 金 Au 铂 Pt稀有气体元素:氦 He 氖 Ne 氩 Ar原子团:硫酸根 SO4 碳酸根 CO3 氢氧根 OH 硝酸根 NO3 铵根NH4离子:硫酸根离子SO42- 碳酸根CO32- 氢氧根OH - 硝酸根NO3- 铵根 NH4+物质的化学符号:单质:氧气 O2 氢气 H2 氯气 Cl2 氮气 N2 臭氧 O3 硫磺 S 木炭C 铁 Fe氧化物:二氧化硫SO2 二氧化氮NO2 一氧化碳CO 二氧化碳CO2 氧化镁MgO 四氧化三铁Fe3O4 二氧化锰MnO2 过氧化氢H2O2 五氧化二磷 P2O5 氧化铜 CuO 三氧化二铝 Al2O3化合物:氯酸钾KclO3 氯化钾KCl 锰酸钾K2MnO4 硫酸锌ZnSO4 硫酸 H2SO4硫酸镁 MgSO4 氢氧化钙 Ca(OH)2 硫酸铜CuSO4 碳酸钙 CaCO3 碳酸H2CO3 盐酸HCl 高锰酸钾KMnO4 酒精C2H5OH 甲烷CH4氯化钙 CaCl2拓展阅读:人教版九年级上册化学目录第一单元走进化学世界课题1 物质的变化和性质课题2 化学是一门以实验为基础的科学课题3 走进化学实验室第二单元我们周围的空气课题1 空气课题2 氧气课题3 制取氧气第三单元物质构成的奥秘课题1 分子和原子课题2 原子的结构课题3 元素第四单元自然界的水课题1 爱护水资源课题2 水的'净化课题3 水的组成课题4 化学式与化合价第五单元化学方程式课题1 质量守恒定律课题2 如何正确书写化学方程式课题3 利用化学方程式的简单计算第六单元碳和碳的氧化物课题1 金刚石、石墨和C60课题2 二氧化碳制取的研究课题3 二氧化碳和一氧化碳第七单元燃料及其利用课题1 燃烧和灭火课题2 燃料的合理利用与开发人教版九年级下册化学目录第八单元金属和金属材料课题1 金属材料课题2 金属的化学性质课题3 金属资源的利用和保护第九单元溶液课题1 溶液的形成课题2 溶解度课题3 溶液的浓度第十单元酸和碱课题1 常见的酸和碱课题2 酸和碱的中和反应第十一单元盐化肥课题1 生活中常见的盐课题2 化学肥料第十二单元化学与生活课题1 人类重要的营养物质课题2 化学元素与人体健康课题3 有机合成材料。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初三上册化学所有的化学方程式
1. 过氧化氢反应的方程式:2H2O2 → 2H2O + O2
2. 硝酸反应的方程式:HNO3 + NaOH → NaNO3 + H2O
3. 氯酸反应的方程式:HCl + NaOH → NaCl + H2O
4. 酸性固形物溶解反应的方程式:H2CO3 + H2O → H3O+ + HCO3–
5. 碳酸反应的方程式:H2CO3 → H2O + CO2
6. 烧碱反应的方程式:Na2CO3 + H2SO4 → Na2SO4 + H2O + CO2
7. 氧化性水溶液反应的方程式:MnO4–+ H2SO4 + H2O → Mn2+ + SO42– + H3O+
8. 氢氧化钠反应的方程式:2Na + 2H2O → 2NaOH + H2
9. 氯化钠溶液的方程式:NaCl + H2O → Na+ + Cl– + H2O
10.氧化铜溶液的方程式:Cu + O2 + H2O → Cu2+ + OH–
11.碳酸氢钠溶液的方程式:Na2CO3 + H2O → HCO3– + Na+ + OH–
12.醋酸反应的方程式:CH3COOH + H2O → CH3CO O– + H3O+
13.氯化钾反应的方程式:KCl + H2O → K+ + Cl– + H2O
14.硫酸反应的方程式:H2SO4 + NaOH → Na2SO4 + H2O
15.铁(II)硫酸根的反应的方程式:FeS2 + HCl → FeCl2 + H2S
16.还原酸反应的方程式:Fe3+ + H2C2O4 → Fe2+ + H2O + CO2
17.硝酸乙酯反应的方程式:C2H5ONO2 + H2O → C2H5OH + HNO3
18.甲醛的反应的方程式:CH2O + H2O → HCHO + H3O+
19.硫酸钡的反应的方程式:BaSO4 + H2SO4 → Ba2+ + SO42– + H2O
20.氧化锌的反应的方程式:Zn + O2 + H2O → Zn2+ + OH–。
