磷酸钙骨水泥作为药物缓释载体的研究进展
磷酸钙骨水泥药物缓释体系的研究应用

中国组织工程研究与临床康复第13卷第47期 2009–11–19出版Journal of Clinical Rehabilitative Tissue Engineering Research November 19, 2009 Vol.13, No.47 ISSN 1673-8225 CN 21-1539/R CODEN: ZLKHAH9317 1Department of Traumatic Orthopedics, Second Clinical College of Lanzhou University, Lanzhou 730000, Gansu Province, China; 2Department of Orthopedics, Lanzhou General Hospital of Lanzhou Military Area Command of Chinese PLA, Lanzhou 730050, Gansu Province, ChinaYe Xiang-yang★, Studying for master’s degree, Attending physician, Department of Traumatic Orthopedics, Second Clinical College of Lanzhou University, Lanzhou 730000, Gansu Province, Chinayexyang2008@ Correspondence to: Zhen Ping, Chief physician, Master’s supervisor, Department of Orthopedics, Lanzhou General Hospital of Lanzhou Military Area Command of Chinese PLA, Lanzhou 730050, Gansu Province, China zhenpingok@Received: 2009-09-29 Accepted: 2009-11-01磷酸钙骨水泥药物缓释体系的研究应用★叶向阳1,甄平2,李晓飞1,张增山1,赵东华1Application of calcium phosphate cement as drug delivery systemYe Xiang-yang1, Zhen Ping2, Li Xiao-fei1, Zhang Zeng-shan1, Zhao Dong-hua1AbstractOBJECTIVE: To review the characteristics changes of calcium phosphate cement (CPC) as drug delayed release carrier before and after carrying different drugs, analyze dynamic principle and influential factors of drug delayed release system, and summarize new advances of CPC in animal experiments and clinical studies.DATA SOURCES: A computer-based online search of CNKI (/index.htm) and PubMed(/PubMed) was performed for articles published between 1985 and 2009 with the key words of “calcium phosphate cement, CPC, drug delivery system, release” in Chinese and English.DATA SELECTION: Articles highly related with CPC; articles concerning CPC as drug delivery system. Repetitive articles were excluded.MAIN OUTCOME MEASURES: Changes in physico-chemical properties and drug release dynamics of CPC as delivery carrier of different drugs.RESULTS: CPC is an outstanding skeletal defect restorative material. Considering physico-chemical properties, drug release dynamics and histocompatibility, CPC is good delayed release carrier of drugs. However, its clinical application is limited only in bone defect repair of unloading sites due to its bad compressive strength and adhesivity. Therefore, studies on these aspects require exploration.CONCLUSION: CPC as a drug delivery system is a novel administration method. It can repair bone defect and release drug to achieve favorable treatment effects. CPC has been extensively used in osteomyelitis, bone tuberculosis, bone tumor, bone fracture, bone nonunion, and artificial joint replacement.Ye XY, Zhen P, Li XF, Zhang ZS, Zhao DH.Application of calcium phosphate cement as drug delivery system.Zhongguo Zuzhi Gongcheng Yanjiu yu Linchuang Kangfu. 2009;13(47): 9317-9320. [ ]摘要目的:综述磷酸钙骨水泥作为药物缓释载体负载不同药物前后的特征性变化,分析药物缓释体系的动力学原理及其影响药物缓释的因素,评述磷酸钙骨水泥药物缓释体系在动物实验和临床研究中的新进展。
磷酸钙骨水泥复合去甲万古霉素后理化性质改变及药物释放规律的研究_苗军

磷酸钙骨水泥复合去甲万古霉素后理化性质改变及药物释放规律的研究苗军王继芳郝利波毛克亚唐佩福刘春蓉刘志新汤宇在现代社会,由于高速交通和体育运动的发展,使由高能量损伤所致的严重的开放性骨折很常见,感染发生率可达=/>?@/>,治疗非常困难。
局部血液循环差,抗菌素不能到达局部形成有效血药浓度,是造成全身给药疗效不佳的主要原因,故局部给药是一种行之有效的方法。
0A0是近年来发展起来的一种新型生物活性骨替代材料,能够原位固化,固化反应温和,对药物活性无影响,可做为多种药物的载体,固化产物能诱导骨的生长并同步降解,不需要二次手术取出。
本研究所采用的0BC 骨水泥是0A0的一种,制备了含去甲万古霉素0BC 骨水泥,并对其理化特性及体外药物释放规律进行了研究。
材料与方法一、材料与仪器0BC 骨水泥(解放军总医院研制),固相成份为磷酸氢钙、碳酸钙及磷酸三钙等,液相为磷酸钠盐水溶液;去甲万古霉素(华北制药厂,批号/.==/D );EF!"/基金项目:国家自然科学基金G DH!I/ID=J作者单位:=//#@D 北京市,解放军总医院骨科(苗军、王继芳、郝利波、毛克亚、唐佩福、刘志新、汤宇);D//=!.天津市武警医学院(刘春蓉)苗军(=HI"K ),男,医学博士,医师。
研究方向:人工关节,生物材料。
通讯作者:王继芳【摘要】目的研究磷酸钙骨水泥(&6;&(7-4’+L4’6,9&9-9),80A0)复合抗生素后理化性质的改变及体外药物释放规律。
方法将0A0中复合=>、D>、@>的去甲万古霉素,观察水泥的固化时间,测试固化强度,通过M 线衍射(MNE )及傅立叶变换红外光谱分析(O5PN )检测固化产物,将抗生素骨水泥浸泡于生理盐水中,定期取浸泡液,用紫外分光光度计测定抗生素浓度,观察抗生素释放特点。
结果随着加入去甲万古霉素浓度的增加,骨水泥固化时间缩短,固化强度降低,含量为@>时,抗压强度最低为./%=QA6,但仍高于正常松质骨强度。
可注射磷酸钙骨水泥的研究进展_陶艳

可注射磷酸钙骨水泥的研究进展*陶 艳,李东旭,李延报(南京工业大学材料科学与工程学院,材料化学工程国家重点实验室,南京210009)摘要 可注射磷酸钙骨水泥以其良好的生物相容性、骨传导性和可降解性等优点被广泛应用于临床的骨替换和修复等领域。
综述了磷酸钙骨水泥(CP C )注射性能的评价指标,提出了评价CPC 注射性能的有效方法,讨论了骨水泥的注射体系、制备方法和组成等对CPC 注射性能的改进措施,并在此基础上探讨了CPC 存在的问题及对策。
关键词 磷酸钙 骨水泥 注射性Development of Injectable Calcium Phosphate Bone C ementTAO Yan ,LI Dong xu ,LI Yanbao(State Key Labo rato ry o f M aterials -o riented Chemical Engineering ,Co llege of M aterials Science and Engineering ,N anjing U niver sity o f T echnolog y ,N anjing 210009)Abstract T he injectable calcium pho sphate cement has been widely applied in many clinical fields such as bone implant and repair because of g ood bioco mpatibility ,o steo conductio n and biodeg radation .I ts eva luatio n inde x and the effective assessment are summa rized ,differ ent im pr ovements o f the injec tability of CPC through chang ing its injecting system ,prepara tion and composition a re evaluated ,and the pr oblems which still bew ilder many scholars as w ell as the po ssible solutions a re explo red .Key words calcium phospha te ,bo ne cement ,injec tability *国家自然科学基金资助项目(20573055) 陶艳:女,1987年生,硕士 李东旭:通讯作者,教授,博士生导师 E -mail :dongx uli @njut .edu .cn0 前言磷酸钙骨水泥(Calcium phosphate cem ent ,CPC )是一种具有自固性能的非陶瓷型羟基磷灰石类人工骨材料,由Brow n 等[1]于1985年研制成功。
促磷酸钙骨水泥吸收的研究进展

中国矫形外科杂志 2004 年 11 月第 12 卷第 21~22 期 Orthop J Chin , Vol112 , No121~22 November 2004
磷酸钙骨水泥对骨形态发生蛋白缓释作用的体外实验研究

磷酸钙骨水泥对骨形态发生蛋白缓释作用的体外实验研究张伟;侯春林;刘昌胜;陈爱民;匡勇【期刊名称】《中国矫形外科杂志》【年(卷),期】2001(8)8【摘要】目的 :研究CPC对BMP的体外缓释作用及其药代动力学 ,为将CPC与BMP制成复合型生物活性人工骨提供理论依据。
方法 :以单纯CPC为对照组 ,以按1gCPC固相配 5mgrhBMP -2的配比将CPC与rhBMP -2复合作为实验组 ,浸入0 .0 1mol/L的磷酸盐缓冲液中 ,分别在第 1、2、3、4、7、14、30、90、180、36 0d取缓释液 ,用高效液相色谱仪分析不同时间rhBMP -2缓释量 ,绘制rhBMP -2缓释曲线 ,总结药代动力学规律。
结果 :第 1~ 7drhBMP -2出现快速释放 ,释放曲线呈快速上升直线 ;第 7~ 14drhBMP -2释放处于平台期 ;第 14~ 360drhBMP -2出现缓慢而持久的释放 ,释放符合Higuchi方程。
结论 :CPC能对rhBMP -2有缓慢而持久的体外缓释作用 ,有望充当rhBMP -2的缓释载体。
【总页数】4页(P783-786)【关键词】磷酸钙水泥;骨形态发生蛋白;缓释系统;药代动力学【作者】张伟;侯春林;刘昌胜;陈爱民;匡勇【作者单位】第二军医大学长征医院骨科;华东理工大学瑞邦生物材料研究所【正文语种】中文【中图分类】R392-33;R68【相关文献】1.丝素蛋白/双相磷酸钙/半水硫酸钙/重组人骨形态发生蛋白-2骨水泥的制备及修复椎体骨缺损的实验研究 [J], 王根林;陈广东;朱雪松;朱志军;谢瑞娟;卢神州;张波;夏太宝;杨惠林2.磷酸钙骨水泥/顺铂复合体体外药物缓释及体内抑瘤和修复骨缺损的实验研究 [J], 刘彦宁;刘淼;任鹏宇3.磷酸钙骨水泥复合骨形态发生蛋白对兔实验性股骨头缺血性坏死的修复作用 [J], 苏云;张伟;胡春明;徐爽;张贵雨;吕涛;武首先4.自制磷酸钙骨水泥缓释体中顺铂的体外缓释效能 [J], 黄波;范清宇;潘朝晖;刘云燕5.磷酸钙骨水泥/氨磷汀/顺铂复合体体外药物缓释及体内修复骨缺损和抑瘤实验[J], 刘彦宁;刘淼;任鹏宇因版权原因,仅展示原文概要,查看原文内容请购买。
磷酸钙材料在药物缓释中的应用
磷酸钙载体材料在药物缓释中的应用09级赵新宇健康是与人类自身密不可分的话题。
随着经济的发展,人类对健康提出更高的要求。
大家都知道,生病了要吃药,然而药物在治好病症的同时,多少都会有副作用,这也就是老百姓常说的“是药三分害”。
那么,药物的“害”怎么引起的?有没有消除的方法呢?要回答这个问题,我们先要了解药物进入人体后的作用过程。
传统的药物是没有保护层的,即使有一些药物包裹着糖衣,但进入体内,糖衣就会被消化掉,里面的药物分子是没有保护的。
因此,药物分子一旦释放出来,浓度会迅速升高,局部浓度会超过最小致毒浓度,对体内正常的组织器官产生毒副作用,同时,由于药物分子没有保护,很快会被新陈代谢系统所稀释,药物浓度又会低于有效浓度,失去疗效。
因此,传统的药物药效持续时间短,需多次服药。
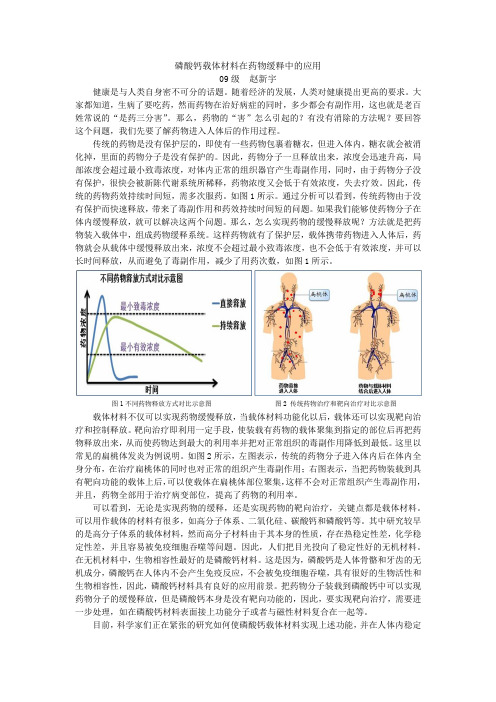
如图1所示。
通过分析可以看到,传统药物由于没有保护而快速释放,带来了毒副作用和药效持续时间短的问题。
如果我们能够使药物分子在体内缓慢释放,就可以解决这两个问题。
那么,怎么实现药物的缓慢释放呢?方法就是把药物装入载体中,组成药物缓释系统。
这样药物就有了保护层,载体携带药物进入人体后,药物就会从载体中缓慢释放出来,浓度不会超过最小致毒浓度,也不会低于有效浓度,并可以长时间释放,从而避免了毒副作用,减少了用药次数,如图1所示。
图1不同药物释放方式对比示意图图2 传统药物治疗和靶向治疗对比示意图载体材料不仅可以实现药物缓慢释放,当载体材料功能化以后,载体还可以实现靶向治疗和控制释放。
靶向治疗即利用一定手段,使装载有药物的载体聚集到指定的部位后再把药物释放出来,从而使药物达到最大的利用率并把对正常组织的毒副作用降低到最低。
这里以常见的扁桃体发炎为例说明。
如图2所示,左图表示,传统的药物分子进入体内后在体内全身分布,在治疗扁桃体的同时也对正常的组织产生毒副作用;右图表示,当把药物装载到具有靶向功能的载体上后,可以使载体在扁桃体部位聚集,这样不会对正常组织产生毒副作用,并且,药物全部用于治疗病变部位,提高了药物的利用率。
自制磷酸钙骨水泥对顺铂缓释作用的动物体内实验

自制磷酸钙骨水泥对顺铂缓释作用的动物体内实验黄波;范清宇;潘朝晖【期刊名称】《现代肿瘤医学》【年(卷),期】2006(14)8【摘要】目的:研究自制含顺铂磷酸钙骨水泥(CPC)植入体在实验动物体内的药物缓释性能.方法:将顺铂与CPC固相按1:19的比例混合后制成含顺铂磷酸钙骨水泥植入体,对照为不含顺铂的磷酸钙骨水泥植入体;以家兔为实验对象,实验组兔股骨远侧干骺端放置含顺铂植入体,对照组相同部位放置不含顺铂植入体并由耳缘静脉注射0.1%顺铂溶液,术后于不同时间点取血液及局部骨组织标本,用原子吸收分光光度仪检测顺铂含量.结果:与对照组相比,实验组兔血清中顺铂浓度低,局部骨组织中顺铂含量高,药物并不出现明显释放波峰,缓释体在兔体内释放顺铂时间长达16周以上,第16周时局部骨组织中顺铂含量仍有13.58μg/g,磷酸钙骨水泥植入体在局部骨组织中不出现明显溶解吸收现象.结论:自制含顺铂磷酸钙骨水泥载体对顺铂有缓慢而持久的体内释放作用,可望成为临床治疗骨肿瘤的一种新方法.【总页数】3页(P1007-1009)【作者】黄波;范清宇;潘朝晖【作者单位】第四军医大学唐都医院全军骨肿瘤研究所,陕西,西安,710038;第四军医大学唐都医院全军骨肿瘤研究所,陕西,西安,710038;第四军医大学唐都医院全军骨肿瘤研究所,陕西,西安,710038【正文语种】中文【中图分类】R738.1【相关文献】1.TCRP1在口腔鳞癌中介导顺铂耐药的体内实验研究 [J], 谷依学;范莎莎;王成昆;彭波;张为家;贺智敏2.自制磷酸钙骨水泥缓释体中顺铂的体外缓释效能 [J], 黄波;范清宇;潘朝晖;刘云燕3.采用体内实验探讨IL-17A促进卵巢癌腹腔种植瘤顺铂耐药的机制 [J], 陈燕; 牛秀珑; 郁春艳; 李岩; 邓为民4.磷酸钙骨水泥对骨形态发生蛋白缓释作用的体外实验研究 [J], 张伟;侯春林;刘昌胜;陈爱民;匡勇5.磷酸钙骨水泥/BMP复合人工骨的理化性能及缓释作用 [J], 孙明林;胡蕴玉;雷伟;袁志;吴永辉;丛锐因版权原因,仅展示原文概要,查看原文内容请购买。
磷酸钙骨水泥的临床应用与研究进展

折和骨不连等领域有广阔的应用前景。 目前所载药物
的种类主要有三类: 抗肿瘤药 、 生素和生物活性物 抗 质。
苗军等嘲 研究 了复合抗生素对磷酸钙骨水泥理 化性质的影响 。将不同剂量的头孢他啶和去甲万古 霉素与磷酸钙骨水泥复合 , 检测固化时间、 抗压强度 及固化产物。发现在加入量小于 5 %的情况下 , 随着
降低, 但仍高于正常松质骨抗压强度 , 固化产物仍为 碳酸化羟基磷灰石 。因此 , P C C复合一定量抗生素对
其理化性质影响不大 , 是理想的抗生素载体。 Mi a u 等将含有 1mg g r 0 / 顺铂 (D P k C D )的 C C P 植入到大鼠肢体骨肉瘤模型的瘤体 中, 4周后检测瘤
需 要灵活 地进 行个 体化 治疗 。
解, 以致达不到预期效果 。 如果使用 C C作为 B P MP
的载体使其逐步释放 , 则对发挥功效有重要的作用。
O ua h r 等将复合不同剂量 r MP 2(. n ,. n ) h B 一 1 6g 6 8g 2 2
体体积变化和转移的结节数 目,发现载有 C D D P的
C C显示出良好的抑瘤效果 ; P 同时将其与 5 g g m / 静 k
收稿日期:06 0 — 6 20 — 3 1 作者简介 : 李建华 , 工程师 女,
维普资讯
《 陶瓷学报) 0 6年第 3期 ) 0 2
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
万方数据库,CNKI.PUBMED 1998年1月一2008年12月期间的相关文章,检索词为“药物载体,药物缓 释,磷酸钙骨水泥”,并对资料进行提炼与分析。结果:磷酸钙骨水泥是一种自固化、生物陶瓷璎骨水泥, 与周围组织相容性高,具有大量的微孑L结构,不改变药物的特性。结论:磷酸钙骨水泥所载药物释药稳 定,具有可注射性、低温自固化,以及良好的生物相容性和骨传导性,有望成为治疗多种骨骼系统疾病 理想的药物载体。 【关键词】缓释;药物;载体;磷酸钙;骨水泥 doi:10.3969/j.issn.1673-7163.2009.04.028
as good biocompatibility and
ideal medicamentous carrier in
bone
cement is expected
to
become
an
the treatment of many kinds of diseases in skeletal system.
【Key words】
structures,does
not
change
the property of
Cal'-
drug.Condnsions:The
drugs which had been carrint have
advantages
of stable releasing,syringeability,self—curing under low temperature,as well bone conductivity.The calcium phosphate
【中图分类号】
Research Progress of WU Sheng-xiang,LIU
R453【文献标识码】A【文章编号】
Calcium Phosphate Cement
as
1671-7163(2009)04-0297-03
Drug Defivery Carrier of Bengbu
Quan,NIU
297
磷酸钙骨水泥作为药物缓释载体的研究进展
吴胜祥刘泉牛国旗
作者单位:233000安徽蚌埠,蚌埠医学院第一附属医院骨科组织移植安徽省重点实验室 作者简介:吴胜祥(1976一),硕士研究生.研究方向:关节外科 通信作者:刘泉,E—mail:liuquanbangbu@yahoo.com
【摘要】
目的:探讨磷酸钙骨水泥的优良性质,以作为骨骼系统理想药物载体的应用。方法:检索
a
Was analyzed and reviewed.
self—curing,bioceramic bone cement,which has hiSh histocom-
patibility with surrounding tissues,possesses lots of microporous lied
phosphate
述如下。
1
CPC的理化性质 力学强度是评价骨修复材料的一个重要指标,CPC的力
学强度取决于其微孔大小、孔隙率、颗粒大小及固化时受压 大小等。CPC的脆性大,强度低,限制了其在临床上的应用。 目前CPC研究蓖点主要在于:(1)如何促进新骨的长入和爬 行替代;(2)作为药物载体的研究;(3)增加其抗压强度。 良好的生物相容性和生物安全性是作为药物载体的材 料必备的两基本条件。相关实验证明,CPC在人体生理环境 下最终转化为与人体骨结构相似的HA,具有高度的组织相 容性。动物实验表明,在动物体内CPC与周围组织相容性良 好,不引起周围组织的变性坏死,未发现脏器出现病理情况 也没发现正常生理过程出现紊乱,证明了其生物安全性心J。 新骨首先从CPC表面的微孔长入,逐步向深部推进,与自体 骨和异体骨替代过程非常吻合,这说明CPC的生物降解的同
look for the related articles
published from Jan.
Dec.2008 in the database of Wanfang,CNKI,PUBMED,the words”drug carder,drug delayed re—
lease and calcium phosphate bone cement”acted鹊docuterms.The obmined data Results:The calcium phosphate cement is
Guo—qi.Department of Orthopaedics,the first Affiliated Hospital
Medical Colloge,Anhui key laboratory of Tissue Transplantation,Bengbu,Anhui 233004,China
(monolithic matrix systenx),其所载药物的释药过程是通过弥
散机制从微孔内释放,药物释放速率与CPC厚度无关而与药 物在CPC内的弥散度和复合量有关。 除高度的生物相容性外,CPC还有随意塑形和在体内填 充骨缺损时自固特化,同化过程恒温性等特点,而且CPC呵 在令部材料内结合药物,随着材料的缓慢降解更长久地释放 药物,具有修复和治疗的双霞功效。这些特点在很人程度上 符合一个理想的药物载体的特点。 2.1抗牛素 20世纪80年代以来,由于开放性创伤、高能量创伤急骤 增加.骨折修复术、假体植入术以及脊柱手术等的术后感染 率和慢性骨髓炎发病率逐渐增高,早期应用大剂虽的敏感抗 生素是其他治疗的前提”J。抗牛素的应用有全身和局部用 药,局部应用可不需通过血液循环系统代谢及重分布,而是 将抗生素直接用于需要部位而起作用。而采用抗生素u服 或静脉等全身给药来预防和治疗感染,很少能在局部可以持 续长时间抗感染,并且增加_r全身的副作用。 Sasaki等∞1在彻底清除病灶的基础I:将含有抗生素的 CPC植入兔股骨中,用以治疗慢性骨髓炎,骨髓炎得到有效 控制并有新生骨组织形成。Joosten等…采用同样的方法治 疗兔股骨慢件骨髓炎,也取得r同样的疗效。金黄色葡萄球 菌是人工关节置换术后继发感染的主要致病菌,万占霉素是 唯一能够有效治疗金黄色葡萄球菌感染的药物。千茂源 等博1将万古霉素CPC复合体(VCM-CPC)应用于全髋置换术 后感染一:期翻修术,术后感染复发率明显降低,提高r翻修 成功率。张进军等一1将分别含头孢哌铜钠0%、0.2%、2. 9%、4.8%、7.4%质量比的头孢哌铜钠一CPC复合体进行力学 实验和超微结构观察,发现CPC承载头孢哌铜钠药域在0— 4.8%之间对其理化特性无显著影响,复合体存在自然孔隙, 并具有较强的抗压性能。 将万古霉素载入CPC中制成标准试件进行力学测试,发 现手动搅拌下万古霉素和骨水泥质鼍配比不超过5.0%时不 影响骨水泥的压缩强度,配比时手动与真空下搅拌相比CPC 具有更高的强度。更多研究表明,载抗生素CPC不仅能治疗 骨感染,也可充填和修复骨质缺损H…。 2.2化疗药 过去20年中,骨肿瘤在治疗上发生了深刻的变化,从上 世纪70年代开始的大剂量综合化疗,到现在的新辅助化疗,
Controlled—release;Drug;Carrier;Calcium phosphate;Bone cement
随着老龄化社会的到来,骨质疏松症、骨关节病、骨肿瘤 和炎症等的发病率不断提高,给患者带来了巨大的痛苦,于 是预防和治疗这些疾病的药物受到广泛重视。目前这些疾 病的早期阶段有一些药物町以有效治疗,但这些药物如抗炎 镇痛类、化疗类等全身用药有很大的毒副作用,并且到达病 变部位的药物浓度也很低,因此治疗效果受到一定影响,在 治疗疾病的同时又带来新的损害。如何将治疗药物只针对 靶目标而且能有效控制药物释放,从而达到局部的有效药物 浓度,全身副反应又很少…,就成为一个重要的课题。20世 纪80年代中期,美国的Brown和Chow发明了一种新型的自 固化生物活性骨缺损修复材料—磷酸钙骨水泥(Calcium
cements,CPC)。这种材料在人体生理环境下最终
转化为与人体骨结构相似的羟基磷灰石(Ca,(PO。),OH, HA)。CPC的出现,可能使上述目标有望变成现实。本文就 CPC作为药物缓释载体参阅了近年来国内外相关文献,综
万方数据
298
鲤剖兰蝤压!Q塑生!旦筮!璺鲞筮垒羽△!型!堡!婴4堡!迎!!,叁竖:呈Q盟,y!!:!垒盟!:兰 已使骨肉瘤的五年生存率从以前的10%一20%提高到现在 的50%~80%…J,大部分患者叮选择瘤段切除与莺建的保 肢手术来取代传统的高佗截肢术。 肿瘤化疗效果依赖药物刹量的观点已得到普遍认同。 目前临床上恶性骨肿瘤的化疗主要有静脉给药和局部动脉 化疗等。但大剂鼍全身性化疗困严蕈毒副反应而限制其在 临床的应用。同时,恶性肿瘤,包括部分良性肿瘤,即使在广 泛手术和系统性辅助化疗下,仍可能局部复发。骨肿瘤术后 形成骨缺损,应用既能充填缺损又能长时f'日J在局部缓慢释放 药物以保持局部高水平的药物浓度的生物材料修复,是最理 想的治疗方法。 Tahara等1121对顺铂.CPC复合体研究表明,载药10%载 体有较高的临床应用价值。同样将顺铂与CPC制成植入体, 以家兔为实验对象,第16周时局部骨组织中药物含量仍有 较高浓度H“。 对分别载入0.1%,0.2%,0.5%质量比甲氨喋呤 (MTX)的CPC进行力学和显微结构观察,发现CPC中加入 适量MTX,其基本晶体结构不会发生变化,CPC凝固时间无 明显影响。质量比为0.1%、0.2%组与对照组力学强度尤统 计学差异,质量比为0.5%组的力学强度与对照组有统计学 差异,但其压缩强度位于松质骨与皮质骨之间,符合临床应 用条件¨“。吴芳等¨副以CPC混合阿霉索制备的载药系统 进行体外释约试验,发现早期有释约冲击效应,3天体系的每 日释药量随时问的增长而缓慢减小,溶出速率趋于稳定,且 释药冲击鼍及药物溶出速率随药物包埋量的增大而增大。 观察至32天时释药百分率仍维持在3.5%~3.8%,释放规 律基本符合Higuchi提出的一维假稳态释药模型。后期可能 因骨水泥微孔结构改变,导致释药率与模型存在一定偏差。 本体系释药曲线较平稳,据此预计有较长的释药周期。 2.3生长因子 动物模型和I临床实验已经证实许多成骨因子、肽和小分 子可以促进骨愈合。它们大都是多肽,通过信号传递影响细 胞内的活动。重组技术使得T业化生产出大量高纯度的生 长因子,单独将牛长因子植入体内由于缺少载体的支撑作用 易被血液冲刷掉而不能最大限度地发挥诱导成骨作用,因为 蛋白质在植入点弥散非常快。体外实验研究用CPC结合这 些生长因子,因其所载成骨因子可以渐进释放促进骨生 长‘1 61。 Ruhe等¨73利用固化后CPC载rhBMP-2复合体修复兔 颅骨缺损处,定馈分析显示2周后材料外即有显著新生骨形 成。在不同的大型动物模型中进行了复合成骨因子的注射 式载体的一系列试验,均证实CPC是复合rhBMP-2的最佳载 体¨“圳。刘洪等【21 3将CPC与外源性神经生长因子复合移 植修复兔桡骨缺损,分别于2,3,4,8周4个时间点观察并取 标本,发现实验组2周即见到新骨长入,4周骨缺损修复基本 完成,材料被部分吸收,剩余材料与新骨结合紧密;而对照组 成骨鼍明显少于实验组,成骨速度缓慢。对于“CPC+生长 因子”的临床应用及远期疗效还有待进一步研究。 2.4抗炎药及其他药物 黄粤等H。在将3%、5%和10%萘普生钠载入CPC制成 药物缓释体系的研究时发现药物的引入未影响材料的操作
