黄曲霉毒素免疫亲和柱重复利用的探讨_赵丽元
酶联免疫吸附法和免疫亲和柱-高效液相色谱法在检测饲料中黄曲霉毒素B1含量中的比对研究
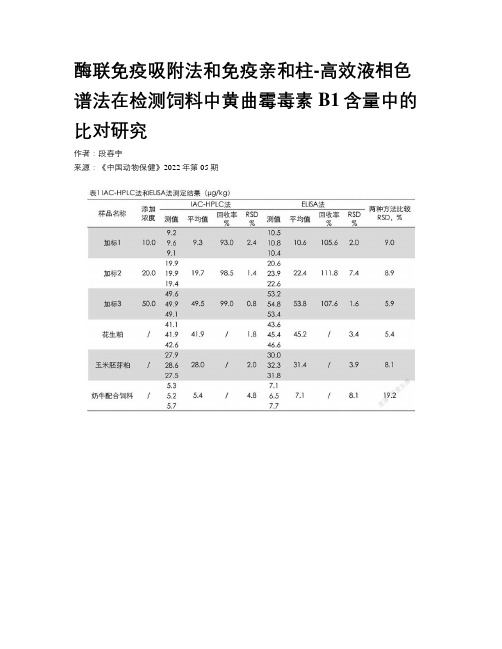
酶联免疫吸附法和免疫亲和柱-高效液相色谱法在检测饲料中黄曲霉毒素B1含量中的比对研究作者:***来源:《中国动物保健》2022年第05期摘要:为了探讨酶联免疫吸附法检测饲料中黄曲霉毒素B1含量的可行性,试验采用酶联免疫吸附法(ELISA法)比对免疫亲和柱-高效液相色谱法(IAC-HPLC法),对饲料中黄曲霉毒素B1含量进行了检测,对检测结果的准确度、精密度和样品加标回收率进行了分析。
ELISA法线性方程相关系数为0.9952,相对标准偏差(RSD)为1.6%~8.1%,平均加标回收率为105.6%~111.8%。
结果表明,ELISA法的准确性、重现性、稳定性好;且ELISA法检测结果与IAC-HPLC法检测结果的相对标准偏差(RSD)为5.4%~19.2%,两种方法的检测结果的偏差可以接受,表明ELISA法能满足检测需求。
关键词:酶联免疫吸附法;免疫亲和柱-高效液相色谱法;饲料;黄曲霉毒素B1黄曲霉毒素,是黄曲霉菌和寄生曲霉菌分泌的次级代谢产物,主要分为B、G类,其中黄曲霉毒素B1的含量最多,危害性最大,该毒素具有强致癌性、致畸性、致突变性。
黄曲霉毒素B1可以侵害畜禽肝脏,导致肝脏变性、坏死等,进而导致畜禽肺脏、肾脏、脾脏、胃、直肠等器官发生病变;导致畜禽的免疫力降低;導致畜禽生长发育迟缓,采食量降低、食物利用率低;母畜不育或产仔少等问题。
黄曲霉毒素B1主要污染粮食作物及其副产品,其中,花生和玉米及其副产品污染最为严重,几乎无法避免,该毒素性质稳定,持续高压灭菌2h仅能降低其25%~33%的毒力,而且只有在282℃的高温下才能被裂解,所以世界各国都严格设定“限量标准”。
黄曲霉毒素B1污染饲料主要源于原料污染、储存条件不当饲料霉变污染和加工过程污染。
要预防黄曲霉毒素B1毒害畜禽,就要及时准确测定饲料原料及饲料成品中黄曲霉毒素B1含量,因而制定准确实用的检测方案至关重要,进而加强原料的筛选、饲料的品控,更好的保护畜禽健康,发挥畜禽生产性能,将饲料价值充分发挥。
免疫亲和柱净化柱后光化学衍生高效液相色谱-荧光检测法同时测定制马肾中4种黄曲霉毒素

免疫亲和柱净化柱后光化学衍生高效液相色谱-荧光检测法同时测定制马肾中4种黄曲霉毒素作者:孙艳杰赵磊李正刚王路宏来源:《中国民族民间医药·上半月》2023年第12期【摘要】目的:建立免疫親和柱净化柱后光化学衍生高效液相色谱-荧光检测法同时测定制马肾中黄曲霉毒素B1、B2、G1、G2的含量。
方法:样品采用70%甲醇作为提取溶剂,经免疫亲和柱净化、高效液相色谱分离、光化学柱后衍生后,通过荧光检测器测定其中黄曲霉毒素的含量。
结果:黄曲霉毒素B1的线性范围为0.0104~0.0520 ng(r=0.999 9)、黄曲霉毒素B2的线性范围为0.0038~0.0190 ng(r=0.999 8)、黄曲霉毒素G1的线性范围为0.0108~0.0540 ng(r=0.999 8)、黄曲霉毒素G2的线性范围为0.0038~0.0190 ng(r=0.9998),线性关系良好,回收率在89.68%~101.44%之间,RSD≤3.5%。
结论:该方法操作简便,灵敏度高、重复性好、结果准确,可用于制马肾中黄曲霉毒素的测定。
【关键词】制马肾;免疫亲和柱;光化学衍生;高效液相色谱-荧光检测器;黄曲霉毒素【中图分类号】R284.1 【文献标志码】 A 【文章编号】1007-8517(2023)23-0019-04DOI:10.3969/j.issn.1007-8517.2023.23.zgmzmjyyzz202323005Simultaneous Determination of Content of Four Aflatoxins in EQUI PENIS ET TESTIVULUS by Mmunoaffinity Column Clean-up and HPLC-FLD with Post-column Photochemical DerivatizationSUN Yanjie ZHAO Lei LI Zhenggang WANG Luhong*Siping Institute for Food and Drug Control,Siping 13600,ChinaAbstract:Objective To establish the contamination method of aflatoxin B1,B2,G1 and G2 in EQUI PENIS ET TESTIVULUS by immunoaffinity column clean-up and HPLC-FLD with post-column photochemical derivatization.Methods After extraction with 70% Methanol and purification by immunoaffinity columns,aflatoxin B1,B2,G1 and G2 in samples were anlyzed by HPLC-FLD with post-column photochemical derivatization.Results The linearity of Aflatoxin B1 was at 0.0104-0.0520 ng(r=0.9999), Aflatoxin B2 was at 0.0038-0.0190 ng(r=0.9998), Aflatoxin G1 was at 0.0108-0.0540 ng(r=0.9998), Aflatoxin G2 was at 0.0038~0.0190 ng(r=0.9998), The average recoveries were within 89.68%-101.44% wi th RSD≤3.5%. Conclusion The above method has demonstrated convenient operation,good repeatability,highsensitity and accuracy.This method is suitable for the determination of AF in Renshenguipi pills.Keywords:Equi Penis Et Testivulus;Immunoaffinity Column;Photochemical Derivation;HPLC-FLD;Aflatoxi马肾药材标准收载在《吉林省中药材标准》第二册2019版[1],为马科动物成年马Equus caballus Linnaeus雄性的干燥阴茎及睾丸。
免疫亲和柱净化-高效液相色谱法测定玉米油中F-2毒素含量的研究

免疫亲和柱净化-高效液相色谱法测定玉米油中F-2毒素含量的研究罗建光【摘要】建立免疫亲和柱净化-高效液相色谱法测定玉米油中F-2毒素的方法.样品经前处理后通过免疫亲和柱净化,采用高效液相色谱仪-荧光检测器进行检测.该方法最佳测定条件为:选用IAC-AZ型免疫亲和柱,柱吸附容量4μg;流动相乙腈-甲醇-水(体积比46∶ 46∶8),流速1.0mL/min;提取溶剂乙腈-水(体积比90∶10).F-2毒素的质量浓度在0~ 250 ng/mL的范围内与峰面积呈良好的线性关系,方法检出限为0.06 μg/kg,平均回收率为92.46%,RSD为0.942%~1.758%.该方法操作简便快捷、准确度高、重现性好,适用于玉米油中F-2毒素的测定.%A method for determination of F-2 toxin in corn oil by immune-affinity column purification and HPLC was established.The sample was firstly pretreated,then purified by immune-affinity column and determined by HPLC with fluorescence detector.The optimal determination conditions were obtained as follows:IAC-AZ immune-affinity column,column adsorption capacity 4 μg,acetonitrile-methanol-water (volume ratio 46∶ 46∶ 8) as mobile phase,flow rate 1.0 mL/min,extraction solvent acetonitrile-water (volume ratio 90∶ 10).The results showed that the mass concentration of F-2 toxin had good linear relation ship with peak area in the range of 0-250 ng/mL,the recovery was 92.46% with RSD 0.942%-1.758%,and the limit of detection was 0.06 μg/kg.The method was simple and easy to operate with high accuracy and good reproducibility,and it was suitable for the determination of F-2 toxin in corn oil.【期刊名称】《中国油脂》【年(卷),期】2018(043)005【总页数】4页(P88-91)【关键词】F-2毒素;玉米油;免疫亲和柱;高效液相色谱法【作者】罗建光【作者单位】江苏食品药品职业技术学院食品学院,江苏淮安223003【正文语种】中文【中图分类】TS225.1;TQ646F-2毒素(ZEN)又称玉米赤霉烯酮,主要由禾谷镰刀菌、三线镰刀菌和雪腐镰刀菌等菌种产生的一种真菌毒素[1-2]。
免疫亲和柱净化-HPLC柱后光化学衍生技术同时检测何首乌中的4种黄曲霉毒素

940 引言何首乌始载于《开宝本草》,为我国较为常用的中草药材之一,在全国各地均有分布,广东、湖南、河南和广西是其栽培品的主要几大产区。
何首乌中包含有二苯乙烯类、蒽醌类、黄酮类、磷酯类、酚类及鞣质类等131种化合物[1]。
最近的研究表明,二苯乙烯类化合物可以作为抗衰老和抗动脉粥样硬化因子,减少脑病理萎缩,促进学习和记忆[2];含蒽醌的组分对心肌提供了剂量依赖性的保护缺血-再灌注损伤,并减少脑缺血引起的梗死体积[3]。
早在2010年,何首乌及其制作方法被中国药典收录,何首乌也被广泛用作补药和泻药,以治疗失忆症、高脂血症和便秘[4]。
何首乌经炮制后,极其容易发霉而变质,不仅其药效受到影响,发霉后会产生黄曲霉毒素B1、B2、G1、G2,均是致癌物质,严重影响身体健康。
世界卫生组织已将黄曲霉毒素(Aflatoxin)释质谱(HPLC-IDMS)[15]、高效液相色谱-串联质谱(HPLC-MS/MS)[16]、高效液相色谱-高分辨质谱(HPLC-HMRS)[17]和免疫亲和柱-高效液相色谱法(HPLC-IAC)等[18]。
使用酶联免疫吸附法和免疫亲和柱-荧光分光光度法对其进行检测时,样品中的某些结构类似物也会被抗体吸附而产生荧光,造成假阳性[19]。
Arroyo-Manzanares等[20]提出了一种HPLC-MS/MS方法测定黄曲霉毒素,以水/丙酮/乙腈(30:35:35,v/v/v)为萃取溶剂,萃取后测定干血斑或干血清斑中的黄曲霉毒素,取得了很好的结果,检测限为0.05至0.1 ng/mL。
免疫亲和色谱法(Immunoaffinity Chromatography,IAC)基于抗体-抗原的特异性吸附原理进行选择性分离,方法的准确性和灵敏度都很高[22],是检测黄曲霉毒素的最佳方法之一。
发展何首乌中的致癌物质黄曲霉毒素B1、B2、G1、G2的高效、准确检测方法至关重要。
由于Afla Bl和Afla Gl荧光强度相对较弱,通常需96公司、吐温-20采购自梯希爱(上海)化成工业发展有限公司(货号T0543);超纯水(自制)。
采用免疫亲和柱高效液相色谱法检测稻米中的黄曲霉毒素B1

采用免疫亲和柱高效液相色谱法检测稻米中的黄曲霉毒素B1李旭;马力【摘要】采用免疫亲和柱净化高效液相色谱法检测稻米中的黄曲霉毒素B1(AFB1).稻米样品经甲醇/水(80/20,v/v)粗提取,再经免疫亲和柱净化和三氟乙酸衍生化,最后经高效液相色谱法测定.经检测,AFB1含量在0.01 ~2.50 ng范围内,所得到的AFB1标准曲线呈良好的线性关系,回归方程为Y=60.355x+0.054 3,相关系数为0.999 7.该方法检出限为0.1μg/kg,加标回收率为89.26%~99.45%,SD为2.48%~3.74%.由于该方法操作的选择性高、灵敏度高、检测效果好,因此适于较大批量粮油作物中黄曲霉毒素的检测,便于示范推广.【期刊名称】《西华大学学报(自然科学版)》【年(卷),期】2014(033)004【总页数】4页(P72-75)【关键词】稻米;黄曲霉毒素B1;免疫亲和柱;高效液相色谱法【作者】李旭;马力【作者单位】西华大学生物工程学院,四川成都610072;西华大学生物工程学院,四川成都610072【正文语种】中文【中图分类】TS252.7黄曲霉毒素是由黄曲霉和寄生曲霉等产毒菌株所产生的次生代谢产物[1],微溶于水,易溶于甲醇、乙腈和氯仿等有机溶剂,具有很强的毒性、致癌性、致突变性和致畸性[2]。
1993年黄曲霉毒素被国际癌症研究机构定为I类致癌物,其中毒性最强的是黄曲霉毒素B1(AFB1)[3]。
由于黄曲霉毒素对人类和动物危害严重,国际上要求对黄曲霉毒素进行严格监管和防范,检测方法研究进展较快,主要有薄层色谱法(TLC)[4]、酶联免疫吸附法(ELISA)[5]、荧光光度法(FLM)[6]和高效液相色谱法(HPLC)[7-8]等,其中最常见的是HPLC法。
针对稻米中黄曲霉毒素的加标回收率低的问题,本研究采用德国Lctech公司的免疫亲和柱(AflaCleanTM)净化稻米样品,再通过高效液相色谱法检测稻米中AFB1,研究该净化柱对稻米样品的净化处理效果,优化样品提取、净化和检测等条件,建立快速、准确、高效液相色谱检测稻米样品中黄曲霉毒素的方法。
黄曲霉M1检测方案2

黄曲霉毒素M1检测方案方案一、免疫亲和层析净化高效液相色谱法(GB 5413.37-2010第二法)一、原理:亲和柱内含有的黄曲霉毒素M1特异性单克隆抗体交联在固体支持物上,当试样通过亲和柱时,抗体选择性的与黄曲霉毒素M1(抗原)键合,形成抗体—抗原复合体。
用水洗柱除去柱内杂质,然后用洗脱剂洗脱吸附在柱上的黄曲霉毒素M1,收集洗脱液。
用带有荧光检测器的高效液相色谱仪测定洗脱液中黄曲霉毒素M1含量。
二、所需仪器1、高效液相色谱仪(配荧光检测器—具有365 nm激发波长、435 nm发射波长,在适当的色谱条件下能够测定0.02 ng 的黄曲霉毒素M1(相当于5倍噪音))2、离心机(转容50ml角转子,转速10000r/min)3、氮吹仪4、固相萃取装置(带真空系统)5、水浴锅(温控30℃±2℃,50℃±2℃;温范25℃~60℃)6、天平:感量为0.01 g7、PH计:精度0.018、旋转蒸发仪(奶油样品制备)9、紫外分光光度计(标液浓度的校正,波长范围为200nm~400nm)三、试剂及耗材1、黄曲霉毒素M1免疫亲和柱2、黄曲霉毒素M1标准品3、反相色谱柱C18 4.6*250 加有反相色谱材料的保护柱5、移液管:1ml, 2ml, 50ml6、烧杯:50ml, 250ml7、分液漏斗:250ml(干酪和奶油样品制备)8、容量瓶:100ml9、一次性注射器:10ml, 50ml10、针式过滤器(水系)0.22um,Φ1311、乙腈(CH3CN):色谱醇12、甲醇:分析醇13、三氯甲烷:分析醇14、石油醚:分析醇15、带刻度的磨口锥形玻璃试管:5 mL、10 mL、20 mL16、离心管:50ml四、操作方法依据GB 5413.37-2010第二法方案二、酶联免疫吸附法(可定性、定量检测牛乳及其他乳制品等样本中的黄曲霉毒素M1)一、原理标准溶液和样品试液加入各自板孔,游离的黄曲霉毒素M1与微孔中包被的黄曲霉毒素M1抗体结合,没有结合的物质在洗涤中被清除。
黄曲霉毒素免疫亲和柱重复利用的探讨

黄曲霉毒素免疫亲和柱重复利用的探讨赵丽元;郝爱鱼;刘英慧【摘要】目的考察中药材类别和亲和柱处理方法对黄曲霉毒素免疫亲和柱重复利用的影响,探讨亲和柱重复利用的可能性.方法通过在不同中药材中加入黄曲霉毒素对照品,经免疫亲和柱净化-HPLC-柱后光衍生分析,考察亲和柱重复利用后的回收率;考察不同的亲和柱处理方法对回收率的影响.结果中药材类别对免疫亲和柱重复利用的影响差异很大,部分种子类中药材使用后亲和柱重复利用3次回收率无明显变化,部分根茎类使用后,亲和柱回收率降低明显,特别是G2更易受影响.亲和柱处理时有机溶剂,空气暴露和复性时间均可影响柱子重复利用.结论中药材类别和处理方法对黄曲霉毒素免疫亲和柱的重复利用均有显著影响.【期刊名称】《中国现代药物应用》【年(卷),期】2014(008)001【总页数】3页(P31-33)【关键词】黄曲霉毒素;免疫亲和柱;回收率;重复利用【作者】赵丽元;郝爱鱼;刘英慧【作者单位】116021,大连市食品药品检验所;116021,大连市食品药品检验所;116021,大连市食品药品检验所【正文语种】中文免疫亲和柱是20世纪90年代在分析领域得到应用的一种新技术,它是将一定量的单克隆抗体偶联在合适的担体上,制成相应的免疫亲和柱。
该柱具有高选择性吸附和抗干扰的特性,净化效果好,检测灵敏度高,是目前国际上较为常用的检测真菌毒素样品前处理方法之一[1]。
《中国药典》2010年版一部[2]、《欧洲药典》7.0[3]、GB/T 18979-2003[4]中均采用该方法进行黄曲霉毒素的测定。
随着《中国药典》中收载需检测黄曲霉毒素的中药材和制剂的品种的增加,以及中药中黄曲霉毒素残留研究的深入[5-9],免疫亲和柱的使用将会越来越广泛。
但从文献报道来看,免疫亲和柱的使用条件和回收处理条件研究并不是很多。
仅有王莹等[1]人对M1免疫亲和柱的制备及使用条件进行了优化;李佩暖等[10]人对黄曲霉毒素前处理方法进行了优化;李卫岗等[11]人重复使用了3次无明显影响。
总黄曲霉毒素免疫亲和柱

总黄曲霉毒素免疫亲和柱总黄曲霉毒素(Aflatoxin B1,AFB1)是一种由黄曲霉菌(Aspergillus flavus)和黄曲霉素菌(Aspergillus parasiticus)产生的一种强烈致癌的化合物。
该化合物在人类和动物体内会引起多种癌症,如肝癌、食管癌、胃癌等。
因此,检测和去除环境和食品中的总黄曲霉毒素对于保障人类健康至关重要。
为了检测和去除总黄曲霉毒素,研究人员开发了多种方法,其中之一就是使用总黄曲霉毒素免疫亲和柱。
这种免疫亲和柱是通过利用特异性抗体对总黄曲霉毒素进行捕捉,从而实现检测和去除的目的。
总黄曲霉毒素免疫亲和柱的制备过程通常包括以下步骤:首先,需要获得针对总黄曲霉毒素的特异性抗体。
这可以通过免疫小鼠(如小鼠、兔子等)或体外合成的方法获得。
然后,将抗体与固相材料(如琼脂糖、硅胶等)结合,形成免疫亲和柱。
接下来,将待测样品加入免疫亲和柱中,允许总黄曲霉毒素与抗体结合。
最后,用适当的缓冲液洗脱并收集样品,得到含有总黄曲霉毒素的纯净溶液。
总黄曲霉毒素免疫亲和柱的检测原理是基于特异性抗体与总黄曲霉毒素的亲和作用。
一旦待测样品中存在总黄曲霉毒素,它们会与免疫亲和柱中的抗体结合。
通过洗脱的步骤,可以将结合的总黄曲霉毒素从样品中分离出来,从而完成检测过程。
除了检测相关,总黄曲霉毒素免疫亲和柱还可以用于去除总黄曲霉毒素。
已经结合总黄曲霉毒素的免疫亲和柱可以用于净化食品和饲料,去除其中的毒素。
这是因为抗体与毒素之间的结合力较强,可以有效地捕捉和去除总黄曲霉毒素。
总的来说,总黄曲霉毒素免疫亲和柱是一种有效的工具,可以用于检测和去除环境和食品中的总黄曲霉毒素。
通过结合特异性抗体和固相材料,免疫亲和柱可以捕捉和去除总黄曲霉毒素。
然而,需要注意的是,免疫亲和柱的制备过程较为繁琐且耗时,因此需要进行全面的实验准备和操作。
对于总黄曲霉毒素的免疫亲和柱的研究和应用仍在不断发展中。
随着技术的不断进步,相信将有更多的改进和创新,提高总黄曲霉毒素的检测和去除效果,进一步保障人类的健康安全。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
回收率 /% G1
99. 71 97. 10 94. 98 95. 46
B2 98. 44 95. 06 98. 55 96. 91
B1 98. 77 99. 89 96. 61 95. 24
由表 1 可见,亲和柱经过四次试验,回收率的结果无明 泽泻( 阴性样品) 和泽泻 + 33 ng 黄曲霉毒素( 阳性样品) 进
中国现代药物应用 2014 年 1 月第 8 卷第 1 期 Chin J Mod Drug Appl,Jan 2014,Vol. 8,No. 1
·31·
黄曲霉毒素免疫亲和柱重复利用的探讨
赵丽元 郝爱鱼 刘英慧
【摘要】 目的 考察中药材类别和亲和柱处理方法对黄曲霉毒素免疫亲和柱重复利用的影响,探 讨亲和柱重复利用的可能性。方法 通过在不同中药材中加入黄曲霉毒素对照品,经免疫亲和柱净化HPLC-柱后光衍生分析,考察亲和柱重复利用后的回收率; 考察不同的亲和柱处理方法对回收率的影响。 结果 中药材类别对免疫亲和柱重复利用的影响差异很大,部分种子类中药材使用后亲和柱重复利用 3 次回收率无明显变化,部分根茎类使用后,亲和柱回收率降低明显,特别是 G2 更易受影响。亲和柱处理 时有机溶剂,空气暴露和复性时间均可影响柱子重复利用。结论 中药材类别和处理方法对黄曲霉毒 素免疫亲和柱的重复利用均有显著影响。
基金项目: 大连市科技计划基金项目( 项目编号: 2011E15SF121) 作者单位: 116021 大连市食品药品检验所 通讯作者: 赵丽元 E-mail: liyuan0422@ sohu. com
元范围内。由于此免疫亲和柱为一次性使用,不建议重复使 用,因此一份样品的检验成本就要近 200 元,对于一般的实 验室或将进行黄曲霉素的深入研究的实验室,检验或科研成 本将大大增加,从而限制了黄曲霉毒素的研究工作的开展。 本文选用了使用最广泛的美国 VICAM 公司的 AflaTest@ P 免 疫亲和柱为研究对象,对其重复利用的影响因素进行研究。 1 仪器与试药
【关键词】 黄曲霉毒素; 免疫亲和柱; 回收率; 重复利用
Study on repeated usings of aflatoxins immunoaffinity columns ZHAO Li-yuan,HAO Ai-yu,LIU Yinghui. Dalian Institute for Food and Drug Control,Dalian 116021,China
2695e 高效液相色谱仪; 光衍生器 UVE( LC Tech 公司) ; 黄曲霉毒素混合对照品( Supelco 公司; 批号: LB82382) ; 免疫 亲和柱( AflaTest@ P,1 mL,VICAM 公司) 。 2 方法 2. 1 供试品溶液的制备 供试品溶液制备方法参考《中国 药典》2010 年版一部。PBS 缓冲液: 2. 9 g Na2 HPO4 ·12H2 O + 0. 27 g KH2 PO4 + 0. 2 g KCl + 8. 0 g NaCl 用超纯水溶解 至 1000 ml,调节 pH 值至 7. 4,加热煮沸,冷却待用。 2. 2 使用过的免疫亲和柱的处理方法 使用过的免疫亲和 柱用 5 ml 水洗,5 mlPBS 缓冲液过柱,洗后用 PBS 缓冲液填 充柱子,室温放置 1 ~ 2 h 后,置 2 ~ 8℃ 冰箱内放置过夜。 2. 4 色谱条件 用 Zobax SB-C18 色谱柱,以乙腈-甲醇-水为 流动相,梯度洗脱。 3 结果 3. 1 无基质干扰时亲和柱重复利用情况 取黄曲霉毒素对 照品 33 ng( 黄曲霉毒素 B1 12. 5 ng) ,用水稀释成甲醇浓度 14% 的溶液作为样品溶液,进行回收试验,重复使用 4 次,结 果见表 1。
显差异,仍在 90% 以上,由此可见,在药材干扰的情况下,亲 行考察,结果见表 2 和 3。第一次: 制备阴性中药材和阳性中
和柱可重复使用 4 次。
药材使用一次后的亲和柱; 第二次: 均加入泽泻 + 33 ng 黄曲
3. 2 不同中药材使用后亲和柱重复利用情况
霉毒素考察回收率; 第三次: 均加入泽泻 + 33 ng 黄曲霉毒素
3. 2. 1 阴性与阳性中药材使用后亲和柱重复利用情况 取 考察回收率。
表 2 阴性样品回收试验结果
使用次数
第一次 第二次 第三次
总量 0
82. 38 64. 01
G2 0 16. 24 3. 71
回收率 /% G1 0
89. 78 74. 74
B2 0 86. 83 57. 26
B1 0 100. 86 89. 56
【Key words】 Aflatoxin; Immunoaffinity columns; Recoveries; Repeated usings
免疫亲和柱是 20 世纪 90 年代在分析领域得到应用的 一种新技术,它是将一定量的单克隆抗体偶联在合适的担体 上,制成相应的免疫亲和柱。该柱具有高选择性吸附和抗干 扰的特性,净化效果好,检测灵敏度高,是目前国际上较为常 用的检 测 真 菌 毒 素 样 品 前 处 理 方 法 之 一[1]。《中 国 药 典》 2010 年版一部[2]、《欧洲药典》7. 0[3]、GB / T 18979-2003[4]中 均采用该方法进行黄曲霉毒素的测定。随着《中国药典》中 收载需检测黄曲霉毒素的中药材和制剂的品种的增加,以及 中药中黄曲霉毒素 残 留 研 究 的 深 入[5-9] ,免 疫 亲 和 柱 的 使 用 将会越来越广泛。但从文献报道来看,免疫亲和柱的使用条 件和回收处理条件研究并不是很多。仅有王莹等[1]人对 M1 免疫亲和柱的制备及使用条件进行了优化; 李佩暖等[10] 人 对黄曲霉毒素前处理方法进行了优化; 李卫岗等[11] 人重复 使用了 3 次无明显影响。以上文章是以牛奶和花生为样品 对黄曲霉毒素免疫亲和柱前处理方法进行的研究,未见有人 以中药材为样品对黄曲霉毒素免疫亲和柱的回收纯化及重 复利用进行研究,本文即以中药材为样品对黄曲霉毒素免疫 亲和柱的重复利用的影响因素进行研究。目前,黄曲霉毒素 免疫亲和柱的生产厂家较少,美国 VICAM,德国 LC-Tech 及 北京华安麦科生物技术有限公司为较常见,价格在 100 ~ 200
表 3 阳性样品回收试验结果
使用次数
第一次 第二次 第三次
总量98. 59 79. 19 63. 92
G2 98. 21 22. 47 4. 08
回收率 /% G1
94. 89 87. 08 71. 13
B2 98. 06 86. 73 59. 74
B1 98. 78 91. 72 88. 92
由表 2 和表 3 可见,亲和柱经过三次试验,无论是阴性 分析原因可能是泽泻中某些物质对亲和柱中抗体造成破坏 样品柱还是阳性样品柱,回收率的结果无明显差异,黄曲霉 或抑制其结合,因此作者进行不同的中药材亲和柱重复利用 毒素总量第二次使用后回收率为 82. 4% 和 79. 2% ,第三次 的考察。 使用后回收率为 64. 0% ,63. 9% ,因此中药材中是否含有黄 3. 2. 2 种子类中药材亲和柱重复利用情况 选取容易产生 曲酶毒素不是影响亲和柱回收利用的主要因素。从结果可 黄曲霉毒素的种子类中药材杏仁,薏苡仁和柏子仁进行亲和 见,黄曲霉毒素的回收率随着使用次数的增加在逐渐降低, 柱的回收情况的考察,每份样品中同时加入 33 ng 黄曲霉毒 特别是 G2 回 收 率 降 低 明 显,第 二 次 使 用 后 回 收 率 降 低 至 素对照品进行回收,结果见表 4。 16. 2% 和 22. 5% ,第三次使用后回收率降低至 3. 7% ,4. 1% 。
【Abstract】 Objective To investigate the influence of categories of traditional Chinese medicinal materials and treatment methods on repeated usings of immunoaffinity columns in determination of aflatoxins,and study the possibility of repeated usings. Methods The different samples including aflatoxins control substance were analyzed by the immunoaffinity column purification coupled with HPLC and post-column fluorescence detection,and recoveries were obtained after repeated usings of immunoaffinity columns. At the same time we studied on recoveries in different treatment methods of immunoaffinity columns. Results The influence of categories of traditional Chinese medicinal materials on repeated usings of immunoaffinity columns is very large. Some immunoaffinity columns aftering purificating seed species Chinese medicinal materials can be reused three times with high recovery,some rhizoma species with reducing recoveries significantly,especially the recovery of G2. Organic solvent,air exposure and renaturation tione can effect the repeated usings of immunoaffinity columns. Conclusion Categories of traditional Chinese medicinal materials and treatment methods have a significant effect on repeated usings of immunoaffinity columns in determination of aflatoxins.
