实验动物麻醉药物使用指南
常用实验动物全身性麻醉药物的使用

常用实验动物全身性麻醉药物的使用实验动物全身性麻醉药物的使用在科研和医学领域具有重要意义。
全身性麻醉药物可以抑制动物神经系统,使其处于无痛觉、无意识状态,以便于进行实验操作或治疗。
本文将介绍全身性麻醉药物的分类、使用方法、注意事项及发展趋势。
全身性麻醉药物可根据作用机制分为吸入性麻醉药物和静脉麻醉药物两类。
吸入性麻醉药物通过动物呼吸系统进入体内,主要包括氟烷、甲氧氟烷等。
这类药物可以在动物体内迅速分布,起效快,但排出也较快,需要连续给药以维持麻醉状态。
静脉麻醉药物则通过静脉注射进入动物体内,如丙泊酚、硫喷妥钠等。
这类药物起效较慢,但维持时间较长,且对动物循环系统影响较小。
在使用全身性麻醉药物时,需根据实验需求和动物种类选择合适的药物。
吸入法适用于短期、小型实验,可以通过面罩或注射器给予。
静脉注射法则适用于大型、长期实验,需通过静脉穿刺或导管给予。
在用药过程中,需密切动物的呼吸、心率、体温等指标,以及药物使用量和时间。
使用全身性麻醉药物时需注意以下事项:要严格控制药物剂量,根据动物体重、体型等因素进行个性化给药。
要避免使用时间过长,以免动物出现耐药性或药物残留。
要动物的生命体征,一旦出现异常情况,应立即停止给药并采取相应救治措施。
应尽量选择不良反应小的全身性麻醉药物,以减少对动物的损害。
近年来,随着科技的不断进步,全身性麻醉药物的研究和开发也取得了很多进展。
新型麻醉药物的研发不仅可以提高麻醉效果,还可以降低不良反应发生率。
随着麻醉监控技术的发展,对麻醉药物的用量和麻醉深度的把握更加准确,从而提高了实验的准确性和安全性。
实验动物全身性麻醉药物的使用在科研和医学领域中具有重要作用。
在选择和使用全身性麻醉药物时,需遵循科学、规范的原则,动物的生理变化和药物的不良反应。
随着科技的不断进步,相信未来全身性麻醉药物的研发和麻醉监控技术将取得更加显著的成果,为科研和医学事业的发展做出更大的贡献。
动物实验中,麻醉剂的选择至关重要。
标准操作规程(SOP)——实验动物的麻醉

标准操作规程(SOP)——一、目的该文件用以说明实验动物麻醉的具体操作以及操作规范,以保证麻醉剂量准确,使实验动物处于麻醉状态,实验顺利进行。
同时保证操作人员的安全。
二、范围适用于中国国家流感中心的所有技术人员对实验动物进行麻醉。
三、程序(一)生物安全要求动物实验涉及到H5、H7亚型高致病性禽流感病毒,H2N2亚型流感病毒的时候,动物麻醉操作需要在ABSL-3级实验室进行操作。
操作其他病毒的时候,动物麻醉操作需要在ABSL-2级实验室中进行。
(二)材料1.实验动物:中小型实验动物,如:小鼠、大鼠、豚鼠、兔及雪貂等。
2.动物实验中常用的麻醉剂分为三类,即挥发性麻醉剂、非挥发性麻醉剂和中药麻醉剂。
(1)挥发性麻醉剂这类麻药包括乙醚、氯仿等。
乙醚吸入麻醉适用于各种动物,其麻醉量和致死量差距大,所发安全度亦大,动物麻醉深度容易掌握,而且麻后苏醒较快。
其缺点是对局部刺激作用大,可引起上呼吸道粘膜液体分泌增多,再通过神经反射可影响呼吸、血压和心跳活动,并且容易引起窒息,故在乙醚吸入麻醚时必须有人照看,以防麻醉过深而出现上情况。
(2)非挥发性麻醉剂这类麻醉剂种类较多,包括苯巴比妥钠、戊巴比妥钠、硫喷妥钠等巴比妥类的衍生物,氨基甲酸乙脂和水合氯醛。
这些麻醉剂使用方便,一次给药可维持较长的麻醉时间,麻醉过程较平衡,动物无明显挣扎现象。
但缺点是苏醒较慢。
(3)中药麻醉剂动物实验时有时也用到象洋金花和氢溴酸东莨菪碱等中药麻醉剂,但由于其作用不够稳定,而且常需加佐剂麻醉效果才能理想,故在使用过程中不能得到普及,因而,多数实验室不选用这类麻醉剂进行麻醉。
(三)实验步骤1.吸入法用一块圆玻璃板和一个钟罩或一个密闭的玻璃箱作为挥发性麻醉剂的容器,多选用乙醚作麻醉药。
麻醉时用几个棉球,将乙醚倒可其中,迅速转入钟罩或箱内,让其挥发,然后把待麻醉动物投入,约隔4-6min即可麻醉,麻醉后应立即取出,并准备一个蘸有乙醚的棉球小烧杯,在动物麻醚变浅时给套在鼻上使其补吸麻醉药。
实验动物麻醉药物使用指南教案

实验动物麻醉药物使用指南教案一、教学目标1.了解实验动物麻醉药物的分类和作用机制。
2.了解实验动物麻醉药物的常用剂量和给药途径。
3.掌握实验动物麻醉药物的使用指南。
二、教学重点1.实验动物麻醉药物的分类和作用机制。
2.实验动物麻醉药物的常用剂量和给药途径。
三、教学难点1.实验动物麻醉药物的使用指南。
四、教学内容1.实验动物麻醉药物的分类和作用机制:(1)麻醉药物可分为全身麻醉药物和局部麻醉药物。
(2)全身麻醉药物可分为静脉全身麻醉药物和吸入全身麻醉药物。
(3)主要作用机制有镇痛、镇静、肌肉松弛和失去意识。
2.实验动物麻醉药物的常用剂量和给药途径:(1)注射剂量:根据动物种类和体重进行计算和调整。
(2)给药途径:静脉注射、肌肉注射、皮下注射、口服等。
3.实验动物麻醉药物的使用指南:(1)选择适当的麻醉药物和剂量。
(2)选择合适的给药途径。
(3)注意麻醉药物的副作用和不良反应。
(4)掌握动物麻醉的监测指标及方法。
五、教学方法1.讲授:通过讲解的方式向学生介绍实验动物麻醉药物的分类、作用机制、常用剂量和给药途径。
2.讨论:带领学生进行讨论,让学生思考实验动物麻醉药物的使用指南,以及如何进行监测和调整。
3.案例分析:通过实际案例分析的方式,让学生运用所学知识解决实际问题。
六、教学过程1.引入:提问学生实验动物使用麻醉药物的意义和目的。
2.讲解:介绍实验动物麻醉药物的分类和作用机制。
3.讲解:介绍实验动物麻醉药物的常用剂量和给药途径。
4.讨论:带领学生进行讨论,让学生思考实验动物麻醉药物的使用指南。
5.案例分析:通过实际案例分析的方式,让学生运用所学知识解决实际问题。
6.总结:对所学知识进行总结,强调实验动物麻醉药物的使用指南。
七、教学资源1.实验动物麻醉药物的教材资料。
2.实验室中常见的麻醉药物。
八、教学评估1.课堂讨论:通过课堂上的讨论,评估学生对实验动物麻醉药物的理解和应用能力。
2.案例分析:通过案例分析,评估学生运用所学知识解决实际问题的能力。
家兔麻醉剂量

家兔麻醉剂量《家兔麻醉剂量》一、常用麻醉药物家兔可以使用甲强龙(Ketamine)作为麻醉药物,常用剂量为80-110mg/kg。
二、小动物常用麻醉剂量1.甲强龙(Ketamine):80-120mg/kg2.瑞芬太尼(Ropivacaine):0.2-0.4ml/kg3.阿片类(opiates):5-10mg/kg4.咪唑胺(Midazolam):0.1-0.2mg/kg5.布比卡因(Bupivacaine):0.3-0.5ml/kg三、用药说明1.甲强龙(Ketamine):应按体重以80-120mg/kg计算,用醋酸甲强龙可混入2-5%糖水或0.9%氯化钠溶液或果糖溶液,每次给药量不超过1ml,用针注射,肌肉注射,耳静脉注射,口服均可,每次服药间隔不应少于2小时。
用药后可观察到家兔微微发抖,但不会引起太多痛苦。
2.瑞芬太尼(Ropivacaine):应按体重以0.2-0.4ml/kg计算,必须在0.9%氯化钠溶液或0.2%碳酸氢钠溶液中稀释,以减少刺激性,降低副作用。
每次给药量不超过1ml,可静脉或肌肉注射,每次服药间隔不应少于2小时。
3.阿片类(opiates):应按体重以5-10mg/kg计算,给药量不超过0.3ml,可静脉注射,也可肌肉注射,每次服药间隔不应少于2小时。
4.咪唑胺(Midazolam):应按体重以0.1-0.2mg/kg计算,可静脉注射,也可肌肉注射,每次给药量不超过0.2ml,每次服药间隔不应少于2小时。
5.布比卡因(Bupivacaine):应按体重以0.3-0.5ml/kg计算,必须稀释,稀释溶液可使用0.9%氯化钠溶液或0.2%碳酸氢钠溶液,可静脉或肌肉注射,每次给药量不超过1ml,每次服药间隔不应少于2小时。
四、注意事项1、用药前应全面检查家兔的体温、心率、呼吸率等,并合理安排麻醉剂量。
2、用药应在专业人员的指导下进行,用药完毕后应定期进行观察,及时发现异常反应,采取必要的措施。
动物麻醉用药指南Anesthesia and Analgesia in Laboratory Animals.1997
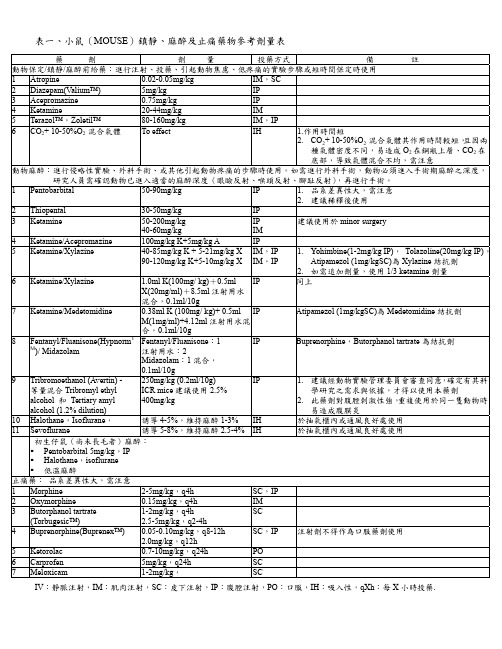
表一、小鼠(MOUSE)鎮靜、麻醉及止痛藥物參考劑量表藥劑劑量投藥方式備註動物保定/鎮靜/麻醉前給藥:進行注射、投藥、引起動物焦慮、低疼痛的實驗步驟或短時間保定時使用1 Atropine 0.02-0.05mg/kg IM,SC2 Diazepam(Valium™) 5mg/kg IP3 Acepromazine 0.75mg/kg IP4 Ketamine 20-44mg/kg IM5 Terazol™,Zoletil™ 80-160mg/kg IM,IP6 CO2+ 10-50%O2 混合氣體 Toeffect IH 1.作用時間短2.CO2+ 10-50%O2 混合氣體其作用時間較短,且因兩種氣體密度不同,易造成O2在鋼瓶上層、CO2在底部,導致氣體混合不均,需注意動物麻醉:進行侵略性實驗、外科手術、或其他引起動物疼痛的步驟時使用。
如需進行外科手術,動物必須進入手術期麻醉之深度,研究人員需確認動物已進入適當的麻醉深度(眼瞼反射、喉頭反射、腳趾反射),再進行手術。
1 Pentobarbital 50-90mg/kg IP 1.品系差異性大,需注意2.建議稀釋後使用2 Thiopental 30-50mg/kg IP3 Ketamine 50-200mg/kg40-60mg/kg IPIM建議使用於minor surgery4 Ketamine/Acepromazine 100mg/kgK+5mg/kgA IP5 Ketamine/Xylazine 40-85mg/kg K + 5-21mg/kg X90-120mg/kg K+5-10mg/kg X IM,IPIM,IP1.Yohimbine(1-2mg/kg IP), Tolazoline(20mg/kg IP),Atipamezol (1mg/kgSC)為Xylazine結抗劑2.如需追加劑量,使用1/3 ketamine劑量6 Ketamine/Xylazine 1.0ml K(100mg/ kg)+0.5mlX(20mg/ml)+8.5ml注射用水混合,0.1ml/10gIP 同上7 Ketamine/Medetomidine 0.38ml K (100mg/ kg)+ 0.5mlM(1mg/ml)+4.12ml注射用水混合,0.1ml/10gIP Atipamezol (1mg/kgSC)為Medetomidine結抗劑8 Fentanyl/Fluanisone(Hypnorm TM)/ Midazolam Fentanyl/Fluanisone:1注射用水:2Midazolam:1混合,0.1ml/10gIP Buprenorphine,Butorphanol tartrate為結抗劑9 Tribromoethanol(Avertin)- 等量混合Tribromyl ethylalcohol 和 Tertiary amylalcohol (1.2% dilution) 250mg/kg (0.2ml/10g)ICR mice建議使用2.5%400mg/kgIP 1.建議經動物實驗管理委員會審查同意,確定有其科學研究之需求與依據,才得以使用本藥劑2.此藥劑對腹腔刺激性強,重複使用於同一隻動物時易造成腹膜炎10 Halothane,Isoflurane,誘導4-5%,維持麻醉1-3% IH 於抽氣櫃內或通風良好處使用11 Sevoflurane 誘導5-8%,維持麻醉2.5-4%IH 於抽氣櫃內或通風良好處使用初生仔鼠(尚未長毛者)麻醉:Pentobarbital 5mg/kg,IPHalothane,isoflurane低溫麻醉止痛藥:品系差異性大,需注意1 Morphine 2-5mg/kg,q4h SC,IP2 Oxymorphine 0.15mg/kg,q4h IM3 Butorphanoltartrate (Torbugesic™) 1-2mg/kg,q4h2.5-5mg/kg,q2-4hSC4 Buprenorphine(Buprenex™) 0.05-0.10mg/kg,q8-12h2.0mg/kg,q12hSC,IP 注射劑不得作為口服藥劑使用5 Ketorolac 0.7-10mg/kg,q24h PO6 Carprofen 5mg/kg,q24h SC7 Meloxicam 1-2mg/kg, SCIV:靜脈注射,IM:肌肉注射,SC:皮下注射,IP:腹腔注射,PO:口服,IH:吸入性,qXh:每X小時投藥.表二、大鼠(RAT)鎮靜、麻醉及止痛藥物參考劑量表藥劑劑量投藥方式備註動物保定/鎮靜/麻醉前給藥:進行注射、投藥、引起動物焦慮、低疼痛的實驗步驟或短時間保定時使用1 Atropine 0.04-0.1mg/kg IM,SC2 Diazepam(Valium™) 0.5-15mg/kg IP3 Ketamine 22-50mg/kg IM4 CO2 + 10-50%O2 To effect IH 1.作用時間短2.C O2+ 10-50%O2 混合氣體其作用時間較短,且因兩種氣體密度不同,易造成O2在鋼瓶上層、CO2在底部,導致氣體混合不均,需注意動物麻醉:進行侵略性實驗步驟、外科手術、或其他引起動物疼痛的步驟時使用1 Pentobarbital 30-40mg/kg30-60mg/kg IVIP1.以低卡路里飼料飼養的公鼠需使用較高劑量2.重複注射時,會產生抗藥性2 Thiopental (2.5%) 30-100mg/kg30mg/kg IP IV3 Ketamine 100-200mg/kg50-100mg/kg IPIM建議使用於minor surgery4 Ketamine/Xylazine 50-100mg/kgK+10mg/kgX IM,IP 1.Yohimbine(1-2mg/kgIP),Tolazoline(20mg/kgIP),Atipamezol (1mg/kgSC)為Xylazine結抗劑2.如需追加劑量,使用1/3 ketamine劑量5 Terazol™,Zoletil™ 40mg/kg20mg/kg IPIM測量麻醉深度之檢查如眼瞼反應、腳趾、喉頭反射等,在使用此藥劑時不適用6 Zoletil/Xylazine 20-40mg/kgZ+5-10mg/kgX IP 測量麻醉深度之檢查如腳趾反射,在使用此劑量時不適用,需注意7 Ketamine/Medetomidine 60-75mg/kgK+0.25-0.5mg/kgMIP8 Fentanyl/Fluanisone(Hypnorm TM)/ Midazolam Fentanyl/Fluanisone :注射用水:2Midazolam:1混合,2.7-4.0ml/kgIP Buprenorphine, Butorphanol tartrate為結抗劑9 Chloral hydrate(5%) 300-500mg/kg IP 1.建議經動物實驗管理委員會審查同意,確定有其科學研究之需求與依據,才得以使用本藥劑2.此藥劑對腹腔刺激性強,易造成腹膜炎及胃腸道異常蠕動,需注意10 Halothane,Isoflurane,誘導4-5%,維持麻醉1-3% IH 於抽氣櫃內或通風良好處使用Sevoflurane 誘導5-8%,維持麻醉2.5-4%IH 於抽氣櫃內或通風良好處使用11 初生仔鼠(尚未長毛者)麻醉:Pentobarbital 5mg/kg,IPHalothane,isoflurane低溫麻醉止痛藥1 Morphin 1.5-6mg/kg, q2-4h SC2 Butorphanol tartrate(Torbugesic™) 1-2mg/kg,q4h2.5-5mg/kg,q2hSC3 Buprenorphine(Buprenex™) 0.01-0.05mg/kg SC,IP 注射劑不得作為口服藥劑使用4 Ketorolac 3-5mg/kg,q12-24h1 mg/kg,q12-24h PO IM5 Carprofen 5mg/kg,q12h SC6 Meloxicam 1 mg/kg,q24h SC,POIV:靜脈注射,IM:肌肉注射,SC:皮下注射,IP:腹腔注射,PO:口服,IH:吸入性,qXh:每X小時投藥藥劑劑量投藥方式備註動物保定/鎮靜/麻醉前給藥:進行注射、投藥、引起動物焦慮、低疼痛的實驗步驟或短時間保定時使用1 Atropine 0.1mg/kg IP,IM,SC2 Ketamine 22-44mg/kg IM動物麻醉:進行侵略性實驗步驟、外科手術、或其他引起動物疼痛的步驟時使用1 Pentobarbital 50-90mg/kg IP 1.麻醉深度上個體差異大2.會逐漸產生抗藥性2 Ketamine/Xylazine 50-200mg/kg K+ 10mg/kgX IP 1.Yohimbine(1-2mg/kgIP),Tolazoline(20mg/kgIP)為Xylazine結抗劑2.如需追加劑量,使用1/3 ketamine劑量3 Terazol™,Zoletil™ 50-80mg/kg IM,IP4 Zoletil+Xylaxine 20-30mg/kgZ+10mg/kgX IP 測量麻醉深度之檢查如腳趾反射,在使用此劑量時不適用,需注意5 Fentanyl/Fluanisone(Hypnorm TM)/ Midazolam Fentanyl/Fluanisone:1注射用水:2Midazolam:1混合,4ml/kgIP Buprenorphine, Butorphanol tartrate為結抗劑6 Halothane,Isoflurane,誘導4-5%,維持麻醉1-3% IH 於抽氣櫃內或通風良好處使用7 Sevoflurane 誘導5-8%,維持麻醉2.5-4%IH 於抽氣櫃內或通風良好處使用止痛藥1 Butorphanol tartrate(Torbugesic™)1-5mg/kg,q2-4h SC,IM2 Buprenorphine(Buprenex™) 0.05-0.1mg/kg,q8-12h SC,IMIV:靜脈注射,IM:肌肉注射,SC:皮下注射,IP:腹腔注射,PO:口服,IH:吸入性,qXh:每X小時投藥藥劑劑量投藥方式備註動物保定/鎮靜/麻醉前給藥:進行注射、投藥、引起動物焦慮、低疼痛的實驗步驟或短時間保定時使用1 Atropine 0.1mg/kg IP,IM,SC2 Ketamine 44-100mg/kg IM3 Ketamine/Xylazine 50mg/kg K+ 2mg/kgX IM動物麻醉:進行侵略性實驗步驟、外科手術、或其他引起動物疼痛的步驟時使用1 Pentobarbital 36-100mg/kg IP2 Ketamine 150-200mg/kg IP3 Terazol™,Zoletil™ 60mg/kg IM4 Fentanyl/Fluanisone(Hypnorm TM)/ Midazolam Fentanyl/Fluanisone :1注射用水:2Midazolam:1混合,8ml/kgIP Buprenorphine,Butorphanol tartrate為結抗劑5 Tribromoethanol (Avertin) -等量混合Tribromyl ethylalcohol 和 Tertiary amylalcohol (1.25% dilution)250-325mg/kg IP6 Halothane, Isoflurane,誘導4-5%,維持麻醉1-3% IH 於抽氣櫃內或通風良好處使用7 Sevoflurane 誘導5-8%,維持麻醉2.5-4%IH 於抽氣櫃內或通風良好處使用止痛藥1 Butorphanol tartrate(Torbugesic™)0.05-5mg/kg,q2-4h SC2 Buprenorphine(Buprenex™) 0.05-1mg/kg, q8-12h SC,IMIV:靜脈注射,IM:肌肉注射,SC:皮下注射,IP:腹腔注射,PO:口服,IH:吸入性,qXh:每X小時投藥表五、天竺鼠(GUINEA PIG)鎮靜、麻醉及止痛藥物參考劑量表藥劑劑量投藥方式備註動物保定/鎮靜/麻醉前給藥:進行注射、投藥、引起動物焦慮、低疼痛的實驗步驟或短時間保定時使用1 Atropine 0.05mg/kg SC2 Ketamine 22-30mg/kg IM 肌肉注射後易出現自殘行為及肌肉潰爛,需注意3 Diazepam 2.5-5.0mg/kg IM,SC,IV4 Acetylpromazine 5-10mg/kg IM5 Terazol™,Zoletil™ 10-80mg/kg IM,IP 鎮靜時間長動物麻醉:進行侵略性實驗步驟、外科手術、或其他引起動物疼痛的步驟時使用1 Pentobarbital 15-40mg/kg IP2 Thiopental 20mg/kg IV3 Ketamine/Xylazine 44mg/kg K+5-13mg/kgX27mg/kgK+0.6mg/kgX,配合局部投予 0.5ml 1% lidocaine+1:200,000 epinephrine IMIM1.Yohimbine(1-2mg/kgIP),Tolazoline(20mg/kgIP)為Xylazine結抗劑2.如需追加劑量,使用1/3 ketamine劑量4 Fentanyl/Fluanisone(HypnormTM)/ Midazolam Fentanyl/Fluanisone :1注射用水:2Midazolam:1混合,8ml/kgIP Buprenorphine, Butorphanol tartrate為結抗劑5 Terazol™,Zoletil™ 60mg/kg,配合局部投予0.5ml 1% lidocaine + 1:200,000 epinephrineIM,IP 建議使用於minor surgery6 Halothane, Isoflurane,誘導4-5%,維持麻醉1-3% IH 1. 剛吸入藥劑時天竺鼠易憋氣,需注意2. 於抽氣櫃內或通風良好處使用Sevoflurane 誘導5-8%,維持麻醉2.5-4%IH 1.剛吸入藥劑時天竺鼠易憋氣,需注意2. 於抽氣櫃內或通風良好處使用止痛藥1 Butorphanol tartrate(Torbugesic™)0.25-0.4mg/kg SC,IV2 Morphine 2-10mg/kg, q4h SC,IM3 Buprenorphine(Buprenex™) 0.05mg/kg, q8-12h SC4 Aspirin 86mg/kg PO5 Carprofen 2.5mg/kg, q24h POIV:靜脈注射,IM:肌肉注射,SC:皮下注射,IP:腹腔注射,PO:口服,IH:吸入性,qXh:每X小時投藥註:天竺鼠的盲腸可能影麻醉響藥物的吸收及效應。
(精选)动物麻醉剂及麻醉剂量

动物麻醉方法及给药剂量一、动物麻醉的目的1.清醒状态的动物虽然更加接近其生理状态,但是试验过程中的各种强刺激容易引起动物大脑皮质的抑制,使动物机体发生生理机能障碍影响到实验的结果。
甚至引起动物死亡或休克。
2.防止动物伤害实验操作者。
3.基于人道主义的考虑,麻醉是动物保护所必需采取的措施。
二、麻醉的类型和方法1.全身麻醉的方法:吸入麻醉:吸入麻醉是将挥发性麻醉剂或气体的麻醉剂经过动物的呼吸道进入体内产生麻醉的效果。
常见的麻醉剂有乙醚、安氟醚、三氟乙烷等,其中乙醚因麻醉深度容易掌握、安全、动物容易恢复等优点,使用最为广泛。
1)大鼠、小鼠、豚鼠的乙醚麻醉:将含有乙醚的棉球/纱布放在大烧杯中,将动物放入,封口。
动物先兴奋后抑制,自行倒下。
当动物角膜反应迟钝,肌肉紧张度降低时,即可取出动物。
如果动物逐渐恢复肌肉紧张(挣扎),可重复麻醉一次,待平静后即可开始试验。
如果试验时间较长,可将动物固定在其口鼻处放置含有乙醚的棉球或纱布,并在实验中注意动物的反应,适时追加乙醚的吸入量,以维持麻醉的深度和实践。
2)猫、兔的乙醚麻醉:将动物放进内装含有乙醚的棉球/纱布的麻醉瓶中,封口。
经过1~2min,从动物后腿依次出现麻痹现象,而后失去运动能力,表明动物进入麻醉状态。
4~6min后可以将动物麻醉,如观察到动物倾斜不能站立、跌倒时,说明动物已经深度麻醉,立即取出动物,这时动物肌肉松弛、四肢紧张度降低,角膜反射迟钝,皮肤痛觉消失,可进行试验。
3)犬的乙醚麻醉:首先将犬用绳子绑定,根据犬的大小选择适合的麻醉口罩,将纱布/棉花放到口罩内,加入乙醚。
一人固定犬的前后肢,另一人用膝盖顶住犬的胸颈处,一手捏住头颈(注意力量,防止窒息),将口罩套在犬嘴上。
开始乙醚用量可大一些,之后逐渐减少。
犬开始兴奋后出现挣扎、呼吸不规则现象,而后呼吸逐渐平稳,肌肉紧张度逐渐消失,角膜反射迟钝,对皮肤刺激无反应,此时可开始试验。
乙醚吸入如果出现呼吸窒息应暂停吸入乙醚,等呼吸恢复后在继续吸入。
实验动物麻醉药物使用指南

实验动物⿇醉药物使⽤指南实验动物⿇醉药物使⽤指南第⼀部分不同类型⿇醉药物的⼀般特性⼀、镇静剂和安定剂镇静剂使⽤前动物的⽣理状态能显著影响镇静的程度。
给药前攻击性强的、不听话的、极其兴奋的动物会⽐较难处理,除⾮给予⾼剂量的呼吸抑制药物。
1.吩噻嗪类Phenothiazines常⽤制剂:⼄酰丙嗪acepromazine,氯丙嗪chlorpromazine,丙嗪promazine理想疗效●增强⿇醉剂、安眠药和⿇醉性镇痛药的效果(包括减少药物剂量,延长作⽤时间和顺利地从⿇醉中恢复)●⽌吐作⽤●促进⾻骼肌松弛●引起兔⽿静脉⾎管扩张不良反应●中度低⾎压●导致低体温症潜在的、与研究相关的并发症●基底神经节多巴胺阻塞●降低⾃发肌动活动●阻塞⼉茶酚胺的外周作⽤●下丘脑⼉茶酚胺耗尽引起的低体温症●⾼剂量阻碍FSH和LH的释放●提⾼⿏、绵⽺和⼭⽺的催乳素⽔平●发⽣肾上腺素通过肾上腺髓质释放引起的⾼⾎糖●应⽤于猫,⼩剂量可减⼩肾上腺素导致的⾎管加压作⽤,⼤剂量可翻转⾎管加压作⽤●减少动物的⾎细胞⽐容●拮抗阿朴吗啡诱发的⽝呕吐●可能引起⽝⼼律不齐●⾼剂量的氯丙嗪使猫产⽣颤动和僵硬●可能导致胎⿏产⽣唇裂和腭裂●长时间使⽤可产⽣眼部病变2.苯⼆氮平类药物Benzodiazepines常⽤制剂:地西泮diazepam,咪达唑仑midazolam理想疗效●镇静作⽤因物种⽽异(作⽤最⼩的是⽝,最⼤的是兔⼦和⿏)●增强⼤部分⿇醉药和⿇醉镇痛药的药效●良好的松弛⾻骼肌作⽤不良反应●正常剂量下⽆不良反应●管制药物潜在的、与研究相关的并发症●主要通过作⽤脑⼲⽹状结构抑制中枢神经系统●阻断脊髓多突触反射作⽤●减少⼤⿏脑和纹状体边缘区多巴胺的合成●增强GABA介导的中枢神经系统抑制●在⽝静脉注射后产⽣瞬时的动脉降⾎压作⽤●⼈的腭裂的发⽣与怀孕期间母体摄⼊该药物有关其他●应通过静脉注射地西泮,肌⾁注射和⽪下注射会引起全⾝不均⼀的吸收。
地西泮在溶液中不与其他药物相溶,因此不应与其他药物在同⼀注射器内混合(除氯胺酮)●咪达唑仑可以通过肌⾁注射或⽪下注射途径给药,也可与某些其他药物联合使⽤3.α-2-肾上腺素受体激动剂常⽤制剂:美托咪定xylazine,甲苯噻嗪medetomidine,地托咪定detomidine理想疗效●中枢神经系统抑制剂,镇痛肌⾁松弛剂,⾮⿇醉镇静剂●对⼤多数⿇醉剂有增强作⽤不良反应●当作为主要⿇醉剂时,动物会出现疼痛反应●可产⽣⾼⾎糖和多尿症●⼼⾎管系统的影响多样,常见低⾎压现象●反刍动物需要的剂量是⾷⾁动物的⼗分之⼀●引起缓慢性⼼律失常和⼼输出量减少潜在的、与研究有关的并发症●由于直接刺激中枢神经系统的催吐中⼼,引起⽝诱导性呕吐●抑制⼼肌收缩⼒,减少⼼输出量●增加⼼脏对肾上腺素的敏感性,导致室性⼼律失常,包括纤维性颤动●⽝静脉注射后,动脉⾎压⼀过性升⾼,动脉⾎pH值,氧分压,⼆氧化碳分压不改变●对未经治疗的猪没有影响●⽝的吞⽓症引发的⽓胀恶化●可能导致流产其他●甲苯噻嗪(Xylazine)是⼀种强效的镇静药和中枢神经系统的抑制剂。
实验动物的麻醉方法

实验动物的麻醉方法
实验动物的麻醉方法是根据实验的目的和动物物种的不同而有所区别。
以下是一些常用的麻醉方法:
1. 全身麻醉:使用全身麻醉药物,如氯化乙酰胺或异氟醚等,通过静脉注射或吸入的方式进行麻醉。
这种方法适用于大型动物或需要长时间麻醉的实验。
2. 局部麻醉:使用局部麻醉药物,如利多卡因或普鲁卡因等,通过局部注射或浸润的方式进行麻醉。
这种方法适用于小型动物或需要局部麻醉的实验。
3. 镇静剂:使用镇静剂,如地西泮或苯巴比妥等,通过口服或注射的方式进行麻醉。
这种方法适用于需要轻度麻醉或对镇静剂敏感的动物。
4. 吸入麻醉气体:使用麻醉气体,如笑气或七氟醚等,通过吸入的方式进行麻醉。
这种方法适用于小鼠或需要快速麻醉的实验。
需要注意的是,麻醉方法的选择应根据实验的需要和动物的安全性来确定,并且应严格按照相关伦理和法规要求进行操作。
另外,麻醉时应监测动物的生理指标,确保其在麻醉状态下保持稳定。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验动物麻醉药物使用指南第一部分不同类型麻醉药物的一般特性一、镇静剂和安定剂镇静剂使用前动物的生理状态能显著影响镇静的程度。
给药前攻击性强的、不听话的、极其兴奋的动物会比较难处理,除非给予高剂量的呼吸抑制药物。
1. 吩噻嗪类Phenothiazines常用制剂:乙酰丙嗪acepromazine ,氯丙嗪chlorpromazine ,丙嗪promazine理想疗效增强麻醉剂、安眠药和麻醉性镇痛药的效果(包括减少药物剂量,延长作用时间和顺利地从麻醉中恢复)止吐作用促进骨骼肌松弛引起兔耳静脉血管扩张不良反应中度低血压导致低体温症潜在的、与研究相关的并发症基底神经节多巴胺阻塞降低自发肌动活动阻塞儿茶酚胺的外周作用下丘脑儿茶酚胺耗尽引起的低体温症高剂量阻碍FSH 和LH 的释放提高鼠、绵羊和山羊的催乳素水平发生肾上腺素通过肾上腺髓质释放引起的高血糖应用于猫,小剂量可减小肾上腺素导致的血管加压作用,大剂量可翻转血管加压作用减少动物的血细胞比容拮抗阿朴吗啡诱发的犬呕吐可能引起犬心律不齐高剂量的氯丙嗪使猫产生颤动和僵硬可能导致胎鼠产生唇裂和腭裂长时间使用可产生眼部病变2. 苯二氮平类药物Benzodiazepines常用制剂:地西泮diazepam,咪达唑仑midazolam理想疗效镇静作用因物种而异(作用最小的是犬, 最大的是兔子和鼠)增强大部分麻醉药和麻醉镇痛药的药效良好的松弛骨骼肌作用不良反应正常剂量下无不良反应管制药物潜在的、与研究相关的并发症主要通过作用脑干网状结构抑制中枢神经系统阻断脊髓多突触反射作用减少大鼠脑和纹状体边缘区多巴胺的合成增强GABA 介导的中枢神经系统抑制在犬静脉注射后产生瞬时的动脉降血压作用人的腭裂的发生与怀孕期间母体摄入该药物有关其他应通过静脉注射地西泮,肌肉注射和皮下注射会引起全身不均一的吸收。
地西泮在溶液中不与其他药物相溶,因此不应与其他药物在同一注射器内混合(除氯胺酮)咪达唑仑可以通过肌肉注射或皮下注射途径给药,也可与某些其他药物联合使用3. a-2-肾上腺素受体激动剂常用制剂:美托咪定xylazine,甲苯噻嗪medetomidine,地托咪定detomidine理想疗效中枢神经系统抑制剂,镇痛肌肉松弛剂,非麻醉镇静剂对大多数麻醉剂有增强作用不良反应当作为主要麻醉剂时,动物会出现疼痛反应可产生高血糖和多尿症心血管系统的影响多样,常见低血压现象反刍动物需要的剂量是食肉动物的十分之一引起缓慢性心律失常和心输出量减少潜在的、与研究有关的并发症由于直接刺激中枢神经系统的催吐中心,引起犬诱导性呕吐抑制心肌收缩力,减少心输出量增加心脏对肾上腺素的敏感性,导致室性心律失常,包括纤维性颤动犬静脉注射后,动脉血压一过性升高,动脉血pH 值,氧分压,二氧化碳分压不改变对未经治疗的猪没有影响犬的吞气症引发的气胀恶化可能导致流产其他甲苯噻嗪( Xylazine )是一种强效的镇静药和中枢神经系统的抑制剂。
它被用在与其他药物的组合产生麻醉作用。
它的肌肉松弛和镇痛作用都非常好。
但会导致很强的心血管抑制。
美托咪定(Medetomidine)和地托咪定(detomidine)是新开发的、更特效的a-2受体激动剂,导致比甲苯噻嗪作用时间更长、镇静和镇痛作用更强大,并减少对心血管的副作用。
、注射用麻醉剂1. 氯胺酮(Ketamine),最常见注射用麻醉剂之一,可以产生一种分离麻醉状态,其特征是僵直状、浅镇静、遗忘与显著镇痛,并能进入梦境、出现幻觉。
麻醉深度与剂量有关。
可选择性抑制丘脑内侧核,阻滞脊髓网状结构束的上行传导,兴奋边缘系统。
注射后迅速在肝脏中经肝P-450微粒系统代谢为去甲氯胺酮(脱甲基氯胺酮) 。
主要的代谢物通过尿液和胆汁排出体外。
理想疗效对大多数哺乳动物物种的安全、有效无严重的呼吸系统或心血管系统的抑制或肝,肾功能的变化与a-2-肾上腺素能激动剂(甲苯噻嗪)联合使用,增加镇静和镇痛作用许多反射保持不变:角膜瞬目反射,喉,咽反射不良反应不适合单独作为手术麻醉药物,必须与其它麻醉剂联合使用唾液分泌物增加,可能会阻塞呼吸道,使用阿托品预防伴随刺激产生自发的运动动物保持睁眼,可能会导致角膜干燥,使用温和的眼用软膏预防副作用可能包括恢复过程中的抽搐、眩晕和兴奋与苯二氮平类药物(地西泮)联用可缓解肌肉僵硬症状潜在的、与科研相关的并发症可选择性抑制丘脑内侧核、兴奋边缘系统中枢神经系统中GABA 结合的强效抑制剂阻断单胺类神经递质的传导过程,如5 - 羟色胺,多巴胺和去甲肾上腺素发挥选择性的激活心肌作用增加心输出量,平均主动脉压,肺动脉压,中心静脉压,心率增加心肌耗氧量咽和喉反射维持不变,导致喉痉挛的发病率增加,由咽或喉部的分泌物引发的支气管痉挛和咳嗽增加犬脑血流量的80%对甲苯噻嗪的影响,当与氯酮氨联合使用时,甲苯噻嗪是育亨宾的拮抗剂,a-2-肾上腺素受体阻断剂2. 替来他明(乙胺噻吩环己酮)/唑拉西泮(Tiletamine/zolazepam),替来他明是一种注射用麻醉剂,化学结构与氯胺酮相近。
唑拉西泮是一个二氮杂酮类的轻微镇静剂。
理想疗效安全,有效的麻醉时间长达25 分钟适用于小手术,但不适用腹部手术咽喉反射保持正常提供轻度至中度的镇痛不良反应产生似强直性昏厥的麻醉效果;颅神经和脊髓反射良好并可能引起一些运动,该运动与麻醉深度无关动物保持睁眼,瞳孔放大;必须使用温和的眼药膏,以防止角膜干燥建议采用有疼痛反应的刺激监测动物的麻醉深度角膜和踏板反射保持不变,该指标不能代表麻醉深度产生大量唾液,可通过阿托品预处理来控制注射可产生疼痛潜在的、与科研相关的并发症使犬产生持续性心动过速,心博量下降,伴随净心输出量微小变化增加收缩压和舒张压呼吸频率倍增,潮气量降低到一半以下,动脉氧分压水平下降穿过胎盘屏障,抑制新生儿呼吸3. 巴比妥类( Barbiturates )不同于其他镇静剂和麻醉剂,在达到麻醉状态前,它的剂量与抑制的深度正相关。
但使用中间剂量的巴比妥类药物可能诱导兴奋。
巴比妥类药物的主要用途是诱导和保持全身麻醉。
根据巴比妥类静脉注射后麻醉时间的不同分为四组药物:(1) 超短效:美索比妥( methohexital )(作用时间5-15 分钟)(2) 短效:硫戊巴比妥钠( thiamylal sodium ),硫喷妥钠( thiopental sodium )(作用时间10-45 分钟)(3) 中效:戊巴比妥钠( pentobarbital sodium )(作用时间1-3 小时)(4) 长效作用:苯巴比妥( phenobarbital ), 仲丁硫巴比妥( inactin )(作用时间8-24 小时)理想疗效对大多数物种的静脉注射产生平稳快速的作用效果通常给予1/3-1/2 静脉注射剂量即达到有效的血药浓度,然后再静注到手术需要的水平不良反应手术麻醉所需剂量与导致呼吸衰竭所需剂量相近心血管系统和呼吸系统抑制较为常见啮齿动物腹腔内快速注射存在种内差异镇痛作用差血管周围注射可能会引起局部组织坏死(保持在2%以下) 戊巴比妥恢复时间延长,重复注射麻醉时间缩短,静脉注射后出现呼吸暂停是常见的现象与葡萄糖,肾上腺素和氯霉素共同用药可能会延长恢复时间管制药物潜在的、与科研相关的并发症降低脑耗氧量高达55%降低多突触连接对乙酰胆碱的去极化作用的敏感性提高脊髓反射的阈值戊巴比妥对犬的血液动力学效应:平均动脉压先下降,然后恢复到控制水平,最终略有下降,动脉收缩压显著降低,心输出量开始上升,然后逐渐下降,总外周阻力最初下降,然后上升到高于控制值,每搏输出量显著下降,心肌收缩力显著下降。
心室纤维性颤动发生率增加动脉内注射引起动脉壁痉挛,可能会导致坏疽。
在大鼠中,如果在正常的促性腺激素的释放之前注射戊巴比妥,阻止LH和FSH 的释放外周血管舒张加重低体温症反复使用产生由肝微粒体酶的代谢率增加引起的耐药。
4. 丙泊酚( Propofol )是酚衍生物,可作为单一麻醉剂进行短效操作或作为诱导剂在全身麻醉前使用。
它是一种油基的乳剂,必须由静脉给药。
它药效迅速,但持续时间短。
必须每3? 5 分钟一次静推注射或持续性滴注以维持麻醉。
即使是长时间麻醉,复苏时间也很短。
丙泊酚不作为单一麻醉剂应用在大型侵入性外科手术中,因其镇痛作用不够。
它可与其他药物联合使用,如地西泮,产生更持久的麻醉效果和平缓的麻醉后恢复过程。
在与其他药物如地西泮联合使用时,丙泊酚的使用剂量应减少来降低不良反应(如低血压) 。
理想疗效安全剂量范围较宽麻醉后恢复时间短有效的帮助兔的气管插管术不良反应可能引起复杂的心血管系统和呼吸系统抑制开瓶不能存储超过8 小时可能出现兔的呼吸系统抑制兔不产生有效镇痛5. 尿烷(Urethane ),该药物在临床兽医学没有应用,只在较少的研究中使用,通常只有特殊的或非存活性程序中。
理想疗效持久(8-10 小时),麻醉平稳提供足够的小型啮齿动物手术所需的镇痛作用仅有微小的心血管和呼吸抑制不良反应仅适用于非存活性程序中致癌物质,有细胞毒性,应尽量减少或避免使用安全使用剂量范围较窄潜在的、与科研相关的并发症缓慢的进入氨基酸和乙醇代谢途径产生肝损害长时间麻醉后产生肺水肿处理建议:尿烷是已知的动物致癌物质,应被视为一个潜在的人类致癌物。
处理建议如下:处理聚氨酯的结晶或粉末状时,需戴口罩、防护眼镜和手套应在通风橱中混合,防止吸入应戴手套处理尿烷麻醉动物的血液或血清承装尿烷的容器,应密封,防止挥发如果发生意外接触皮肤,眼睛或粘膜,应用大量清水清洗孕妇不使用尿烷6. 三溴乙醇(TBE )是一种不挥发的注射性麻醉剂,导致广义的中枢神经系统抑制,包括呼吸和心血管系统。
它由肝脏代谢,并以三溴乙醇的葡糖醛酸的形式从尿液中排出体外。
药物级别的三溴乙醇(例如圣阿韦坦)已经退出市场,用非药物级别的TBE 溶解于叔戊醇中来取代。
该试剂不应用在临床兽医学中,但科研中广泛应用于产生基因工程大鼠小鼠的胚胎移植手术中。
但该试剂应用于啮齿动物日常麻醉是有争议的,因此采用有效的药物级的其他药物替代。
在实验动物中的三溴乙醇使用必须经IACUC 审查和批准。
如果有足够的科学必要性,该试剂的使用可被批准,实验室负责人需要保障该药物准备,储存和使用的过程,以确保其稳定,无菌和有效(准备和处理建议见下)。
推荐三溴乙醇仅用在非存活性程序中。
理想疗效对大部分的啮齿类动物产生手术麻醉作用良好的肌肉松弛作用不良反应麻醉持续时间不稳定常用的腹腔注射时,伴随严重的不良反应(腹腔炎或死亡)建议该药物尽量用在非存活性程序中。
如果实验动物经腹腔注射三溴乙醇后,需要连续几天的悉心照料和密切监视,如出现任何病症和死亡应报告校园兽医所用的溶剂,要远离火源,存储在防爆冰箱中三溴乙醇刺激皮肤,眼睛和呼吸道,应在通风橱中准备和处理,并戴手套,口罩,防护眼镜和穿白大褂。
