人教版化学必修二2.2 化学能与电能 讲课课件优品课件ppt
合集下载
人教版化学必修二2.2-化学能与电能-配套讲课课件

A.CH3OH(g)+O2(g)===H2O(l)+CO2(g)+2H+(aq)+2e- B.O2(g)+4H+(aq)+4e-===2H2O(l)
C.CH3OH(g)+H2O(l) -6e- ===CO2(g)+6H+(aq) D.O2(g)+2H2O(l)+4e-===4OH-(aq)
【答案】 C 【点拨】 甲醇燃料电池是甲醇在负极发生氧化反应,氧气在 正极发生还原反应,故B、D错误;A项不是电极反应式。
特点:高能电池,电压高,质量轻, 贮存时间长等。
用途:电脑、手表、心脏起搏器等。
(3)燃料电池
氢氧燃料电池(碱性介质):
负极:
2H2+4OH— -4e— =4H2O (氧化反应)
正极:
氢氧燃料电池结构
O2+H2O+4e—=4OH—(还原反应) 总反应:2H2+O2=2H2O
练习 科学家近年来研制出一种新型细菌燃料电池,利 用细菌将有机物转化为氢气,氢气进入以磷酸为电解质的 燃料电池发电,电池负极反应为( )
阳离子向正极移动 阴离子向负极移动
练习2:请在图上标出电子的流动方向和电流方向,
并判断正负极,写出电极反应式和总反应式.
I e-
e- I
Ag
Fe
Zn
Cu
H2SO4 (aq)
CuSO4 (aq)
负极( Fe ): Fe-2e - = Fe 2+ . 负极( Zn): Zn-2e - = Zn2+ .
人教版高一化学必修二第二章第二节化学能和电能
间接:化学能燃烧热能蒸汽机械能发动机电能
装置
直接:
原电池
工 作
概
构 成
原念条
理
件
原电池知识要点
C.CH3OH(g)+H2O(l) -6e- ===CO2(g)+6H+(aq) D.O2(g)+2H2O(l)+4e-===4OH-(aq)
【答案】 C 【点拨】 甲醇燃料电池是甲醇在负极发生氧化反应,氧气在 正极发生还原反应,故B、D错误;A项不是电极反应式。
特点:高能电池,电压高,质量轻, 贮存时间长等。
用途:电脑、手表、心脏起搏器等。
(3)燃料电池
氢氧燃料电池(碱性介质):
负极:
2H2+4OH— -4e— =4H2O (氧化反应)
正极:
氢氧燃料电池结构
O2+H2O+4e—=4OH—(还原反应) 总反应:2H2+O2=2H2O
练习 科学家近年来研制出一种新型细菌燃料电池,利 用细菌将有机物转化为氢气,氢气进入以磷酸为电解质的 燃料电池发电,电池负极反应为( )
阳离子向正极移动 阴离子向负极移动
练习2:请在图上标出电子的流动方向和电流方向,
并判断正负极,写出电极反应式和总反应式.
I e-
e- I
Ag
Fe
Zn
Cu
H2SO4 (aq)
CuSO4 (aq)
负极( Fe ): Fe-2e - = Fe 2+ . 负极( Zn): Zn-2e - = Zn2+ .
人教版高一化学必修二第二章第二节化学能和电能
间接:化学能燃烧热能蒸汽机械能发动机电能
装置
直接:
原电池
工 作
概
构 成
原念条
理
件
原电池知识要点
人教版高中化学必修二课件-2.2化学能与电能

第二节 化学能与电能
思考:火力发电有什么缺点?
1.煤炭是非可再生资源,会造成能源危机
2.煤炭燃烧会产生污染性气体 3.经多次转换,能量损耗大,燃料的利用率低
直接?
原电池:把化学能转变为电能的装置。
探究:原电池由几部分组成,它的构成条件是什么?
第一组: 原电池 的两级
第二组: 原电池 的溶液
第三组: 原电池 的电路
G
G Cu
G Cu
不偏转
NaCl溶 液
偏转
偏转
电极材料均插入 电解中质。溶液
第三组: 原电池 的电路
实验探究1
G
G Cu
电流计 指针是 否偏转
构成原 电池的 条件三:
不偏转
两极相连形成
偏转
闭。合电路
一、原电池
1、构成原电池的条件(两极一液一连线) ★电极:有两种活泼性不同的金属(或一 种是能导电的非金属单质)作电极 ★溶液:电极材料均插入电解质溶液中 ★导线:两极相连形成闭合电路
3.现有如下两个反应:
(A)NaOH+HCl===NaCl+H2O
(B)Cu+2Ag+===Cu2+
(1)根据两反应本质,判断能否设计成原电池_________。 (2)如果不能,说明其原因_______________。 (3)如果可以,则写出正、负极材料、 其电极反应式、反应类型(“氧化反应”或“还原反应”): 负极:________,__________________,________。 正极:________,_____________________,________。
【当堂过关】 1.下列装置能形成原电池的是( )
A.①②③⑦ C.①②③④
B.①②⑤⑥ D.①②③⑥⑦
思考:火力发电有什么缺点?
1.煤炭是非可再生资源,会造成能源危机
2.煤炭燃烧会产生污染性气体 3.经多次转换,能量损耗大,燃料的利用率低
直接?
原电池:把化学能转变为电能的装置。
探究:原电池由几部分组成,它的构成条件是什么?
第一组: 原电池 的两级
第二组: 原电池 的溶液
第三组: 原电池 的电路
G
G Cu
G Cu
不偏转
NaCl溶 液
偏转
偏转
电极材料均插入 电解中质。溶液
第三组: 原电池 的电路
实验探究1
G
G Cu
电流计 指针是 否偏转
构成原 电池的 条件三:
不偏转
两极相连形成
偏转
闭。合电路
一、原电池
1、构成原电池的条件(两极一液一连线) ★电极:有两种活泼性不同的金属(或一 种是能导电的非金属单质)作电极 ★溶液:电极材料均插入电解质溶液中 ★导线:两极相连形成闭合电路
3.现有如下两个反应:
(A)NaOH+HCl===NaCl+H2O
(B)Cu+2Ag+===Cu2+
(1)根据两反应本质,判断能否设计成原电池_________。 (2)如果不能,说明其原因_______________。 (3)如果可以,则写出正、负极材料、 其电极反应式、反应类型(“氧化反应”或“还原反应”): 负极:________,__________________,________。 正极:________,_____________________,________。
【当堂过关】 1.下列装置能形成原电池的是( )
A.①②③⑦ C.①②③④
B.①②⑤⑥ D.①②③⑥⑦
高中化学第二节化学能与电能课件新人教必修2.ppt
实验探
究
Zn
Cu
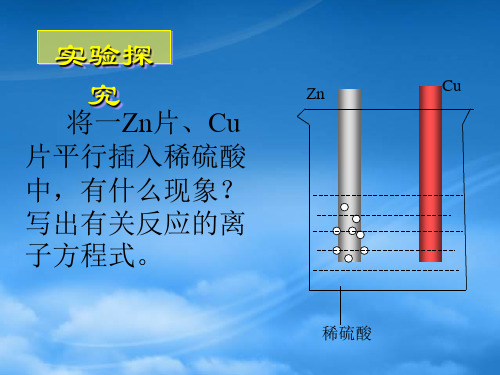
将一Zn片、Cu
片平行插入稀硫酸
中,有什么现象?
写出有关反应的离 子方程式。
稀硫酸
实验探 究
将Zn片、Cu片 上端连接插入稀硫 酸中,有什么现象? 为什么?
稀硫酸
实验探
Zn
Cu
究
稀硫酸
Zn
Cu 现象
(1)电流表指针有偏转
(2)铜片上有气泡产生
(3)锌片不断溶解
稀硫酸
Zn
ee-
Zn
Cu
(E) 酒精
(F) 稀硫酸Zn源自Cu(G)稀硫酸
稀硫酸
4、构成条件: (1)活泼性不同的两种金属
(或金属与非金属导体)做电极 (2)形成闭合回路
(3) 电解质溶液
(4) 自发的氧化还原反应
练习1:下列烧杯中盛放的都是稀硫酸, 在铜电极上能产生气泡的是哪个?写出 电极反应及总反应。
练习2:利用Fe + Cu2+=Fe2++Cu设计一个 原电池,画出示意图,写出电极反应。
探究
Cu
e-
稀硫酸
e-
H+
SO42-
H+ SO42-
H+
H+
Zn
Cu
ee-
H+ Zn2+
H+
稀硫酸
-
Zn ee-
Zn2+
+ Cu-Zn原电池:
Cu 负极:(氧化反应)
锌片:Zn-2e-=Zn2+
正极:(还原反应)
铜片:2H++2e-=H2↑
H+
总反应:
H+
究
Zn
Cu
将一Zn片、Cu
片平行插入稀硫酸
中,有什么现象?
写出有关反应的离 子方程式。
稀硫酸
实验探 究
将Zn片、Cu片 上端连接插入稀硫 酸中,有什么现象? 为什么?
稀硫酸
实验探
Zn
Cu
究
稀硫酸
Zn
Cu 现象
(1)电流表指针有偏转
(2)铜片上有气泡产生
(3)锌片不断溶解
稀硫酸
Zn
ee-
Zn
Cu
(E) 酒精
(F) 稀硫酸Zn源自Cu(G)稀硫酸
稀硫酸
4、构成条件: (1)活泼性不同的两种金属
(或金属与非金属导体)做电极 (2)形成闭合回路
(3) 电解质溶液
(4) 自发的氧化还原反应
练习1:下列烧杯中盛放的都是稀硫酸, 在铜电极上能产生气泡的是哪个?写出 电极反应及总反应。
练习2:利用Fe + Cu2+=Fe2++Cu设计一个 原电池,画出示意图,写出电极反应。
探究
Cu
e-
稀硫酸
e-
H+
SO42-
H+ SO42-
H+
H+
Zn
Cu
ee-
H+ Zn2+
H+
稀硫酸
-
Zn ee-
Zn2+
+ Cu-Zn原电池:
Cu 负极:(氧化反应)
锌片:Zn-2e-=Zn2+
正极:(还原反应)
铜片:2H++2e-=H2↑
H+
总反应:
H+
人教版化学必修二2.2 化学能与电能-原电池 同步讲课课件最新课件PPT

ZN+CU2+===ZN2++CU,此反应的原电池的正确组成是
()
C
努力,未来老婆的婚纱都是租的。只有你的笑才能让你在无尽黑暗中找到光明。我受过的伤都是我的勋章。知世故而不世故,是最善良的成熟。愿你早日领 教过这世界深深的恶意,然后开启爱他吗谁谁的快意人生。第二名就意味着你是头号输家——科比·布莱恩特。当你感觉累的时候,你正在走上坡路。如果 每个人都理解你,那你得普通成什么样。赚钱的速度一定要超过父母变老的速度。不断地发现以前的自己是个傻逼的过程,就是成长。脾气永远不要大于本 事。你那能叫活着么?你那“你如今的气质里,藏着你走过的路,读过的书,和爱过的人。”素质是家教的问题,和未成年没关系。总会有人是第一,那为 什么不能是我?你可以没钱没颜,但你不可以不努力。如果今天我取得了成功,一定是昨天我拼上了全部努力。阳光里做个孩子风雨里做个大人。枯木逢春
为什么在海水中行驶的船特别容易腐蚀?
为了解决这个问题,在船底绑 很多的锌块,这是什么原理呢?
填空:锌铜-硫酸铜电池
负
氧化
锌片: 极 ,Z发n-生2e-=反Zn应2+,
电极反应: ________________
铜片:_正__极 发生 _还__原___反应,
电极反应:__C_u_2_+_+_2_e_-__=_C_u_____
2001年我国发电总量构成图
火电站工作原理示意图
1.我国煤炭资源丰富,廉价方便.
1.排出大量的温室效应气体. 2.有废气可能导致酸雨 3.废料 4.废水 5.能量转换效率低
小结:
1、原电池的定义: 2、工作原理: 3、反应本质: 4、电子流向(外电路) : 5、溶液中(内电路)离子移动: 6、如何判断原电池的正负极: 7、原电池原理的应用:
人教版高中化学必修2-2.2 化学能和电能-课件(共16张PPT)

第2节 化学能与电能
电无处不在:
热 电
太 阳
能
风 电
水 电
核
电
电---我们自己做
化学能 ? 电能
实验探究:
Zn片
实验1
锌片
现象
Zn表面冒气泡,Zn溶解 Zn+2H+ = Zn2++H2↑ (发生氧化还原反应)
Cu片
现象
实验2
铜片 无明显现象 铜不与硫酸反应
实验3
铜片 锌片
实验4
现象
Cu表面冒气泡 Zn片溶解
同的电极
构成 条件
闭合 回路
电解质溶液
电---我们自己发
再也不用担心手机没电了!
课堂总结
原电池中浮(负极)只羊(氧化)
回回忆忆归 归纳 纳
组成 工作 条件 原理
负化极学能两转极化正为极电 失氧应能电化的子反 装一 一置液回路得还电原子反应
定义
原电池
课堂检测
1.由铜锌和稀硫酸组成的原电池的有关叙述错误 的是( ) C A.锌为负极发生氧化反应 B、铜为正极,不易失去电子而受到保护 C、负极发生还原反应正极发生氧
铜片 锌片 电流表
现象
Cu片有气泡产生 Zn片溶解
电流表指针偏转
原电池:把化学能转变为电能的装置, 叫做原电池。
1)电流计指针为什么会发生偏转? 2)电子从哪里来到哪里去? 3)电流流动的方向如何? 4)硫酸溶液中的阴、阳离子应该怎样运动?
原电池工作原理:
还原剂失去的 电子从锌极流 出
负极
还原剂(Zn)失去电 子,发生氧化反应
Zn-2e-=Zn2+
经外电路
H+
SO42-
电无处不在:
热 电
太 阳
能
风 电
水 电
核
电
电---我们自己做
化学能 ? 电能
实验探究:
Zn片
实验1
锌片
现象
Zn表面冒气泡,Zn溶解 Zn+2H+ = Zn2++H2↑ (发生氧化还原反应)
Cu片
现象
实验2
铜片 无明显现象 铜不与硫酸反应
实验3
铜片 锌片
实验4
现象
Cu表面冒气泡 Zn片溶解
同的电极
构成 条件
闭合 回路
电解质溶液
电---我们自己发
再也不用担心手机没电了!
课堂总结
原电池中浮(负极)只羊(氧化)
回回忆忆归 归纳 纳
组成 工作 条件 原理
负化极学能两转极化正为极电 失氧应能电化的子反 装一 一置液回路得还电原子反应
定义
原电池
课堂检测
1.由铜锌和稀硫酸组成的原电池的有关叙述错误 的是( ) C A.锌为负极发生氧化反应 B、铜为正极,不易失去电子而受到保护 C、负极发生还原反应正极发生氧
铜片 锌片 电流表
现象
Cu片有气泡产生 Zn片溶解
电流表指针偏转
原电池:把化学能转变为电能的装置, 叫做原电池。
1)电流计指针为什么会发生偏转? 2)电子从哪里来到哪里去? 3)电流流动的方向如何? 4)硫酸溶液中的阴、阳离子应该怎样运动?
原电池工作原理:
还原剂失去的 电子从锌极流 出
负极
还原剂(Zn)失去电 子,发生氧化反应
Zn-2e-=Zn2+
经外电路
H+
SO42-
化学必修二化学能与电能 ppt课件

次充电使用。
用途:目前汽车上使用的电瓶大多仍是铅蓄电池,它还
广泛用于国防、生产、生活等领域。
PPT课件
35
2、充电电池
二次电池:氧化还原反应在充电时 可以逆向进行。 优缺点: 可充电,比干电池使用
寿命长;但体积大,有污染
应用: 汽车上使用的电瓶等 总反应:
放电
铅蓄电池 2PbSO4+2H2O
PbO2+Pb+2H2SO4
(二)原电池 1.概念:将化学能直接转变为电能的装置
I
e-
负极 Zn
A
正极 Cu
H+ SO42-H+
PPT课件 9
2.原电池的电极反应:
锌片: Zn - 2e- = Zn2+ (负极)
+ + 2e- = 2H 铜片: (正极)
氧化反应
H2 ↑ 还原反应
电池反应: Zn (总反应)
+
2H+ =
Zn2+ +
PPT课件
22
微观判断
电子流出的极 ——负极
原电池的正负极的判断方法
(根据电子流动 电子流入的极 ——正极 方向)
宏观判断:方法四
较活泼的电极材料 ——负极 ①根据电极材料
②根据原电池电极 发生的反应
较不活泼的电极材料——正极 发生氧化反应的极 ——负极
发生还原反应的极 ——正极 质量增加的电极 ——正极 ③根据电极增重还是减重 工作后 质量减少的电极 ——负极 ④根据电极有气泡冒出: 工作后,有气泡冒出的电极为正极
镉有致癌作用,有被镍氢电池取代的趋势。
PPT课件 38
锂离子电池
锂离子电池是新一代可充电的绿色电池。 特点:高能电池,电压高,质量轻,贮存时间长等。
用途:目前汽车上使用的电瓶大多仍是铅蓄电池,它还
广泛用于国防、生产、生活等领域。
PPT课件
35
2、充电电池
二次电池:氧化还原反应在充电时 可以逆向进行。 优缺点: 可充电,比干电池使用
寿命长;但体积大,有污染
应用: 汽车上使用的电瓶等 总反应:
放电
铅蓄电池 2PbSO4+2H2O
PbO2+Pb+2H2SO4
(二)原电池 1.概念:将化学能直接转变为电能的装置
I
e-
负极 Zn
A
正极 Cu
H+ SO42-H+
PPT课件 9
2.原电池的电极反应:
锌片: Zn - 2e- = Zn2+ (负极)
+ + 2e- = 2H 铜片: (正极)
氧化反应
H2 ↑ 还原反应
电池反应: Zn (总反应)
+
2H+ =
Zn2+ +
PPT课件
22
微观判断
电子流出的极 ——负极
原电池的正负极的判断方法
(根据电子流动 电子流入的极 ——正极 方向)
宏观判断:方法四
较活泼的电极材料 ——负极 ①根据电极材料
②根据原电池电极 发生的反应
较不活泼的电极材料——正极 发生氧化反应的极 ——负极
发生还原反应的极 ——正极 质量增加的电极 ——正极 ③根据电极增重还是减重 工作后 质量减少的电极 ——负极 ④根据电极有气泡冒出: 工作后,有气泡冒出的电极为正极
镉有致癌作用,有被镍氢电池取代的趋势。
PPT课件 38
锂离子电池
锂离子电池是新一代可充电的绿色电池。 特点:高能电池,电压高,质量轻,贮存时间长等。
人教版必修2化学:2.2 化学能与电能 课件(共26张PPT)1

书写原电池电极反应式时注意事项
1、正确判断原电池的正负极,确定两极上 发生的反应。 2、判断电极上得失电子的产物能否与电解质 反应,若能,则书写反应后的电极反应式。
1.我国煤炭资源丰富,廉价方便. 2.电能清洁安全,又快捷方便.
1.排出大量的温室效应气体. 2.有废气可能导致酸雨 3.废料 4.废水 5.能量转换效率低
(燃料)燃烧 蒸汽
发电机
化学能 热能
机械能
电能
燃料中的化学能能否直接转换成电能?
燃料燃烧:氧化还原反应
燃料电池
氢氧燃料电池
酸性电解质溶液 氢氧燃料电池
的电池取出来?
铅蓄电池
二次电池
负极反应方程式:
Pb - 2e- + SO42-= PbSO4 正极反应方程式:
PbO2 +4H+ + SO42- + 2e- = PbSO4+ 2H2O 总反应方程式: PbO2 + Pb + 2H2SO充放4电电=== 2PbSO4 + 2H2O
镍铬电池
Cd为负极,NiO(OH)为正 极,以KOH为电解质 锂电池 最轻的金属,活动性极强
(可以)
(不可以)
(不可以) (不可以)
探究构成原电池的条件
通过以上实验和探究,试说明化学电池由几部 分组成,它的组成条件是什么?
正极、负极、电解质溶液、容器
本质条件:氧化还原反应 电路条件:①电极:两种活泼性不同的金属
(或一种金属和另一种非金属导体) ②电解质溶液 ③闭合回路
判断下列装置能否构成原电池
A
B
C
稀H2SO4溶液
思考:比较装置A和C中铁棒的溶解速度
高中化学必修二课件-2.2化学能与电能-人教版

三、原电池
1. 定义:将化学能直接转化为电能的装置 2. 电极:
负极: 正极:
电流流进的方向 电子流出的方向
电流流出的方向 电子流入的方向
e-
__ 锌
++ 铜
稀硫酸
3、电极反应式
负极: 失电子,发生氧化反应 Zn _ 2e- = Zn2+
总:Zn+2H+=Zn2++H2
正极:得电子,发生还原反应 2H+ + 2e- = H2
_ 锌
eA
+ 铜
稀硫酸
例:请分析如图所示原电池,写出发生的氧化还原反应, 判断电极,并写出电极反应式
得电子,发生还原反应
Zn+CuSO4=ZnSO4+Cu
失电子,发生氧化反应
负极:Zn _ 2e- = Zn2+ 正极:Cu2+ + 2e- = Cu
_ Zn
+ Cu
CuSO4
4、粒子的流向
电子
(外电路):
实验现象:
锌
铜
稀硫酸
Zn表面有气泡产生 Cu表面无气泡产生
二、实验探究
3、Zn—Cu与稀H2SO4
锌
铜
稀硫酸
实验现象:
Zn表面有气泡产生
Cu表面也有气泡产生
2H+ 2e- H2 猜想:
锌失电子流向铜
二、实验探究
4、Zn—Cu与稀H2SO4
A
锌
铜
稀硫酸
现象:
锌片、铜片均有气泡, 电流表指针偏转
结论: 导线中有电流通过,即Zn失去 电子通过导线移动到铜的表面
第二节 化学能与电能
