依那西普注射液说明书
国内上市的抗体类药物
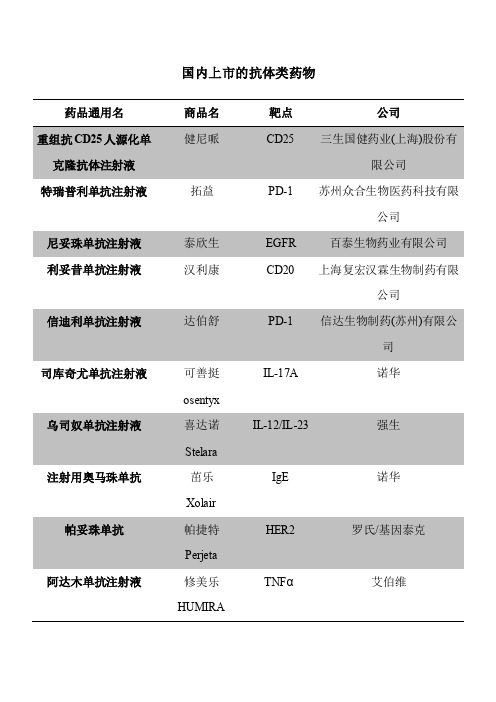
国内上市的抗体类药物药品通用名商品名靶点公司重组抗CD25人源化单克隆抗体注射液健尼哌CD25 三生国健药业(上海)股份有限公司特瑞普利单抗注射液拓益PD-1 苏州众合生物医药科技有限公司尼妥珠单抗注射液泰欣生EGFR 百泰生物药业有限公司利妥昔单抗注射液汉利康CD20 上海复宏汉霖生物制药有限公司信迪利单抗注射液达伯舒PD-1 信达生物制药(苏州)有限公司司库奇尤单抗注射液可善挺osentyxIL-17A 诺华乌司奴单抗注射液喜达诺StelaraIL-12/IL-23 强生注射用奥马珠单抗茁乐XolairIgE 诺华帕妥珠单抗帕捷特PerjetaHER2 罗氏/基因泰克阿达木单抗注射液修美乐HUMIRATNFα艾伯维艾美赛珠单抗注射液舒友立乐HEMLIBRAFIX/FX 罗氏阿柏西普眼内注射溶液艾力雅Eylea(VEGF 拜耳依库珠单抗注射液舒立瑞Soliris补体C5 Alexion Europe SAS依洛尤单抗注射液Evolocumab瑞百安PCSK9 安进帕博利珠单抗可瑞达KeytrudaPD-1 默沙东曲妥珠单抗赫赛汀HerceptinHER2 罗氏/基因泰克纳武利尤单抗欧狄沃OPDIVOPD-1 百时美施贵宝依达赛珠单抗注射液泰毕安PraxbindPraxbind 勃林格殷格翰依那西普注射液恩利EnbrelTNF 辉瑞利妥昔单抗美罗华MabTheraCD20 罗氏/基因泰克贝伐珠单抗安维汀AvastinVEGF-A 罗氏/基因泰克注射用英夫利西单抗类克TNF-α强生RemicadeIL-6R 罗氏托珠单抗注射液雅美罗ActemraCD25 诺华注射用巴利昔单抗舒莱SimulectVEGF 诺华雷珠单抗注射液诺适得LucentisTNF-α强生戈利木单抗注射液欣普尼SimponiEGFR 默克西妥昔单抗爱必妥Erbitux。
依替米星注射液说明书

依替米星注射液说明书标题:依替米星注射液说明书一、药品名称依替米星注射液二、成分每毫升依替米星注射液含有依替米星5毫克。
三、性状本品为无色透明液体。
四、注意事项1. 依替米星注射液仅供医院内使用,由专业医务人员进行注射。
2. 注射前必须由医生评估患者的病情和用药历史,确保合适的使用剂量。
3. 对本品过敏者禁用,同时对亚胺类药物过敏者慎用。
4. 临床使用过程中如出现药物不良反应,请立即停用,并告知医生或药品生产商。
5. 孕妇、哺乳期妇女和儿童慎用。
五、药理作用依替米星为一种抗生素,通过抑制细胞壁合成酶的活性,破坏细菌的细胞壁,从而导致细菌死亡。
六、适应症本品适用于敏感菌引起的感染,包括但不限于肺炎、骨关节感染和泌尿道感染。
七、用法和用量1. 依替米星注射液应由医生根据患者的病情和体重确定剂量和使用频率。
2. 常用剂量为每日2次,每次5毫克/公斤体重,静脉滴注,每次不超过60分钟。
3. 疗程一般为7-14天,具体治疗时长应根据病情严重程度和临床判断进行调整。
八、不良反应1. 常见的不良反应包括恶心、呕吐、腹泻和皮疹等。
2. 严重的不良反应如过敏反应、肝功能损害等少见,如遇到此类情况,请立即停止使用并告知医生。
九、禁忌症1. 本品对依替米星过敏者禁用。
2. 对亚胺类抗生素过敏者慎用。
十、药物相互作用1. 与本品合并使用的其他药物可能产生相互作用,请在使用前告知医生您正在使用的其他药物,以便进行调整。
2. 本品与肌松药物同时使用可能增加肌松效应。
十一、贮藏1. 请将本品存放在阴凉干燥处,避免阳光直射和高温。
2. 请将本品置于儿童无法触及的地方。
十二、生产企业本品由XXX公司生产。
十三、有效期本品有效期为XX年XX月。
本说明书仅为依替米星注射液的简要说明,具体用药请遵循医生的指导。
如有任何疑问,请咨询医生或药品生产商。
泰爱(Telitacicept)注射剂说明书

【药品名称】通用名称:注射用泰它西普商品名称:泰爱英文名称:T elitacicept for Injection汉语拼音:Zhusheyong Taitaxipu【成份】活性成份:泰它西普(重组人B淋巴细胞刺激因子受体-抗体融合蛋白)辅料:盐酸组氨酸、盐酸精氨酸、甘露醇、蔗糖、氢氧化钠【性状】本品应为白色至淡黄色疏松体,复溶后为无色至淡黄色、澄明液体。
【适应症】本品与常规治疗联合,适用于在常规治疗基础上仍具有高疾病活动(例如:抗ds-DNA抗体阳性及低补体、SELENA-SLEDAI评分≥8)的活动性、自身抗体阳性的系统性红斑狼疮(SLE)成年患者。
该适应症是基于一项接受常规治疗仍具有高疾病活动的系统性红斑狼疮成年患者的Ⅱ期临床试验结果给予的附条件批准。
本适应症的完全批准将取决于确证性随机对照临床试验能否证实本品在该患者人群的临床获益。
【规格】80 mg/支。
【用法用量】本品需要在有诊断和治疗系统性红斑狼疮经验的医生指导下使用。
给药方法本品采用皮下注射给药。
注射部位为腹部。
本品为冻干粉,将本品每支(80 mg)用1 ml灭菌注射用水复溶,复溶溶液浓度为每ml含80 mg泰它西普。
复溶时应将灭菌注射用水的水流朝向药瓶的一侧,沿瓶壁缓慢加入,以尽量减少泡沫形成。
复溶期间,将药瓶置于室温条件下,缓慢旋转约60秒,静置至泡沫消退。
切勿摇晃。
待药物溶解后,再次轻轻旋转,药液将会完全混匀。
通常在加入灭菌注射用水后15分钟内完成复溶,但也可能长达30分钟。
复溶后药液为无色至淡黄色、澄明液体。
如观察到可见颗粒,应弃用。
药物溶解后溶液如有小空气泡,不影响使用,但在抽取至无菌注射器后应排除气泡。
本品从复溶到完成皮下注射的总时间不应超过4小时。
剂量本品推荐使用剂量为160 mg/次,每周给药一次。
本品给药期间,经临床医生充分评估患者使用本品的安全耐受性后决定是否需要下调剂量。
如需下调剂量可将每次给药剂量下调为80 mg/次。
最新2021年国家医保目录协议期内谈判部分

乙 110 甲磺酸阿美替尼片
编号
药品名称
176元(55mg/片) 医保支付标准
乙 111 盐酸安罗替尼胶囊
*
药品分类 药品分类 代码
乙 112 克唑替尼胶囊 乙 113 塞瑞替尼胶囊 乙 114 盐酸阿来替尼胶囊 乙 115 培唑帕尼片
乙 116 阿昔替尼片 乙 117 瑞戈非尼片 乙 118 甲磺酸阿帕替尼片
胰高血糖素样肽-1(GLP-1)类似物
*
乙 11 艾塞那肽注射液
*
乙 12 利拉鲁肽注射液
*
乙 13 利司那肽注射液
*
乙 14 贝那鲁肽注射液
乙 15 度拉糖肽注射液 乙 16 聚乙二醇洛塞那肽注射液
*
110元(0.5ml:0.1mg/支); 187元(0.5ml:0.2mg/支)
乙 17 司美格鲁肽注射液
编号
药品名称
乙 48 利奥西呱片
乙 49 马昔腾坦片
XC07 XC07A XC07AB
β-受体阻滞剂 β-受体阻滞剂 选择性β-受体阻滞剂 乙 50
注射用盐酸兰地洛尔
XC08 XC08C XC08CA
XC09 XC09C
XC09D
钙通道阻滞剂 主要作用于血管的选择性钙通道阻滞剂 二氢吡啶衍生物类
乙 51 氨氯地平叶酸片(II)
乙 94 盐酸阿比多尔颗粒
3元(0.1g/袋)
乙 95 法维拉韦片(又称:法匹拉韦片) 3.69元(0.2g/片)
乙 96 玛巴洛沙韦片
XL
抗肿瘤药及免疫调节剂
药品分类 药品分类 代码
编号
药品名称
XL01
抗肿瘤药
XL01B
抗代谢药
XL01BC
依奇珠单抗注射液Ixekizumab-详细说明书与重点

依奇珠单抗注射液Ixekizumab详细说明书与重点一、药品概述依奇珠单抗注射液(Ixekizumab)是一种针对中重度斑块状银屑病和活动性银屑病关节炎的创新生物制剂。
本药品通过靶向抑制白介素17A(IL17A)的作用,有效缓解银屑病症状,提高患者生活质量。
二、成分及作用机制依奇珠单抗注射液主要成分为人源化单克隆抗体,能特异性结合IL17A,阻止其与受体结合,从而降低炎症反应。
IL17A是一种关键炎症因子,参与银屑病等疾病的发病过程。
三、适应症1. 中重度斑块状银屑病;2. 活动性银屑病关节炎。
四、用法用量依奇珠单抗注射液通过皮下注射给药。
具体用药方案如下:1. 成人患者(体重≥50kg):首次剂量为160mg,之后每两周注射一次80mg,或每月注射一次240mg;2. 成人患者(体重<50kg):首次剂量为80mg,之后每两周注射一次40mg,或每月注射一次160mg。
请在专业医生指导下进行用药,并根据病情调整剂量。
五、不良反应1. 常见不良反应:上呼吸道感染、注射部位反应、真菌感染等;2. 少见不良反应:关节痛、皮肤瘙痒、结膜炎等;3. 极少数患者可能出现过敏反应,如皮疹、呼吸困难等。
六、禁忌症1. 对本品活性成分或辅料过敏的患者;2. 患有严重感染的患者;3. 孕妇及哺乳期妇女。
请务必在医生指导下使用本药品,以确保用药安全。
七、注意事项1. 治疗期间,请密切关注身体状况,如出现感染症状,应及时告知医生。
2. 本药品可能会增加结核病的风险,请在用药前进行结核筛查。
3. 对于患有慢性或复发性感染、免疫抑制状态或免疫系统疾病的患者,使用本药品需谨慎。
4. 老年患者使用本药品时,无需调整剂量,但需注意身体状况的变化。
5. 驾驶或操作重型机械的患者在使用本药品后,若出现头晕、疲劳等不适,请避免进行这些活动。
八、药物相互作用1. 活疫苗:使用本药品期间,应避免接种活疫苗。
2. 免疫抑制剂或生物制剂:与其他免疫抑制剂或生物制剂同时使用可能会增加感染风险,请咨询医生。
依马利尤单抗注射液说明书

核准日期:修改日期:依马利尤单抗注射液说明书本品为附条件批准上市,请仔细阅读说明书并在医师指导下使用。
【药品名称】通用名称:依马利尤单抗注射液商品名称:伽蜜芬®/Gamifant®英文名称:Emapalumab Injection汉语拼音:Yimaliyou Dankang Zhusheye【成份】活性成份:依马利尤单抗依马利尤单抗是一种高亲和力全人源化IgG1 λ2型单克隆抗体,与可溶性和受体结合型的IFNγ结合,中和其生物活性。
辅料:L-组氨酸、L-组氨酸盐酸盐一水合物、氯化钠、聚山梨酯80。
【性状】澄清至微浊、无色至微黄色溶液。
【适应症】本品适用于难治性、复发性或进展性、或对常规疗法不耐受的原发性噬血细胞性淋巴组织细胞增多症(HLH)成人和儿童(新生儿及以上)患者。
本品基于境外数据获得附条件批准上市,治疗中国患者的有效性和安全性尚待上市后进一步确证。
【规格】10 mg(2 ml)/瓶。
【用法用量】安全性评估监测在开始本品治疗之前在开始本品治疗之前,通过结核菌素皮肤试验(PPD)或IFNγ释放试验进行潜伏结核感染检测,并评估患者罹患结核的危险因素。
对存在罹患结核风险或已知PPD试验结果呈阳性或IFNγ释放试验结果阳性的患者进行预防性抗结核治疗。
本品治疗期间每2周监测一次结核、腺病毒、EBV和CMV,并根据临床指征进行监测。
预防治疗及合并用药治疗前预防治疗在本品给药前,应进行带状疱疹、耶氏肺孢子虫和真菌感染预防性治疗。
治疗期间合并用药对于基线未接受地塞米松治疗的患者,在本品治疗的前一天开始给予地塞米松,日剂量至少5至10 mg/m2。
对于基线正在接受地塞米松治疗的患者,可以继续常规剂量治疗(日剂量至少为5 mg/m2)。
可以根据临床医师的评估对地塞米松进行逐渐减量(见【临床试验】)。
推荐剂量本品推荐起始剂量为1 mg/kg,静脉输注,每周2次(每3至4天一次),每次输注时间需大于1小时。
山西省2023版“双通道”药品名单

附件:1山西省2023版“双通道”药品名单序号药品名称/通用名备注1昂丹司琼口溶膜按说明书使用2奈妥匹坦帕洛诺司琼胶囊按说明书使用3精氨酸谷氨酸注射液限肝性脑病。
4利那洛肽胶囊限成人便秘型肠易激综合征(IBS-C)O5曲前列尼尔注射液限肺动脉高压(PAH,WHO分类1)。
6重组人血小板生成素注射液限实体瘤化疗后所致的血小板减少症或原发免疫性血小板减少症(ITP)O7注射用罗普司亭限对其他治疗(例如皮质类固醇、免疫球蛋白)治疗反应不佳的成人(218周岁)慢性原发免疫性血小板减少症(ITP)患者。
8注射用罗特西普限P-地中海贫血成人患者。
9拉那利尤单抗注射液限12岁及以上患者预防遗传性血管性水肿(HAE)发作。
10阿布昔替尼片限其他系统治疗(如激素或生物制剂)应答不佳或不适宜上述治疗的难治性、中重度特应性皮炎成人患者。
11泊沙康哩口服混悬液限:1.预防移植后(干细胞及实体器官移植)及恶性肿瘤患者有重度粒细胞缺乏的侵袭性曲霉菌和念球菌感染;2.伊曲康哩或氟康哩难治性口咽念珠菌病;3.接合菌纲类感染。
12注射用硫酸艾沙康哩限侵袭性曲霉病或侵袭性毛霉病的成人患者。
13恩替卡韦颗粒限乙型肝炎。
14艾米替诺福韦按说明书使用15多拉米替片限艾滋病。
16阿兹夫定片按说明书使用17来特莫韦片按说明书使用18来特莫韦注射液按说明书使用19醋酸戈舍瑞林缓释植入剂限子宫内膜异位症使用20盐酸美金刚口溶膜按说明书使用21美泊利珠单抗注射液按说明书使用22环抱素滴眼液(in)限4岁及以上儿童和青少年的严重性春季角结膜炎。
23托伐普坦片按说明书使用24注射用多黏菌素E 甲磺酸钠按说明书使用25泊沙康哩肠溶片限13岁和13岁以上重度免疫缺陷患者。
26泊沙康哩注射液限18岁和18岁以上重度免疫缺陷患者。
27枸椽酸托法替布缓释片按说明书使用28普瑞巴林口服溶液按说明书使用29注射用两性霉素B 胆固醇硫酸酯复合物限患有深部真菌感染的患者;因肾损伤或药物毒性而不能使用有效剂量的两性霉素B 的患 者,或已经接受过两性霉素B 治疗无效的患者均可使用。
依替巴肽注射液(依非巴特注射液) Eptifibatide-详细说明书与重点

依替巴肽注射液(依非巴特注射液) Eptifibatide 英文名称: Eptifibatide Injection。
【成分】本品主要成份为本品主要成份为依替巴肽。
化学名称:N6-(氨基亚氨基甲基)-N2-(3-巯基丙酰基)-L-赖氨酰-甘氨酰-L-α-门冬氨酰-L-色氨酰-L-脯氨酰-L-半胱氨酸氨,环(1 6)-二硫化物。
分子式:C35H49N11O9S2,分子量:831.96。
【性状】本品为无色的澄明液体。
【适应症】用于急性冠状动脉综合征(不稳定型心绞痛/非ST段抬高性心肌梗死)患者,包括接受药物治疗的患者和进行经皮冠状动脉介入术(PCI)的患者,以降低死亡或新发生心肌梗死的联合终点发生率。
用于进行经皮冠状动脉介入术(PCI)的患者,包括进行冠状动脉内支架置入术的患者。
以降低死亡、新发生心肌梗死或需要紧急介入治疗的联合终点发生率。
【规格】10ml∶20mg【用法用量】使用依替巴肽前,应通过以下实验室检测确定是否存在止血异常:红细胞压积或血红蛋白、血小板计数、血清肌酐、凝血酶原时间(PT)/部分凝血活酶时间(aPTT)。
接受PCI的患者还需测定活化凝血时间(ACT)。
如果不进行PCI,aPTT应维持在50~70秒。
在应用肝素治疗的患者,通过严密监测aPTT和ACT 可使出血的可能性降至最低。
1.急性冠状动脉综合征(ACS)的用药剂量∶接受依替巴肽治疗应按以下参数同时给予肝素:药物治疗期间:aPTT目标值50~70秒。
PCI期间:ACT目标值200~300秒。
•若在PCI术前开始给予肝素,则术中应另外给予肝素,将ACT控制在200~300秒。
•PCI术后不建议使用肝素。
2.经皮冠状动脉介入术(PCI):•应同时给予肝素治疗,使ACT维持在目标值200~300秒。
PCI手术前6小时未用肝素治疗的患者,先给予肝素静脉推注。
•在PCI术期间,为了维持ACT目标值,应加用适量肝素静脉推注。
手术中另外给予一定剂量的肝素,以维持ACT水平(200~300秒)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
恶性肿瘤,有些是致命的。
Version No.: 20171121
Page 1 of 28
【药品名称】 通用名称:依那西普注射液 商 品 名:恩利(Enbrel) 英文名称:Etanercept Solution for Injection 汉语拼音:Yinaxipu Zhusheye
【性状】 澄清、无色至黄色溶液。
【适应症】 类风湿关节炎(RA)
中度至重度活动类风湿关节炎的成年患者对包括甲氨蝶呤(如果不禁忌使用)在内 的 DMARD(改善病情的抗风湿药)无效时,可用依那西普与甲氨蝶呤联用治疗。
已证实依那西普单独使用或与甲氨蝶呤联用时,可降低 X 线检测相的关节损害进展 率,并改善关节功能。
良性、恶性和性质不明的肿瘤(包括囊肿和息肉)
少见:
非黑色素瘤皮肤癌(参见【注意事项】)
罕见:
黑色素瘤; 淋巴瘤(参见【注意事项】)
未知:
Merkel 细胞癌;白血病(参见【注意事项】)
感染和侵染:
很常见:
感染(包括上呼吸道感染、支气管炎、膀胱炎、皮肤感染)*
注射前,一次性的预填充注射液需先达到室温(大约 15 至 30 分钟)。在达到室温 的过程中针头的保护盖不应移除。溶液澄清、无色或淡黄色溶液,或包含小的透明或白 色的蛋白粒。
【不良反应】 安全信息汇总
Version No.: 20171121
Page 3 of 28
最常见的不良反应报告为注射部位反应(比如疼痛,肿胀,瘙痒,红斑和注射部位 出血),感染(比如上呼吸道感染,支气管炎, 膀胱感染和皮肤感染) ,变态反应, 自 身抗体形成,瘙痒和发热。
【成份】 主要成份:依那西普 辅料:L-精氨酸盐酸盐,氯化钠,蔗糖,磷酸氢二钠二水合物,磷酸二氢钠二水合
物和注射用水。 活性成份来源:依那西普是利用中国仓鼠卵巢(CHO)细胞表达系统产生的人肿瘤
坏死因子受体 p75 Fc 融合蛋白。二聚体由人肿瘤坏死因子受gG1 的 Fc 片段连接组成。组成依那西普的 Fc 包括 CH2、CH3 及连 接部位,但不包括 IgG1 的 CH1 部分。依那西普包括 934 个氨基酸,分子量约为 150kD。
依那西普也有严重不良反应的报道。肿瘤坏死因子抑制剂,比如依那西普,会影响 免疫系统,他们的使用也许会影响患者自身对感染和肿瘤的抵抗能力。依那西普治疗后 出现严重感染的患者小于 1/100。安全性报告中也包含致命或威胁生命的感染和脓毒血 症。使用依那西普的患者也有各种恶性肿瘤的报告,包括乳腺癌,皮肤癌和淋巴瘤。
也有严重的血液系统、神经系统异常以及自身免疫反应的报告。这些包括罕见的全 血细胞减少和非常罕见的再生障碍性贫血。使用依那西普的患者还有中枢和外周神经系 统脱髓鞘病变的报告,分别为罕见和非常罕见。另外还有罕见的狼疮,狼疮相关表现和 血管炎的报告。 不良反应汇总于以下列表
下述不良反应是基于在成人进行的临床试验报告和上市后监测报告。 在各器官系统中,将不良反应按发生率(可能出现该不良反应的患者数)高低分类列 出,分类标准如下:很常见(>1/10);常见(>1/100,1/10);少见(>1/1000,1/ 100);罕见(>1/10000,1/1000);非常罕见(1/10000);未知(无法根据现有数据 评估发生率)。
推荐剂量为 25 mg 每周二次(间隔 72-96 小时)或 50 mg 每周一次。 老年患者(≥65 岁)
无需进行剂量调整。用法用量与 18-64 岁的成人相同。 肝肾功能损害的患者
无需进行剂量调整。 注射部位
本品的注射部位为大腿、腹部和上臂,注射方式为皮下注射。每次在不同部位注射, 与前次注射部位至少相距 3 cm。禁止注射于皮肤柔嫩、瘀伤、发红或发硬部位。注射部 位的选择和注射方法的详细信息请参见“依那西普注射液的使用说明”。
变。患者使用依那西普前和用药过程中,应检测潜伏性的结核感染。使用依那西普治疗 前必须治疗潜伏性的结核感染。 侵袭性真菌感染,包括组织胞浆菌病,球孢子菌病,念珠菌病,曲霉病,芽生菌病,和 肺孢子虫病。患者有组织胞浆菌病或其他侵袭性真菌感染者,可能呈现播散性而非局限 性病变。一些活动性感染患者的组织胞浆菌病的抗原和抗体检测可能为阴性。患者的侵 袭性真菌感染有发展为严重全身性疾病风险时,应考虑给予经验性抗真菌治疗。 因机会致病菌导致的细菌性、病毒性和其他感染, 包括军团菌属和利斯塔氏菌属。 慢性或反复感染的患者使用依那西普治疗之前,应当仔细评估其承担的风险和受益。 使用依那西普治疗时和治疗后,应严密监测患者感染症状和体征的变化,包括那些治疗 前的潜伏性结核感染检测结果呈阴性而可能发生结核感染的患者。
核准日期: 2017 年 11 月 21 日 修改日期:
依那西普注射液说明书
请仔细阅读说明书并在医师指导下使用。 警告 严重感染
使用依那西普进行治疗的患者发生严重感染的风险增高,可能导致住院或死亡(见警告 和不良反应)。而绝大多数出现上述情况的患者同时合用免疫抑制剂,如甲氨蝶呤或皮质激 素。 一旦患者发生严重感染或脓毒血症应停用依那西普。 已报告的感染包括: 活动性结核感染,包括复发的潜伏性结核感染。结核感染患者反复出现播散性或肺外病
强直性脊柱炎(AS) 重度活动性强直性脊柱炎的成年患者对常规治疗无效时可使用依那西普治疗。
【规格】 Version No.: 20171121
Page 2 of 28
0.47ml: 25mg。 0.94ml: 50mg。
【用法用量】 本品需在有诊断和治疗类风湿关节炎和强直性脊柱炎经验的专科医生的指导下使
用。 尚未进行药物相容性研究,禁止将依那西普与其他药物混合使用。 本品的制备和使用方法请参见说明书的“依那西普注射液的使用说明”部分。
成人(18-64 岁) 类风湿关节炎
推荐剂量为 25 mg 每周二次(间隔 72-96 小时)或 50mg 每周一次,已证实 50mg 每 周一次的给药方案是安全有效的(参见【药理毒理】)。 强直性脊柱炎
